Proteína A
La proteína A es una proteína de superficie de 42 kDa que se encuentra originalmente en la pared celular de la bacteria Staphylococcus aureus. Está codificada por el gen spa y su regulación está controlada por la topología del ADN, la osmolaridad celular y un sistema de dos componentes llamado ArlS-ArlR. Se ha utilizado en la investigación bioquímica debido a su capacidad para unirse a las inmunoglobulinas. Está compuesta por cinco dominios homólogos de unión a Ig que se pliegan en un haz de tres hélices. Cada dominio puede unirse a proteínas de muchas especies de mamíferos, especialmente a las IgG. Se une a la cadena pesada dentro de la región Fc de la mayoría de las inmunoglobulinas y también dentro de la región Fab en el caso de la familia VH3 humana. A través de estas interacciones en el suero, donde las moléculas de IgG están unidas en la orientación incorrecta (en relación con la función normal de los anticuerpos), la bacteria altera la opsonización y la fagocitosis.
Historia
Como subproducto de su trabajo sobre antígenos de estafilococos específicos de tipo, Verwey informó en 1940 que una fracción proteica preparada a partir de extractos de estas bacterias precipitaba de forma no específica antisueros de conejo generados contra diferentes tipos de estafilococos. En 1958, Jensen confirmó el hallazgo de Verwey y demostró que los sueros de conejo previos a la inmunización, así como los sueros humanos normales, se unían al componente activo del extracto de estafilococo; designó a este componente como Antígeno A (porque se encontraba en la fracción A del extracto), pero pensó que era un polisacárido. La clasificación errónea de la proteína fue el resultado de pruebas defectuosas, pero no pasó mucho tiempo después (1962) cuando Löfkvist y Sjöquist corrigieron el error y confirmaron que el Antígeno A era de hecho una proteína de superficie en la pared bacteriana de ciertas cepas de S. aureus. El grupo de Bergen, de Noruega, denominó la proteína "Proteína A" en honor a la fracción antigénica aislada por Jensen.
Proteína Un anticuerpo vinculante
Se ha demostrado mediante refinamiento cristalográfico que el sitio de unión principal de la proteína A se encuentra en la región Fc, entre los dominios CH2 y CH3. Además, se ha demostrado que la proteína A se une a moléculas de IgG humanas que contienen fragmentos F(ab')2 de IgG de la familia de genes VH3 humanos.
La proteína A puede unirse con fuerte afinidad a la porción Fc de la inmunoglobulina de ciertas especies, como se muestra en la siguiente tabla.
| Especies | Subclase | Binding |
|---|---|---|
| Human | IgA | variable |
| IgD | débil o ninguno | |
| IgE | débil o ninguno | |
| IgG1 | fuerte | |
| IgG2 | fuerte | |
| IgG3 | débil o ninguno | |
| IgG4 | fuerte | |
| IgM | variable | |
| Yema de huevo aviar | IgY | débil o ninguno |
| Bovine | mediano | |
| Canine | mediano | |
| Goat | débil o ninguno | |
| Guiso | IgG1 | fuerte |
| Hamster | débil | |
| Caballo | mediano | |
| Koala | débil o ninguno | |
| Llama | débil o ninguno | |
| Mono (rhesus) | fuerte | |
| Murine | IgG1 | débil |
| IgG2a | fuerte | |
| IgG2 | mediano a fuerte | |
| IgG3 | mediano | |
| IgM | variable | |
| Pig | mediano a fuerte | |
| Conejo | fuerte | |
| Rat | IgG1 | débil o ninguno |
| IgG2a | débil o ninguno | |
| IgG2b | débil o ninguno | |
| IgG3 | débil | |
| Oveja | débil o ninguno |
Otras proteínas de unión anticuerpos
Además de la proteína A, otras proteínas bacterianas unidas a la inmunoglobulina como la proteína G, la proteína A/G y la proteína L se usan comúnmente para purificar, inmovilizar o detectar inmunoglobulinas.
Papel en la patogénesis
Como patógeno, el Staphylococcus aureus utiliza la proteína A, junto con una serie de otras proteínas y factores de superficie, para favorecer su supervivencia y virulencia. Para ello, la proteína A desempeña un papel multifacético:
- Al encuadernar la porción Fc de anticuerpos, la proteína A los hace inaccesibles a las osoninas, lo que perjudica la faagocitosis de la bacteria a través del ataque celular inmune.
- Proteína A facilitates the adherence of S. aureus al factor humano von Willebrand (vWF)-coated superficies, aumentando así la infecibilidad de las bacterias en el sitio de la penetración de la piel.
- Proteína Un tejido pulmonar puede inflamar por unión a los receptores del factor de necrosis tumoral 1 (TNFR-1). Esta interacción ha demostrado desempeñar un papel clave en la patogénesis de la neumonía staphylococcal.
- Proteína A se ha demostrado que la inmunidad humoral (mediada por el anticuerpo) es crítica, lo que a su vez significa que los individuos pueden infectarse repetidamente S. aureus ya que no pueden montar una respuesta anticuerpo fuerte.
- Proteína A ha demostrado promover la formación de biofilms tanto cuando la proteína está ligada covalentemente a la pared celular bacteriana como a la solución.
La proteína A ayuda a inhibir la fagocitosis y actúa como un disfraz inmunológico. Se han asociado niveles más elevados de proteína A en diferentes cepas de S. aureus con la portación nasal de esta bacteria.
Los mutantes de S. aureus que carecen de proteína A se fagocitan de manera más eficiente in vitro y los mutantes en modelos de infección tienen una virulencia reducida.
Producción
La proteína A se produce y purifica en fermentación industrial para su uso en inmunología, investigación biológica y aplicaciones industriales (ver más abajo). La proteína A natural (o nativa) se puede cultivar en Staphylococcus aureus y contiene las cinco regiones de unión de anticuerpos homólogos descritas anteriormente y una región C-terminal para la unión a la pared celular. Hoy en día, la proteína A se produce más comúnmente de forma recombinante en Escherichia coli. (También se ha demostrado que Brevibacillus es un huésped eficaz). Las versiones recombinantes de la proteína A también contienen los cinco dominios de unión de anticuerpos homólogos, pero pueden variar en otras partes de la estructura para facilitar el acoplamiento a sustratos porosos. También hay disponibles versiones diseñadas de la proteína, la primera de las cuales fue rProtein A, B4, C-CYS. Las versiones diseñadas son multímeros (normalmente tetrámeros, pentámeros o hexámeros) de un único dominio que se ha modificado para mejorar la usabilidad en aplicaciones industriales.
Research
La proteína A suele estar acoplada a otras moléculas, como un colorante fluorescente, enzimas, biotina, oro coloidal o yodo radiactivo, sin afectar el sitio de unión del anticuerpo. Algunos ejemplos incluyen la tinción de proteína A-oro (PAG) que se utiliza en el marcaje inmuno-oro, la proteína A acoplada a fluoróforo para inmunofluorescencia y la proteína A acoplada a la cadena de acoplamiento de ADN para la obtención de imágenes de ADN-PAINT. También se utiliza ampliamente acoplada a perlas magnéticas, de látex y de agarosa.
La proteína A se suele inmovilizar sobre un soporte sólido y se utiliza como un método fiable para purificar la IgG total a partir de mezclas de proteínas crudas, como suero o líquido ascítico, o se combina con uno de los marcadores anteriores para detectar la presencia de anticuerpos. El primer ejemplo de proteína A acoplada a una perla porosa para la purificación de IgG se publicó en 1972. Los estudios de inmunoprecipitación con proteína A conjugada a perlas también se utilizan habitualmente para purificar proteínas o complejos proteicos indirectamente a través de anticuerpos contra la proteína o el complejo proteico de interés.
Papel en la purificación industrial de anticuerpos
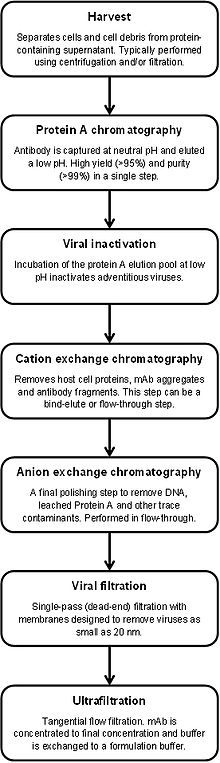
La primera referencia en la literatura a una resina cromatográfica de proteína A disponible comercialmente apareció en 1976. Hoy en día, la separación cromatográfica utilizando proteína A inmovilizada en sustratos porosos es el método más ampliamente establecido para purificar anticuerpos monoclonales (mAb) a partir del sobrenadante de cultivo celular recolectado. La elección de la proteína A como el método preferido se debe a la alta pureza y rendimiento que se logran de manera fácil y confiable. Esto forma la base para una "plataforma" general de purificación de anticuerpos que simplifica las operaciones de fabricación y reduce el tiempo y el esfuerzo necesarios para desarrollar procesos de purificación. A la derecha se muestra un proceso típico de purificación de mAb. A pesar de la larga historia de la cromatografía de proteína A para la producción de anticuerpos, el proceso aún se está mejorando en la actualidad. La cromatografía continua, más precisamente la cromatografía periódica a contracorriente, aumenta enormemente la productividad del paso de purificación.
Referencias
- ^ Graille M, Stura EA, Corper AL, Sutton BJ, Taussig MJ, Charbonnier JB, Silverman GJ (mayo de 2000). "Cristal structure of a Staphylococcus aureus protein Un dominio complejo con el fragmento Fab de un anticuerpo IgM humano: base estructural para el reconocimiento de los receptores de células B y la actividad de superantigeno". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América. 97 (10): 5399–404. Código:2000PNAS...97.5399G. doi:10.1073/pnas.97.10.5399. PMC 25840. PMID 10805799.
- ^ Idusogie EE, Presta LG, Gazzano-Santoro H, Totpal K, Wong PY, Ultsch M, et al. (abril de 2000). "Mapping of the C1q binding site on rituxan, a chimeric antibody with a human IgG1 Fc". Journal of Immunology. 164 (8): 4178–84. doi:10.4049/jimmunol.164.8.4178. PMID 10754313.
- ^ Keener AB, Thurlow LT, Kang S, Spidale NA, Clarke SH, Cunnion KM, et al. (Febrero de 2017). "Staphylococcus aureus Protein A Disrupts Immunity Mediated by Long-Lived Plasma Cells". Journal of Immunology. 198 (3): 1263–1273. doi:10.4049/jimmunol.1600093. PMC 5266639. PMID 28031339.
- ^ Verwey WF (abril de 1940). "Una proteína antígena específica de tipo derivada del staphylococcus". The Journal of Experimental Medicine. 71 (5): 635–44. doi:10.1084/jem.71.5.635. PMC 2135093. PMID 19870987.
- ^ Jensen, K (1958). "Un anticuerpo de stafilococococo en suero humano". Acta Pathol. Microbiol. Scand. 44 (4): 421–428. doi:10.1111/j.1699-0463.1958.tb01093.x. PMID 17504410.
- ^ Dixon, Frank J. (Ago 11, 1982). AVANCES IN IMMUNOLOGY. Academic Press. p. 158. ISBN 9780120224333.
- ^ Löfkvist T, Sjöquist J (noviembre de 1962). "Análisis químico y serológico de los preparativos del antígeno del staphylococcus aureus". Acta Pathologica et Microbiologica Scandinavica. 56 (3): 295–304. doi:10.1111/j.1699-0463.1962.tb04908.x.
- ^ Grov A, Myklestad B, Oeding P (1964). "Estudios inmunoquímicos sobre preparación de antígenos de staphylococcus aureus. 1. Isolación y caracterización química del antígeno A". Acta Pathologica et Microbiologica Scandinavica. 61 (4): 588–96. doi:10.1111/apm.1964.61.4.588. PMID 14185494.
- ^ Deisenhofer J (abril de 1981). "Refinación cisterna y modelos atómicos de un fragmento humano de Fc y su complejo con fragmento B de proteína A de Staphylococcus aureus a 2.9- y 2.8-A resolución". Bioquímica. 20 (9): 2361–70. doi:10.1021/bi00512a001. PMID 7236608.
- ^ Sasso EH, Silverman GJ, Mannik M (septiembre 1991). "Human IgA and IgG F(ab')2 que se unen a la proteína staphylococcal A pertenecen al subgrupo VHIII". Journal of Immunology. 147 (6): 1877–83. doi:10.4049/jimmunol.147.6.1877PMID 1909733. S2CID 35812099.
- ^ Affinity Chromatography (PDF). Vol. 1: Anticuerpos (AF ed.). GE Healthcare. 2016. p. 48.
- ^ "El cuchillo suizo del Ejército de Patógeno". Pequeñas cosas consideradas. Retrieved 2016-08-25.
- ^ Muthukrishnan G, Quinn GA, Lamers RP, Diaz C, Cole AL, Chen S, Cole AM (abril de 2011). "Exoproteome de Staphylococcus aureus revela determinantes putative del carruaje nasal". Journal of Proteome Research. 10 (4): 2064–78. doi:10.1021/pr200029r. PMC 3070068. PMID 21338050.
- ^ Goodyear CS, Silverman GJ (mayo de 2003). "Muerte por un superantigeno celular B: In vivo VH-targeted apoptotic supraclonal B cell deletion by a Staphylococcal Toxin". The Journal of Experimental Medicine. 197 (9): 1125–39. doi:10.1084/jem.20020552. PMC 2193973. PMID 12719481.
- ^ Kosugi A, JP, Yajima K, JP (Noviembre 18, 2014), Estados Unidos Patentes: 8889389 - Proceso para la producción de proteína A-como proteína con uso de bacterias Brevibacillus genus, recuperado 2016-08-26
- ^ "usp31nf26s1_c130". www.uspbpep.com. Capítulos generales: PROTEÍNA A LOS ATRIBUTOS DE CALIDAD. Retrieved 2016-08-26.
- ^ Hober S (12 de junio de 2012), Estados Unidos Patentes: 8198404 - proteína inmunoglobulina mutada, recuperado 2016-08-26
- ^ Schlichthaerle T, Ganji M, Auer A, Kimbu Wade O, Jungmann R (abril 2019). "Bacterially Derived Antibody Binders as Small Adapters for DNA-PAINT Microscopy". ChemBioChem. 20 (8): 1032-1038. doi:10.1002/cbic.201800743. Hdl:21.11116/0000-0003-E68E-APMID 30589198. S2CID 58547594.
- ^ Hjelm H, Hjelm K, Sjöquist J (noviembre de 1972). "Proteína A de Staphylococcus aureus. Su aislamiento por la cromatografía de afinidad y su uso como inmunosorbent para el aislamiento de las inmunoglobulinas". Cartas FEBS. 28 (1): 73–6. doi:10.1016/0014-5793(72)80680-X. PMID 4630462. S2CID 8733702.
- ^ Skvaril, F. (1976-10-01). "La cuestión de la especificidad en las subclases de IgG humano vinculantes a la proteína A-sefarose". Inmunoquímica. 13 (10): 871–872. doi:10.1016/0019-2791(76)90188-9. PMID 12109.
- ^ Shukla AA, Hubbard B, Tressel T, Guhan S, Low D (marzo de 2007). "Procesamiento del Downstream de anticuerpos monoclonales - aplicación de enfoques de plataforma". Journal of Chromatography. B, Tecnologías analíticas en ciencias biomédicas y de la vida. Policlonal y Monoclonal Antibody Production, Purification, Process and Product Analytics. 848 (1): 28–39. doi:10.1016/j.jchromb.2006.09.026. PMID 17046339.
- ^ Liu HF, Ma J, Winter C, Bayer R (2010-09-01). "Recovery and purification process development for monoclonal antibody production". m Abs. 2 (5): 480–99. doi:10.4161/mabs.2.5.12645. PMC 2958570. PMID 20647768.