Prolina
Prolina (símbolo Pro o P) es un ácido orgánico clasificado como un aminoácido proteinogénico (utilizado en la biosíntesis de proteínas), aunque no contiene el grupo amino -NH
2 pero es más bien una amina secundaria. El nitrógeno de la amina secundaria se encuentra en forma protonada (NH2+) en condiciones biológicas, mientras que el grupo carboxilo se encuentra en la forma desprotonada −COO− formulario. La "cadena lateral" del carbono α se conecta al nitrógeno formando un bucle de pirrolidina, clasificándolo como un aminoácido alifático. No es esencial en humanos, lo que significa que el cuerpo puede sintetizarlo a partir del aminoácido no esencial L-glutamato. Está codificado por todos los codones que comienzan con CC (CCU, CCC, CCA y CCG).
La prolina es el único aminoácido secundario proteinogénico que es una amina secundaria, ya que el átomo de nitrógeno está unido tanto al carbono α como a una cadena de tres carbonos que juntos forman un anillo de cinco miembros.
Historia y etimología
La prolina fue aislada por primera vez en 1900 por Richard Willstätter, quien obtuvo el aminoácido mientras estudiaba la N-metilprolina y la sintetizó mediante la reacción de la sal sódica de dietilmalonato con 1,3-dibromopropano. Al año siguiente, Emil Fischer aisló la prolina de la caseína y los productos de descomposición del éster γ-ftalimido-propilmalónico y publicó la síntesis de prolina a partir del éster propilmalónico de ftalimida.
El nombre prolina proviene de pirrolidina, uno de sus componentes.
Biosíntesis
La prolina se deriva biosintéticamente del aminoácido L-glutamato. El glutamato-5-semialdehído se forma primero por la glutamato 5-quinasa (dependiente de ATP) y la glutamato-5-semialdehído deshidrogenasa (que requiere NADH o NADPH). Esto puede luego ciclarse espontáneamente para formar ácido 1-pirrolina-5-carboxílico, que se reduce a prolina por la pirrolina-5-carboxilato reductasa (usando NADH o NADPH), o se convierte en ornitina por la ornitina aminotransferasa, seguida de ciclación por la ornitina ciclodeaminasa. para formar prolina.
Actividad biológica
Se ha descubierto queL-prolina actúa como un agonista débil del receptor de glicina y de los receptores ionotrópicos de glutamato tanto NMDA como no NMDA (AMPA/kainato). Se ha propuesto que es una posible excitotoxina endógena. En las plantas, la acumulación de prolina es una respuesta fisiológica común a diversos tipos de estrés, pero también forma parte del programa de desarrollo en los tejidos generativos (por ejemplo, el polen).
Una dieta rica en prolina se relacionó con un mayor riesgo de depresión en humanos en un estudio de 2022 que se probó en un ensayo preclínico limitado en humanos y principalmente en otros organismos. Los resultados fueron significativos en los otros organismos.
Propiedades en la estructura de las proteínas
La estructura cíclica distintiva de la cadena lateral de la prolina le da a la prolina una rigidez conformacional excepcional en comparación con otros aminoácidos. También afecta la tasa de formación de enlaces peptídicos entre la prolina y otros aminoácidos. Cuando la prolina se une como una amida en un enlace peptídico, su nitrógeno no se une a ningún hidrógeno, lo que significa que no puede actuar como donante de enlaces de hidrógeno, pero puede ser un aceptor de enlaces de hidrógeno.
La formación de enlaces peptídicos con Pro-tRNAPro entrante es considerablemente más lenta que con cualquier otro tRNA, lo cual es una característica general de los N-alquilaminoácidos. La formación de enlaces peptídicos también es lenta entre un tRNA entrante y una cadena que termina en prolina; siendo la creación de enlaces prolina-prolina la más lenta de todas.
La rigidez conformacional excepcional de la prolina afecta la estructura secundaria de las proteínas cerca de un residuo de prolina y puede explicar la mayor prevalencia de prolina en las proteínas de los organismos termófilos. La estructura secundaria de la proteína se puede describir en términos de los ángulos diédricos φ, ψ y ω del esqueleto de la proteína. La estructura cíclica de la cadena lateral de la prolina bloquea el ángulo φ en aproximadamente −65°.
La prolina actúa como disruptor estructural en medio de elementos regulares de estructura secundaria, como hélices alfa y láminas beta; sin embargo, la prolina se encuentra comúnmente como el primer residuo de una hélice alfa y también en las hebras de borde de las láminas beta. La prolina también se encuentra comúnmente en los giros (otro tipo de estructura secundaria) y ayuda en la formación de giros beta. Esto puede explicar el hecho curioso de que la prolina suele estar expuesta a disolventes, a pesar de tener una cadena lateral completamente alifática.
Múltiples prolinas y/o hidroxiprolinas seguidas pueden crear una hélice de poliprolina, la estructura secundaria predominante en el colágeno. La hidroxilación de la prolina por la prolil hidroxilasa (u otras adiciones de sustituyentes atractores de electrones como el flúor) aumenta significativamente la estabilidad conformacional del colágeno. Por lo tanto, la hidroxilación de la prolina es un proceso bioquímico crítico para mantener el tejido conectivo de los organismos superiores. Enfermedades graves como el escorbuto pueden resultar de defectos en esta hidroxilación, por ejemplo, mutaciones en la enzima prolil hidroxilasa o falta del cofactor ascorbato (vitamina C) necesario.
Isomerización cis-trans
Los enlaces peptídicos a la prolina y a otros aminoácidos sustituidos con N (como la sarcosina), pueden poblar tanto el cis como el trans isómeros. La mayoría de los enlaces peptídicos adoptan abrumadoramente el isómero trans (normalmente el 99,9 % en condiciones sin tensión), principalmente porque el hidrógeno de la amida (isómero trans) ofrece menos repulsión estérica al Cα que el siguiente átomo de Cα (isómero cis). Por el contrario, los isómeros cis y trans del enlace peptídico X-Pro (donde X representa cualquier aminoácido) experimentan choques estéricos con la sustitución vecina y tienen una relación mucho más baja. diferencia de energía Por lo tanto, la fracción de enlaces peptídicos X-Pro en el isómero cis bajo condiciones sin tensión es significativamente elevada, con fracciones cis típicamente en el rango de 3-10%. Sin embargo, estos valores dependen del aminoácido precedente, con Gly y residuos aromáticos que producen mayores fracciones del isómero cis. Se han identificado fracciones Cis de hasta el 40 % para enlaces peptídicos aromáticos-prolina.
Desde un punto de vista cinético, la isomerización de prolina cis–trans es un proceso muy lento que puede impedir el progreso del plegamiento de proteínas al atrapar uno o más residuos de prolina cruciales para el plegamiento en el isómero no nativo, especialmente cuando la proteína nativa requiere el isómero cis. Esto se debe a que los residuos de prolina se sintetizan exclusivamente en el ribosoma en forma de isómero trans. Todos los organismos poseen enzimas prolil isomerasas para catalizar esta isomerización, y algunas bacterias tienen prolil isomerasas especializadas asociadas con el ribosoma. Sin embargo, no todas las prolinas son esenciales para el plegamiento, y el plegamiento de proteínas puede proceder a un ritmo normal a pesar de tener confórmeros no nativos de muchos enlaces peptídicos X-Pro.
Usos
La prolina y sus derivados se utilizan a menudo como catalizadores asimétricos en las reacciones de organocatálisis de prolina. La reducción de CBS y la condensación aldólica catalizada por prolina son ejemplos destacados.
En la elaboración de cerveza, las proteínas ricas en prolina se combinan con polifenoles para producir turbidez.
L-Proline es un osmoprotector y por lo tanto se utiliza en muchas aplicaciones farmacéuticas y biotecnológicas.
El medio de cultivo utilizado en el cultivo de tejidos vegetales puede complementarse con prolina. Esto puede aumentar el crecimiento, quizás porque ayuda a la planta a tolerar el estrés del cultivo de tejidos. Para conocer el papel de la prolina en la respuesta al estrés de las plantas, consulte § Actividad biológica.
Especialidades
La prolina es uno de los dos aminoácidos que no siguen la típica trama de Ramachandran, junto con la glicina. Debido a la formación del anillo conectado al carbono beta, los ángulos ψ y φ sobre el enlace peptídico tienen menos grados de rotación permitidos. Como resultado, a menudo se encuentra en "giros" de proteínas, ya que su entropía libre (ΔS) no es comparativamente tan grande como la de otros aminoácidos y, por lo tanto, en una forma plegada frente a una forma desplegada, el cambio en la entropía es menor. Además, la prolina rara vez se encuentra en las estructuras α y β, ya que reduciría la estabilidad de tales estructuras, porque el nitrógeno α de su cadena lateral solo puede formar un enlace de nitrógeno.
Además, la prolina es el único aminoácido que no forma un color rojo púrpura cuando se revela rociándolo con ninhidrina para su uso en cromatografía. La prolina, en cambio, produce un color amarillo anaranjado.
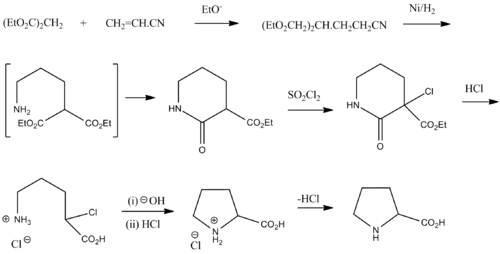
Síntesis
La prolina racémica se puede sintetizar a partir de malonato de dietilo y acrilonitrilo:
Contenido relacionado
Gimnosfaérido
Concentración
Amida