Producción de hidrógeno
El gas hidrógeno se produce mediante varios métodos industriales. Casi la totalidad del suministro actual de hidrógeno del mundo se crea a partir de combustibles fósiles. La mayor parte del hidrógeno es hidrógeno gris, que se obtiene mediante el reformado de metano con vapor. En este proceso, el hidrógeno se produce a partir de una reacción química entre vapor y metano, el principal componente del gas natural. La producción de una tonelada de hidrógeno mediante este proceso emite entre 6,6 y 9,3 toneladas de dióxido de carbono. Cuando se utiliza la captura y el almacenamiento de carbono para eliminar una gran fracción de estas emisiones, el producto se conoce como hidrógeno azul.
Por lo general, se entiende que el hidrógeno verde se produce a partir de electricidad renovable mediante la electrólisis del agua. Con menor frecuencia, las definiciones de hidrógeno verde incluyen el hidrógeno producido a partir de otras fuentes de bajas emisiones, como la biomasa. La producción de hidrógeno verde es actualmente más cara que la producción de hidrógeno gris, y la eficiencia de la conversión de energía es inherentemente baja. Otros métodos de producción de hidrógeno incluyen la gasificación de biomasa, la pirólisis de metano y la extracción de hidrógeno subterráneo.
A partir de 2023, menos del 1 % de la producción de hidrógeno específico será de bajo carbono, es decir, hidrógeno azul, hidrógeno verde e hidrógeno producido a partir de biomasa.
En 2020, se produjeron aproximadamente 87 millones de toneladas de hidrógeno en todo el mundo para diversos usos, como la refinación de petróleo, la producción de amoníaco mediante el proceso Haber y la producción de metanol mediante la reducción del monóxido de carbono. El mercado mundial de generación de hidrógeno se valoró en 155.000 millones de dólares en 2022 y se espera que crezca a una tasa anual compuesta del 9,3 % entre 2023 y 2030.
Sinopsis
Se descubrió hidrógeno molecular en el pozo superprofundo de Kola. No está claro cuánto hidrógeno molecular hay disponible en los yacimientos naturales, pero al menos una empresa se especializa en la perforación de pozos para extraer hidrógeno. La mayor parte del hidrógeno de la litosfera está unido al oxígeno del agua. La fabricación de hidrógeno elemental requiere el consumo de un portador de hidrógeno, como un combustible fósil o agua. El primer portador consume el recurso fósil y en el proceso de reformado de metano con vapor (SMR) produce dióxido de carbono, un gas de efecto invernadero. Sin embargo, en el proceso más reciente de pirólisis de metano no se produce dióxido de carbono, un gas de efecto invernadero. Estos procesos normalmente no requieren un aporte adicional de energía más allá del combustible fósil.
La descomposición del agua, este último portador, requiere de un aporte de electricidad o calor, generado a partir de alguna fuente de energía primaria (combustible fósil, energía nuclear o energía renovable). El hidrógeno producido por electrólisis del agua utilizando fuentes de energía renovables como la eólica y la solar, se denomina hidrógeno verde. Cuando se obtiene a partir de gas natural mediante pirólisis de metano con cero emisiones de gases de efecto invernadero, se denomina hidrógeno turquesa.
Cuando el combustible fósil genera emisiones de gases de efecto invernadero, generalmente se lo denomina hidrógeno gris. Si se captura la mayor parte de las emisiones de dióxido de carbono, se lo denomina hidrógeno azul. El hidrógeno producido a partir del carbón puede denominarse hidrógeno marrón o negro.
Clasificación basada en el método de producción
El hidrógeno suele designarse con distintos colores para indicar su origen (quizás porque el gris simboliza el "hidrógeno sucio").
| Color | Fuente de producción | Notas | Referencias | |
|---|---|---|---|---|
| Verde | En la mayoría de las definiciones, la electricidad renovable vía electrolisis del agua. Menos frecuentemente, definiciones de hidrógeno verde incluyen hidrógeno producido de otras fuentes de baja emisión, como la biomasa. | |||
| Turquesa | Dicción térmica del metano | Pirolisis de metano | ||
| Azul | Hidrocarburos con captura y almacenamiento de carbono | Redes CCS requeridas | ||
| Gray | Hidrocarburos fósiles, principalmente la reforma del gas natural | |||
| Marrón o negro | Hidrocarburos fósiles: marrón (lignita) o carbón negro | Gasificación de carbón o en un reactor adecuado | ||
| Rojo, rosa o morado | Energía nuclear | Seccionamiento de agua termoquímica, electrolisis de agua, o aporte de vapor a la reforma del gas natural | ||
| Amarillo | A veces se entiende por fotovoltaica solar | Fotovoltaica | ||
| Oro o blanco | Hidrógeno que ocurre naturalmente profundo dentro de la corteza terrestre | Obtenido por la minería; también conocido como blanco | ||
Métodos de producción actuales
Reforma de vapor – gris o azul
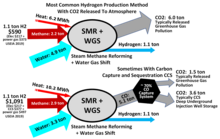
El hidrógeno se produce industrialmente a partir del reformado con vapor (SMR), que utiliza gas natural. El contenido energético del hidrógeno producido es de alrededor del 74% del contenido energético del combustible original, ya que parte de la energía se pierde en forma de calor excesivo durante la producción. En general, el reformado con vapor emite dióxido de carbono, un gas de efecto invernadero, y se lo conoce como hidrógeno gris. Si el dióxido de carbono se captura y se almacena, el hidrógeno producido se conoce como hidrógeno azul.
El reformado de metano con vapor (SMR) produce hidrógeno a partir de gas natural, principalmente metano (CH4), y agua. Es la fuente más barata de hidrógeno industrial, ya que representa casi el 50% del hidrógeno del mundo. El proceso consiste en calentar el gas a 700–1100 °C (1300–2000 °F) en presencia de vapor sobre un catalizador de níquel. La reacción endotérmica resultante forma monóxido de carbono e hidrógeno molecular (H2).
En la reacción de conversión de agua en gas, el monóxido de carbono reacciona con vapor para obtener más cantidades de H2. La WGSR también requiere un catalizador, normalmente sobre óxido de hierro u otros óxidos. El subproducto es CO2. Dependiendo de la calidad de la materia prima (gas natural, nafta, etc.), una tonelada de hidrógeno producida también producirá entre 9 y 12 toneladas de CO2, un gas de efecto invernadero que puede ser capturado.
Para este proceso, el vapor a alta temperatura (H2O) reacciona con metano (CH4) en una reacción endotérmica para producir gas de síntesis.
- CH4 + H2O → CO + 3 H2
En una segunda etapa, se genera hidrógeno adicional mediante una reacción de desplazamiento de agua-gas exotérmica a menor temperatura, que se lleva a cabo a unos 360 °C (680 °F):
- CO + H2O → CO2 + H2
Básicamente, el átomo de oxígeno (O) se extrae del agua adicional (vapor) para oxidar el CO a CO2. Esta oxidación también proporciona energía para mantener la reacción. El calor adicional necesario para impulsar el proceso generalmente se obtiene quemando una parte del metano.
De agua
Los métodos para producir hidrógeno sin el uso de combustibles fósiles implican el proceso de división del agua, o la división de la molécula de agua (H2O) en sus componentes oxígeno e hidrógeno. Cuando la fuente de energía para la división del agua es renovable o baja en carbono, el hidrógeno producido a veces se denomina hidrógeno verde. La conversión se puede lograr de varias maneras, pero actualmente todos los métodos se consideran más costosos que los métodos de producción basados en combustibles fósiles.
Electrolisis del agua: verde, rosa o amarillo
El hidrógeno se puede producir mediante electrólisis de alta presión, electrólisis de agua a baja presión o mediante una serie de otros procesos electroquímicos emergentes, como la electrólisis a alta temperatura o la electrólisis asistida por carbón. Sin embargo, los mejores procesos actuales para la electrólisis del agua tienen una eficiencia eléctrica efectiva del 70-80%, de modo que producir 1 kg de hidrógeno (que tiene una energía específica de 143 MJ/kg o aproximadamente 40 kWh/kg) requiere entre 50 y 55 kWh de electricidad.
En algunas partes del mundo, el reformado de metano con vapor cuesta entre 1 y 3 dólares por kilo en promedio, sin contar el costo de presurización del gas hidrógeno. Esto hace que la producción de hidrógeno mediante electrólisis ya sea competitiva en costos en muchas regiones, como lo señalan Nel Hydrogen y otros, incluido un artículo de la AIE que examina las condiciones que podrían generar una ventaja competitiva para la electrólisis.
Una pequeña parte (2% en 2019) se produce mediante electrólisis utilizando electricidad y agua, consumiendo aproximadamente entre 50 y 55 kilovatios-hora de electricidad por kilogramo de hidrógeno producido.

La electrólisis del agua consiste en utilizar electricidad para dividir el agua en hidrógeno y oxígeno. En 2020, menos del 0,1 % de la producción de hidrógeno procede de la electrólisis del agua. La electrólisis del agua tiene una eficiencia del 70 al 80 % (una pérdida de conversión del 20 al 30 %), mientras que el reformado con vapor del gas natural tiene una eficiencia térmica de entre el 70 y el 85 %. Se espera que la eficiencia eléctrica de la electrólisis alcance el 82-86 % antes de 2030, manteniendo al mismo tiempo la durabilidad a medida que se avanza a buen ritmo en esta área.
La electrólisis del agua puede funcionar a 50–80 °C (120–180 °F), mientras que la reformación de metano con vapor requiere temperaturas de 700–1100 °C (1300–2000 °F). La diferencia entre los dos métodos es la energía primaria utilizada: electricidad (para la electrólisis) o gas natural (para la reformación de metano con vapor). Debido a que utilizan agua, un recurso fácilmente disponible, la electrólisis y otros métodos similares de separación del agua han atraído el interés de la comunidad científica. Con el objetivo de reducir el coste de la producción de hidrógeno, se han buscado fuentes de energía renovables para permitir la electrólisis.
Existen tres tipos principales de celdas electrolíticas: celdas electrolíticas de óxido sólido (SOEC), celdas de membrana electrolítica polimérica (PEM) y celdas de electrólisis alcalina (AEC). Tradicionalmente, los electrolizadores alcalinos son más económicos en términos de inversión (generalmente utilizan catalizadores de níquel), pero menos eficientes; los electrolizadores PEM, por el contrario, son más caros (generalmente utilizan catalizadores costosos de metales del grupo del platino), pero son más eficientes y pueden operar a densidades de corriente más altas, por lo que pueden ser posiblemente más económicos si la producción de hidrógeno es lo suficientemente grande.
Las SOEC funcionan a altas temperaturas, normalmente alrededor de 800 °C (1500 °F). A estas altas temperaturas, una cantidad significativa de la energía requerida se puede proporcionar en forma de energía térmica (calor), y por eso se denomina electrólisis de alta temperatura. La energía térmica se puede obtener de varias fuentes diferentes, incluido el calor industrial residual, las centrales nucleares o las plantas termosolares concentradas. Esto tiene el potencial de reducir el costo general del hidrógeno producido al reducir la cantidad de energía eléctrica necesaria para la electrólisis.
Las celdas de electrólisis PEM suelen funcionar a temperaturas inferiores a 100 °C (212 °F). Estas celdas tienen la ventaja de ser comparativamente simples y pueden diseñarse para aceptar entradas de voltaje muy variables, lo que las hace ideales para su uso con fuentes de energía renovables, como paneles solares fotovoltaicos. Las AEC funcionan de manera óptima a altas concentraciones de electrolito (KOH o carbonato de potasio) y a altas temperaturas, a menudo cercanas a los 200 °C (392 °F).
Producción industrial y eficiencia
La eficiencia de los generadores de hidrógeno modernos se mide por la energía consumida por volumen estándar de hidrógeno (MJ/m3), suponiendo una temperatura y presión estándar del H2. Cuanto menor sea la energía utilizada por un generador, mayor será su eficiencia; un electrolizador con una eficiencia del 100% consumiría 39,4 kilovatios-hora por kilogramo (142 MJ/kg) de hidrógeno, 12.749 julios por litro (12,75 MJ/m3). La electrólisis práctica normalmente utiliza un electrolizador rotatorio, donde la fuerza centrífuga ayuda a separar las burbujas de gas del agua. Un electrolizador de este tipo a una presión de 15 bares puede consumir 50 kilovatios-hora por kilogramo (180 MJ/kg), y otros 15 kilovatios-hora (54 MJ) si el hidrógeno se comprime para su uso en automóviles de hidrógeno.
La electrólisis alcalina convencional tiene una eficiencia de alrededor del 70%, sin embargo, existen electrolizadores de agua alcalina avanzados con una eficiencia de hasta el 82%. Si se tiene en cuenta el uso del valor calorífico más alto (ya que la ineficiencia a través del calor se puede redirigir de nuevo al sistema para crear el vapor que necesita el catalizador), las eficiencias de trabajo promedio para la electrólisis PEM son de alrededor del 80%, o del 82% utilizando los electrolizadores alcalinos más modernos.
Se espera que la eficiencia de los electrolizadores PEM aumente aproximadamente hasta el 86 % antes de 2030. Se prevé que la eficiencia teórica de los electrolizadores PEM sea de hasta el 94 %.

En 2020, el costo del hidrógeno por electrólisis rondaba los 3-8 dólares por kilo. Si se considera la producción industrial de hidrógeno y se utilizan los mejores procesos actuales para la electrólisis del agua (PEM o electrólisis alcalina), que tienen una eficiencia eléctrica efectiva del 70-82 %, producir 1 kg de hidrógeno (que tiene una energía específica de 143 MJ/kg o unos 40 kWh/kg) requiere entre 50 y 55 kWh de electricidad. Con un costo de electricidad de 0,06 dólares por kilowh, tal como se establece en los objetivos de producción de hidrógeno del Departamento de Energía para 2015, el costo del hidrógeno es de 3 dólares por kilo.
El precio objetivo del Departamento de Energía de EE. UU. para el hidrógeno en 2020 es de 2,30 dólares/kg, lo que requiere un coste de electricidad de 0,037 dólares/kWh, algo alcanzable dadas las recientes licitaciones de PPA para energía eólica y solar en muchas regiones. El informe de IRENA.ORG es un extenso informe factual sobre la producción industrial actual de hidrógeno que consume entre 53 y 70 kWh por kg y que podría reducirse a unos 45 kWh/kg H
2. La energía termodinámica necesaria para el hidrógeno mediante electrólisis se traduce en 33 kWh/kg, que es superior a la del reformado con vapor con captura de carbono y superior a la de la pirólisis de metano.
Una de las ventajas de la electrólisis con respecto al hidrógeno obtenido mediante reformado con vapor de metano (SMR) es que el hidrógeno se puede producir in situ, lo que significa que se evita el costoso proceso de entrega por camión o tubería.
Electrolisis con asistencia química
Además de reducir el voltaje necesario para la electrólisis mediante el aumento de la temperatura de la celda de electrólisis, también es posible consumir electroquímicamente el oxígeno producido en un electrolizador introduciendo un combustible (como carbón, metanol, etanol, ácido fórmico, glicerol, etc.) en el lado de oxígeno del reactor. Esto reduce la energía eléctrica necesaria y tiene el potencial de reducir el costo del hidrógeno a menos del 40~60%, y la energía restante se obtiene de esta manera.
La electrólisis de agua asistida por carbono/hidrocarburos (CAWE) tiene el potencial de ofrecer un método más limpio y con menor consumo de energía para utilizar la energía química en diversas fuentes de carbono, como carbones de bajo y alto contenido de azufre, biomasa, alcoholes y metano (gas natural), donde el CO2 puro producido se puede secuestrar fácilmente sin necesidad de separación.
Hidrógeno de la biomasa – verde
La biomasa se convierte en gas de síntesis mediante gasificación y el gas de síntesis se convierte a su vez en hidrógeno mediante la reacción de desplazamiento de agua-gas (WGSR).
Hidrogen como subproducto de otros procesos químicos
La producción industrial de cloro y sosa cáustica por electrólisis genera una cantidad considerable de hidrógeno como subproducto. En el puerto de Amberes, una planta de energía de pila de combustible de demostración de 1 MW funciona con este subproducto. Esta unidad está en funcionamiento desde finales de 2011. El exceso de hidrógeno se suele gestionar con un análisis de hidrógeno.
El gas generado en los hornos de coque para la producción de acero es similar al gas de síntesis, con un 60 % de hidrógeno en volumen. El hidrógeno se puede extraer del gas del horno de coque de forma económica.
Otros métodos de combustibles fósiles
oxidación parcial
La producción de hidrógeno a partir de gas natural e hidrocarburos más pesados se logra mediante oxidación parcial. Una mezcla de combustible y aire o de combustible y oxígeno se quema parcialmente, lo que da como resultado un gas de síntesis rico en hidrógeno y monóxido de carbono. Luego se obtiene más hidrógeno y dióxido de carbono a partir del monóxido de carbono (y agua) mediante la reacción de conversión de agua en gas. El dióxido de carbono se puede coalimentar para reducir la relación hidrógeno-monóxido de carbono.
La reacción de oxidación parcial se produce cuando una mezcla subestequiométrica de combustible y aire o de combustible y oxígeno se quema parcialmente en un reformador o reactor de oxidación parcial. Se hace una distinción entre oxidación parcial térmica (TPOX) y oxidación parcial catalítica (CPOX). La reacción química adopta la forma general:
- 2 CnHm + nO2 → 2n CO + mH2
Los ejemplos idealizados para combustible para calefacción y carbón, asumiendo composiciones C12H24 y C24H12 respectivamente, son los siguientes:
- C12H24 + 6 O2 → 12 CO + 12 H2
- C24H12 + 12 O2 → 24 CO + 6 H2
Plasma pyrolysis
El proceso Kværner o proceso de negro de carbono e hidrógeno de Kvaerner (CB&H) es un método de pirólisis de plasma, desarrollado en la década de 1980 por una empresa noruega del mismo nombre, para la producción de hidrógeno y negro de carbono a partir de hidrocarburos líquidos (CnHm). De la energía disponible de la carga, aproximadamente el 48% está contenida en el hidrógeno, el 40% está contenida en el carbón activado y el 10% en el vapor sobrecalentado. En el proceso no se produce CO2.
En 2009 se presentó una variante de este proceso que utiliza tecnología de eliminación de desechos por arco de plasma para la producción de hidrógeno, calor y carbono a partir de metano y gas natural en un convertidor de plasma.
Carbón
Para producir hidrógeno a partir de carbón se utiliza la gasificación del carbón. El proceso de gasificación del carbón utiliza vapor y oxígeno para romper los enlaces moleculares del carbón y formar una mezcla gaseosa de hidrógeno y monóxido de carbono. El dióxido de carbono y los contaminantes se pueden eliminar más fácilmente del gas obtenido de la gasificación del carbón que de la combustión del carbón. Otro método de conversión es la carbonización del carbón a baja y alta temperatura.
El gas de horno de coque producido a partir de la pirólisis (calentamiento sin oxígeno) del carbón contiene aproximadamente un 60% de hidrógeno, y el resto es metano, monóxido de carbono, dióxido de carbono, amoníaco, nitrógeno molecular y sulfuro de hidrógeno (H2S). El hidrógeno se puede separar de otras impurezas mediante el proceso de adsorción por oscilación de presión. Las empresas siderúrgicas japonesas han llevado a cabo la producción de hidrógeno mediante este método.
Coqueto de petróleo
El coque de petróleo también se puede convertir en gas de síntesis rico en hidrógeno mediante la gasificación del carbón. El gas de síntesis producido se compone principalmente de hidrógeno, monóxido de carbono y H2S del azufre presente en la alimentación del coque. La gasificación es una opción para producir hidrógeno a partir de casi cualquier fuente de carbono.
pozos de aceite agotados
La inyección de microbios apropiados en pozos petrolíferos agotados permite extraer hidrógeno del petróleo restante, que no se puede recuperar. Dado que los únicos insumos son los microbios, los costos de producción son bajos. El método también produce CO
2 concentrado que, en principio, podría capturarse.
Radiolisis
La radiación nuclear puede romper los enlaces de agua mediante radiólisis. En la mina de oro de Mponeng, en Sudáfrica, los investigadores encontraron bacterias en una zona de alta radiación natural. La comunidad bacteriana, en la que predominaba un nuevo filotipo de Desulfotomaculum, se alimentaba principalmente de hidrógeno producido por radiolisis.
Termolisis
El agua se disocia espontáneamente alrededor de los 2500 °C, pero esta termólisis se produce a temperaturas demasiado altas para las tuberías y equipos de proceso habituales, lo que da como resultado un potencial de comercialización bastante bajo.
Pirolisis en biomasa
La pirólisis se puede dividir en diferentes tipos según la temperatura de pirólisis, a saber, pirólisis lenta a baja temperatura, pirólisis rápida a temperatura media y pirólisis instantánea a alta temperatura. La fuente de energía es principalmente la energía solar, con la ayuda de microorganismos fotosintéticos para descomponer el agua o la biomasa para producir hidrógeno. Sin embargo, este proceso tiene rendimientos de hidrógeno relativamente bajos y un alto costo operativo. No es un método viable para la industria.
Termolisis con ayuda nuclear
El reactor refrigerado por gas de alta temperatura (HTGR) es una de las técnicas nucleares libres de CO2 más prometedoras para producir hidrógeno mediante la división del agua a gran escala. En este método, se seleccionaron el ciclo termoquímico de yodo-azufre (IS) para la división del agua y la electrólisis de vapor a alta temperatura (HTSE) como los principales procesos para la producción nuclear de hidrógeno. El ciclo S-I sigue tres reacciones químicas:
Reacción de Bunsen: I2+SO2+2H2O→H2SO4+2HI
Descomposición HI: 2HI→H2+I2
Descomposición del ácido sulfúrico: H2SO4→SO2+1/2O2+H2O
La tasa de producción de hidrógeno del reactor de alta temperatura con ciclo IS es de aproximadamente 0,68 kg/s, y el costo de capital para construir una unidad de planta de energía es de 100 millones de dólares.
Ciclo termoquímico
Los ciclos termoquímicos combinan únicamente fuentes de calor (termo) con reacciones químicas para descomponer el agua en sus componentes de hidrógeno y oxígeno. El término ciclo se utiliza porque, además del agua, el hidrógeno y el oxígeno, los compuestos químicos utilizados en estos procesos se reciclan continuamente. Si se utiliza parcialmente electricidad como insumo, el ciclo termoquímico resultante se define como híbrido.
El ciclo de azufre-yodo (ciclo S-I) es un proceso termoquímico que genera hidrógeno a partir del agua con una eficiencia de aproximadamente el 50%. El azufre y el yodo utilizados en el proceso se recuperan y reutilizan, y no se consumen en el proceso. El ciclo se puede realizar con cualquier fuente de temperaturas muy altas, aproximadamente 950 °C, como los sistemas de energía solar de concentración (CSP) y se considera que es muy adecuado para la producción de hidrógeno mediante reactores nucleares de alta temperatura y, como tal, se está estudiando en el reactor de prueba de ingeniería de alta temperatura en Japón. Hay otros ciclos híbridos que utilizan tanto altas temperaturas como algo de electricidad, como el ciclo de cobre-cloro, que se clasifica como un ciclo termoquímico híbrido porque utiliza una reacción electroquímica en uno de los pasos de reacción, opera a 530 °C y tiene una eficiencia del 43 por ciento.
Método Ferrosilicon
El ferrosilicio es utilizado por los militares para producir rápidamente hidrógeno para globos. La reacción química utiliza hidróxido de sodio, ferrosilicio y agua. El generador es lo suficientemente pequeño como para caber en un camión y requiere sólo una pequeña cantidad de energía eléctrica, los materiales son estables y no combustibles, y no generan hidrógeno hasta que se mezclan. El método se ha utilizado desde la Primera Guerra Mundial. Un recipiente de acero pesado a presión se llena con hidróxido de sodio y ferrosilicio, se cierra y se añade una cantidad controlada de agua; la disolución del hidróxido calienta la mezcla a unos 93 °C y comienza la reacción; se produce silicato de sodio, hidrógeno y vapor.
Agua fotobiológica dividida

El hidrógeno biológico se puede producir en un biorreactor de algas. A finales de los años 90 se descubrió que si se priva a las algas de azufre, pasan de la producción de oxígeno, es decir, la fotosíntesis normal, a la producción de hidrógeno. Parece que la producción es ahora económicamente viable, superando la barrera del 7-10 por ciento de eficiencia energética (la conversión de la luz solar en hidrógeno), con una tasa de producción de hidrógeno de 10-12 ml por litro de cultivo por hora.
Agua fotocatalítica dividida
La conversión de energía solar en hidrógeno mediante el proceso de desdoblamiento del agua es una de las formas más interesantes de conseguir sistemas energéticos limpios y renovables. Sin embargo, si este proceso se ve asistido por fotocatalizadores suspendidos directamente en agua en lugar de utilizar fotovoltaica y un sistema electrolítico (la reacción se produce en un solo paso), se puede hacer más eficiente. Los sistemas actuales, sin embargo, tienen un bajo rendimiento para su implementación comercial.
Rutas de biohidrógeno
En principio, los flujos de biomasa y desechos se pueden convertir en biohidrógeno mediante la gasificación de biomasa, el reformado con vapor o la conversión biológica, como la electrólisis biocatalizada o la producción de hidrógeno por fermentación.
Entre los métodos de producción de hidrógeno, las vías biológicas son potencialmente menos intensivas en energía. Además, se puede utilizar una amplia variedad de desechos y materiales de bajo valor, como la biomasa agrícola, como fuentes renovables, para producir hidrógeno mediante vías bioquímicas o termoquímicas. Sin embargo, en la actualidad el hidrógeno se produce principalmente a partir de combustibles fósiles, en particular el gas natural, que son fuentes no renovables. El hidrógeno no solo es el combustible más limpio, sino que también se utiliza ampliamente en diversas industrias, especialmente en las de fertilizantes, petroquímica y alimentaria.
Las rutas bioquímicas para obtener hidrógeno se clasifican como procesos de fermentación oscura y fotofermentación. En la fermentación oscura, los carbohidratos se convierten en hidrógeno por microorganismos fermentativos, incluidas las bacterias anaerobias estrictas y las anaerobias facultativas. Se puede producir un máximo teórico de 4 mol de H2/mol de glucosa. Los azúcares se pueden convertir en ácidos grasos volátiles (AGV) y alcoholes como subproductos durante este proceso. Las bacterias fotofermentativas pueden generar hidrógeno a partir de AGV. Por lo tanto, los metabolitos formados en la fermentación oscura se pueden utilizar como materia prima en la fotofermentación para mejorar el rendimiento general de hidrógeno.
Producción fermentaria de hidrógeno
La producción de hidrógeno por fermentación convierte los sustratos orgánicos en hidrógeno. Un grupo diverso de bacterias promueve esta transformación. La fotofermentación se diferencia de la fermentación oscura porque solo se produce en presencia de luz. Por ejemplo, la fotofermentación con Rhodobacter sphaeroides SH2C se puede emplear para convertir algunos ácidos grasos en hidrógeno.
La producción de hidrógeno fermentativo se puede realizar mediante biofotólisis directa por algas verdes, biofotólisis indirecta por cianobacterias, fotofermentación por bacterias fotosintéticas anaeróbicas y fermentación oscura por bacterias fermentativas anaeróbicas. Por ejemplo, en la literatura se han publicado estudios sobre la producción de hidrógeno utilizando H. salinarium, una bacteria fotosintética anaeróbica, acoplada a un donador de hidrogenasa como E. coli. Enterobacter aerogenes es otro productor de hidrógeno.
Generación de hidrógeno enzimático
Se han diseñado diversas vías enzimáticas para generar hidrógeno a partir de azúcares.
Electrolisis biocatalysed

Además de la fermentación oscura, otra posibilidad es la electrohidrogénesis (electrólisis con microbios). Mediante el uso de celdas de combustible microbianas, se pueden utilizar aguas residuales o plantas para generar energía. La electrólisis biocatalizada no debe confundirse con la producción biológica de hidrógeno, ya que esta última solo utiliza algas y, en este último caso, las propias algas generan el hidrógeno de forma instantánea, mientras que en el caso de la electrólisis biocatalizada, esto sucede después de pasar por la celda de combustible microbiana y se pueden utilizar diversas plantas acuáticas, como la hierba dulce, el esparto, el arroz, los tomates, los lupinos y las algas.

polvo de aleación de aluminio nanogalvanico
El polvo de aleación de aluminio reacciona con el agua para producir gas hidrógeno al entrar en contacto con ella. Según se informa, genera hidrógeno al 100 por ciento del rendimiento teórico. No se han encontrado métodos rentables para generar la aleación de aluminio.
CC-HOD
CC-HOD (Carbón Catalítico – Hidrógeno a Demanda) es un proceso de baja temperatura en el que el carbono y el aluminio se sumergen y se calientan a aproximadamente 80 °C (176 °F), lo que provoca una reacción química que produce hidrógeno.
hidrógeno natural

El hidrógeno también está presente de forma natural bajo tierra. Este hidrógeno natural, también llamado hidrógeno blanco o hidrógeno dorado, se puede extraer de pozos de manera similar a los combustibles fósiles como el petróleo y el gas natural.
Se podría encontrar o producir hidrógeno blanco en el sistema del Rift centrocontinental a gran escala para una economía de hidrógeno renovable. Se podría bombear agua hasta rocas calientes ricas en hierro para extraer el hidrógeno.
Métodos de producción experimentales
Pirolisis de metano – turquesa
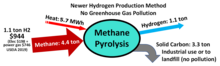
La pirólisis de metano (gas natural) con un proceso de un solo paso que consiste en burbujear metano a través de un catalizador de metal fundido es un método "sin gases de efecto invernadero" para producir hidrógeno que se demostró en condiciones de laboratorio en 2017 y que ahora se está probando a mayor escala. El proceso se lleva a cabo a altas temperaturas (1065 °C). Producir 1 kg de hidrógeno requiere aproximadamente 18 kWh de electricidad para el calor del proceso. La pirólisis de metano se puede expresar mediante la siguiente ecuación de reacción.
- CH
4g) → C(s) + 2 H
2g) ΔH° = 74,8 kJ/mol
El carbón sólido de calidad industrial puede venderse como materia prima para la fabricación o depositarse en vertederos.
Las tecnologías de pirólisis de metano se encuentran en las primeras etapas de desarrollo a partir de 2023. Tienen numerosos obstáculos que superar antes de su comercialización.
Producción biológica
La producción de hidrógeno por fermentación es la conversión fermentativa de sustrato orgánico en biohidrógeno que se manifiesta por un grupo diverso de bacterias que utilizan sistemas multienzimáticos que implican tres pasos similares a la conversión anaeróbica. Las reacciones de fermentación oscura no requieren energía lumínica, por lo que son capaces de producir hidrógeno de manera constante a partir de compuestos orgánicos durante el día y la noche. La fotofermentación se diferencia de la fermentación oscura porque solo se produce en presencia de luz. Por ejemplo, la fotofermentación con Rhodobacter sphaeroides SH2C se puede emplear para convertir ácidos grasos de moléculas pequeñas en hidrógeno. La electrohidrogénesis se utiliza en celdas de combustible microbianas donde el hidrógeno se produce a partir de materia orgánica (por ejemplo, de aguas residuales o materia sólida) mientras se aplican 0,2 – 0,8 V.
El hidrógeno biológico se puede producir en un biorreactor de algas. A finales de los años 90 se descubrió que si se priva a las algas de azufre, éstas pasan de la producción de oxígeno (es decir, la fotosíntesis normal) a la producción de hidrógeno.
El hidrógeno biológico se puede producir en biorreactores que utilizan materias primas distintas de las algas, siendo las más comunes las corrientes de desechos. El proceso implica que las bacterias se alimenten de hidrocarburos y excreten hidrógeno y CO2. El CO2 se puede secuestrar con éxito mediante varios métodos, dejando gas hidrógeno. En 2006-2007, NanoLogix demostró por primera vez un prototipo de biorreactor de hidrógeno que utiliza desechos como materia prima en la fábrica de jugo de uva de Welch en el noreste de Pensilvania (EE. UU.).
Electrolisis biocatalysed
Además de la electrólisis convencional, la electrólisis con microbios es otra posibilidad. Con la electrólisis biocatalizada, se genera hidrógeno después de pasar por la celda de combustible microbiana y se pueden utilizar una variedad de plantas acuáticas, como la hierba dulce, el pasto cordón, el arroz, los tomates, los lupinos y las algas.
Electrolisis de alta presión
La electrólisis de alta presión es la electrólisis del agua mediante la descomposición del agua (H2O) en oxígeno (O2) y gas hidrógeno (H2) mediante una corriente eléctrica que pasa a través del agua. La diferencia con un electrolizador estándar es la salida de hidrógeno comprimido de alrededor de 120-200 bares (1740-2900 psi, 12-20 MPa). Al presurizar el hidrógeno en el electrolizador, a través de un proceso conocido como compresión química, se elimina la necesidad de un compresor de hidrógeno externo; el consumo medio de energía para la compresión interna es de alrededor del 3%. La planta de producción de hidrógeno más grande de Europa (1 400 000 kg/a, electrólisis de agua a alta presión, tecnología alcalina) está en funcionamiento en Kokkola, Finlandia.
Electrolisis de alta temperatura
El hidrógeno se puede generar a partir de energía suministrada en forma de calor y electricidad mediante electrólisis de alta temperatura (HTE). Dado que parte de la energía en HTE se suministra en forma de calor, se debe convertir menos energía dos veces de calor a electricidad y luego a hidrógeno. Por lo tanto, potencialmente se requiere menos energía para producir hidrógeno. El calor nuclear se podría utilizar para separar el hidrógeno del agua. Los reactores nucleares refrigerados por gas de alta temperatura (950–1000 °C) tienen el potencial de separar el hidrógeno del agua por medios termoquímicos utilizando calor nuclear. La electrólisis de alta temperatura se ha demostrado en un laboratorio, a 108 MJ (térmicos) por kilogramo de hidrógeno producido, pero no a escala comercial. Además, se trata de hidrógeno de grado "comercial" de menor calidad, no apto para su uso en pilas de combustible.
Agua fotoelectroquímica dividida
El uso de la electricidad producida por sistemas fotovoltaicos ofrece la forma más limpia de producir hidrógeno. El agua se descompone en hidrógeno y oxígeno mediante electrólisis, un proceso de célula fotoelectroquímica (PEC) que también se denomina fotosíntesis artificial. William Ayers, de Energy Conversion Devices, demostró y patentó el primer sistema fotoelectroquímico de unión múltiple de alta eficiencia para la división directa del agua en 1983. Este grupo demostró la división directa del agua, ahora conocida como "hoja artificial" o "división solar inalámbrica del agua" con una lámina multiunión de silicio amorfo de película fina y de bajo costo sumergida directamente en el agua.
El hidrógeno se desarrolló en la superficie de silicio amorfo frontal decorada con varios catalizadores, mientras que el oxígeno se desarrolló a partir del sustrato metálico posterior. Una membrana de Nafion sobre la celda multiunión proporcionó una ruta para el transporte de iones. Su patente también enumera una variedad de otros materiales semiconductores multiunión para la división directa del agua, además del silicio amorfo y las aleaciones de silicio-germanio. La investigación continúa para desarrollar tecnología de celdas multiunión de alta eficiencia en universidades y en la industria fotovoltaica. Si este proceso es asistido por fotocatalizadores suspendidos directamente en agua en lugar de usar un sistema fotovoltaico y electrolítico, la reacción se realiza en un solo paso, lo que puede mejorar la eficiencia.
Producción fotoelectrocatalítica
Un método estudiado por Thomas Nann y su equipo en la Universidad de East Anglia consiste en un electrodo de oro cubierto de capas de nanopartículas de fosfuro de indio (InP). Introdujeron un complejo de hierro y azufre en la disposición de capas, que al sumergirlo en agua e irradiarlo con luz bajo una pequeña corriente eléctrica, produjo hidrógeno con una eficiencia del 60%.
En 2015, se informó que Panasonic Corp. había desarrollado un fotocatalizador basado en nitruro de niobio que puede absorber el 57% de la luz solar para favorecer la descomposición del agua y producir gas hidrógeno. La empresa planea lograr su aplicación comercial "lo antes posible", no antes de 2020.
Concentración solar térmica
Para disociar el agua en hidrógeno y oxígeno se necesitan temperaturas muy altas. Para que el proceso funcione a temperaturas factibles, se necesita un catalizador. El calentamiento del agua se puede lograr mediante el uso de energía solar concentrada. Hydrosol-2 es una planta piloto de 100 kilovatios en la Plataforma Solar de Almería (España) que utiliza la luz solar para obtener los 800 a 1.200 °C necesarios para calentar el agua. Hydrosol II está en funcionamiento desde 2008. El diseño de esta planta piloto de 100 kilovatios se basa en un concepto modular. Como resultado, es posible que esta tecnología pueda ampliarse fácilmente al rango de megavatios multiplicando las unidades de reactor disponibles y conectando la planta a campos de helióstatos (campos de espejos que siguen al sol) de un tamaño adecuado.
Producción termoquímica
Existen más de 352 ciclos termoquímicos que se pueden utilizar para la descomposición del agua; alrededor de una docena de estos ciclos, como el ciclo del óxido de hierro, el ciclo de óxido de cerio (IV)-óxido de cerio (III), el ciclo de óxido de zinc-zinc, el ciclo de azufre-yodo, el ciclo de cobre-cloro y el ciclo híbrido de azufre y el ciclo de óxido de aluminio-aluminio, se encuentran en fase de investigación y prueba para producir hidrógeno y oxígeno a partir de agua y calor sin utilizar electricidad. Estos procesos pueden ser más eficientes que la electrólisis de alta temperatura, con una eficiencia típica de entre el 35% y el 49% de LHV. La producción termoquímica de hidrógeno utilizando energía química a partir de carbón o gas natural generalmente no se considera, porque la vía química directa es más eficiente.
Ninguno de los procesos termoquímicos de producción de hidrógeno ha sido demostrado a niveles de producción, aunque varios de ellos se han demostrado en laboratorios.
Proceso de Kværner
El proceso Kværner o proceso de negro de carbono e hidrógeno de Kvaerner (CB&H) es un método, desarrollado en la década de 1980 por una empresa noruega del mismo nombre, para la producción de hidrógeno a partir de hidrocarburos (CnHm), como metano, gas natural y biogás. De la energía disponible de la alimentación, aproximadamente el 48% está contenida en el hidrógeno, el 40% está contenida en carbón activado y el 10% en vapor sobrecalentado.
Extracción del hidrógeno natural – Hidrogen Blanco
A partir de 2019, el hidrógeno se utiliza principalmente como materia prima industrial, sobre todo para la producción de amoníaco y metanol, y en la refinación de petróleo. Aunque inicialmente se pensó que el gas hidrógeno no se producía de forma natural en depósitos convenientes, ahora se ha demostrado que no es así; actualmente se está explotando un sistema de hidrógeno cerca de Bourakebougou, en la región de Koulikoro en Mali, que produce electricidad para las aldeas circundantes. En los últimos años se han realizado más descubrimientos de hidrógeno de origen natural en entornos geológicos continentales y terrestres, lo que abre el camino al nuevo campo del hidrógeno natural o nativo, lo que respalda los esfuerzos de transición energética.

Se podría encontrar o producir hidrógeno blanco en el sistema del Rift centrocontinental a gran escala para una economía de hidrógeno renovable. Se podría bombear agua hasta rocas calientes ricas en hierro para producir hidrógeno y extraerlo.
Impacto ambiental
La mayor parte del hidrógeno se produce a partir de combustibles fósiles, lo que genera emisiones de dióxido de carbono. El hidrógeno producido mediante esta tecnología se ha descrito como hidrógeno gris cuando las emisiones se liberan a la atmósfera, e hidrógeno azul cuando las emisiones se capturan mediante la captura y almacenamiento de carbono (CCS). Se ha estimado que el hidrógeno azul tiene una huella de gases de efecto invernadero un 20% mayor que la quema de gas o carbón para generar calor y un 60% mayor en comparación con la quema de diésel para generar calor, suponiendo tasas de fuga de metano en las fases inicial y media de producción en Estados Unidos y la producción mediante reformadores de metano a vapor (SMR) modernizados con captura de dióxido de carbono.
El uso de reformadores autotérmicos (ATR) con captura integrada de dióxido de carbono permite tasas de captura más altas con eficiencias energéticas satisfactorias y las evaluaciones del ciclo de vida han demostrado menores emisiones de gases de efecto invernadero para dichas plantas en comparación con los SMR con captura de dióxido de carbono. Se ha evaluado que la aplicación de la tecnología ATR con captura integrada de dióxido de carbono en Europa tiene una huella de gases de efecto invernadero menor que la quema de gas natural, por ejemplo, para el proyecto H21 con una reducción reportada del 68% debido a una intensidad de dióxido de carbono reducida del gas natural combinada con un tipo de reactor más adecuado para la captura de dióxido de carbono.
El hidrógeno producido a partir de fuentes de energía renovables se suele denominar hidrógeno verde. Se afirma que existen dos formas prácticas de producir hidrógeno a partir de fuentes de energía renovables. Una es utilizar la energía eléctrica para producir hidrógeno a partir de la electrólisis del agua, y la otra es utilizar gas de vertedero para producir hidrógeno en un reformador de vapor. El combustible de hidrógeno, cuando se produce a partir de fuentes de energía renovables como la eólica o la solar, es un combustible renovable. El hidrógeno producido a partir de energía nuclear mediante electrólisis a veces se considera un subconjunto del hidrógeno verde, pero también se lo puede denominar hidrógeno rosa. La central nuclear de Oskarshamn llegó a un acuerdo en enero de 2022 para suministrar hidrógeno rosa comercial en el orden de kilogramos por día.
A partir de 2020, los costos de producción estimados son de 1 a 1,80 dólares por kilo para el hidrógeno gris y el hidrógeno azul, y de 2,50 a 6,80 dólares para el hidrógeno verde.
En 2022, se producirán 94 millones de toneladas de hidrógeno gris a nivel mundial utilizando combustibles fósiles, principalmente gas natural, y por lo tanto son una fuente importante de emisiones de gases de efecto invernadero.
Usos de hidrógeno
El hidrógeno se utiliza para la conversión de fracciones pesadas de petróleo en fracciones más ligeras mediante hidrocraqueo. También se utiliza en otros procesos, como el proceso de aromatización, la hidrodesulfuración y la producción de amoníaco mediante el proceso Haber, el principal método industrial para la producción de fertilizantes nitrogenados sintéticos para el cultivo del 47 por ciento de los alimentos en todo el mundo.
El hidrógeno puede utilizarse en pilas de combustible para la generación local de electricidad o, potencialmente, como combustible para el transporte.
El hidrógeno se produce como subproducto de la producción industrial de cloro mediante electrólisis. Aunque requiere tecnologías costosas, el hidrógeno se puede enfriar, comprimir y purificar para su uso en otros procesos in situ o vender a un cliente a través de tuberías, cilindros o camiones. El descubrimiento y desarrollo de métodos menos costosos de producción de hidrógeno a granel es importante para el establecimiento de una economía del hidrógeno.
Véase también
- Producción de amoníaco
- fotosíntesis artificiales
- Biohidrogen
- Analizador de hidrógeno
- Compresor de hidrógeno
- Economía de hidrógeno § Códigos de color
- Hidrogen embrittlement
- Pruebas de fuga de hidrógeno
- Transporte hidrogeno
- Purificador de hidrógeno
- Seguridad de hidrógeno
- Sensor de hidrógeno
- Almacenamiento de hidrógeno
- Estación de hidrógeno
- Tanque de hidrógeno
- Depósito de hidrógeno
- Tecnologías de hidrógeno
- Válvula de hidrógeno
- Gas industrial
- hidrógeno líquido
- Planta nuclear de próxima generación (en parte para producción de hidrógeno)
- Hy4Heat
- Productor de hidrógeno de carril
- Proceso de Linde-Frank-Caro
- Almacenamiento subterráneo de hidrógeno
Referencias
- ^ Fan, Lixin; Tu, Zhengkai; Chan, Siew Hwa (2021). "Reciente desarrollo de tecnologías de hidrógeno y células de combustible: una revisión". Energy Reports. 7: 8421–8446. doi:10.1016/j.egyr.2021.08.003.
- ^ Reed, Stanley; Ewing, Jack (13 de julio de 2021). "El hidrógeno es una respuesta al cambio climático. Hacerlo es la parte difícil". El New York Times.
- ^ Rosenow, Jan (27 de septiembre de 2022). "¿Es calentar casas con hidrógeno todo menos un sueño de tubería? Una revisión de evidencia". Joule. 6 (10): 2225–2228. Bibcode:2022Joule...6.2225R. doi:10.1016/j.joule.2022.08.015. S2CID 252584593. Artículo en prensa.
- ^ Bonheure, Mike; Vandewalle, Laurien A.; Marin, Guy B.; Van Geem, Kevin M. (March 2021). ¿Dream o Reality? Electrification of the Chemical Process Industries". CEP Magazine. American Institute of Chemical Engineers. Archivado desde el original el 17 de julio de 2021. Retrieved 6 de julio 2021.
- ^ Griffiths, Steve; Sovacool, Benjamin K.; Kim, Jinsoo; Bazilian, Morgan; Uratani, Joao M. (Octubre 2021). "Decarbonización industrial a través del hidrógeno: Una revisión crítica y sistemática de los desarrollos, sistemas sociotécnicos y opciones de política". Energy Research & Social Science. 80: 102208. Bibcode:2021ERSS...8002208G. doi:10.1016/j.erss.2021.102208.
- ^ Squadrito, Gaetano; Maggio, Gaetano; Nicita, Agatino (noviembre 2023). "La revolución del hidrógeno verde". Energía renovable. 216: 119041. Bibcode:2023REne..21619041S. doi:10.1016/j.renene.2023.119041.
- ^ a b Deign, Jason (2020-06-29). "¿Qué es exactamente el hidrógeno verde?". Greentechmedia. Archivado desde el original el 2022-03-23. Retrieved 2022-02-11.
- ^ Squadrito, Gaetano; Maggio, Gaetano; Nicita, Agatino (noviembre 2023). "La revolución del hidrógeno verde". Energía renovable. 216: 119041. Bibcode:2023REne..21619041S. doi:10.1016/j.renene.2023.119041.
- ^ Evans, Simon; Gabbatiss, Josh (30 de noviembre de 2020). "Cuatro profunda: ¿Necesita el mundo hidrógeno para resolver el cambio climático?". Carbon Brief. Archivado desde el original el 1 de diciembre de 2020. Retrieved 1 de diciembre 2020.
- ^ "Natural Hydrogen: A Potential Clean Energy Beneath Our Feet". Yale E360. Retrieved 2024-03-23.
- ^ a b c Hassanpouryouzband, Aliakbar; Wilkinson, Mark; Haszeldine, R Stuart (2024). "Los futuros de energía hidrógeno – forraje o agricultura?". Chemical Society Reviews. 53 (5): 2258–2263. doi:10.1039/D3CS00723E. hdl:20.500.11820/b23e204c-744e-44f6-8cf5-b6761775260d. PMID 38323342.
- ^ "Hydrogen". Si.10 de julio de 2023. Sección "Energía". Retrieved 2023-09-21.
- ^ Collins, Leigh (2021-05-18). "Un mundo net-zero requeriría 306 millones de toneladas de hidrógeno verde al año para 2050": IEA vivir recarga". Últimas noticias de energía renovable. Archivado desde el original el 2021-05-21.
- ^ "Global Hydrogen Generation Market Size Report, 2030".
- ^ "Natural Hydrogen Energy LLC". Archivado desde el original el 21 de diciembre de 2012. Retrieved 2020-09-29.
- ^ "Definition of Green Hydrogen" (PDF). Clean Energy Partnership. Retrieved 2014-09-06.
- ^ Schneider, Stefan; Bajohr, Siegfried; Graf, Frank; Kolb, Thomas (octubre 2020). "Estado del arte de la producción de hidrógeno a través de la pirolisis del gas natural". ChemBioEng Reseñas. 7 (5): 150–158. doi:10.1002/cben.202000014.
- ^ Sampson2019-02-11T10:48:00+00:00, Joanna (11 de febrero de 2019). "El hidrógeno azul para un futuro verde". Gasworld. Archivado desde el original en 2019-05-09. Retrieved 2019-06-03.
{{cite web}}: CS1 maint: nombres numéricos: lista de autores (link) - ^ "Brown carbón la economía de hidrógeno pisando piedra Silencioso ECT". Archivado desde el original en 2019-04-08. Retrieved 2019-06-03.
- ^ a b "¿Puede una industria viable emerger del batido de hidrógeno?". El economista. Retrieved 2023-09-26.
- ^ "Hydrogen Color Explicado". Sensonic. Retrieved 2023-11-22.
- ^ a b Rejilla nacional. "El espectro del color de hidrógeno". National Grid GroupLondres, Reino Unido. Retrieved 2022-09-29.
- ^ "¿Qué potencial para hidrógeno natural?". Energy Observer. Retrieved 2023-07-03.
- ^ a b c BMWi (junio 2020). Estrategia nacional de hidrógeno (PDF). Berlín, Alemania: Ministerio Federal de Asuntos Económicos y Energía (BMWi). Archivado (PDF) del original el 2020-12-13. Retrieved 2020-11-27.
- ^ a b c Van de Graaf, Thijs; Overland, Indra; Scholten, Daniel; Westphal, Kirsten (diciembre 2020). "¿El nuevo aceite? La geopolítica y la gobernanza internacional del hidrógeno". Energy Research & Social Science. 70: 101667. Bibcode:2020ERSS...7001667V. doi:10.1016/j.erss.2020.101667. PMC 7326412. PMID 32835007.
- ^ Sansom, Robert; Baxter, Jenifer; Brown, Andy; Hawksworth, Stuart; McCluskey, Ian (2020). Transición al hidrógeno: evaluación de los riesgos e incertidumbres de ingeniería (PDF). Londres, Reino Unido: La Institución de Ingeniería y Tecnología (IET). Archivado (PDF) original el 2020-05-08. Retrieved 2020-03-22.
- ^ Bruce, S; Temminghoff, M; Hayward, J; Schmidt, E; Munnings, C; Palfreyman, D; Hartley, P (2018). Hoja de ruta nacional de hidrógeno: caminos hacia una industria de hidrógeno económicamente sostenible en Australia (PDF). Australia: CSIRO. Archivado (PDF) del original el 2020-12-08. Retrieved 2020-11-28.
- ^ Departamento de Ciencias de la Tierra (12 de septiembre de 2022). "Gold hidrógeno". Department of Earth Sciences, Oxford University. Oxford, Reino Unido. Retrieved 2022-09-29.
- ^ Hassanpouryouzband, Aliakbar; Wilkinson, Mark; Haszeldine, R Stuart (2024). "Los futuros de energía hidrógeno – forraje o agricultura?". Chemical Society Reviews. 53 (5): 2258–2263. doi:10.1039/D3CS00723E. hdl:20.500.11820/b23e204c-744e-44f6-8cf5-b6761775260d. PMID 38323342.
- ^ "Actual Worldwide Hydrogen Production from..." Arno A Evers. Diciembre de 2008. Archivado desde el original en 2015-02-02. Retrieved 2008-05-09.
- ^ Velazquez Abad, A.; Dodds, P.E. (2017). "Producción de hidrógeno". Encyclopedia of Sustainable Technologies. pp. 293–304. doi:10.1016/B978-0-12-409548-9.10117-4. ISBN 978-0-12-804792-7.
- ^ Dincer, Ibrahim; Acar, Canan (septiembre 2015). "Revisar y evaluar métodos de producción de hidrógeno para una mejor sostenibilidad". International Journal of Hydrogen Energy. 40 (34): 11094-11111. código:2015IJHE...4011094D. doi:10.1016/j.ijhydene.2014.12.035.
- ^ a b c Press, Roman J.; Santhanam, K. S. V.; Miri, Massoud J.; Bailey, Alla V.; Takacs, Gerald A. (2008). Introducción al hidrógeno Tecnología. John Wiley ' Sons. p. 249. ISBN 978-0-471-77985-8.
- ^ Collodi, Guido (2010-03-11). "Hydrogen Production via Steam Reforming with CO2 Capture" (PDF). CISAP4 4a Conferencia Internacional sobre Seguridad y Medio Ambiente en la Industria del Proceso. Retrieved 2015-11-28.
- ^ "HFCIT Hydrogen Production: Natural Gas Reforming". Departamento de Energía de EE.UU. 2008-12-15.
- ^ Badwal, Sukhvinder P. S.; Giddey, Sarbjit S.; Munnings, Christopher; Bhatt, Anand I.; Hollenkamp, Anthony F. (24 de septiembre de 2014). "Las nuevas tecnologías de conversión y almacenamiento de energía electroquímica". Fronteras en Química. 2: 79. Bibcode:2014FrCh....2...79B. doi:10.3389/fchem.2014.00079. PMC 4174133. PMID 25309898.
- ^ Werner Zittel; Reinhold Wurster (1996-07-08). "Capítulo 3: Producción de hidrógeno. Parte 4: Producción de electricidad mediante electrolisis". HyWeb: Conocimiento – Hidrógeno en el Sector de la Energía. Ludwig-Bölkow-Systemtechnik GmbH. Archivado desde el original el 01/02/2007. Retrieved 2010-10-01.
- ^ Bjørnar Kruse; Sondre Grinna; Cato Buch (2002-02-13). "Hydrogen – Estado y posibilidades". La Fundación Bellona. Archivado desde el original (PDF) el 2011-07-02.
Se predicen factores de eficiencia para electrolizadores PEM hasta un 94%, pero esto es sólo teórico en este momento.
- ^ "Ecolisis de agua 3D de alta calidad y alta eficiencia". Grid-shift.com. Archivado desde el original el 2012-03-22. Retrieved 2011-12-13.
- ^ "Wide Spread Adaption of Competitive Hydrogen Solution" (PDF). nelhydrogen.com. Nel ASA. Archivado (PDF) del original en 2018-04-22. Retrieved 22 de abril 2018.
- ^ Philibert, Cédric. "Commentario: Producir hidrógeno industrial de energía renovable". iea.org. International Energy Agency. Archivado desde el original el 22 de abril de 2018. Retrieved 22 de abril 2018.
- ^ IEA H2 2019, p. 37
- ^ "¿Cuánto se necesita electricidad/agua para producir 1 kg de H2 por electrolisis?". Archivado desde el original el 17 de junio de 2020. Retrieved 17 de junio 2020.
- ^ Petrova, Magdalena (2020-12-04). "El hidrógeno verde está ganando tracción, pero todavía tiene enormes obstáculos para superar". CNBC. Retrieved 2021-06-20.
- ^ "ITM – Infraestructura de reabastecimiento de hidrógeno – Febrero 2017" (PDF). nivel-network.com. Retrieved 17 de abril 2018.
- ^ "Reducción y aumento de rendimiento de los electrolizadores PEM" (PDF). fch.europa.eu. Células de combustible y conjunto de hidrógeno. Retrieved 17 de abril 2018.
- ^ Kalamaras, Christos M.; Efstathiou, Angelos M. (2013). "Hydrogen Production Technologies: Current State and Future Developments". Conference Papers in Energy. 20131-9. doi:10.1155/2013/690627.
- ^ "Reducción y aumento de rendimiento de los electrolizadores PEM" (PDF). fch.europa.eu. Instalación conjunta de células de combustible e hidrógeno. Retrieved 17 de abril 2018.
- ^ "Informe y estados financieros 30 abril 2016" (PDF). itm-power.com. Retrieved 17 de abril 2018.
- ^ "Hydrogen Production: Natural Gas Reforming". energy.gov. US Department of Energy. Retrieved 17 de abril 2018.
- ^ a b Hordeski, M. F. Combustibles alternativos: el futuro del hidrógeno. 171–199 (The Fairmont Press, inc., 2007).
- ^ Badwal, Sukhvinder P.S.; Giddey, Sarbjit; Munnings, Christopher (2013). "Producción de hidrógeno a través de rutas electrolíticas sólidas". Wiley Interdisciplinary Reseñas: Energía y Medio Ambiente. 2 (5): 473-487. Código:2013WIREE...2..473B. doi:10.1002/wene.50. S2CID 135539661.
- ^ Sebbahi, Seddiq; Nabil, Nouhaila; Alaoui-Belghiti, Amine; Laasri, Said; Rachidi, Samir; Hajjaji, Abdelowahed (2022). "Evaluación de las tres tecnologías de electrolisis de agua más desarrolladas: Electrolisis de Agua Alkaline, Membrana Proton Exchange y Electrolisis de Oxido Sólido". Materiales Hoy: Proceedings. 66: 140–145. doi:10.1016/j.matpr.2022.04.264.
- ^ a b Ogden, J.M. (1999). "Prospectos para construir una infraestructura energética de hidrógeno". Annual Review of Energy and the Environment. 24: 227–279. doi:10.1146/annurev.energy.24.1.227.
- ^ Hauch, Anne; Ebbesen, Sune Dalgaard; Jensen, Søren Højgaard; Mogensen, Mogens (2008). "Exilisis de alta temperatura altamente eficiente". Journal of Materials Chemistry. 18 (20): 2331–40. doi:10.1039/b718822f.
- ^ En el laboratorio se puede hacer electrolisis de agua con un aparato simple como un voltímetro Hofmann:"Electrolisis del agua y el concepto de carga". Archivado desde el original el 2010-06-13.
- ^ "Las centrales nucleares pueden producir hidrógeno para alimentar la "economía del hidrógeno" (Libertad de prensa). American Chemical Society. 25 de marzo de 2012. Archivado desde el original el 10 de diciembre de 2019. Retrieved 9 de marzo 2013.
- ^ Clarke, R.E.; Giddey, S.; Ciacchi, F.T.; Badwal, S.P.S.; Paul, B.; Andrews, J. (2009). "Acoplamiento directo de un electrolizador a un sistema PV solar para generar hidrógeno". International Journal of Hydrogen Energy. 34 (6): 2531–42. doi:10.1016/j.ijhydene.2009.01.053.
- ^ Luca Bertuccioli; et al. (7 de febrero de 2014). "Development of water electrolysis in the European Union" (PDF). Células de Combustible Cliente y Junta de Hidrógeno. Archivado desde el original (PDF) el 31 de marzo de 2015. Retrieved 2 de mayo 2018.
- ^ L. Lao; C. Ramshaw; H. Yeung (2011). "Intensificación del proceso: electrolisis del agua en un campo de aceleración centrífuga". Journal of Applied Electrochemistry. 41 (6): 645–656. doi:10.1007/s10800-011-0275-2. hdl:1826/6464. S2CID 53760672. Retrieved 12 de junio, 2011.
- ^ Stensvold, Tore (26 de enero de 2016). «Coca-Cola-oppskrift» kan gjøre hidrógeno til nytt norsk industrieventyr. Teknisk Ukeblad,
- ^ Stolten, Detlef (Jan 4, 2016). Hydrogen Science and Engineering: Materiales, Procesos, Sistemas y Tecnología. John Wiley ' Sons. p. 898. ISBN 9783527674299. Retrieved 22 de abril 2018.
- ^ Tossenkrupp. "Hydrogen from water electrolysis – solutions for sustainability". tissenkrupp-uhde-chlorine-engineers.com. Archivado desde el original el 19 de julio de 2018. Retrieved 28 de julio 2018.
- ^ "ITM – Infraestructura de reabastecimiento de hidrógeno – Febrero 2017" (PDF). nivel-network.com. Retrieved 17 de abril 2018.
- ^ "Reducción y aumento de rendimiento de los electrolizadores PEM" (PDF). fch.europa.eu. Células de combustible y conjunto de hidrógeno. Retrieved 17 de abril 2018.
- ^ Bjørnar Kruse; Sondre Grinna; Cato Buch (13 de febrero de 2002). "Hydrogen—Estatus y posibilidades" (PDF). The Bellona Foundation. p. 20. Archivado desde el original el 16 de septiembre de 2013.
{{cite web}}: CS1 maint: URL infit (link) - ^ Fickling, David (2 de diciembre de 2020). "Hydrogen es una apuesta del Dólar Trillion en el futuro". Bloomberg.com. Archivado desde el original el 2 de diciembre de 2020.
hidrógeno verde.. precio actual de alrededor de $3 a $8 por kilogramo.. hidrógeno gris, que cuesta tan poco como $1
- ^ Werner Zittel; Reinhold Wurster (1996-07-08). "Capítulo 3: Producción de hidrógeno. Parte 4: Producción de electricidad mediante electrolisis". HyWeb: Conocimiento – Hidrógeno en el Sector de la Energía. Ludwig-Bölkow-Systemtechnik GmbH.
- ^ Bjørnar Kruse; Sondre Grinna; Cato Buch (2002-02-13). "Hydrogen—Status y Posibilidades". La Fundación Bellona. Archivado desde el original (PDF) el 2011-07-02.
Se predicen factores de eficiencia para electrolizadores PEM hasta un 94%, pero esto es sólo teórico en este momento.
- ^ "Ecolisis de agua 3D de alta calidad y alta eficiencia". Grid-shift.com. Archivado desde el original el 2012-03-22. Retrieved 2011-12-13.
- ^ "DOE Technical Targets for Hydrogen Production from Electrolysis". energy.gov. US Department of Energy. Retrieved 22 de abril 2018.
- ^ Deign, Jason. "Xcel Attracts 'Unprecedented' Low Prices for Solar and Wind Paired with Storage". greentechmedia.com. Wood MacKenzie. Retrieved 22 de abril 2018.
- ^ acceso al 22 de junio de 2021
- ^ Giddey, S; Kulkarni, A; Badwal, S.P.S (2015). "Fuente generación de hidrógeno de emisión a través de electrolisis asistida al carbono". International Journal of Hydrogen Energy. 40 (1): 70-4. Código:2015IJHE...40...70G. doi:10.1016/j.ijhydene.2014.11.033.
- ^ Sunghyun; Jeon, Hongrae; Kim, Tae Jin; Lee, Jaeyoung (2012). "Producción de hidrógeno limpia de soluciones de agua de metanol a través del proceso de reforma electrolítica ahorrado por el poder". Journal of Power Sources. 198: 218–22. doi:10.1016/j.jpowsour.2011.09.083.
- ^ Ju, Hyungkuk; Giddey, Sarbjit; Badwal, Sukhvinder P.S (2017). "El papel de SnO nanosizado2 en electrocatalistas basados en Pt para la producción de hidrógeno en electrolisis de agua asistida de metanol". Electrochimica Acta. 229: 39–47. doi:10.1016/j.electacta.2017.01.106.
- ^ Ju, Hyungkuk; Giddey, Sarbjit; Badwal, Sukhvinder P.S; Mulder, Roger J (2016). "Conversión eléctrica-catalítica de etanol en células electrolíticas sólidas para la generación de hidrógeno distribuida". Electrochimica Acta. 212: 744–57. doi:10.1016/j.electacta.2016.07.062.
- ^ a b Lamy, Claude; Devadas, Abirami; Simoes, Mario; Coutanceau, Christophe (2012). "Clean hydro generation through the electrocatalytic oxidation of formic acid in a Proton Exchange Membrane Electrolysis Cell (PEMEC)". Electrochimica Acta. 60: 112–20. doi:10.1016/j.electacta.2011.11.006.
- ^ a b Badwal, Sukhvinder P. S; Giddey, Sarbjit S; Munnings, Christopher; Bhatt, Anand I; Hollenkamp, Anthony F (2014). "Las nuevas tecnologías de conversión y almacenamiento de energía electroquímica". Fronteras en Química. 2: 79. Bibcode:2014FrCh....2...79B. doi:10.3389/fchem.2014.00079. PMC 4174133. PMID 25309898.
- ^ Ju, H; Badwal, S.P.S; Giddey, S (2018). "Una revisión integral de electrolisis de agua asistida de carbono e hidrocarburos para la producción de hidrógeno". Energía aplicada. 231: 502–533. Código:2018ApEn..231..502J. doi:10.1016/j.apenergy.2018.09.125. S2CID 117669840.
- ^ Ju, Hyungkuk; Badwal, Sukhvinder; Giddey, Sarbjit (2018). "Una revisión integral de la electrolisis de agua asistida de carbono e hidrocarburos para la producción de hidrógeno". Energía aplicada. 231: 502–533. Código:2018ApEn..231..502J. doi:10.1016/j.apenergy.2018.09.125. S2CID 117669840.
- ^ a b Sasidhar, Nallapaneni (30 noviembre 2023). "Carbon Neutral Fuels and Chemicals from Standalone Biomass Refineries". Indian Journal of Environment Engineering. 3 (2): 1-8. doi:10.54105/ijee.B1845.113223.
- ^ http://www.nedstack.com/images/stories/news/documents/20120202_Press%20release%20Solvay%20PEM%20Power%20Plant%20start%20up.pdf Archivado 2014-12-08 en el Wayback Machine Nedstack
- ^ "Gas diferenciados de procesos de producción de acero". Archivado desde el original el 27 de marzo de 2016. Retrieved 5 de julio 2020.
- ^ "Producción de hidrógeno licuado proveniente de COG" (PDF). Archivado (PDF) del original el 8 de febrero de 2021. Retrieved 8 de julio 2020.
- ^ "Tecnologías de hidrógeno". www.interstatetraveler.us.
- ^ [1]
- ^ "Kværner-process with plasma arc waste disposal technology". Archivado desde el original el 13 de julio de 2014. Retrieved 2009-10-13.
- ^ "Emisiones Ventajas de la Gasificación". National Energy Technology Laboratory. Departamento de Energía de EE.UU.
- ^ "Emisiones de carbón ardiente". U.S. EIA. U.S. Energy Information Administration.
- ^ Lee, Woon-Jae; Lee, Yong-Kuk (2001). "Características de presión interna de gas generadas durante la carbonización de carbón en un horno de coca". Energy " Fuels. 15 (3): 618–23. doi:10.1021/ef990178a.
- ^ Gemayel, Jimmy El; MacChi, Arturo; Hughes, Robin; Anthony, Edward John (2014). "Simulación de la integración de una instalación de actualización de betún y un proceso IGCC con captura de carbono". Fuel. 117: 1288–97. Bibcode:2014Fuel..117.1288G. doi:10.1016/j.fuel.2013.06.045.
- ^ Blain, Loz (2022-10-04). "Los microbios que comen suelo excreten el hidrógeno "limpio" más barato del mundo". Nuevo Atlas. Retrieved 2022-10-06.
- ^ Introducción a la química de radiación Capítulo 7
- ^ Manual de producción de hidrógeno nuclear Capítulo 8
- ^ Li-Hung Lin; Pei-Ling Wang; Douglas Rumble; Johanna Lippmann-Pipke; Erik Boice; Lisa M. Pratt; Barbara Sherwood Lollar; Eoin L. Brodie; Terry C. Hazen; Gary L. Andersen; Todd Z. DeSantis; Duane P. Moser; Dave Kershaw; T. C. Onstot (2006). "Sostenibilidad a largo plazo de una bioma de alta energía y baja diversidad". Ciencia. 314 (5798): 479–82. Código:2006...314..479L. doi:10.1126/ciencia.1127376. PMID 17053150. S2CID 22420345.
- ^ ¿Dream o Reality? Electrification of the Chemical Process Industries". www.aiche-cep.com. Retrieved 2021-08-22.
- ^ Guoxin, Hu; Hao, Huang (mayo de 2009). "Hydrogen rica producción de gas por gasificación de biomasa húmeda utilizando un CO2 sorbent". Biomasa y Bioenergía. 33 (5): 899–906. doi:10.1016/j.biombioe.2009.02.006.
- ^ Ping, Zhang; Laijun, Wang; Songzhe, Chen; Jingming, Xu (enero 2018). "Progreso de la producción de hidrógeno nuclear a través del proceso de yodo-sulfur en China". Reseñas de Energía Renovable y Sostenible. 81: 1802-1812. Código:2018RSERv..81.1802P. doi:10.1016/j.rser.2017.05.275.
- ^ Producir hidrógeno: Los ciclos termoquímicos
- ^ IEA Energy Technology Essentials – Hydrogen Production & Distribution Archived 2011-11-03 at the Wayback Machine, April 2007
- ^ "HTTR High Temperature engineering Test Reactor". Httr.jaea.go.jp. Archivado desde el original el 13 de diciembre de 2012. Retrieved 2014-01-23.
- ^ https://smr.inl.gov/Document.ashx?path=DOCS%2FGCR-Int%2FNHDDELDER.pdf Archivado 2016-12-21 en la máquina Wayback. Progresos en la energía nuclear Calor nuclear para la producción de hidrógeno: Cobertura de una temperatura muy alta / alta reactor a una planta de producción de hidrógeno. 2009
- ^ Informe del Estado 101 – Reactor de alta temperatura de turbina de gas (GTHTR300C)" (PDF).
- ^ "Jaea's VHTR for HYDROGEN AND ELECTRICITY COGENERATION: GTHTR300C" (PDF). Archivado desde el original (PDF) on 2017-08-10. Retrieved 2013-12-04.
- ^ Chukwu, C., Naterer, G. F., Rosen, M. A., "Process Simulation of Nuclear-Produced Hydrogen with a Cu-Cl Cycle", 29th Conference of the Canadian Nuclear Society, Toronto, Ontario, Canada, 1–4, 2008. "Simulación de procesos de producción de hidrógeno termoquímico con base nuclear con un ciclo de cloro de cobre" (PDF). Archivado desde el original (PDF) on 2012-02-20. Retrieved 2013-12-04.
- ^ Informe No 40: El proceso de ferrosilicon para la generación de hidrógeno
- ^ Candid science: conversations with known chemists, István Hargittai, Magdolna Hargittai, p. 261, Imperial College Press (2000) ISBN 1-86094-228-8
- ^ Hemschemeier, Anja; Melis, Anastasios; Happe, Thomas (2009). "Acercamientos analíticos a la producción fotobiológica de hidrógeno en algas verdes no lineales". Photosynthesis Research. 102 (2–3): 523–40. código:2009PhoRe.102..523H. doi:10.1007/s11120-009-9415-5. PMC 2777220. PMID 19291418.
- ^ "DOE 2008 Report 25 %" (PDF). Archivado desde el original (PDF) on 2017-06-17. Retrieved 2009-03-06.
- ^ Jenvanitpanjakul, Peesamai (3 a 4 de febrero de 2010). Renewable Energy Technology and Prospect on Biohydrogen Study In Thailand (PDF). Reunión del Comité Directivo y Taller de la Red de Investigación de la APEC para la Tecnología de Biohidrógeno Avanzado. Taichung: Feng Chia University. Archivado desde el original (PDF) el 4 de julio de 2013.
- ^ Navarro Yerga, Rufino M.; Álvarez Galván, M. Consuelo; Del Valle, F.; Villoria De La Mano, José A.; Fierro, José L. G. (2009). "Water Splitting on Semiconductor Catalysts under Visible-Light Irradiation". ChemSusChem. 2 (6): 471–85. Código:2009ChSCh...2..471N. doi:10.1002/csc.200900018. PMID 19536754.
- ^ Navarro, R.M.; Del Valle, F.; Villoria De La Mano, J.A.; Álvarez-Galván, M.C.; Fierro, J.L.G. (2009). "Agua fotocatalítica dividida bajo luz visible: desarrollo de conceptos y catalizadores". Fotocatalítica Tecnología. Avances en Ingeniería Química. Vol. 36. pp. 111–43. doi:10.1016/S0065-2377(09)00404-9. ISBN 978-0-12-374763-1.
- ^ Ropero-Vega, J.L.; Pedraza-Avella, J.A.; Niño-Gómez, M.E. (septiembre de 2015). "Producción de hidrógeno por fotoelectrolisis de soluciones acuosas de fenol mediante semiconductores mixtos de óxido de Bi–Nb–M–O (M=Al, Fe, Ga, In) como fotonodos". Catalisis Hoy. 252: 150–156. doi:10.1016/j.cattod.2014.11.007.
- ^ Bajo, Jingxiang; Yu, Jiaguo; Jaroniec, Mietek; Wageh, Swelm; Al-Ghamdi, Ahmed A. (Mayo 2017). "Heterojunción Photocatalysts". Materiales avanzados. 29 (20). Bibcode:2017AdM....2901694L. doi:10.1002/adma.201601694. PMID 28220969. S2CID 21261127.
- ^ Djurišić, Aleksandra B.; He, Yanling; Ng, Alan M. C. (Marzo 2020). "Fotos de luz visible: perspectivas y desafíos". APL Materials. 8 (3): 030903. Código:2020APLM....8c0903D. doi:10.1063/1.5140497.
- ^ a b Häussinger, Peter; Lohmüller, Reiner; Watson, Allan M. (2011). "Hydrogen, 1. Propiedades y Occurrence". Enciclopedia de Ullmann de Química Industrial. doi:10.1002/14356007.a13_297.pub2. ISBN 978-3-527-30673-2.
- ^ a b Asadi, Nooshin; Karimi Alavijeh, Masih; Zilouei, Hamid (enero de 2017). "Desarrollo de una metodología matemática para investigar la producción de biohidrógeno de residuos agrícolas regionales y nacionales: Un estudio de caso de Irán". International Journal of Hydrogen Energy. 42 (4): 1989–2007. Bibcode:2017IJHE...42.1989A. doi:10.1016/j.ijhydene.2016.10.021.
- ^ Tao, Y; Chen, Y; Wu, Y; Él, Y; Zhou, Z (2007). "El alto rendimiento de hidrógeno de un proceso de dos pasos de la fermentación oscura y foto de la sucrosa". International Journal of Hydrogen Energy. 32 (2): 200-6. Código:2007IJHE...32..200T. doi:10.1016/j.ijhydene.2006.06.034.
- ^ Rajanandam, Brijesh; Kiran, Siva (2011). "Optimización de la producción de hidrógeno por salinarium de Halobacterium junto con E coli utilizando plasma lácteo como sustrato fermentativo". Journal of Biochemical Technology. 3 (2): 242–4. Archivado desde el original el 2013-07-31. Retrieved 2013-03-09.
- ^ Asadi, Nooshin; Zilouei, Hamid (marzo de 2017). "Optimización del pretratamiento organosolv de paja de arroz para la producción de biohidrógeno mejorada utilizando aerógenos enterobacter". Bioresource Technology. 227: 335–344. Bibcode:2017BiTec.227..335A. doi:10.1016/j.biortech.2016.12.073. PMID 28042989.
- ^ Percival Zhang, Y-H; Sun, Jibin; Zhong, Jian-Jiang (2010). "Producción de Biofuel por vía in vitro sintética enzimática biotransformación". Opinión actual en Biotecnología. 21 (5): 663–9. doi:10.1016/j.copbio.2010.05.005. PMID 20566280.
- ^ Strik, David P. B. T. B.; Hamelers (Bert), H. V. M.; Snel, Jan F. H.; Buisman, Cees J. N. (2008). "Producción de electricidad verde con plantas vivas y bacterias en una célula de combustible". International Journal of Energy Research. 32 (9): 870–6. Código:2008 IJER...32..870S. doi:10.1002/er.1397. S2CID 96849691.
- "Las plantas vivientes producen energía". Wageningen University and Research Centre (Libertad de prensa). Archivado desde el original el 2010-05-17.
- ^ Timmers, Ruud (2012). Generación de electricidad por plantas vivas en una célula de combustible microbiano de planta (Tesis PhD). Universidad Wageningen. ISBN 978-94-6191-282-4.
- ^ "Aluminum Based Nanogalvanic Alloys for Hydrogen Generation". U.S Army Combat Capabilities Development Command Army Research Laboratory. Retrieved 6 de enero 2020.
- ^ McNally, David (25 de julio de 2017). "El descubrimiento Army puede ofrecer nueva fuente de energía". U.S. Army. Retrieved 6 de enero 2020.
- ^ Gaucher, Éric C. (Febrero 2020). "Nuevas Perspectivas en la Exploración Industrial para Hidrogeno Nativo". Elementos: Revista Internacional de Mineralurgia, Geoquímica y Petrología. 16 (1): 8-9. Código:2020Eleme..16....8G. doi:10.2138/gselements.16.1.8.
- ^ Mano, Eric. "Hidden hidrógeno". science.org. Ciencia. Retrieved 9 de diciembre 2023.
- ^ "El potencial para el hidrógeno geológico para la energía de la próxima generación tóxico U.S. Geological Survey".
- ^ Fernández, Sonia. "Los investigadores desarrollan tecnologías potencialmente de bajo costo y bajas emisiones que pueden convertir metano sin formar CO2". Phys-Org. Instituto Americano de Física. Archivado desde el original el 19 de octubre de 2020. Retrieved 19 de octubre 2020.
- ^ BASF. "Los investigadores de la BBASF trabajando en procesos de producción fundamentalmente nuevos y de bajo carbono, Methane Pyrolysis". Sostenibilidad de los Estados Unidos. BASF. Archivado desde el original el 19 de octubre de 2020. Retrieved 19 de octubre 2020.
- ^ Schneider, Stefan; Bajohr, Siegfried; Graf, Frank; Kolb, Thomas (octubre 2020). "Estado del arte de la producción de hidrógeno a través de la pirolisis del gas natural". ChemBioEng Reseñas. 7 (5): 150–158. doi:10.1002/cben.202000014.
- ^ Upham, D. Chester; Agarwal, Vishal; Khechfe, Alexander; Snodgrass, Zachary R.; Gordon, Michael J.; Metiu, Horia; McFarland, Eric W. (17 de noviembre de 2017). "Catalytic molten metals for the direct conversion of methane to hydro and separable carbon". Ciencia. 358 (6365): 917–921. Bibcode:2017Sci...358..917U. doi:10.1126/science.aao5023. PMID 29146810. S2CID 206663568.
- ^ Palmer, Clarke; Upham, D. Chester; Smart, Simon; Gordon, Michael J.; Metiu, Horia; McFarland, Eric W. (enero 2020). "La reforma del metano catalizada por aleaciones de metal fundido". Nature Catalysis. 3 (1): 83–89. doi:10.1038/s41929-019-0416-2. S2CID 210862772.
- ^ Cartwright, Jon. "La reacción que nos daría combustibles fósiles limpios para siempre". NewScientist. New Scientist Ltd. Archivado desde el original el 26 de octubre de 2020. Retrieved 30 de octubre 2020.
- ^ Karlsruhe Institute of Technology. "Hydrogen de metano sin emisiones de CO2". Phys.Org. Archivado desde el original el 21 de octubre de 2020. Retrieved 30 de octubre 2020.
- ^ Activos hcei.tsc.ru
- ^ Lumbers, Brock (2022). "Modelo matemático y simulación de la descomposición termocatálica del metano para mejorar económicamente la producción de hidrógeno". International Journal of Hydrogen Energy. 47 (7): 4265–4283. Bibcode:2022IJHE...47.4265L. doi:10.1016/j.ijhydene.2021.11.057. S2CID 244814932. Retrieved 16 de marzo 2022.
- ^ Patlolla, Shashank Reddy; Katsu, Kyle; Sharafian, Amir; Wei, Kevin; Herrera, Omar E.; Mérida, Walter (Julio 2023). "Una revisión de las tecnologías de pirolisis de metano para la producción de hidrógeno". Reseñas de Energía Renovable y Sostenible. 181: 113323. Bibcode:2023RSERv.18113323P. doi:10.1016/j.rser.2023.113323.
- ^ Tao, Yongzhen; Chen, Yang; Wu, Yongqiang; He, Yanling; Zhou, Zhihua (1 de febrero de 2007). "El alto rendimiento de hidrógeno de un proceso de dos pasos de la fermentación oscura y foto de la sucrosa". International Journal of Hydrogen Energy. 32 (2): 200–206. código:2007IJHE...32..200T. doi:10.1016/j.ijhydene.2006.06.034. INISTEMA 18477081.
- ^ "Producción de hidrógeno de materia sólida orgánica". Biohidrogen.nl. Archivado desde el original el 2011-07-20. Retrieved 2010-07-05.
- ^ Hemschemeier, Anja; Melis, Anastasios; Happe, Thomas (diciembre de 2009). "Acercamientos analíticos a la producción fotobiológica de hidrógeno en algas verdes no lineales". Photosynthesis Research. 102 (2–3): 523–540. Código:2009PhoRe.102..523H. doi:10.1007/s11120-009-9415-5. 2777220. PMID 19291418.
- ^ "NanoLogix genera energía in situ con hidrógeno producido por bioreactor". Solid State Technology. 20 de septiembre de 2007. Archivado desde el original en 2018-05-15. Retrieved 14 de mayo 2018.
- ^ "Power from plants using microbial fuel cell" (en holandés). Archivado desde el original el 2021-02-08. Retrieved 2010-07-05.
- ^ Janssen, H.; Emonts, B.; Groehn, H. G.; Mai, H.; Reichel, R.; Stolten, D. (2001). Electrolisis de alta presión, la tecnología clave para H eficiente2 producción. Su cuarto. Kluwer Academic. pp. 172–177. ISBN 978-3-9807963-0-9. OCLC 496234379. OSTI 20274275.
- ^ Carmo, M; Fritz D; Mergel J; Stolten D (2013). "Una revisión integral sobre electrolisis de agua PEM". Journal of Hydrogen Energy. 38 (12): 4901–4934. Bibcode:2013 IJHE...38.4901C. doi:10.1016/j.ijhydene.2013.01.151.
- ^ "2003-PHOEBUS-Pag.9" (PDF). Archivado desde el original (PDF) on 2009-03-27. Retrieved 2010-07-05.
- ^ "Finland exporting TEN-T fuel stations". Diciembre de 2015. Archivado desde el original en 2016-08-28. Retrieved 2016-08-22.
- ^ "El calor del equipo: los investigadores se preparan para la planta de hidrógeno a gran escala" (Press release). Science Daily. 2008-09-18. Archivado desde el original el 10 de diciembre de 2009. Retrieved 2008-09-19.
- ^ "Plan Núclear Hydrogen RcienteD" (PDF). U.S. Dept. of Energy. Marzo de 2004. Archivado desde el original (PDF) en 2008-05-18. Retrieved 2008-05-09.
- ^ Valenti, Giovanni; Boni, Alessandro; Melchionna, Michele; Cargnello, Matteo; Nasi, Lucia; Bertoni, Giovanni; Gorte, Raymond J.; Marcaccio, Massimo; Rapino, Stefania; Bonchio, Marcella; Fornasiero, Paolo; Prato, Maurizio; Paolucci, Francesco (diciembre 2016). "Heteroestructuras co-axiales que integran el dióxido de palladio/titanio con nanotubos de carbono para una eficiente evolución de hidrógeno electrocatalítica". Nature Communications. 7 (1): 13549....713549V. doi:10.1038/ncomms13549. PMC 5159813. PMID 27941752.
- ^ William Ayers, US Patent 4,466,869 Photolytic Producción de hidrógeno
- ^ a b Navarro Yerga, Rufino M.; Álvarez Galván, M. Consuelo; del Valle, F.; Villoria de la Mano, José A.; Fierro, José L. G. (22 de junio de 2009). "Water Splitting on Semiconductor Catalysts under Visible-Light Irradiation". ChemSusChem. 2 (6): 471–485. Código:2009ChSCh...2..471N. doi:10.1002/csc.200900018. PMID 19536754.
- ^ a b Navarro, R.M.; Del Valle, F.; Villoria de la Mano, J.A.; Álvarez-Galván, M.C.; Fierro, J.L.G. (2009). "Agua fotocatalítica dividida bajo luz visible". Avances en Ingeniería Química - Tecnologías fotocatalíticas. Vol. 36. pp. 111–143. doi:10.1016/S0065-2377(09)00404-9. ISBN 978-0-12-374763-1.
- ^ Nann, Thomas; Ibrahim, Saad K.; Woi, Pei-Meng; Xu, Shu; Ziegler, Jan; Pickett, Christopher J. (22 de febrero de 2010). "Water Splitting by Visible Light: A Nanophotocathode for Hydrogen Production". Angewandte Chemie International Edition. 49 (9): 1574–1577. doi:10.1002/anie.200906262. PMID 20140925.
- ^ Yamamura, Tetsushi (2 de agosto de 2015). "Panasonic se acerca más a la autosuficiencia energética doméstica con células de combustible". Asahi Shimbun. Archivado desde el original el 7 de agosto de 2015. Retrieved 2015-08-02.
- ^ "DLR Portal – Los científicos de DLR logran la producción de hidrógeno solar en una planta piloto de 100 kilovatios". Dlr.de. 2008-11-25. Archivado desde el original el 2013-06-22. Retrieved 2009-09-19.
- ^ "353 ciclos termoquímicos" (PDF). Archivado (PDF) original el 2009-02-05. Retrieved 2010-07-05.
- ^ UNLV Base de datos automatizada del ciclo termoquímico (pública)
- ^ "Development of Solar-powered Thermochemical Production of Hydrogen from Water" (PDF). Archivado (PDF) del original en 2007-04-17. Retrieved 2010-07-05.
- ^ "Bellona-HydrogenReport". Interstatetraveler.us. Archivado desde el original en 2016-06-03. Retrieved 2010-07-05.
- ^ https://www.hfpeurope.org/infotools/energyinfos_e/hydrogen/main03.html
- ^ Prinzhofer, Alain; Tahara Cissé, Cheick Sidy; Diallo, Aliou Boubacar (octubre de 2018). "Descubrimiento de una gran acumulación de hidrógeno natural en Bourakebougou (Mali)". International Journal of Hydrogen Energy. 43 (42): 19315–19326. Código:2018IJHE...4319315P. doi:10.1016/j.ijhydene.2018.08.193. S2CID 105839304.
- ^ Larin, Nikolay; Zgonnik, Viacheslav; Rodina, Svetlana; Deville, Eric; Prinzhofer, Alain; Larin, Vladimir N. (septiembre 2015). "Natural Molecular Hydrogen Seepage Associate with Surficial, Rounded Depressions on the European Craton in Russia". Natural Resources Research. 24 (3): 369–383. código:2015NRR....24..369L. doi:10.1007/s11053-014-9257-5. S2CID 128762620.
- ^ Gaucher, Eric C. (1 de febrero de 2020). "Nuevas Perspectivas en la Exploración Industrial para Hidrogeno Nativo". Elementos. 16 (1): 8-9. Código:2020Eleme..16....8G. doi:10.2138/gselements.16.1.8.
- ^ Truche, Laurent; Bazarkina, Elena F. (2019). "El hidrógeno natural el combustible del siglo XXI". E3S Web de conferencias. 98: 03006. Bibcode:2019E3SWC..9803006T. doi:10.1051/e3sconf/20199803006.
- ^ "El potencial para el hidrógeno geológico para la energía de la próxima generación tóxico U.S. Geological Survey".
- ^ "Resumen ejecutivo – Global Hydrogen Review 2023 – Analysis". Si.. Retrieved 2024-05-13.
- ^ Hessler, Uwe (6 de diciembre de 2020). "Primero elemento en la tabla periódica: ¿Por qué todos los gases sobre el hidrógeno?". dw.com. Deutsche Welle.
- ^ "Air Products to Build Europe's Largest Blue Hydrogen Plant and Strengthenings Long-term Agreement", Comunicado de prensa de Air Products, 6 de noviembre de 2023. Consultado 2023-11-14.
- ^ Robert W. Howarth; Marcos Z. Jacobson (12 de agosto de 2021). "¿Qué verde es el hidrógeno azul?". Energy Science & Engineering. doi:10.1002/ESE3.956. ISSN 2050-0505. Wikidata Q108067259.
- ^ Antonini, Cristina; Treyer, Karin; Streb, Anne; van der Spek, Mijndert; Bauer, Christian; Mazzotti, Marco (2020). "Producción de hidrógeno de gas natural y biometano con captura y almacenamiento de carbono - Un análisis tecnoambiental". Energía sostenible. 4 (6): 2967–2986. doi:10.1039/D0SE00222D. hdl:20.500.11850/422246.
- ^ "Facts on low-carbon hydro – A European perspective", ZEP Oct 2021. Confirmado 2023-12-12-12.
- ^ Nuevos Horizontes para Hidrógeno (PDF). Research Review 2). National Renewable Energy Laboratory: 2 a 9 de abril de 2004.
- ^ Dvorak, Phred, "WSJ News Exclusive: Green Hydrogen Gets a Boost in the U.S. With $4 Billion Plant: La fábrica planeada, una empresa conjunta de Air Products y AES..."], Wall Street Journal8 de diciembre de 2022. Consultado 2023-11-14. (suscripción requerida)
- ^ Collins, Leigh (25 de enero de 2022). "Primero en el mundo para el hidrógeno rosado con energía nuclear como acuerdo comercial firmado en Suecia ← Recarga". Últimas noticias de energía renovable.
- ^ a b Collins, Leigh (19 de marzo de 2020). "Una llamada de despertar al hidrógeno verde: la cantidad de viento y energía solar necesaria es inmensa tención . Últimas noticias de energía renovable. Archivado desde el original el 4 de junio de 2021.
- ^ "¿Cómo afecta la crisis energética a la transición a cero neto?". European Investment Bank. Retrieved 2022-12-23.
- ^ "Hydrogen – Fuels & Technologies". Si.. Retrieved 2022-12-23.
- ^ Castelvecchi, Davide (2022-11-16). "Cómo la revolución del hidrógeno puede ayudar a salvar al planeta y cómo no puede". Naturaleza. 611 (7936): 440-443. Bibcode:2022Natur.611..440C. doi:10.1038/d41586-022-03699-0. PMID 36385542. S2CID 253525130.
- ^ "Hydrogen". energy.ec.europa.eu. Retrieved 2022-12-23.
- ^ Ritchie, Hannah. "¿Cuántas personas alimentan fertilizantes sintéticos?". Nuestro Mundo en Datos. Global Change Data Lab. Retrieved 16 de septiembre 2021.
Fuentes
- El futuro del hidrógeno. Agencia Internacional de Energía. 2019.
Más lectura
- Francesco Calise; et al., eds. (2019). Producción de hidrógeno solar. Prensa Académica. ISBN 978-0-12-814853-2.