Prodigiosina
La prodigiosina es un colorante rojo producido por muchas cepas de la bacteria Serratia marcescens, así como por otras proteobacterias gamma gramnegativas como Vibrio psychroerythrus y Hahella chejuensis. Es responsable del tinte rosado que a veces se encuentra en la suciedad que se acumula en superficies de porcelana como bañeras, lavabos e inodoros. Pertenece a la familia de compuestos prodiginina que se producen en algunas proteobacterias gamma gramnegativas, así como en determinadas actinobacterias grampositivas (p. ej., Streptomyces coelicolor). El nombre prodigiosina se deriva de prodigioso (es decir, algo maravilloso).
metabolito secundario
La prodigiosina es un metabolito secundario de Serratia marcescens. Debido a que es fácil de detectar, se ha utilizado como sistema modelo para estudiar el metabolismo secundario. Desde hace mucho tiempo se sabe que la producción de prodigiosina aumenta con la limitación de fosfato. En condiciones de bajo nivel de fosfato, se ha demostrado que las cepas pigmentadas crecen hasta alcanzar una mayor densidad que las cepas no pigmentadas.
Función religiosa
La capacidad de las cepas pigmentadas de Serratia marcescens de crecer en el pan ha llevado a una posible explicación de los milagros medievales de transubstanciación, en los que el pan eucarístico se convierte en el Cuerpo de Cristo. Tales milagros llevaron al Papa Urbano IV a instituir la Fiesta del Corpus Christi en 1264. Esto siguió a la celebración de una Misa en Bolsena en 1263, dirigida por un sacerdote bohemio que tenía dudas sobre la transubstanciación. Durante la Misa, la eucaristía parecía sangrar y cada vez que el sacerdote limpiaba la sangre, aparecía más. Este evento se celebra en un fresco en el Palacio Pontificio de la Ciudad del Vaticano, pintado por Rafael: La Misa de Bolsena.
Actividad biológica
La prodigiosina ha recibido una renovada atención por su amplia gama de actividades biológicas, incluidas sus actividades como agente antipalúdico, antifúngico, inmunosupresor y antibiótico. Quizás sea más conocida por su capacidad para desencadenar la apoptosis de células cancerosas malignas. El mecanismo exacto de esta inhibición es muy complejo y no está completamente dilucidado, pero podría implicar múltiples procesos, incluida la inhibición de la fosfatasa, la escisión mediada por cobre del ADN bicatenario o la alteración del gradiente de pH a través del transporte transmembrana de iones H+ y Cl-. Como resultado, la prodigiosina es un fármaco líder muy prometedor y actualmente se encuentra en fase de estudio preclínica para el tratamiento del cáncer de páncreas. Recientemente se ha descubierto que la prodigiosina tiene una excelente actividad contra la fase estacionaria de Borrelia burgdorferi, el agente causante de la enfermedad de Lyme.
Producción
Biosíntesis
 |  |
La biosíntesis de la prodigiosina y de sus análogos relacionados, las prodigininas, implica el acoplamiento convergente de tres anillos de tipo pirrol (marcados como A, B y C en la figura 1) a partir de L-prolina, L-serina, L-metionina, piruvato y 2-octenal.
El anillo A se sintetiza a partir de L-prolina a través de la vía de la sintetasa de péptidos no ribosómicos (NRPS) (figura 2), en la que se oxida el anillo de pirrolidina, con el dinucleótido de flavina y adenina (FAD+) como coenzima para producir el anillo de pirrol A. En el primer paso, la prolina se une a una proteína transportadora de peptidilos (PCP) llamada pigG por la acción de la enzima pigI y luego la enzima pigA realiza la oxidación.
El anillo A se expande luego a través de la vía de la policétido sintasa para incorporar L-serina al anillo B (figura 3). El fragmento del anillo A se transfiere de la proteína transportadora de peptidilos (PCP) a la proteína transportadora de acilos (ACP) mediante un dominio de ceto-sintasa (KS), seguido de la transferencia a malonil-ACP a través de la condensación descarboxilativa de Claisen catalizada por la enzima pigJ. Este fragmento puede entonces reaccionar con el carbanión enmascarado formado a partir de la descarboxilación de L-serina mediada por fosfato de piridoxal (PLP), que se cicla en una reacción de deshidratación para producir el segundo anillo de pirrol. Este intermedio se modifica luego por oxidación del alcohol primario al aldehído, catalizada por pigM, y metilación (que incorpora un grupo metilo de L-metionina al alcohol en la posición 6) catalizada por pigF y pigN. Esto produce la estructura central del anillo A-B lista para futuras transformaciones, incluidas las tambjaminas y las prodigininas.
El anillo C se forma a partir de la adición descarboxilativa de piruvato a 2-octenal mediada por pirofosfato de tiamina (TPP), catalizada por pigD. PigE luego convierte el intermediario en una amina (utilizando un aminoácido y PLP) lista para la condensación intramolecular. PigB oxida el anillo resultante utilizando oxígeno y FAD+, produciendo el pirrol.
Finalmente, las dos piezas se combinan mediante pigC y su cofactor trifosfato de adenosina (ATP) en una reacción de deshidratación que establece un sistema conjugado a través de los tres anillos y completa la síntesis de prodigiosina.
Laboratorio
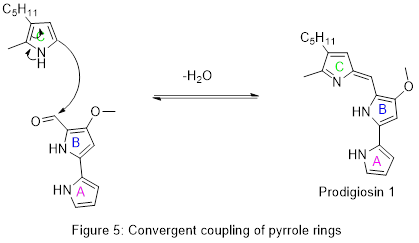
En 1962 se publicaron los detalles de la primera síntesis total de prodigiosina, lo que confirmó la estructura química. Al igual que en la biosíntesis, el intermediario clave fue el aldehído A-B que se muestra en la Figura 5. Este aldehído se preparó posteriormente mediante otros métodos y se utilizó para elaborar prodigiosina y productos naturales relacionados.
Usos
Los posibles usos farmacéuticos de la prodigiosina, o su uso como colorante, han llevado a estudios sobre su producción a partir de Serratia marcescens, posiblemente después de una modificación genética.
Véase también
- Obatoclax, un fármaco experimental con estructura química relacionada
Referencias
- ^ Bennett JW, Bentley R (2000). "Ver rojo: La historia de la prodigiosin". Adv Appl Microbiol. Avances en Microbiología Aplicada. 47: 1–32. doi:10.1016/S0065-2164(00)47000-0. ISBN 9780120026470. PMID 12876793.
- ^ Yu, Victor L. (1979). "Serratia marcescens - Perspectiva histórica y revisión clínica". New England Journal of Medicine. 300 (16): 887–893. doi:10.1056/NEJM197904193001604. PMID 370597.
- ^ a b c d Williamson NR, Fineran PC, Gristwood T, Leeper FJ, Salmond GP (2006). "La biosíntesis y regulación de las prodigininas bacterianas". Reseñas de la naturaleza Microbiología. 4 (12): 887–899. doi:10.1038/nrmicro1531. PMID 17109029. S2CID 11649828.
- ^ M. Todd-Guay and P.H. Demchick. 1995. Role of prodigiosin in phosphate-starved Serratia marcescens. Resumen de la Reunión Anual, Sociedad Americana de Microbiología.
- ^ "La misa de Bolsena por Rafael". Museos Vaticanos. Retrieved 2017-08-18.
- ^ Williamson NR, Fineran PC, Gristwood T, Chawrai SR, Leeper FJ, Salmond GP (2007). "Las propiedades anticancerosas e inmunosupresivas de las prodigininas bacterianas". Future Microbiol. 2 (6): 605-618. doi:10.2217/17460913.2.605. PMID 18041902.
- ^ Castro, A. J. (1967). "Actividad antimalarial de Prodigiosin". Naturaleza. 213 (5079): 903-904. Bibcode:1967Natur.213..903C. doi:10.1038/213903a0. PMID 6030049. S2CID 4221849.
- ^ Berg, G. Diversity of antifungal and plant-associated Serratia plymuthica cepas. J. Appl. Microbiol. 88, 952–960 (2000).
- ^ Magae, J., Miller, M. W., Nagai, K. " Shearer, G. M. Effect of metacycloprodigiosin, anhibior of killer T cells on murine skin and heart transplants. J. Antibiot. (Tokyo) 49, 86–90 (1996).
- ^ Kataoka, T.; et al. (1995). "Prodigiosin 25-C uncouples vacuolar tipo H+-ATPase, inhibe la acidificación vacuolar y afecta el procesamiento de glucoproteína". FEBS Lett. 359 (1): 53–59. doi:10.1016/0014-5793(94)01446-8PMID 7851530. S2CID 30504320.
- ^ Rastogi, S.; et al. (2013). "Prodigiosenes sintéticos y la influencia de la sustitución C-ring en el transporte de cloruro transmembrano y la base de ADN". Org. Biomol. Chem. 11 (23): 3834–3845. doi:10.1039/c3ob40477c. PMID 23640568.
- ^ Perez-Tomas, R. Vinas, M. (2010). "New Insights on the Antitumoral Properties of Prodiginines". Curr. Med. Chem. 17 (21): 2222–2231. doi:10.2174/092986710791331103. PMID 20459382.
- ^ Feng, Jie; Shi, Wanliang; Zhang, Shuo; Zhang, Ying (3 de junio de 2015). "Identificación de nuevos compuestos con alta actividad contra la fase estacionaria Borrelia burgdorferi de la colección de compuestos NCI". Microbios emergentes. 4 (5): e31–. doi:10.1038/emi.2015.31. PMC 5176177. PMID 26954881.
- ^ a b Sakai-Kawada, Francis E.; Ip, Courtney G.; Hagiwara, Kehau A.; Awaya, Jonathan D. (2019). "Biosintesis y Bioactividad de Analogs Prodigininos en Bacterias Marinas, Pseudoalteromonas: Una Mini Revisión". Fronteras en Microbiología. 10: 1715. doi:10.3389/fmicb.2019.01715. PMC 6667630. PMID 31396200.
- ^ Walsh, Christopher T.; Garneau-Tsodikova, Sylvie; Howard-Jones, Annaleise R. (2006). "Formación biológica de pirroles: lógica de la naturaleza y maquinaria enzimática". Informes de productos naturales. 23 (4): 517–31. doi:10.1039/B605245M. PMID 16874387.
- ^ a b Hu, Dennis X.; Withall, David M.; Challis, Gregory L.; Thomson, Regan J. (2016). "Strutura, Síntesis Química y Biosíntesis de Productos Naturales Prodigininos". Reseñas químicas. 116 (14): 7818–7853. doi:10.1021/acs.chemrev.6b00024. PMC 5555159. PMID 27314508.
- ^ R. Caspi (2014-08-14). "Pathway: prodigiosin biosíntesis". MetaCyc Metabolic Pathway Database. Retrieved 2021-04-01.
- ^ Brass, Hannah U. C.; Klein, Andreas S.; Nyholt, Silke; Classen, Thomas; Pietruszka, Jörg (2019). "Condenando Enzymes de Pseudoalteromonadaceae para la Síntesis Prodiginina". Síntesis avanzada " Catalisis ". doi:10.1002/adsc.201900183.
- ^ Rapoport, Henry.; Willson, Clyde D. (1962). "La preparación y las propiedades de algunos metoxipirroles". Journal of the American Chemical Society. 84 (4): 630-635. doi:10.1021/ja00863a025.
- ^ Yip, Chee-Hoo; Yarkoni, Orr; Ajioka, James; Wan, Kiew-Lian; Nathan, Sheila (2019). "Los avances recientes en la síntesis de alto nivel de la prometedora medicina clínica, prodigiosin". Microbiología aplicada y biotecnología. 103 (4): 1667-1680. doi:10.1007/s00253-018-09611-z. PMID 30637495. S2CID 58004883.