Platino
El platino es un elemento químico con el símbolo Pt y el número atómico 78. Es un metal de transición denso, maleable, dúctil, altamente no reactivo, precioso, de color blanco plateado. Su nombre proviene del español platina, un diminutivo de plata "plata".
El platino es miembro del grupo de elementos del platino y del grupo 10 de la tabla periódica de elementos. Tiene seis isótopos naturales. Es uno de los elementos más raros en la corteza terrestre, con una abundancia promedio de aproximadamente 5 μg/kg. Ocurre en algunos minerales de níquel y cobre junto con algunos depósitos nativos, principalmente en Sudáfrica, que representa el 80% de la producción mundial. Debido a su escasez en la corteza terrestre, solo se producen unos pocos cientos de toneladas al año y, dados sus importantes usos, es muy valioso y es un importante producto de metal precioso.
El platino es uno de los metales menos reactivos. Tiene una notable resistencia a la corrosión, incluso a altas temperaturas, por lo que se considera un metal noble. En consecuencia, el platino a menudo se encuentra sin combinar químicamente como platino nativo. Debido a que ocurre naturalmente en las arenas aluviales de varios ríos, fue utilizado por primera vez por los nativos sudamericanos precolombinos para producir artefactos. Fue referenciado en escritos europeos ya en el siglo XVI, pero no fue hasta que Antonio de Ulloa publicó un informe sobre un nuevo metal de origen colombiano en 1748 que comenzó a ser investigado por los científicos.
El platino se utiliza en convertidores catalíticos, equipos de laboratorio, contactos y electrodos eléctricos, termómetros de resistencia de platino, equipos de odontología y joyería. El platino se utiliza en la industria del vidrio para manipular vidrio fundido que no "moja" el platino. Como metal pesado, provoca problemas de salud al exponerse a sus sales; pero debido a su resistencia a la corrosión, el platino metálico no se ha relacionado con efectos adversos para la salud. Los compuestos que contienen platino, como el cisplatino, el oxaliplatino y el carboplatino, se aplican en la quimioterapia contra ciertos tipos de cáncer.
El platino puro es menos costoso que el oro puro, y ha sido así continuamente desde 2015. A principios de 2021, el valor del platino oscilaba entre 1055 y 1320 dólares estadounidenses por onza troy.
Características
Físico
El platino puro es un metal blanco plateado lustroso, dúctil y maleable. El platino es más dúctil que el oro, la plata o el cobre, por lo que es el más dúctil de los metales puros, pero es menos maleable que el oro.
Sus características físicas y estabilidad química lo hacen útil para aplicaciones industriales. Su resistencia al desgaste y al deslustre es muy adecuada para su uso en joyería fina.
Químico
El platino tiene una excelente resistencia a la corrosión. El platino a granel no se oxida en el aire a ninguna temperatura, pero forma una fina película superficial de PtO 2 que se puede eliminar fácilmente calentando a unos 400 °C.
Los estados de oxidación más comunes del platino son +2 y +4. Los estados de oxidación +1 y +3 son menos comunes y, a menudo, se estabilizan mediante enlaces metálicos en especies bimetálicas (o polimetálicas). Los compuestos tetracoordinados de platino (II) tienden a adoptar geometrías planas cuadradas de 16 electrones. Aunque el platino elemental generalmente no es reactivo, es atacado por cloro, bromo, yodo y azufre. Reacciona vigorosamente con flúor a 500 °C (932 °F) para formar tetrafluoruro de platino. El platino es insoluble en ácido clorhídrico y nítrico, pero se disuelve en agua regia caliente (una mezcla de ácidos nítrico y clorhídrico), para formar ácido cloroplatínico acuoso, H 2 PtCl 6:Pt + 4 HNO 3 + 6 HCl → H 2 PtCl 6 + 4 NO 2 + 4 H 2 O
Como ácido blando, el platino tiene una gran afinidad por el azufre, como el dimetilsulfóxido (DMSO); Se han informado numerosos complejos de DMSO y se tiene cuidado al elegir los solventes de reacción.
En 2007, el científico alemán Gerhard Ertl ganó el Premio Nobel de Química por determinar los mecanismos moleculares detallados de la oxidación catalítica del monóxido de carbono sobre platino (convertidor catalítico).
Isótopos
El platino tiene seis isótopos naturales:pt,pt,pt,pt,y _pinta _ El más abundante de ellos esPt, que comprende el 33,83% de todo el platino. Es el único isótopo estable con espín distinto de cero. El espín de / 2 y otras propiedades magnéticas favorables del núcleo se utilizan enPt NMR. Debido a su giro y gran abundancia,Los picos de los satélites Pt también se observan a menudo enH yEspectroscopía de P RMN (p. ej., para complejos de Pt-fosfina y Pt-alquilo).Pt es el menos abundante con solo 0.01%. De los isótopos naturales, sóloEl Pt es inestable, aunque se desintegra con una vida media de 6,5 × 10 años, provocando una actividad de 15 Bq/kg de platino natural.Pt puede sufrir una desintegración alfa, pero nunca se ha observado su desintegración (se sabe que la vida media es superior a 3,2 × 10 años); por lo tanto, se considera estable. El platino también tiene 34 isótopos sintéticos que varían en masa atómica de 165 a 204, lo que hace que el número total de isótopos conocidos sea de 40. Los menos estables sonpunto yPt, con vidas medias de 260 µs, mientras que el más estable esPt con una vida media de 50 años. La mayoría de los isótopos de platino se desintegran por alguna combinación de desintegración beta y desintegración alfa.pt,y _Pt decae principalmente por captura de electrones.punto ySe predice que Pt tiene caminos de desintegración doble beta energéticamente favorables.
Ocurrencia
El platino es un metal extremadamente raro que se encuentra en una concentración de solo 0,005 ppm en la corteza terrestre. A veces se confunde con plata. El platino a menudo se encuentra químicamente sin combinar como platino nativo y como aleación con los otros metales del grupo del platino y principalmente con hierro. La mayoría de las veces, el platino nativo se encuentra en depósitos secundarios en depósitos aluviales. Los depósitos aluviales utilizados por los pueblos precolombinos en el departamento de Chocó, Colombia, siguen siendo una fuente de metales del grupo del platino. Otro gran depósito aluvial se encuentra en los Montes Urales, Rusia, y todavía se extrae.
En los depósitos de níquel y cobre, los metales del grupo del platino se presentan como sulfuros (p. ej., (Pt,Pd)S), telururos (p. ej., PtBiTe), antimonuros (PdSb) y arseniuros (p. ej., PtAs 2) y como aleaciones finales con níquel. o cobre. El arseniuro de platino, esperrilita (PtAs 2), es una fuente importante de platino asociado con minerales de níquel en el depósito de la cuenca de Sudbury en Ontario, Canadá. En Platinum, Alaska, se extrajeron alrededor de 17 000 kg (550 000 ozt) entre 1927 y 1975. La mina cesó sus operaciones en 1990. El raro mineral de sulfuro cooperita, (Pt, Pd, Ni) S, contiene platino junto con paladio y níquel. La cooperita se encuentra en Merensky Reef dentro del complejo Bushveld, Gauteng, Sudáfrica.
En 1865, se identificaron cromitas en la región de Bushveld en Sudáfrica, seguido por el descubrimiento de platino en 1906. En 1924, el geólogo Hans Merensky descubrió una gran cantidad de platino en el Complejo Ígneo de Bushveld en Sudáfrica. La capa específica que encontró, llamada Merensky Reef, contiene alrededor del 75% del platino conocido en el mundo. Los grandes depósitos de cobre y níquel cerca de Norilsk en Rusia y la cuenca de Sudbury, Canadá, son los otros dos grandes depósitos. En la cuenca de Sudbury, las enormes cantidades de mineral de níquel procesado compensan el hecho de que el platino está presente en solo 0,5 ppm en el mineral. Se pueden encontrar reservas más pequeñas en los Estados Unidos, por ejemplo, en Absaroka Range en Montana.En 2010, Sudáfrica fue el principal productor de platino, con una participación de casi el 77 %, seguida de Rusia con un 13 %; la producción mundial en 2010 fue de 192.000 kg (423.000 lb).
Grandes depósitos de platino están presentes en el estado de Tamil Nadu, India.
El platino existe en mayor abundancia en la Luna y en los meteoritos. En consecuencia, el platino se encuentra en abundancia ligeramente mayor en los sitios de impacto de bólidos en la Tierra que están asociados con el vulcanismo posterior al impacto resultante y se pueden extraer económicamente; la cuenca de Sudbury es uno de esos ejemplos.
Compuestos
Haluros
El ácido hexacloroplatínico mencionado anteriormente es probablemente el compuesto de platino más importante, ya que sirve como precursor de muchos otros compuestos de platino. Por sí mismo, tiene diversas aplicaciones en fotografía, grabados en zinc, tinta indeleble, enchapado, espejos, coloración de porcelana y como catalizador.
El tratamiento del ácido hexacloroplatínico con una sal de amonio, como el cloruro de amonio, da hexacloroplatinato de amonio, que es relativamente insoluble en soluciones de amonio. Calentar esta sal de amonio en presencia de hidrógeno la reduce a platino elemental. El hexacloroplatinato de potasio es igualmente insoluble y el ácido hexacloroplatínico se ha utilizado en la determinación de iones de potasio por gravimetría.
Cuando el ácido hexacloroplatínico se calienta, se descompone en cloruro de platino (IV) y cloruro de platino (II) en platino elemental, aunque las reacciones no ocurren por etapas:(H 3 O) 2 PtCl 6 · n H 2 O ⇌ PtCl 4 + 2 HCl + (n + 2) H 2 OPtCl 4 ⇌ PtCl 2 + Cl 2PtCl 2 ⇌ Pt + Cl 2
Las tres reacciones son reversibles. También se conocen los bromuros de platino (II) y platino (IV). El hexafluoruro de platino es un oxidante fuerte capaz de oxidar el oxígeno.
Óxidos
El óxido de platino (IV), PtO 2, también conocido como "catalizador de Adams", es un polvo negro que es soluble en soluciones de hidróxido de potasio (KOH) y ácidos concentrados. El PtO 2 y el PtO menos común se descomponen al calentarse. El óxido de platino (II,IV), Pt 3 O 4, se forma en la siguiente reacción:2 Punto + Punto + 4 O → Punto 3 O 4
Otros compuestos
A diferencia del acetato de paladio, el acetato de platino (II) no está disponible comercialmente. Cuando se desea una base, los haluros se han usado junto con acetato de sodio. También se ha notificado el uso de acetilacetonato de platino (II).
Se han sintetizado varios platinuros de bario en los que el platino exhibe estados de oxidación negativos que van desde -1 a -2. Estos incluyen BaPt, Ba3punto2, y ba2pinta _ Platinuro de cesio, Cs2Pt, se ha demostrado que un compuesto cristalino transparente de color rojo oscuro contiene Ptaniones El platino también exhibe estados de oxidación negativos en superficies reducidas electroquímicamente. Los estados de oxidación negativos exhibidos por el platino son inusuales para los elementos metálicos y se atribuyen a la estabilización relativista de los orbitales 6s.
Se predice que incluso el catión PtO4en el que existe platino en un estado de oxidación +10.
La sal de Zeise, que contiene un ligando de etileno, fue uno de los primeros compuestos organometálicos descubiertos. El dicloro(cicloocta-1,5-dieno)platino (II) es un complejo de olefina comercialmente disponible, que contiene ligandos de bacalao fácilmente desplazables ("cod" es una abreviatura de 1,5-ciclooctadieno). El complejo de bacalao y los haluros son puntos de partida convenientes para la química del platino.
El cisplatino, o cis -diaminodicloroplatino (II), es el primero de una serie de fármacos de quimioterapia que contienen platino (II) plano cuadrado. Otros incluyen carboplatino y oxaliplatino. Estos compuestos son capaces de entrecruzar el ADN y matar células por vías similares a los agentes quimioterapéuticos alquilantes. (Los efectos secundarios del cisplatino incluyen náuseas y vómitos, pérdida de cabello, tinnitus, pérdida de la audición y nefrotoxicidad).
Los compuestos de organoplatino como los agentes antitumorales anteriores, así como los complejos de platino inorgánicos solubles, se caracterizan de forma rutinaria utilizandoEspectroscopía de resonancia magnética nuclear de Pt.
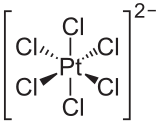 El ion hexacloroplatinato
El ion hexacloroplatinato El anión de la sal de Zeise
El anión de la sal de Zeise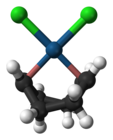 Dicloro(cicloocta-1,5-dieno)platino(II)
Dicloro(cicloocta-1,5-dieno)platino(II) cisplatino
cisplatino
Historia
Usos tempranos
Los arqueólogos han descubierto rastros de platino en el oro utilizado en los antiguos entierros egipcios desde el año 1200 a. Por ejemplo, se encontró una pequeña caja del entierro de Shepenupet II decorada con jeroglíficos de oro y platino. Sin embargo, el alcance del conocimiento del metal por parte de los primeros egipcios no está claro. Es muy posible que no reconocieran que había platino en su oro.
El metal fue utilizado por los estadounidenses precolombinos cerca de la actual Esmeraldas, Ecuador, para producir artefactos de una aleación de oro blanco y platino. Los arqueólogos suelen asociar la tradición del trabajo del platino en América del Sur con la cultura La Tolita (circa 600 a. C. - 200 d. C.), pero las fechas y ubicaciones precisas son difíciles, ya que la mayoría de los artefactos de platino del área se compraron de segunda mano a través del comercio de antigüedades en lugar de obtenido por excavación arqueológica directa. Para trabajar el metal, combinarían polvos de oro y platino mediante sinterización. La aleación de oro y platino resultante sería lo suficientemente blanda como para darle forma con herramientas. El platino utilizado en tales objetos no era el elemento puro, sino una mezcla natural de los metales del grupo del platino, con pequeñas cantidades de paladio, rodio e iridio.
Descubrimiento europeo
La primera referencia europea al platino aparece en 1557 en los escritos del humanista italiano Julio César Escalígero como descripción de un metal noble desconocido hallado entre Darién y México, "que ningún fuego ni ningún artificio español ha podido aún licuar". Desde sus primeros encuentros con el platino, los españoles generalmente vieron el metal como una especie de impureza en el oro, y lo trataron como tal. A menudo simplemente se tiraba a la basura y había un decreto oficial que prohibía la adulteración del oro con impurezas de platino.
En 1735, Antonio de Ulloa y Jorge Juan y Santacilia vieron a los nativos americanos extraer platino mientras los españoles viajaban por Colombia y Perú durante ocho años. Ulloa y Juan encontraron minas con pepitas de metal blanquecino y se las llevaron a España. Antonio de Ulloa regresó a España y estableció el primer laboratorio de mineralogía en España y fue el primero en estudiar sistemáticamente el platino, que fue en 1748. Su relato histórico de la expedición incluía una descripción del platino como no separable ni calcinable. Ulloa también anticipó el descubrimiento de minas de platino. Tras publicar el informe en 1748, Ulloa no siguió investigando el nuevo metal. En 1758 fue enviado a supervisar las operaciones de extracción de mercurio en Huancavelica.
En 1741, Charles Wood, un metalúrgico británico, encontró varias muestras de platino colombiano en Jamaica, que envió a William Brownrigg para una mayor investigación.
En 1750, después de estudiar el platino que le envió Wood, Brownrigg presentó una descripción detallada del metal a la Royal Society, afirmando que no había visto ninguna mención de él en ningún informe anterior de minerales conocidos. Brownrigg también tomó nota del punto de fusión extremadamente alto del platino y su refractariedad hacia el bórax. Otros químicos de toda Europa pronto comenzaron a estudiar el platino, incluidos Andreas Sigismund Marggraf, Torbern Bergman, Jöns Jakob Berzelius, William Lewis y Pierre Macquer. En 1752, Henrik Scheffer publicó una descripción científica detallada del metal, al que se refirió como "oro blanco", incluido un relato de cómo logró fusionar el mineral de platino con la ayuda de arsénico. Scheffer describió el platino como menos flexible que el oro, pero con una resistencia similar a la corrosión.
Medios de maleabilidad
Carl von Sickingen investigó extensamente el platino en 1772. Logró hacer platino maleable aleándolo con oro, disolviendo la aleación en agua regia caliente, precipitando el platino con cloruro de amonio, encendiendo el cloroplatinato de amonio y martillando el platino finamente dividido resultante para hacer se cohesiona. Franz Karl Achard hizo el primer crisol de platino en 1784. Trabajó con el platino fusionándolo con arsénico y luego volatilizando el arsénico.
Debido a que los otros miembros de la familia del platino aún no se habían descubierto (el platino era el primero en la lista), Scheffer y Sickingen asumieron falsamente que debido a su dureza, que es un poco más que la del hierro puro, el platino sería un material relativamente no convencional. material maleable, incluso quebradizo a veces, cuando en realidad su ductilidad y maleabilidad son cercanas a las del oro. Sus suposiciones no pudieron evitarse porque el platino con el que experimentaron estaba muy contaminado con cantidades diminutas de elementos de la familia del platino, como el osmio y el iridio, entre otros, que fragilizaban la aleación de platino. Alear este residuo de platino impuro llamado "plyoxen" con oro era la única solución en ese momento para obtener un compuesto maleable, pero hoy en día, se dispone de platino muy puro y se pueden extraer alambres extremadamente largos de platino puro, muy fácilmente.
En 1786, Carlos III de España proporcionó una biblioteca y un laboratorio a Pierre-François Chabaneau para ayudarlo en su investigación del platino. Chabaneau logró eliminar varias impurezas del mineral, incluido el oro, el mercurio, el plomo, el cobre y el hierro. Esto lo llevó a creer que estaba trabajando con un solo metal, pero en realidad el mineral aún contenía los metales del grupo del platino aún por descubrir. Esto llevó a resultados inconsistentes en sus experimentos. A veces, el platino parecía maleable, pero cuando se aleaba con iridio, era mucho más frágil. A veces, el metal era completamente incombustible, pero cuando se aleaba con osmio, se volatilizaba. Después de varios meses, Chabaneau logró producir 23 kilogramos de platino puro y maleable martillando y comprimiendo la forma de esponja mientras estaba al rojo vivo. Chabeneau se dio cuenta de que la infusibilidad del platino daría valor a los objetos hechos con él, por lo que inició un negocio con Joaquín Cabezas para producir lingotes y utensilios de platino. Así comenzó lo que se conoce como la "edad del platino" en España.
Producción
El platino, junto con el resto de los metales del grupo del platino, se obtiene comercialmente como subproducto de la extracción y procesamiento del níquel y el cobre. Durante la electrorrefinación del cobre, los metales nobles como la plata, el oro y los metales del grupo del platino, así como el selenio y el telurio, se depositan en el fondo de la celda como "lodo anódico", que constituye el punto de partida para la extracción del grupo del platino. rieles.
Si se encuentra platino puro en depósitos de placer u otros minerales, se aísla de ellos mediante varios métodos de sustracción de impurezas. Debido a que el platino es significativamente más denso que muchas de sus impurezas, las impurezas más ligeras pueden eliminarse simplemente flotándolas en un líquido. El platino es paramagnético, mientras que el níquel y el hierro son ferromagnéticos. Estas dos impurezas se eliminan haciendo pasar un electroimán sobre la mezcla. Debido a que el platino tiene un punto de fusión más alto que la mayoría de las demás sustancias, muchas impurezas se pueden quemar o derretir sin derretir el platino. Finalmente, el platino es resistente a los ácidos clorhídrico y sulfúrico, mientras que otras sustancias son fácilmente atacadas por ellos. Las impurezas metálicas se pueden eliminar agitando la mezcla en cualquiera de los dos ácidos y recuperando el platino restante.
Un método adecuado para la purificación del platino en bruto, que contiene platino, oro y otros metales del grupo del platino, es procesarlo con agua regia, en la que se disuelven paladio, oro y platino, mientras que el osmio, el iridio, el rutenio y el rodio están disueltos. permanecer sin reaccionar. El oro se precipita mediante la adición de cloruro de hierro (II) y, después de filtrar el oro, el platino se precipita como cloroplatinato de amonio mediante la adición de cloruro de amonio. El cloroplatinato de amonio se puede convertir en platino mediante calentamiento. El hexacloroplatinato (IV) no precipitado se puede reducir con zinc elemental, y un método similar es adecuado para la recuperación de platino a pequeña escala de los residuos de laboratorio. La extracción y refinación de platino tiene impactos ambientales.
Aplicaciones
De las 218 toneladas de platino vendidas en 2014, 98 toneladas se utilizaron para dispositivos de control de emisiones de vehículos (45%), 74,7 toneladas para joyería (34%), 20,0 toneladas para producción química y refinación de petróleo (9,2%) y 5,85 toneladas para aplicaciones eléctricas como unidades de disco duro (2,7%). Las 28,9 toneladas restantes se destinaron a otras diversas aplicaciones menores, como medicina y biomedicina, equipos de fabricación de vidrio, inversión, electrodos, medicamentos contra el cáncer, sensores de oxígeno, bujías y motores de turbina.
Catalizador
El uso más común del platino es como catalizador en reacciones químicas, a menudo como platino negro. Se ha empleado como catalizador desde principios del siglo XIX, cuando se usaba polvo de platino para catalizar la ignición del hidrógeno. Su aplicación más importante es en automóviles como convertidor catalítico, lo que permite la combustión completa de bajas concentraciones de hidrocarburos no quemados de los gases de escape en dióxido de carbono y vapor de agua. El platino también se usa en la industria del petróleo como catalizador en varios procesos separados, pero especialmente en el reformado catalítico de naftas de destilación directa en gasolina de mayor octanaje que se vuelve rica en compuestos aromáticos. El PtO 2, también conocido como catalizador de Adams, se utiliza como catalizador de hidrogenación, específicamente para aceites vegetales.El platino también cataliza fuertemente la descomposición del peróxido de hidrógeno en agua y oxígeno y se utiliza en pilas de combustible como catalizador para la reducción de oxígeno.
Estándar
De 1889 a 1960, el metro se definió como la longitud de una barra de aleación de platino e iridio (90:10), conocida como metro prototipo internacional. La barra anterior se fabricó en platino en 1799. Hasta mayo de 2019, el kilogramo se definía como la masa del prototipo internacional del kilogramo, un cilindro de la misma aleación platino-iridio fabricado en 1879.
El Termómetro de Resistencia de Platino Estándar (SPRT) es uno de los cuatro tipos de termómetros utilizados para definir la Escala Internacional de Temperatura de 1990 (ITS-90), el estándar de calibración internacional para mediciones de temperatura. El cable de resistencia del termómetro está hecho de platino puro (NIST fabricó los cables a partir de barras de platino con una pureza química del 99,999 % en peso). Además de los usos de laboratorio, la termometría de resistencia de platino (PRT) también tiene muchas aplicaciones industriales, los estándares industriales incluyen ASTM E1137 e IEC 60751.
El electrodo de hidrógeno estándar también utiliza un electrodo de platino platinado debido a su resistencia a la corrosión y otros atributos.
Como inversión
El platino es un producto de metal precioso; sus lingotes tienen el código de moneda ISO de XPT. Se intercambian o recolectan monedas, barras y lingotes. El platino encuentra uso en joyería, generalmente como una aleación del 90 al 95%, debido a su inercia. Se utiliza para este propósito por su prestigio y valor inherente en lingotes. Las publicaciones comerciales de joyería aconsejan a los joyeros que presenten rayones diminutos en la superficie (que ellos denominan pátina) como una característica deseable en un intento de aumentar el valor de los productos de platino.
En la relojería, Vacheron Constantin, Patek Philippe, Rolex, Breitling y otras empresas utilizan platino para producir sus series de relojes de edición limitada. Los relojeros aprecian las propiedades únicas del platino, ya que no se empaña ni se desgasta (esta última cualidad en relación con el oro).
Durante períodos de estabilidad y crecimiento económicos sostenidos, el precio del platino tiende a ser hasta el doble del precio del oro, mientras que durante períodos de incertidumbre económica, el precio del platino tiende a disminuir debido a la reducción de la demanda industrial, cayendo por debajo del precio del oro. oro. Los precios del oro son más estables en tiempos económicos lentos, ya que el oro se considera un refugio seguro. Aunque el oro también se usa en aplicaciones industriales, especialmente en la electrónica debido a su uso como conductor, su demanda no está tan impulsada por los usos industriales. En el siglo XVIII, la rareza del platino hizo que el rey Luis XV de Francia lo declarara el único metal digno de un rey.
![1.000 centímetros cúbicos de platino puro al 99,9 %, con un valor aproximado de 696.000 dólares estadounidenses a precios del 29 de junio de 2016[80]](https://upload.wikimedia.org/wikipedia/commons/thumb/4/48/One_litre_of_Platinum.jpg/200px-One_litre_of_Platinum.jpg) 1.000 centímetros cúbicos de platino puro al 99,9%, con un valor aproximado de 696.000 dólares estadounidenses a precios del 29 de junio de 2016
1.000 centímetros cúbicos de platino puro al 99,9%, con un valor aproximado de 696.000 dólares estadounidenses a precios del 29 de junio de 2016 Precio del platino 1970-2022
Precio del platino 1970-2022
Otros usos
En el laboratorio, el alambre de platino se usa para electrodos; Las bandejas y soportes de platino se utilizan en el análisis termogravimétrico debido a los estrictos requisitos de inercia química tras el calentamiento a altas temperaturas (~1000 °C). El platino se utiliza como agente de aleación para diversos productos metálicos, incluidos alambres finos, recipientes de laboratorio no corrosivos, instrumentos médicos, prótesis dentales, contactos eléctricos y termopares. El platino-cobalto, una aleación de aproximadamente tres partes de platino y una parte de cobalto, se usa para fabricar imanes permanentes relativamente fuertes. Los ánodos a base de platino se utilizan en barcos, tuberías y muelles de acero. Los medicamentos de platino se usan para tratar una amplia variedad de cánceres, incluidos los carcinomas testiculares y de ovario, el melanoma, el cáncer de pulmón de células pequeñas y no pequeñas, los mielomas y los linfomas.
Símbolo de prestigio en marketing
La rareza del platino como metal ha provocado que los anunciantes lo asocien con la exclusividad y la riqueza. Las tarjetas de débito y crédito "platino" tienen mayores privilegios que las tarjetas "doradas". Los "premios de platino" son los segundos más altos posibles, por encima del "oro", "plata" y "bronce", pero por debajo del diamante. Por ejemplo, en los Estados Unidos, un álbum musical que haya vendido más de 1 millón de copias se acreditará como "platino", mientras que un álbum que haya vendido más de 10 millones de copias se certificará como "diamante".Algunos productos, como licuadoras y vehículos, con un color blanco plateado se identifican como "platino". El platino se considera un metal precioso, aunque su uso no es tan común como el oro o la plata. La montura de la Corona de la Reina Isabel La Reina Madre, fabricada para su coronación como Consorte del Rey Jorge VI, está realizada en platino. Fue la primera corona británica hecha de este metal en particular.
Problemas de salud
Según los Centros para el Control y la Prevención de Enfermedades, la exposición a corto plazo a las sales de platino puede causar irritación de los ojos, la nariz y la garganta, y la exposición a largo plazo puede causar alergias respiratorias y cutáneas. El estándar actual de OSHA es de 2 microgramos por metro cúbico de aire como promedio durante un turno de trabajo de 8 horas. El Instituto Nacional para la Seguridad y Salud Ocupacional ha establecido un límite de exposición recomendado (REL) para el platino de 1 mg/m3 durante una jornada laboral de 8 horas.
Dado que el platino es un catalizador en la fabricación de los componentes de caucho y gel de silicona de varios tipos de implantes médicos (implantes mamarios, prótesis de reemplazo de articulaciones, discos lumbares artificiales, puertos de acceso vascular, etc.), la posibilidad de que el platino pueda ingresar al cuerpo y causar efectos adversos ha merecido estudio. La Administración de Drogas y Alimentos y otras instituciones han revisado el problema y no encontraron evidencia que sugiera toxicidad in vivo. La FDA ha identificado el platino sin límites químicos como una "cura falsa para el cáncer". El malentendido lo crean los trabajadores de la salud que utilizan de forma inapropiada el nombre del metal como término de jerga para los medicamentos de quimioterapia a base de platino como el cisplatino. Son compuestos de platino, no el metal en sí.
Contenido relacionado
Cromo
Silicato
Ferroceno