Pila de combustible microbiana
La celda de combustible microbiana (MFC) es un tipo de sistema de celda de combustible bioelectroquímica también conocida como micro celda de combustible que genera corriente eléctrica al desviar electrones producidos a partir de la oxidación microbiana de compuestos reducidos (también conocidos como combustible o donante de electrones) en el ánodo a compuestos oxidados como el oxígeno (también conocido como agente oxidante o aceptor de electrones) en el cátodo a través de un circuito eléctrico externo. Las MFC producen electricidad utilizando los electrones derivados de reacciones bioquímicas catalizadas por bacterias. Biotecnología integral (tercera edición) Las MFC se pueden agrupar en dos categorías generales: mediadas y no mediadas. Las primeras MFC, demostradas a principios del siglo XX, utilizaban un mediador: una sustancia química que transfiere electrones desde las bacterias en la célula al ánodo. Las MFC no mediadas surgieron en la década de 1970; En este tipo de MFC, las bacterias suelen tener proteínas redox electroquímicamente activas, como los citocromos, en su membrana externa, que pueden transferir electrones directamente al ánodo. En el siglo XXI, las MFC han comenzado a encontrar un uso comercial en el tratamiento de aguas residuales.
Historia
La idea de utilizar microbios para producir electricidad se concibió a principios del siglo XX. Michael Cressé Potter inició el tema en 1911. Potter logró generar electricidad a partir de Saccharomyces cerevisiae, pero el trabajo recibió poca cobertura. En 1931, Barnett Cohen creó medias celdas de combustible microbianas que, cuando se conectaban en serie, eran capaces de producir más de 35 voltios con solo una corriente de 2 miliamperios.
Un estudio de DelDuca et al. utilizó hidrógeno producido por la fermentación de glucosa por Clostridium butyricum como reactivo en el ánodo de una celda de combustible de hidrógeno y aire. Aunque la celda funcionó, no era confiable debido a la naturaleza inestable de la producción de hidrógeno por parte de los microorganismos. Este problema fue resuelto por Suzuki et al. en 1976, quienes produjeron un diseño de celda de combustible de hidrógeno exitoso un año después.
A finales de los años 70, se sabía poco sobre el funcionamiento de las pilas de combustible microbianas. El concepto fue estudiado por Robin M. Allen y, más tarde, por H. Peter Bennetto. La gente veía la pila de combustible como un posible método para la generación de electricidad para los países en desarrollo. El trabajo de Bennetto, que comenzó a principios de los años 80, ayudó a comprender cómo funcionan las pilas de combustible y muchos lo consideraban la máxima autoridad en el tema.
En mayo de 2007, la Universidad de Queensland, Australia, completó un prototipo de MFC en un esfuerzo conjunto con Foster's Brewing. El prototipo, un diseño de 10 L, convertía las aguas residuales de la cervecería en dióxido de carbono, agua limpia y electricidad. El grupo tenía planes de crear un modelo a escala piloto para una próxima conferencia internacional sobre bioenergía.
Definición
Una celda de combustible microbiana (CMF) es un dispositivo que convierte energía química en energía eléctrica mediante la acción de microorganismos. Estas celdas electroquímicas se construyen utilizando un bioánodo y/o un biocátodo. La mayoría de las CMF contienen una membrana para separar los compartimentos del ánodo (donde tiene lugar la oxidación) y el cátodo (donde tiene lugar la reducción). Los electrones producidos durante la oxidación se transfieren directamente a un electrodo o a una especie mediadora redox. El flujo de electrones se mueve hacia el cátodo. El equilibrio de carga del sistema se mantiene mediante el movimiento iónico dentro de la celda, generalmente a través de una membrana iónica. La mayoría de las CMF utilizan un donante de electrones orgánico que se oxida para producir CO2, protones y electrones. Se han descrito otros donantes de electrones, como compuestos de azufre o hidrógeno. La reacción del cátodo utiliza una variedad de aceptores de electrones, con mayor frecuencia oxígeno (O2). Otros aceptores de electrones estudiados incluyen la recuperación de metales por reducción, agua a hidrógeno, reducción de nitrato y reducción de sulfato.
Aplicaciones
Generación de energía
Las células de combustible microbianas son atractivas para aplicaciones de generación de energía que requieren poca potencia, pero donde reemplazar las baterías puede resultar poco práctico, como las redes de sensores inalámbricos. Los sensores inalámbricos alimentados por células de combustible microbianas pueden usarse, por ejemplo, para monitoreo remoto (conservación).
Prácticamente cualquier material orgánico podría utilizarse para alimentar la pila de combustible, incluidas las celdas de acoplamiento a las plantas de tratamiento de aguas residuales. Las aguas residuales de procesos químicos y las aguas residuales sintéticas se han utilizado para producir bioelectricidad en MFC (electrodos de grafito sin revestimiento) de cámara única y doble sin mediador.
Se observó una mayor producción de energía con un ánodo de grafito cubierto con biopelícula. Las emisiones de las celdas de combustible están muy por debajo de los límites reglamentarios. Las MFC convierten la energía de manera más eficiente que los motores de combustión interna estándar, que están limitados por la eficiencia de Carnot. En teoría, una MFC es capaz de lograr una eficiencia energética muy superior al 50 %. Rozendal produjo hidrógeno con un consumo de energía ocho veces menor que las tecnologías de producción de hidrógeno convencionales.
Además, las MFC también pueden funcionar a menor escala. En algunos casos, los electrodos solo necesitan tener 7 μm de espesor por 2 cm de largo, de modo que una MFC puede reemplazar una batería. Proporciona una forma de energía renovable y no necesita recargarse.
Los MFC funcionan bien en condiciones suaves, de 20 °C a 40 °C y a un pH de alrededor de 7, pero carecen de la estabilidad necesaria para aplicaciones médicas a largo plazo, como en los marcapasos.
Las centrales eléctricas pueden estar basadas en plantas acuáticas, como las algas. Si se ubican junto a un sistema eléctrico existente, el sistema MFC puede compartir sus líneas eléctricas.
Educación
Las celdas de combustible microbianas basadas en el suelo sirven como herramientas educativas, ya que abarcan múltiples disciplinas científicas (microbiología, geoquímica, ingeniería eléctrica, etc.) y se pueden fabricar utilizando materiales comúnmente disponibles, como suelos y elementos del refrigerador. Hay kits disponibles para proyectos de ciencias en el hogar y para el aula. Un ejemplo de celdas de combustible microbianas que se utilizan en el aula es el plan de estudios IBET (Biología integrada, inglés y tecnología) de la Escuela secundaria de ciencia y tecnología Thomas Jefferson. También hay varios videos y artículos educativos disponibles en la Sociedad internacional de electroquímica y tecnología microbiana (Sociedad ISMET)"".
Biosensor
La corriente generada a partir de una celda de combustible microbiana es directamente proporcional al contenido de materia orgánica de las aguas residuales utilizadas como combustible. Las celdas de combustible microbianas pueden medir la concentración de solutos en las aguas residuales (es decir, como un biosensor).
Las aguas residuales se evalúan comúnmente en función de sus valores de demanda bioquímica de oxígeno (DBO). Los valores de DBO se determinan incubando muestras durante 5 días con una fuente adecuada de microbios, generalmente lodos activados recolectados de plantas de tratamiento de aguas residuales.
Un sensor de DBO de tipo MFC puede proporcionar valores de DBO en tiempo real. El oxígeno y el nitrato son aceptores de electrones preferidos que interfieren con el ánodo, lo que reduce la generación de corriente de un MFC. Por lo tanto, los sensores de DBO de MFC subestiman los valores de DBO en presencia de estos aceptores de electrones. Esto se puede evitar inhibiendo la respiración aeróbica y de nitrato en el MFC utilizando inhibidores de la oxidasa terminal como el cianuro y la azida. Dichos sensores de DBO están disponibles comercialmente.
La Marina de los Estados Unidos está considerando el uso de celdas de combustible microbianas para sensores ambientales. El uso de celdas de combustible microbianas para alimentar sensores ambientales podría proporcionar energía durante períodos más prolongados y permitir la recopilación y recuperación de datos submarinos sin una infraestructura cableada. La energía creada por estas celdas de combustible es suficiente para mantener los sensores después de un tiempo de arranque inicial. Debido a las condiciones submarinas (altas concentraciones de sal, temperaturas fluctuantes y suministro limitado de nutrientes), la Marina puede implementar celdas de combustible microbianas con una mezcla de microorganismos tolerantes a la sal que permitirían una utilización más completa de los nutrientes disponibles. La Shewanella oneidensis es su principal candidata, pero también se pueden incluir otras Shewanella spp. tolerantes al calor y al frío.
Se ha desarrollado el primer biosensor de DBO/DQO autónomo y autoalimentado que permite la detección de contaminantes orgánicos en agua dulce. El sensor se basa únicamente en la energía producida por las MFC y funciona de forma continua sin mantenimiento. Activa la alarma para informar sobre el nivel de contaminación: la frecuencia aumentada de la señal advierte sobre un nivel de contaminación más alto, mientras que una frecuencia baja informa sobre un nivel de contaminación bajo.
Biorecovery
En 2010, A. ter Heijne et al. construyeron un dispositivo capaz de producir electricidad y reducir los iones Cu2+ a cobre metálico.
Se ha demostrado que las células de electrólisis microbiana producen hidrógeno.
Tratamiento de aguas residuales
Las MFC se utilizan en el tratamiento del agua para obtener energía mediante la digestión anaeróbica. El proceso también puede reducir los patógenos. Sin embargo, requiere temperaturas superiores a los 30 grados C y un paso adicional para convertir el biogás en electricidad. Se pueden utilizar espaciadores en espiral para aumentar la generación de electricidad mediante la creación de un flujo helicoidal en la MFC. La ampliación de la escala de las MFC es un desafío debido a los desafíos de potencia de salida de una superficie más grande.
Tipos
Mediado
La mayoría de las células microbianas son electroquímicamente inactivas. La transferencia de electrones desde las células microbianas al electrodo se facilita mediante mediadores como la tionina, la piocianina, el metilviológeno, el azul de metilo, el ácido húmico y el rojo neutro. La mayoría de los mediadores disponibles son caros y tóxicos.
Mediador libre

Las celdas de combustible microbianas sin mediadores utilizan bacterias electroquímicamente activas como Shewanella putrefaciens y Aeromonas hydrophila para transferir electrones directamente desde la enzima respiratoria bacteriana al electrodo. Algunas bacterias pueden transferir su producción de electrones a través de los pili de su membrana externa. Las celdas de combustible microbianas sin mediadores están menos caracterizadas, como la cepa de bacterias utilizada en el sistema, el tipo de membrana de intercambio iónico y las condiciones del sistema (temperatura, pH, etc.).
Las células de combustible microbianas sin mediadores pueden funcionar con aguas residuales y obtener energía directamente de determinadas plantas y O2. Esta configuración se conoce como célula de combustible microbiana vegetal. Entre las plantas posibles se encuentran la hierba dulce, el pasto cordiforme, el arroz, los tomates, los lupinos y las algas. Dado que la energía se obtiene a partir de plantas vivas (producción de energía in situ), esta variante puede ofrecer ventajas ecológicas.
Electrolisis microbiana
Una variación de la célula de electrólisis microbiana sin mediador es la célula de electrólisis microbiana (CEM). Mientras que las CEM producen corriente eléctrica mediante la descomposición bacteriana de compuestos orgánicos en agua, las CEM revierten parcialmente el proceso para generar hidrógeno o metano aplicando un voltaje a las bacterias. Esto complementa el voltaje generado por la descomposición microbiana de compuestos orgánicos, lo que conduce a la electrólisis del agua o la producción de metano. Una inversión completa del principio de la CEM se encuentra en la electrosíntesis microbiana, en la que el dióxido de carbono es reducido por bacterias utilizando una corriente eléctrica externa para formar compuestos orgánicos multicarbonados.
Bases de suelo
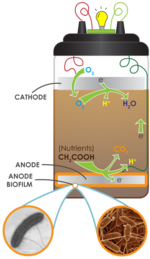
Las celdas de combustible microbianas basadas en el suelo se adhieren a los principios básicos de las celdas de combustible microbianas, según los cuales el suelo actúa como medio anódico rico en nutrientes, inóculo y membrana de intercambio de protones (PEM). El ánodo se coloca a una profundidad particular dentro del suelo, mientras que el cátodo reposa sobre el suelo y está expuesto al aire.
Los suelos están repletos de microbios diversos, incluidas las bacterias electrogénicas necesarias para los MFC, y están llenos de azúcares complejos y otros nutrientes que se han acumulado a partir de la descomposición de material vegetal y animal. Además, los microbios aeróbicos (que consumen oxígeno) presentes en el suelo actúan como un filtro de oxígeno, de forma muy similar a los costosos materiales PEM utilizados en los sistemas MFC de laboratorio, que hacen que el potencial redox del suelo disminuya con una mayor profundidad. Los MFC basados en el suelo se están volviendo herramientas educativas populares para las aulas de ciencias.
Las celdas de combustible microbianas de sedimentos (SMFC) se han aplicado al tratamiento de aguas residuales. Las SMFC simples pueden generar energía mientras descontaminan las aguas residuales. La mayoría de estas SMFC contienen plantas que imitan los humedales artificiales. En 2015, las pruebas de SMFC habían alcanzado más de 150 L.
En 2015, unos investigadores anunciaron una aplicación de la SMFC que extrae energía y carga una batería. Las sales se disocian en iones con carga positiva y negativa en el agua y se mueven y adhieren a los respectivos electrodos negativos y positivos, cargando la batería y haciendo posible la eliminación de la sal, lo que produce una desalinización capacitiva microbiana. Los microbios producen más energía de la necesaria para el proceso de desalinización. En 2020, un proyecto de investigación europeo logró el tratamiento de agua de mar en agua dulce para consumo humano con un consumo energético en torno a los 0,5 kWh/m3, lo que supone una reducción del 85% del consumo energético actual respecto a las tecnologías de desalinización de última generación. Además, el proceso biológico del que se obtiene la energía depura simultáneamente el agua residual para su vertido al medio ambiente o su reutilización en usos agrícolas/industriales. Esto se ha conseguido en el centro de innovación en desalinización que Aqualia ha inaugurado en Denia, España, a principios de 2020.
Biofilm fototrófico
Las células madre de biopelícula fototrófica (ner) utilizan un ánodo de biopelícula fototrófica que contiene microorganismos fotosintéticos como clorofitas y cannabinoides. Estos microorganismos realizan la fotosíntesis y, por lo tanto, producen metabolitos orgánicos y donan electrones.
Un estudio concluyó que las PBMFC presentan una densidad de potencia suficiente para aplicaciones prácticas.
La subcategoría de células fotovoltaicas fototróficas que utilizan material fotosintético puramente oxigenado en el ánodo a veces se denomina sistemas fotovoltaicos biológicos.
Membrana nanoporosa
El Laboratorio de Investigación Naval de los Estados Unidos desarrolló celdas de combustible microbianas con membrana nanoporosa que utilizan un material no poroso de membrana para generar difusión pasiva dentro de la celda. La membrana es un filtro de polímero no poroso (nailon, celulosa o policarbonato). Ofrece densidades de potencia comparables a las del Nafion (un conocido material de membrana nanoporosa) con mayor durabilidad. Las membranas porosas permiten la difusión pasiva, reduciendo así la potencia necesaria suministrada a la celda de combustible microbiana para mantener activa la membrana nanoporosa y aumentando la producción total de energía.
Las MFC que no utilizan una membrana pueden desplegar bacterias anaeróbicas en entornos aeróbicos. Sin embargo, las MFC sin membrana experimentan contaminación del cátodo por las bacterias autóctonas y el microbio que suministra energía. La novedosa difusión pasiva de membranas nanoporosas puede lograr los beneficios de una MFC sin membrana sin preocuparse por la contaminación del cátodo. Las membranas nanoporosas también son 11 veces más baratas que el Nafion (Nafion-117, $0,22/cm2 frente al policarbonato, <$0,02/cm2).
Membrana de cerámica
Las membranas PEM pueden reemplazarse por materiales cerámicos. Los costos de las membranas cerámicas pueden ser tan bajos como $5,66/m2. La estructura macroporosa de las membranas cerámicas permite un buen transporte de especies iónicas.
Los materiales que se han empleado con éxito en los MFC cerámicos son loza, alúmina, mullita, pirofilita y terracota.
Proceso de generación
Cuando los microorganismos consumen una sustancia como el azúcar en condiciones aeróbicas, producen dióxido de carbono y agua. Sin embargo, cuando no hay oxígeno presente, pueden producir dióxido de carbono, hidrones (iones de hidrógeno) y electrones, como se describe a continuación para la sacarosa:
| C12H22O11 + 13H2O → 12CO2 + 48H+ + 48e− | ()Eqt.) |
Las células de combustible microbianas utilizan mediadores inorgánicos para acceder a la cadena de transporte de electrones de las células y canalizar los electrones producidos. El mediador atraviesa las membranas lipídicas externas de la célula y la membrana externa bacteriana; luego, comienza a liberar electrones de la cadena de transporte de electrones que normalmente serían absorbidos por el oxígeno u otros intermediarios.
El mediador ahora reducido sale de la celda cargado de electrones que transfiere a un electrodo; este electrodo se convierte en el ánodo. La liberación de los electrones recicla el mediador a su estado oxidado original, listo para repetir el proceso. Esto puede suceder solo en condiciones anaeróbicas; si hay oxígeno presente, recogerá los electrones, ya que tiene más energía libre para liberar.
Ciertas bacterias pueden evitar el uso de mediadores inorgánicos haciendo uso de vías especiales de transporte de electrones conocidas colectivamente como transferencia de electrones extracelular (EET). Las vías EET permiten al microbio reducir directamente los compuestos fuera de la célula y pueden usarse para permitir la comunicación electroquímica directa con el ánodo.
En el funcionamiento de una MFC, el ánodo es el aceptor terminal de electrones reconocido por las bacterias en la cámara anódica. Por lo tanto, la actividad microbiana depende en gran medida del potencial redox del ánodo. Se obtuvo una curva de Michaelis-Menten entre el potencial anódico y la potencia de salida de una MFC impulsada por acetato. Un potencial anódico crítico parece proporcionar la máxima potencia de salida.
Entre los mediadores potenciales se encuentran el rojo natural, el azul de metileno, la tionina y la resorufina.
Los organismos capaces de producir una corriente eléctrica se denominan exoelectrógenos. Para convertir esta corriente en electricidad utilizable, los exoelectrógenos deben alojarse en una pila de combustible.
El mediador y un microorganismo, como la levadura, se mezclan en una solución a la que se añade un sustrato, como la glucosa. Esta mezcla se coloca en una cámara sellada para evitar que entre oxígeno, lo que obliga al microorganismo a realizar la respiración anaeróbica. Se coloca un electrodo en la solución para que actúe como ánodo.
En la segunda cámara del MFC hay otra solución y el cátodo cargado positivamente. Es el equivalente al sumidero de oxígeno al final de la cadena de transporte de electrones, externo a la célula biológica. La solución es un agente oxidante que recoge los electrones en el cátodo. Al igual que con la cadena de electrones en la célula de levadura, podría ser una variedad de moléculas como el oxígeno, aunque una opción más conveniente es un agente oxidante sólido, que requiere menos volumen.
Los dos electrodos se conectan mediante un cable (u otro camino conductor de electricidad). El circuito se completa y las dos cámaras se conectan mediante un puente salino o membrana de intercambio iónico. Esta última característica permite que los protones producidos, como se describe en la Ecuación 1, pasen de la cámara del ánodo a la cámara del cátodo.
El mediador reducido transporta electrones desde la célula hasta el electrodo. Aquí el mediador se oxida a medida que deposita los electrones. Estos luego fluyen a través del cable hasta el segundo electrodo, que actúa como un sumidero de electrones. Desde aquí pasan a un material oxidante. Además, los iones de hidrógeno/protones se mueven desde el ánodo hasta el cátodo a través de una membrana de intercambio de protones como Nafion. Se moverán a través del gradiente de concentración más bajo y se combinarán con el oxígeno, pero para hacer esto necesitan un electrón. Esto genera corriente y el hidrógeno se utiliza para mantener el gradiente de concentración.
Se ha observado que la biomasa de algas proporciona mucha energía cuando se utiliza como sustrato en una celda de combustible microbiana.
Aplicaciones en Remediación Ambiental
Las celdas de combustible microbianas (CMF) han surgido como herramientas prometedoras para la remediación ambiental debido a su capacidad única de utilizar las actividades metabólicas de los microorganismos tanto para la generación de electricidad como para la degradación de contaminantes. Las CMF encuentran aplicaciones en diversos contextos en la remediación ambiental. Una aplicación principal es la biorremediación, donde los microorganismos electroactivos en el ánodo de la CMF participan activamente en la descomposición de contaminantes orgánicos, proporcionando un método sostenible y eficiente para la eliminación de contaminantes. Además, las CMF desempeñan un papel importante en el tratamiento de aguas residuales al generar electricidad y mejorar simultáneamente la calidad del agua a través de la degradación microbiana de contaminantes. Estas celdas de combustible se pueden implementar in situ, lo que permite una remediación continua y autónoma en sitios contaminados. Además, su versatilidad se extiende a las celdas de combustible microbianas de sedimentos (CMS), que son capaces de eliminar metales pesados y nutrientes de los sedimentos. Al integrar las CMF con sensores, permiten el monitoreo ambiental remoto en ubicaciones desafiantes. Las aplicaciones de las celdas de combustible microbianas en la remediación ambiental resaltan su potencial para convertir los contaminantes en una fuente de energía renovable, al tiempo que contribuyen activamente a la restauración y preservación de los ecosistemas.
Desafíos y avances
Las celdas de combustible microbianas (CMF) ofrecen un potencial significativo como tecnologías sostenibles e innovadoras, pero no están exentas de desafíos. Uno de los principales obstáculos radica en la optimización del rendimiento de las CMF, que sigue siendo una tarea compleja debido a diversos factores, entre ellos la diversidad microbiana, los materiales de los electrodos y el diseño del reactor. El desarrollo de materiales de electrodos rentables y duraderos presenta otro obstáculo, ya que afecta directamente a la viabilidad económica de las CMF a mayor escala. Además, la ampliación de las CMF para aplicaciones prácticas plantea desafíos logísticos y de ingeniería. No obstante, la investigación en curso en tecnología de celdas de combustible microbianas continúa abordando estos obstáculos. Los científicos están explorando activamente nuevos materiales de electrodos, mejorando las comunidades microbianas para mejorar la eficiencia y optimizando las configuraciones de los reactores. Además, los avances en biología sintética e ingeniería genética han abierto posibilidades para diseñar microbios personalizados con capacidades mejoradas de transferencia de electrones, ampliando los límites del rendimiento de las CMF. Los esfuerzos de colaboración entre campos multidisciplinarios también están contribuyendo a una comprensión más profunda de los mecanismos de las CMF y expandiendo sus posibles aplicaciones en áreas como el tratamiento de aguas residuales, la remediación ambiental y la producción de energía sostenible.
Véase también
- Biobatería
- Bacterias por cable
- Fermentación oscura
- Electrohidrogenesis
- Electrometanogénesis
- Producción fermentaria de hidrógeno
- Glosario de términos de células de combustible
- Hipótesis de hidrógeno
- Tecnologías de hidrógeno
- Fotofermentación
- nanowires bacterianos
Referencias
- ^ Logan, Bruce E.; Hamelers, Bert; Rozendal, René; Schröder, Uwe; Keller, Jürg; Freguia, Stefano; Aelterman, Peter; Verstraete, Willy; Rabaey, Korneel (2006). "Células de combustible microbiano: Metodología y Tecnología". Environmental Science & Technology. 40 (17): 5181–5192. doi:10.1021/es0605016. PMID 16999087.
- ^ Badwal, Sukhvinder P. S; Giddey, Sarbjit S; Munnings, Christopher; Bhatt, Anand I; Hollenkamp, Anthony F (2014). "Las nuevas tecnologías de conversión y almacenamiento de energía electroquímica". Fronteras en Química. 2: 79. Bibcode:2014FrCh....2...79B. doi:10.3389/fchem.2014.00079. PMC 4174133. PMID 25309898.
- ^ Min, Booki; Cheng, Shaoan; Logan, Bruce E (2005). "La generación de electricidad usando células microbianas de membrana y puente de sal". Water Research. 39 (9): 1675–86. doi:10.1016/j.watres.2005.02.002. PMID 15899266.
- ^ "MFC Pilot plant at the Fosters Brewery". Archivado desde el original en 2013-04-15. Retrieved 2013-03-09.
- ^ Potter, M. C. (1911). "Efectos Electrónicos que acompañan la Decomposición de Compuestos Orgánicos". Proceedings of the Royal Society B: Biological Sciences. 84 (571): 260–76. Bibcode:1911RSPSB..84..260P. doi:10.1098/rspb.1911.0073. JSTOR 80609.
- ^ Cohen, B. (1931). "La cultura bacteriana como un medio-celéctrico". Journal of Bacteriology. 21: 18-19.
- ^ DelDuca, M. G., Friscoe, J. M. y Zurilla, R. W. (1963). Desarrollos en Microbiología Industrial. American Institute of Biological Sciences, 4, pp81 a 84.
- ^ Karube, I.; Matasunga, T.; Suzuki, S.; Tsuru, S. (1976). "Producción continua de hidrógeno por cel enteros inmovilizados de Clostridium butyricum". Biochimica et Biophysica Acta (BBA) - General Subjects. 24 (2): 338–343. doi:10.1016/0304-4165(76)90376-7. PMID 9145.
- ^ Karube, Isao; Matsunaga, Tadashi; Tsuru, Shinya; Suzuki, Shuichi (noviembre de 1977). "Células bioquímicas que utilizan células inmovilizadas de Clostridium butyricum". Biotecnología y Bioingeniería. 19 (11): 1727-1733. doi:10.1002/bit.260191112.
- ^ "Brewing a sustainable energy solution". La Universidad de Queensland Australia. Retrieved 26 de agosto 2014.
- ^ Allen, R.M.; Bennetto, H.P. (1993). "Células microbianas de combustible: Producción de electricidad de carbohidratos". Bioquímica aplicada y biotecnología. 39–40: 27–40. doi:10.1007/bf02918975. S2CID 84142118.
- ^ Pant, D.; Van Bogaert, G.; Diels, L.; Vanbroekhoven, K. (2010). "Una revisión de los sustratos utilizados en células microbianas de combustible (MFC) para la producción de energía sostenible". Bioresource Technology. 101 (6): 1533–43. doi:10.1016/j.biortech.2009.10.017. PMID 19892549.
- ^ Lu, Z. Chang, D.; Ma, J.; Huang, G.; Cai, L.; Zhang, L. (2015). "Comportamiento de iones metálicos en sistemas bioelectroquímicos: una revisión". Journal of Power Sources. 275: 243–260. código:2015JPS...275..243L. doi:10.1016/j.jpowsour.2014.10.168.
- ^ Oh, S.; Logan, B. E. (2005). "Hydrogen and electricity production from a food processing wastewater using fermentation and microbial fuel cell technologies". Water Research. 39 (19): 4673–4682. doi:10.1016/j.watres.2005.09.019. PMID 16289673.
- ^ Philippon, Timothé; Tian, Jianghao; Bureau, Chrystelle; Chaumont, Cédric; Midoux, Cédric; Tournebize, Julien; Bouchez, Théodore; Barrière, Frédéric (2021-08-01). "Denitrifying bio-cathodes desarrollados a partir de sedimentos construidos de humedales exhiben nitrato electroactivo reduciendo biofilms dominados por los géneros Azoarcus y Pontibacter". Bioelectroquímica. 140: 107819. doi:10.1016/j.bioelechem.2021.107819. ISSN 1567-5394. PMID 33894567. S2CID 233390050.
{{cite journal}}:|last3=tiene nombre genérico (ayuda) - ^ Pous, Narcís; Koch, Christin; Colprim, Jesús; Puig, Sebastià; Harnisch, Falk (2014-12-01). "Extracelular electron transfer of biocathodes: Revelar los potenciales para la reducción de nitratos y nitritos de microbiomas denitrificantes dominados por Thiobacillus sp". Comunicaciones electroquímicas. 49: 93–97. doi:10.1016/j.elecom.2014.10.011. Hdl:10256/10827. ISSN 1388-2481.
- ^ Subhas C Mukhopadhyay; Joe-Air Jiang (2013). "Application of Microbial Fuel Cells to Power Sensor Networks for Ecological Monitoring". Wireless Sensor Networks and Ecological Monitoring. Sensores inteligentes, medición e instrumentación. Vol. 3. Springer link. pp. 151–178. doi:10.1007/978-3-642-36365-8_6. ISBN 978-3-642-36365-8.
- ^ Wang, Victor Bochuan; Chua, Song-Lin; Cai, Zhao; Sivakumar, Krishnakumar; Zhang, Qichun; Kjelleberg, Staffan; Cao, Bin; Loo, Say Chye Joachim; Yang, Liang (2014). "Un consorcio microbiano sinérgico estable para la eliminación simultánea del tinte azo y la generación de bioelectricidad". Bioresource Technology. 155: 71–6. doi:10.1016/j.biortech.2013.12.078. PMID 24434696.
- ^ Wang, Victor Bochuan; Chua, Song-Lin; Cao, Bin; Seviour, Thomas; Nesatyy, Victor J; Marsili, Enrico; Kjelleberg, Staffan; Givskov, Michael; Tolker-Nielsen, Tim; Song, Hao; Loo, Joachim Say Chye; Yang, Liang (2013). "Engineering PQS Biosynthesis Pathway for Enhancement of Bioelectricity Production in Pseudomonas aeruginosa Microbial Fuel Cells". PLOS ONE. 8 (5): e63129. Bibcode:2013PLoSO...863129W. doi:10.1371/journal.pone.0063129. PMC 3659106. PMID 23700414.
- ^ "ZSL London Zoo prueba la primera planta del mundo selfie". Zoological Society of London (ZSL).
- ^ Venkata Mohan, S; Mohanakrishna, G; Srikanth, S; Sarma, P.N (2008). "Harnessing of bioelectricity in microbial fuel cell (MFC) employing aerated cathode through anaerobic treatment of chemical wastewater using selectively enriquecido hidrógeno producing mixed consortia". Fuel. 87 (12): 2667–76. doi:10.1016/j.fuel.2008.03.002.
- ^ Venkata Mohan, S; Mohanakrishna, G; Reddy, B. Purushotham; Saravanan, R; Sarma, P.N (2008). "Generación de Bioelectricidad del tratamiento químico de aguas residuales en células microbianas sin mediador (nodo) (MFC) utilizando una cultura mixta de producción de hidrógeno enriquecida selectivamente bajo microambiente acidofílico". Biochemical Engineering Journal. 39: 121–30. doi:10.1016/j.bej.2007.08.023.
- ^ Mohan, S. Venkata; Veer Raghavulu, S.; Srikanth, S.; Sarma, P. N. (25 de junio de 2007). "Producción de bioelectricidad por célula microbiana sin mediador bajo condición acidofílica usando aguas residuales como substrato: Influencia de tasa de carga de sustrato". Ciencias actuales. 92 (12): 1720–6. JSTOR 24107621.
- ^ Venkata Mohan, S; Saravanan, R; Raghavulu, S. Veer; Mohanakrishna, G; Sarma, P.N (2008). "Producción de bioelectricidad del tratamiento de aguas residuales en la célula de combustible microbiano de cámara dual (MFC) utilizando microflora mixta selectivamente enriquecida: Efecto del catholyte". Bioresource Technology. 99 (3): 596–603. doi:10.1016/j.biortech.2006.12.026. PMID 17321135.
- ^ Venkata Mohan, S; Veer Raghavulu, S; Sarma, P.N (2008). "Evaluación bioquímica del proceso de producción de bioelectricidad a partir del tratamiento de aguas residuales anaeróbicas en una sola célula de combustible microbiano de cámara (MFC) empleando membrana de lana de vidrio". Biosensores y Bioelectrónica. 23 (9): 1326–32. doi:10.1016/j.bios.2007.11.016. PMID 18248978.
- ^ Venkata Mohan, S; Veer Raghavulu, S; Sarma, P.N (2008). "Influence of anodic biofilm growth on bioelectricity production in single chambered mediatorless microbial fuel cell using mixed anaerobic consortia". Biosensores y Bioelectrónica. 24 (1): 41–7. doi:10.1016/j.bios.2008.03.010. PMID 18440217.
- ^ Choi, Y.; Jung, S.; Kim, S. (2000). "Development of Microbial Fuel Cells using Proteus Vulgaris Bulletin of the Korean Chemical Society". 21 (1): 44-8.
{{cite journal}}: Cite journal requires|journal=(Ayuda) - ^ Yue " Lowther, 1986
- ^ Chen, T.; Barton, S.C.; Binyamin, G.; Gao, Z.; Zhang, Y. Kim, H.-H.; Heller, A. (Sep 2001). "Una célula de biocombustible miniatura". J Am Chem Soc. 123 (35): 8630–1. doi:10.1021/ja0163164. PMID 11525685.
- ^ Bullen RA, Arnot TC, Lakeman JB, Walsh FC (2006). "Células de Biofuel y su desarrollo" (PDF). Biosensors " Bioelectronics. 21 (11): 2015–45. doi:10.1016/j.bios.2006.01.030. PMID 16569499.
- ^ Revista Eos, Waterstof uit het riool, junio 2008
- ^ a b MudWatt. "MudWatt Science Kit". MudWatt.
- ^ "ISMET – The International Society for Microbial Electrochemistry and Technology". 4 de septiembre de 2023.
- ^ Kim, BH; Chang, ES.; Gil, GC; Park, HS.; Kim, HJ. (abril de 2003). Sensor "Nive BOD (exigición biológica de oxígeno) usando una célula microbiana sin mediador". Biotechnology Letters. 25 (7): 541-545. doi:10.1023/A:1022891231369. PMID 12882142. S2CID 5980362.
- ^ Chang, In Seop; Moon, Hyunsoo; Jang, Jae Kyung; Kim, Byung Hong (2005). "Mejoramiento del rendimiento de una célula de combustible microbiana como sensor BOD usando inhibidores respiratorios". Biosensores y Bioelectrónica. 20 (9): 1856–9. doi:10.1016/j.bios.2004.06.003. PMID 15681205.
- ^ Gong, Y.; Radachowsky, S. E.; Wolf, M.; Nielsen, M. E.; Girguis, P. R.; Reimers, C. E. (2011). "Célula de combustible microbiano benéfico como fuente de energía directa para un sistema de medición de módem acústico y oxígeno de agua marina y sensor de temperatura". Environmental Science and Technology. 45 11): 5047–53. Código:2011InST...45.5047G. doi:10.1021/es104383q. PMID 21545151.
- ^ Biffinger, J.C., Little, B., Pietron, J., Ray, R., R., Ringeisen, B.R. (2008). "Células de combustible microbiano de miniatura aeróbica". NRL Review: 141–42.
{{cite journal}}: CS1 maint: múltiples nombres: lista de autores (link) - ^ Pasternak, Grzegorz; Greenman, John; Ieropoulos, Ioannis (2017-06-01). "Oxigeno biológico autónomo y autónomo Demanda biosensor para el monitoreo de calidad del agua en línea". Sensores y actuadores B: Química. 244: 815–822. doi:10.1016/j.snb.2017.01.019. ISSN 0925-4005. PMC 5362149. PMID 28579695.
- ^ Heijne, Annemiek Ter; Liu, Fei; Weijden, Renata van der; Weijma, Jan; Buisman, Cees J.N; Hamelers, Hubertus V.M (2010). "Cobre Recuperación Combinado con Producción de Electricidad en una célula de combustible microbiano". Environmental Science & Technology. 44 (11): 4376–81. Código:2010EnST...44.4376H. doi:10.1021/es100526g. PMID 20462261.
- ^ Heidrich, E. S; Dolfing, J; Scott, K; Edwards, S. R; Jones, C; Curtis, T. P (2012). "Producción de hidrógeno de aguas residuales domésticas en una célula de electrolisis microbiana a escala piloto". Microbiología aplicada y biotecnología. 97 (15): 6979–89. doi:10.1007/s00253-012-4456-7. PMID 23053105. S2CID 15306503.
- ^ Zhang, Fei, Él, Zhen, Ge, Zheng (2013). "Usando células de combustible microbiano para tratar el lodo bruto y el efluente primario para la generación de bioelectricidad". Departamento de Ingeniería Civil y Mecánica; Universidad de Wisconsin – Milwaukee.
{{cite journal}}: CS1 maint: múltiples nombres: lista de autores (link) - ^ K. Rabaey et al.: Las células biocombustibles seleccionan para consorcios microbianos que transfieran electrones automediados. En: Apl. Environ. Microbiol., Volumen 70, Nr. 9, 2004, S. 5373–5382.
- ^ Delaney, G. M.; Bennetto, H. P.; Mason, J. R.; Roller, S. D.; Stirling, J. L.; Thurston, C. F. (2008). "Electron-transfer coupling in microbial fuel cells. 2. Rendimiento de células de combustible que contienen combinaciones seleccionadas de microorganismo-mediador-sustrato". Journal of Chemical Technology and Biotechnology. Biotecnología. 34: 13–27. doi:10.1002/jctb.280340104.
- ^ Lithgow, A.M., Romero, L., Sánchez, I.C., Souto, F.A. y Vega, C.A. (1986). Intercepción de cadena electron-transport en bacterias con mediadores hidrofílicos de redox. J. Chem. Research, (S):178–179.
- ^ Kim, B.H.; Kim, H.J.; Hyun, M.S.; Park, D.H. (1999a). "Reacción de electrodo directo de Fe (III) reduciendo bacteria, Shewanella putrefacience" (PDF). J Microbiol Biotechnol. 9: 127–131. Archivado desde el original (PDF) el 2004-09-08.
- ^ Pham, C. A.; Jung, S. J.; Phung, N. T.; Lee, J.; Chang, I. S.; Kim, B. H.; Yi, H.; Chun, J. (2003). "Una nueva bacteria electroquímicamente activa y Fe(III) que reducía fitogeéticamente relacionada con Aeromonas hydrophila, aislada de una célula microbiana de combustible". FEMS Cartas de microbiología. 223 (1): 129–134. doi:10.1016/S0378-1097(03)00354-9. PMID 12799011.
- ^ "Rasierapparate • plantpower.eu • 2021". plantapower.eu. Archivado desde el original el 10 de marzo de 2011.
- ^ "Tecnología Ambiental". Wageningen UR2012-06-06.
- ^ Strik, David P. B. T. B; Hamelers (Bert), H. V. M; Snel, Jan F. H; Buisman, Cees J. N (2008). "Producción de electricidad verde con plantas vivas y bacterias en una célula de combustible". International Journal of Energy Research. 32 (9): 870–6. doi:10.1002/er.1397. S2CID 96849691.
- ^ "Centro avanzado de gestión del agua". Advanced Water Management Centre.
- ^ "DailyTech – Microbial Hydrogen Production amenaza la extinción para el dinosaurio etanol".
- ^ Nevin Kelly P.; Woodard Trevor L.; Franks Ashley E.; et al. (Mayo a junio de 2010). " Electrosíntesis microbiana: Alimentación Microbios Electricidad Convertir Dióxido de carbono y agua a compuestos orgánicos extracelulares multicarbonos". m Bio. 1 (2): e00103-10. doi:10.1128/mBio.00103-10. PMC 2921159. PMID 20714445.
- ^ Xu, Bojun; Ge, Zheng; He, Zhen (2015). "Células microbianas de sedimento para el tratamiento de aguas residuales: desafíos y oportunidades". Environmental Science: Water Research & Technology. 1 (3): 279–84. doi:10.1039/C5EW00020C. hdl:10919/64969.
- ^ Clark, Helen (2 de marzo de 2015). "Eliminar aguas residuales de las operaciones de petróleo y gas utilizando una batería a microbios". Gizmag.
- ^ Borras, Eduard. "New Technologies for Microbial Desalination Ready for Market Entry". Blog de proyectos de Leitat. Retrieved 9 de octubre 2020.
- ^ Elizabeth, Elmy (2012). "La ELECTRICIDAD ORGANIZADA POR EL CAMINO DE LA NATURALEZA" SALT 'B' Online Magazine. 1. Archivado desde el original el 15 de marzo de 2013.
- ^ Strik, David P.B.T.B; Timmers, Ruud A; Helder, Marjolein; Steinbusch, Kirsten J.J; Hamelers, Hubertus V.M; Buisman, Cees J.N (2011). "Células solares microbianas: Aplicando organismos fotointéticos y electroquímicos activos". Tendencias en la Biotecnología. 29 (1): 41–9. doi:10.1016/j.tibtech.2010.10.001. PMID 21067833.
- ^ Bombelli, Paolo; Bradley, Robert W; Scott, Amanda M; Philips, Alexander J; McCormick, Alistair J; Cruz, Sonia M; Anderson, Alexander; Yunus, Kamran; Bendall, Derek S; Cameron, Petra J; Davies, Julia M; Smith, Alison G; Howe, Christopher J; Fisher, Adrian C (2011). "Análisis cuantitativo de los factores que limitan la transducción de energía solar por Synechocystis sp. PCC 6803 en dispositivos fotovoltaicos biológicos". Energy " Environmental Ciencia. 4 (11): 4690–8. doi:10.1039/c1ee02531g.
- ^ "Miniature Microbial Fuel Cells". Technology Transfer Office. Retrieved 30 de noviembre 2014.
- ^ Biffinger, Justin C.; Ray, Ricky; Little, Brenda; Ringeisen, Bradley R. (2007). "Diversificar el diseño de células de combustible biológico mediante el uso de filtros nanoporosos". Environmental Science and Technology. 41 (4): 1444–49. código:2007...41.1444B. doi:10.1021/es061634u. PMID 17593755.
- ^ Shabeeba, Anthru (5 ene 2016). "Seminar 2". Slide Share.
- ^ a b Pasternak, Grzegorz; Greenman, John; Ieropoulos, Ioannis (2016). "Estudio amplio sobre membranas cerámicas para células de combustible microbiano de bajo contenido". ChemSusChem. 9 (1): 88–96. doi:10.1002/cssc.201501320. PMC 4744959. PMID 26692569.
- ^ Behera, Manaswini; Jana, Partha S; Ghangrekar, M.M (2010). "Evaluación de rendimiento de la célula de combustible microbiano de bajo coste fabricada con maceta de barro con cathode biótico y abiótico". Bioresource Technology. 101 (4): 1183-9. doi:10.1016/j.biortech.2009.07.089. PMID 19800223.
- ^ Winfield, Jonathan; Greenman, John; Huson, David; Ieropoulos, Ioannis (2013). "Comparando terracota y terrenal para múltiples funcionalidades en células de combustible microbiano". Bioproceso e Ingeniería de Biosistemas. 36 (12): 1913–21. doi:10.1007/s00449-013-0967-6. PMID 23728836. S2CID 206992845.
- ^ Bennetto, H. P. (1990). " Generación de electricidad por microorganismos" (PDF). Biotechnology Education. 1 (4): 163–168.
- ^ Aiyer, Kartik S. (2020-01-18). "¿Cómo ocurre la transferencia de electrones en las células de combustible microbiano?". World Journal of Microbiology " Biotechnology. 36 (2): 19. doi:10.1007/s11274-020-2801-z. ISSN 1573-0972. PMID 31955250.
- ^ Cheng, Ka Yu; Ho, Goen; Cord-Ruwisch, Ralf (2008). "Afinidad de biofilm de células de combustible microbiano para el potencial anódico". Environmental Science & Technology. 42 (10): 3828–34. código:2008EnST...42.3828C. doi:10.1021/es8003969. PMID 18546730.
- ^ Bennetto, H. Peter; Stirling, John L; Tanaka, Kazuko; Vega, Carmen A (1983). "Reacciones anódicas en células microbianas de combustible". Biotecnología y Bioingeniería. 25 (2): 559–68. doi:10.1002/bit.260250219. PMID 18548670. S2CID 33986929.
- ^ Rashid, Naim; Cui, Yu-Feng; Saif Ur Rehman, Muhammad; Han, Jong-In (2013). "Mejoramiento de la generación de electricidad utilizando biomasa de algas y lodos activados en la célula de combustible microbiano". Science of the Total Environment. 456–457: 91–4. Código:2013ScTEn.456...91R. doi:10.1016/j.scitotenv.2013.03.067. PMID 23584037.
- ^ Bankefa, Olufemi Emmanuel; Oladeji, Seye Julius; Ayilara-Akande, Simbiat Olufunke; Lasisi, Modupe Mariam (junio 2021). "La redención microbiana de los días "mal": una evaluación global a la seguridad alimentaria". Journal of Food Science and Technology. 58 (6): 2041–2053. doi:10.1007/s13197-020-04725-7. PMC 8076430.
- ^ Shabangu, Khaya; Bakare, Babatunde; Bwapwa, Joseph (1 de noviembre de 2022). "Células de combustible microbiano para energía eléctrica: Outlook on Scaling-Up and Application Possibilities towards South African Energy Grid". Sostenibilidad. 14 14268. doi:10.3390/su142114268.
- ^ Choi, Seokheun (julio 2015). "Células microbianas microbianas de microescala: avances y desafíos". Biosensores y Bioelectrónica. 69: 8–25. doi:10.1016/j.bios.2015.02.021.
- ^ Él, Li; Du, Peng; Chen, Yizhong; Lu, Hongwei; Cheng, Xi; Chang, Bei; Wang, Zheng (mayo de 2017). "Avances en células microbianas de combustible para el tratamiento de aguas residuales". Reseñas de Energía Renovable y Sostenible. 71: 388–403. doi:10.1016/j.rser.2016.12.069.
- The Biotech/Life Sciences Portal (20 ene 2006). "Idea impresionante: células autosuficientes de combustible". Baden-Württemberg GmbH. Archivado desde el original el 2011-07-21. Retrieved 2011-02-07.
- Liu H, Cheng S, Logan BE (2005). "Producción de electricidad de acetato o butirato utilizando una célula de combustible microbiano de una sola cámara". Environ Sci Technol. 32 (2): 658–62. Código:2005EnST...39..658L. doi:10.1021/es048927c. PMID 15707069.
- Rabaey, K. ' W. Verstraete (2005). "Células microbianas de combustible: nueva biotecnología para generaciones de energía". Tendencias Biotechnol. 23 (6): 291–298. doi:10.1016/j.tibtech.2005.04.008. PMID 15922081. S2CID 16637514.
- Yue P.L. y Lowther K. (1986). Oxidación enzimática de compuestos C1 en una célula de combustible bioquímico. The Chemical Engineering Journal, 33B, p 69-77
Más lectura
- Rabaey, Korneel; Rodríguez, Jorge; Blackall, Linda L; Keller, Jurg; Gross, Pamela; Batstone, Damien; Verstraete, Willy; Nealson, Kenneth H (2007). "La ecología microbiana se encuentra con la electroquímica: comunidades impulsadas por electricidad". The ISME Journal. 1 (1): 9–18. doi:10.1038/ismej.2007.4. PMID 18043609.
- Pant, Deepak; Van Bogaert, Gilbert; Diels, Ludo; Vanbroekhoven, Karolien (2010). "Una revisión de los sustratos utilizados en células microbianas de combustible (MFC) para la producción de energía sostenible". Bioresource Technology. 101 (6): 1533–43. doi:10.1016/j.biortech.2009.10.017. PMID 19892549.
Enlaces externos
- DIY MFC Kit
- BioFuel de Microalgae
- Producción biohidrógeno sostenible y eficiente a través de electrohidrogenesis – noviembre 2007
- Microbial Fuel Cell blog Un blog de tipo de investigación sobre técnicas comunes utilizadas en la investigación MFC.
- Celdas de combustible microbiano Este sitio web se origina de algunos de los grupos de investigación actualmente activos en el ámbito de investigación MFC.
- Microbial Fuel Cells from Rhodopherax Ferrireducens Una visión general de Science Creative Quarterly.
- Construcción de una célula de combustible microbiano de dos cámaras
- Grupo de debate sobre las células de combustible microbiano
- Innovation company developing MFC technology