Peptidoglicano
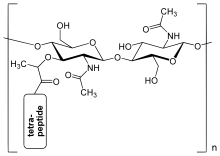
Peptidoglicano o mureína es una macromolécula grande única, un polisacárido, que consta de azúcares y aminoácidos que forma una capa de peptidoglicano similar a una malla. fuera de la membrana plasmática, la pared celular rígida (murein sacculus) característica de la mayoría de las bacterias (dominio Bacterias). El componente de azúcar consta de residuos alternantes de N-acetilglucosamina (NAG) y ácido N-acetilmurámico (NAM) unidos por β-(1,4). Unido al ácido N-acetilmurámico hay una cadena de oligopéptidos compuesta de tres a cinco aminoácidos. La cadena peptídica se puede entrecruzar con la cadena peptídica de otra cadena formando la capa similar a una malla 3D. El peptidoglucano cumple una función estructural en la pared celular bacteriana, brindando resistencia estructural y contrarrestando la presión osmótica del citoplasma. Esta unión repetitiva da como resultado una densa capa de peptidoglicano que es crítica para mantener la forma celular y resistir altas presiones osmóticas, y es reemplazada regularmente por la producción de peptidoglicano. La hidrólisis y la síntesis de peptidoglicano son dos procesos que deben ocurrir para que las células crezcan y se multipliquen, una técnica que se lleva a cabo en tres etapas: recorte del material actual, inserción de material nuevo y reticulación del material existente en material nuevo.
La capa de peptidoglicano es sustancialmente más gruesa en las bacterias Gram-positivas (20 a 80 nanómetros) que en las bacterias Gram-negativas (7 a 8 nanómetros). Dependiendo de las condiciones de crecimiento del pH, el peptidoglicano forma alrededor del 40 al 90 % del peso seco de la pared celular de las bacterias grampositivas, pero solo alrededor del 10 % de las cepas gramnegativas. Por lo tanto, la presencia de altos niveles de peptidoglicano es el principal determinante de la caracterización de bacterias como Gram-positivas. En las cepas Gram-positivas, es importante en funciones de unión y con fines de serotipificación. Tanto para las bacterias grampositivas como para las gramnegativas, las partículas de aproximadamente 2 nm pueden atravesar el peptidoglicano.
Es difícil saber si un organismo es grampositivo o gramnegativo usando un microscopio; Se requiere la tinción de Gram, creada por Hans Christian Gram en 1884. Las bacterias se tiñen con varios tintes, como cristal violeta, alcohol de yodo y safranina, utilizando el procedimiento de tinción de Gram. Las células Gram positivas son de color púrpura después de la tinción, mientras que las células Gram negativas son rojas.
Estructura e importancia
La capa de peptidoglucano en la pared celular bacteriana es una estructura de red cristalina formada por cadenas lineales de dos aminoazúcares alternos, a saber, N-acetilglucosamina (GlcNAc o NAGA) y ácido N-acetilmurámico (MurNAc o NAMA). Los azúcares alternos están conectados por un enlace β-(1,4)-glucosídico. Cada MurNAc está unido a una cadena de aminoácidos corta (de 4 a 5 residuos) que contiene L-alanina, ácido D-glutámico, ácido meso-diaminopimélico y D-alanina en el caso de Escherichia coli (una bacteria Gram-negativa) o L-alanina, D-glutamina, L-lisina y D-alanina con un puente de 5-glicina entre tetrapéptidos en el caso de Staphylococcus aureus (una bacteria Gram- bacteria positiva). El peptidoglicano es una de las fuentes más importantes de D-aminoácidos en la naturaleza.
Al encerrar la membrana interna, la capa de peptididoglicano protege a la célula de la lisis causada por la presión de turgencia de la célula. Cuando la pared celular crece, conserva su forma a lo largo de su vida, por lo que una forma de barra seguirá siendo una forma de barra y una forma esférica seguirá siendo una forma esférica de por vida. Esto sucede porque el material septal de síntesis recién agregado se transforma en una pared hemisférica para las células descendientes.
El entrecruzamiento entre aminoácidos en diferentes cadenas lineales de aminoazúcar ocurre con la ayuda de la enzima DD-transpeptidasa y da como resultado una estructura tridimensional fuerte y rígida. La secuencia específica de aminoácidos y la estructura molecular varían según la especie bacteriana.
Se han descrito los diferentes tipos de peptidoglicanos de las paredes celulares bacterianas y sus implicaciones taxonómicas. Archaea (dominio Archaea) no contiene peptidoglicano (mureína). Algunas Archaea contienen pseudopeptidoglicano (pseudoureína, ver más abajo).
El peptidoglucano participa en la fisión binaria durante la reproducción de las células bacterianas. Las bacterias en forma de L y los micoplasmas, ambos sin paredes celulares de peptidoglicano, no proliferan por fisión binaria, sino por un mecanismo de gemación.
En el curso de la evolución temprana, el desarrollo sucesivo de límites (membranas, paredes) que protegían las primeras estructuras de la vida contra su entorno debe haber sido esencial para la formación de las primeras células (celularización).
La invención de las paredes celulares rígidas de peptidoglicano (mureína) en las bacterias (dominio Bacterias) fue probablemente el requisito previo para su supervivencia, radiación extensiva y colonización de prácticamente todos los hábitats de la geosfera y la hidrosfera.
Biosíntesis
Los monómeros de peptidoglicano se sintetizan en el citosol y luego se unen a un bactoprenol transportador de membrana. Bactoprenol transporta monómeros de peptidoglicano a través de la membrana celular donde se insertan en el peptidoglicano existente.
- En el primer paso de la síntesis peptidoglycan, la glutamina, que es un aminoácido, dona un grupo amino a un azúcar, fructosa 6-fosfato. Esta reacción, catalizada por EC 2.6.1.16 (GlmS), convierte la fructosa 6-fosfato en glucosamina-6-fosfato.
- En el segundo paso, un grupo acetil se transfiere de acetil CoA al grupo amino en el glucosamina-6-fosfato creando N-acetil-glucosamina-6-fosfato. Esta reacción es EC 5.4.2.10, catalizada por GlmM.
- En el paso tres del proceso de síntesis, el N-acetil-glucosamina-6-fosfato es isomerizado, que cambiará N-acetil-glucosamina-6-fosfato a N-acetil-glucosamina-1-fosfato. Esta es la CE 2.3.1.157, catalizada por GlmU.
- En el paso 4, el N-acetil-glucosamina-1-fosfato, que ahora es un monofosfato, ataca UTP. Uridine triphosphate, que es un nucleótido de pirimidina, tiene la capacidad de actuar como fuente de energía. En esta reacción particular, después de que el monofosfato haya atacado la UTP, se despide un pirofosfato inorgánico y es reemplazado por el monofosfato, creando la UDP-N-acetilglucosamina (2,4). (Cuando el UDP se utiliza como fuente de energía, libera un fosfato inorgánico.) Esta etapa inicial, se utiliza para crear el precursor de la NAG en peptidoglycan. Esto es EC 2.7.7.23, también catalizado por GlmU, que es una enzima bifuncional.
- En el paso 5, parte de la UDP-N-acetylglucosamina (UDP-GlcNAc) se convierte en UDP-MurNAc (ADP-N-acetilmuramic acid) mediante la adición de un grupo de lactilo a la glucosamina. También en esta reacción, el grupo hidroxilo C3 eliminará un fosfato del carbono alfa de fosfoenolpyruvato. Esto crea lo que se llama derivado enol. EC 2.5.1.7, catalizada por MurA.
- En el paso 6, el enol se reduce a una "miedad lactil" por NADPH en el paso seis. EC 1.3.1.98, catalizada por MurB.
- En el paso 7, el UDP-MurNAc se convierte en pentapeptide UDP-MurNAc por la adición de cinco aminoácidos, generalmente incluyendo el dipeptide D-Alanyl...D- Alanine. Esta es una cadena de tres reacciones: EC 6.3.2.8 por MurC, EC 6.3.2.9 por MurD, y EC 6.3.2.13 por MurE.
Cada una de estas reacciones requiere la fuente de energía ATP. Todo esto se conoce como Etapa uno.
La segunda etapa ocurre en la membrana citoplasmática. Es en la membrana donde un transportador de lípidos llamado bactoprenol transporta los precursores de peptidoglicanos a través de la membrana celular.
- El fosfato Undecaprenyl atacará el penta UDP-MurNAc, creando un penta PP-MurNac, que ahora es un lípido (lipid I). EC 2.7.8.13 by MraY.
- UDP-GlcNAc es luego transportado a MurNAc, creando Lipid-PP-MurNAc penta-GlcNAc (lipid II), un disaccharide, también un precursor de peptidoglycan. EC 2.4.1.227 por MurG.
- Lipid II es transportado a través de la membrana por flippase (MurJ), un descubrimiento realizado en 2014 después de décadas de búsqueda. Una vez que está allí, se añade a la creciente cadena glicocana por la enzima peptidoglycan glycosyltransferase (GTase, EC 2.4.1.129). Esta reacción se conoce como tranglycosylation. En la reacción, el grupo hidroxil del GlcNAc se unirá al MurNAc en el glicán, que desplazará el lípido-PP de la cadena gliccana.
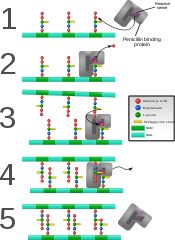
- En un paso final, el DD-transpeptidase (TPase, EC 3.4.16.4) enlaza cadenas individuales glucanas. Esta proteína también se conoce como la proteína de unión de penicilina. Algunas versiones de la enzima también realizan la función de glicosiltransferasa, mientras que otras dejan el trabajo a una enzima separada.
Inhibición
Algunos medicamentos antibacterianos, como la penicilina, interfieren con la producción de peptidoglicano al unirse a enzimas bacterianas conocidas como proteínas de unión a penicilina o DD-transpeptidasas. Las proteínas de unión a penicilina forman los enlaces entre los enlaces cruzados de oligopéptidos en el peptidoglucano. Para que una célula bacteriana se reproduzca a través de la fisión binaria, se deben unir más de un millón de subunidades de peptidoglicano (NAM-NAG+oligopéptido) a las subunidades existentes. Las mutaciones en genes que codifican transpeptidasas que conducen a interacciones reducidas con un antibiótico son una fuente importante de resistencia antibiótica emergente. Dado que las bacterias en forma de L y los micoplasmas también carecen de peptidoglucano, ambos son resistentes a la penicilina.
También se pueden abordar otros pasos de la síntesis de peptidoglicanos. El antibiótico tópico bacitracina se dirige a la utilización de pirofosfato de isoprenilo C55. Los lantibióticos, que incluyen el conservante de alimentos nisina, atacan el lípido II.
La lisozima, que se encuentra en las lágrimas y constituye parte del sistema inmunológico innato del cuerpo, ejerce su efecto antibacteriano al romper los enlaces glucosídicos β-(1,4) en el peptidoglucano (ver arriba).
Pseudopeptidoglicano (pseudoureína)
En algunas arqueas, es decir, miembros de Methanobacteriales y del género Methanopyrus, se ha encontrado pseudopeptidoglicano (pseudoureína). En el pseudopeptidoglucano, los residuos de azúcar son N-acetilglucosamina y ácido N-acetiltalosaminurónico unidos por β-(1,3). Esto hace que las paredes celulares de dichas arqueas sean insensibles a la lisozima. Se ha descrito la biosíntesis de pseudopeptidoglicano.
Contenido relacionado
Mejorana
Rasgo fenotípico
Parálisis