Paramixoviridae
Paramyxoviridae (del griego para- “al lado de” y myxa “moco”) es una familia de virus de ARN de cadena negativa en el orden Mononegavirales. Los vertebrados sirven como huéspedes naturales. Las enfermedades asociadas con esta familia incluyen el sarampión, las paperas y las infecciones del tracto respiratorio. La familia tiene cuatro subfamilias, 17 géneros y 78 especies, tres géneros de los cuales no están asignados a una subfamilia.
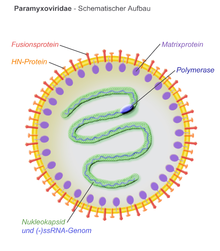
Estructura
Los viriones están envueltos y pueden ser esféricos o pleomórficos y capaces de producir viriones filamentosos. El diámetro es de alrededor de 150 nm. Los genomas son lineales, alrededor de 15 kb de longitud. Las proteínas de fusión y las proteínas de unión aparecen como picos en la superficie del virión. Las proteínas de la matriz dentro de la envoltura estabilizan la estructura del virus. El núcleo de la nucleocápside está compuesto por el ARN genómico, las proteínas de la nucleocápside, las fosfoproteínas y las proteínas de la polimerasa.
Genoma
El genoma es ARN no segmentado de sentido negativo, de 15 a 19 kilobases de longitud, y contiene de seis a diez genes. Las regiones extracistrónicas (no codificantes) incluyen:
- Una secuencia de 3’ líder, 50 nucleótidos de longitud, que actúa como promotor transcripcional.
- Una secuencia de remolque de 5’, nucleótidos de 50–161 largos
- Regiones entre cada gen, que son tres nucleótidos largos para morbillivirus, respirovirus y henipavirus, y longitud variable (nucleótidos uno-56) para rubulavirus.
Cada gen contiene señales de inicio/finalización de la transcripción al principio y al final, que se transcriben como parte del gen.
La secuencia de genes dentro del genoma se conserva en toda la familia debido a un fenómeno conocido como polaridad transcripcional (ver Mononegavirales) en el que los genes más cercanos al extremo 3' del genoma se transcriben en mayor abundancia que aquellos hacia el extremo 5'. Este es el resultado de la estructura del genoma. Después de transcribir cada gen, la ARN polimerasa dependiente de ARN hace una pausa para liberar el nuevo ARNm cuando encuentra una secuencia intergénica. Cuando la polimerasa de ARN se detiene, existe la posibilidad de que se disocie del genoma de ARN. Si se disocia, debe volver a ingresar al genoma en la secuencia líder, en lugar de continuar transcribiendo la longitud del genoma. El resultado es que cuanto más lejos estén los genes corriente abajo de la secuencia líder, menos serán transcritos por la ARN polimerasa.
La evidencia de un modelo de promotor único se verificó cuando los virus se expusieron a la luz ultravioleta. La radiación UV puede causar la dimerización del ARN, lo que impide la transcripción por parte de la ARN polimerasa. Si el genoma viral sigue un modelo de múltiples promotores, el nivel de inhibición de la transcripción debería correlacionarse con la longitud del gen de ARN. Sin embargo, el genoma se describió mejor mediante un modelo de promotor único. Cuando el genoma del paramixovirus se expuso a la luz ultravioleta, el nivel de inhibición de la transcripción fue proporcional a la distancia desde la secuencia líder. Es decir, cuanto más lejos esté el gen de la secuencia líder, mayor será la posibilidad de que la dimerización del ARN inhiba la ARN polimerasa.
El virus aprovecha el modelo de un solo promotor al disponer sus genes en el orden relativo de las proteínas necesarias para una infección exitosa. Por ejemplo, la proteína de la nucleocápside, N, se necesita en mayores cantidades que la ARN polimerasa, L.
Los virus de la familia Paramyxoviridae también son antigénicamente estables, lo que significa que las glicoproteínas de los virus son consistentes entre diferentes cepas del mismo tipo. Se postulan dos razones para este fenómeno: la primera es que el genoma no está segmentado, por lo que no puede sufrir reordenamiento genético. Para que ocurra este proceso, los segmentos necesarios como reordenamiento ocurren cuando los segmentos de diferentes cepas se mezclan para crear una nueva cepa. Sin segmentos, nada se puede mezclar entre sí, por lo que no se produce un cambio antigénico. La segunda razón se relaciona con la idea de deriva antigénica. Dado que la ARN polimerasa dependiente de ARN no tiene una función de verificación de errores, se producen muchas mutaciones cuando se procesa el ARN. Estas mutaciones se acumulan y eventualmente se crean nuevas cepas. Debido a este concepto, cabría esperar que los paramixovirus no fueran antigénicamente estables; sin embargo, se ve que lo contrario es cierto. La principal hipótesis detrás de por qué los virus son antigénicamente estables es que cada proteína y aminoácido tiene una función importante. Así, cualquier mutación conduciría a una disminución o pérdida total de la función, lo que a su vez haría que el nuevo virus fuera menos eficiente. Estos virus no podrían sobrevivir tanto tiempo en comparación con las cepas más virulentas, por lo que se extinguirían.
Muchos genomas de paramixovirus siguen la "regla de los seis". La longitud total del genoma es casi siempre un múltiplo de seis. Esto probablemente se deba a la ventaja de tener todo el ARN unido a la proteína N (ya que N se une a hexámeros de ARN). Si el ARN se deja expuesto, el virus no se replica de manera eficiente. La secuencia del gen es:
- Nucleocapsid – fosfoproteína – matriz – fusión – apego – grande (pomerasa)
Proteínas
- N – la proteína nucleocapsida asocia con ARN genómico (una molécula por hexamer) y protege el ARN de la digestión nucleasa
- P – la fosfoproteína se une a las proteínas N y L y forma parte del complejo de polimerasa RNA. P es el cofactor de la polimerasa.
- M – la proteína matriz se reúne entre el sobre y el núcleo nucleocapsid, organiza y mantiene la estructura virión
- F – la proteína de fusión proyectos de la superficie del sobre como un trimer, y media la entrada celular induciendo la fusión entre el sobre viral y la membrana celular por la fusión de clase I. Una de las características definitorias de los miembros de la familia Paramyxoviridae es el requisito de un pH neutro para la actividad fusógena.
- H/HN/G – las proteínas de apego celular abarcan el sobre viral y el proyecto desde la superficie como picos. Se unen a las proteínas en la superficie de las células objetivo para facilitar la entrada celular. Las proteínas son designadas H (hemagglutinina) para los morbillivirus, ya que poseen actividad de hemagglutinación, observada como una capacidad para causar que los glóbulos rojos se claven en pruebas de laboratorio. Las proteínas de adherencia HN (Hemagglutinin-neuraminidase) se producen en respirovirus, rubulavirus y avulavirus. Estos poseen tanto la hemagglutinación como la actividad neuraminidasa, que acumula ácido siálico en la superficie celular, evitando que las partículas virales vuelvan a atacar a las células previamente infectadas. Las proteínas de apego con ni haemagglutinación ni actividad neuraminidasa son designadas G (glucoproteína). Estos ocurren en henipavirus.
- L – la gran proteína es la subunidad catalítica de la polimerasa RNA dependiente del RNA (RDRP)
- Proteínas accesorios – un mecanismo conocido como edición RNA (ver Mononegavirales) permite que se produzcan múltiples proteínas del gen P. Estos no son esenciales para la replicación, pero pueden ayudar en la supervivencia in vitro o pueden estar involucrados en la regulación del interruptor de la síntesis de mRNA a la síntesis de antígenome.
Ciclo de vida
La replicación viral es citoplasmática. La entrada en la célula huésped se logra mediante la unión viral a la célula huésped. La replicación y la transcripción siguen los modelos de virus de ARN de cadena negativa. La traducción tiene lugar mediante exploración con fugas, derivación ribosómica y terminación-reinicio del ARN. El virus sale de la célula huésped por gemación. Los humanos, los vertebrados y las aves sirven como huéspedes naturales. La vía de transmisión son las partículas en el aire.
Los Paramyxoviridae pueden someterse a la edición de ARNm, que produce diferentes proteínas a partir de la misma transcripción de ARNm retrocediendo una base para leer en un marco de lectura abierto (ORF) diferente debido a la presencia de estructuras secundarias como pseudonudos. Paramyxoviridae también sufre un tartamudeo transcripcional para producir la cola poli (A) al final de las transcripciones de ARNm al retroceder repetidamente un nucleótido a la vez al final de la plantilla de ARN.
Taxonomía
Familia: Paramyxoviridae
- Subfamilia: Avulavirinae, que contiene tres géneros y 22 especies
- Subfamilia: Metaparamixovirinae, que contiene un género y una especie
- Subfamilia: Orthoparamyxovirinae, que contiene ocho géneros y 34 especies
- Subfamilia: Rubulavirinae, que contiene dos géneros y 18 especies
- Géneros no asignados:
- Cynoglossusvirus
- Hoplichthysvirus
- Scoliodonvirus
Paramixovirus patógenos
Varias enfermedades humanas importantes son causadas por paramixovirus. Estos incluyen las paperas, así como el sarampión, que causó alrededor de 733.000 muertes en 2000.
Los virus de la parainfluenza humana (HPIV) son la segunda causa más común de enfermedad de las vías respiratorias en bebés y niños. Hay cuatro tipos de HPIV, conocidos como HPIV-1, HPIV-2, HPIV-3 y HPIV-4. HPIV-1 y HPIV-2 pueden causar síntomas similares a los del resfriado, junto con crup en los niños. HPIV-3 está asociado con bronquiolitis, bronquitis y neumonía. El VPH-4 es menos común que los otros tipos y se sabe que causa enfermedades de las vías respiratorias de leves a graves.
Los paramixovirus también son responsables de una variedad de enfermedades en otras especies animales, por ejemplo, el virus del moquillo canino (perros), el virus del moquillo focino (focas), el morbillivirus de los cetáceos (delfines y marsopas), el virus de la enfermedad de Newcastle (aves) y la peste bovina. virus (ganado). Algunos paramixovirus, como los henipavirus, son patógenos zoonóticos que se encuentran naturalmente en un huésped animal, pero que también pueden infectar a los humanos.
El virus Hendra y el virus Nipah del género Henipavirus han surgido en humanos y ganado en Australia y el sudeste asiático. Ambos virus son contagiosos, altamente virulentos y capaces de infectar a varias especies de mamíferos y causar enfermedades potencialmente mortales. Debido a la falta de una vacuna autorizada o terapias antivirales, el virus Hendra y el virus Nipah están designados como agentes de nivel de bioseguridad (BSL) 4. La estructura genómica de ambos virus es la de un paramixovirus típico.
Diversidad y evolución
En las últimas décadas, se han descubierto paramixovirus de animales terrestres, voladores y acuáticos, lo que demuestra una amplia gama de huéspedes y una gran diversidad genética viral. A medida que avanza la tecnología molecular y se implementan programas de vigilancia viral, aumenta el descubrimiento de nuevos virus en este grupo.
Todavía se debate la evolución de los paramixovirus. Usando los neumovirus (familia mononegaviral Pneumoviridae) como un grupo externo, los paramixovirus se pueden dividir en dos clados: uno que consta de avulavirus y rubulavirus y otro que consta de respirovirus, henipavirus y morbillivirus. Dentro del segundo clado, los respirovirus parecen ser el grupo basal. El clado respirovirus-henipavirus-morbillivirus puede ser basal al clado avulavirus-rubulavirus.
Contenido relacionado
Myliobatiformes
Tim Berra (biólogo)
La enfermedad de Chagas