Oxígeno sólido
oxígeno sólido se forma a presión atmosférica normal a una temperatura inferior a 54,36 K (−218,79 °C, −361,82 °F). El oxígeno sólido O2, al igual que el oxígeno líquido, es una sustancia transparente con un color azul cielo claro causado por la absorción en la parte roja del espectro de luz visible.
Las moléculas de oxígeno han llamado la atención debido a la relación entre la magnetización molecular y las estructuras cristalinas, las estructuras electrónicas y la superconductividad. El oxígeno es la única molécula diatómica simple (y una de las pocas moléculas en general) que transporta un momento magnético. Esto hace que el oxígeno sólido sea particularmente interesante, ya que se considera un oxígeno "controlado por giro". Cristal que muestra orden magnético antiferromagnético en las fases de baja temperatura. Las propiedades magnéticas del oxígeno se han estudiado ampliamente. A presiones muy altas, el oxígeno sólido cambia de un estado aislante a uno metálico; y a temperaturas muy bajas, incluso se transforma a un estado superconductor. Las investigaciones estructurales del oxígeno sólido comenzaron en la década de 1920 y, en la actualidad, se establecen sin ambigüedades seis fases cristalográficas distintas.
La densidad del oxígeno sólido varía desde 21 cm3/mol en la fase α hasta 23,5 cm3/mol en la fase γ.
Fases

Se sabe que existen seis fases diferentes de oxígeno sólido:
- α-fase: azul claro – formularios a 1 atm, abajo 23.8 K, estructura monoclínica de cristal, grupo espacial C2/m (no 12).
- β-fase: azul débil a rosa – formularios a 1 atm, debajo de 43.8 K, estructura cristalina rombohedral, grupo espacial R3m (no 166). A temperatura ambiente y alta presión comienza la transformación al tetraoxigeno.
- γ-fase: azul débil – formularios a 1 atm, por debajo de 54.36 K, estructura de cristal cúbico, Pm3n (No 223).
- δ-phase: naranja – formas a temperatura ambiente a una presión de 9 GPa
- ε-phase: rojo oscuro a negro – formas a temperatura ambiente a presiones superiores a 10 GPa
- . metálico – formas a presión superiores a 96 GPa
Se ha descubierto que el oxígeno se solidifica en un estado llamado fase β a temperatura ambiente aplicando presión y, al aumentar aún más la presión, la fase β sufre transiciones de fase a la fase δ a 9 GPa y la fase ε -fase a 10 GPa; y, debido al aumento de las interacciones moleculares, el color de la fase β cambia a rosa, naranja y luego rojo (la fase estable de octaoxígeno), y el color rojo se oscurece aún más hasta convertirse en negro al aumentar la presión. Se descubrió que aparece una fase ζ metálica a 96 GPa cuando el oxígeno de la fase ε se comprime aún más.
Oxígeno rojo
A medida que la presión del oxígeno a temperatura ambiente aumenta en 10 gigapascales (1.500.000 psi), sufre una dramática transición de fase. Su volumen disminuye significativamente y cambia de color del azul cielo al rojo intenso. Sin embargo, este es un alótropo diferente del oxígeno, O
8, no simplemente una fase cristalina diferente de O2.
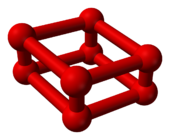 |  |
| Modelo de bola y palo de O8 | Parte de la estructura cristalina del ε-oxygen |
Oxígeno metálico
Aparece una fase ζ a 96 GPa cuando el oxígeno de la fase ε se comprime aún más. Esta fase fue descubierta en 1990 presurizando oxígeno a 132 GPa. La fase ζ con grupo metálico exhibe superconductividad a presiones superiores a 100 GPa y una temperatura inferior a 0,6 K.