Oxidación de Swern
En química orgánica, la oxidación de Swern, llamada así por Daniel Swern, es una reacción química en la que un alcohol primario o secundario (−OH) se oxida a un aldehído (−CH=O) o cetona (>C=O) usando cloruro de oxalilo, sulfóxido de dimetilo (DMSO) y una base orgánica, como trietilamina. Es una de las muchas reacciones de oxidación comúnmente conocidas como 'DMSO activado' oxidaciones. La reacción es conocida por su carácter suave y su amplia tolerancia a los grupos funcionales.
Los subproductos son sulfuro de dimetilo ((CH3)2S), monóxido de carbono (CO), dióxido de carbono (CO2) y, cuando se utiliza trietilamina como base, cloruro de trietilamonio (Et3NHCl). De los subproductos volátiles, el sulfuro de dimetilo tiene un olor fuerte y penetrante y el monóxido de carbono es sumamente tóxico, por lo que la reacción y el tratamiento deben realizarse en una campana extractora. El sulfuro de dimetilo es un líquido volátil (P.E. 37 °C) con un olor desagradable incluso en concentraciones bajas.
Mecanismo
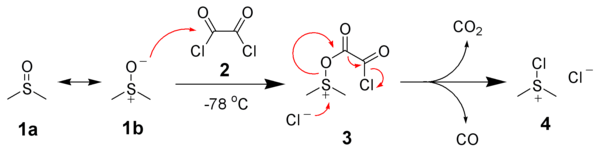
El primer paso de la oxidación de Swern es la reacción a baja temperatura de DMSO, 1a, formalmente como contribuyente de resonancia 1b, con cloruro de oxalilo, 2. El primer intermedio, 3, se descompone rápidamente emitiendo dióxido de carbono y monóxido de carbono y produciendo cloruro de cloro(dimetil)sulfonio, 4.
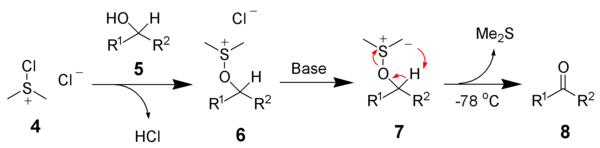
Después de agregar el alcohol 5, el cloruro de cloro(dimetil)sulfonio 4 reacciona con el alcohol para dar el intermedio clave de iones alcoxisulfonio, 6. La adición de al menos 2 equivalentes de base, típicamente trietilamina, desprotonará el ion alcoxisulfonio para dar el iluro de azufre 7. En un estado de transición de anillo de cinco miembros, el iluro de azufre 7 se descompone para dar sulfuro de dimetilo y el compuesto carbonilo deseado 8.
Variaciones
Cuando se usa cloruro de oxalilo como agente de deshidratación, la reacción debe mantenerse a una temperatura inferior a -60 °C para evitar reacciones secundarias. Con cloruro cianúrico o anhídrido trifluoroacético en lugar de cloruro de oxalilo, la reacción se puede calentar a -30 °C sin reacciones secundarias. Otros métodos para la activación de DMSO para iniciar la formación del intermediario clave 6 son el uso de carbodiimidas (oxidación de Pfitzner-Moffatt), un complejo de piridina de trióxido de azufre (oxidación de Parikh-Doering) o anhídrido acético (oxidación de Albright-Goldman). El 4 intermedio también se puede preparar a partir de sulfuro de dimetilo y N-clorosuccinimida (la oxidación de Corey-Kim).
En algunos casos, el uso de trietilamina como base puede conducir a la epimerización en el carbono alfa al carbonilo recién formado. El uso de una base más voluminosa, como la diisopropiletilamina, puede mitigar esta reacción secundaria.
Consideraciones
El sulfuro de dimetilo, un subproducto de la oxidación de Swern, es uno de los olores más notoriamente desagradables que se conocen en la química orgánica. Los humanos pueden detectar este compuesto en concentraciones tan bajas como 0,02 a 0,1 partes por millón. Un remedio simple para este problema es enjuagar la cristalería usada con lejía o solución de oxona, que oxidará el sulfuro de dimetilo de nuevo a dimetilsulfóxido o dimetilsulfona, los cuales son inodoros y no tóxicos.
Las condiciones de reacción permiten la oxidación de compuestos sensibles a los ácidos, que podrían descomponerse en condiciones de oxidación ácidas, como la oxidación de Jones. Por ejemplo, en Thompson & La síntesis de Heathcock del sesquiterpeno isovelleral, el paso final utiliza el protocolo de Swern, evitando la reorganización del resto ciclopropanometanol sensible a los ácidos.
Contenido relacionado
Elemento estable
Haluro
Hg