Oxidación beta
En bioquímica y metabolismo, la beta oxidación (también β-oxidación) es el proceso catabólico mediante el cual las moléculas de ácidos grasos se descomponen en el citosol en los procariotas y en las mitocondrias en los eucariotas para generar acetil- CoA. El acetil-CoA ingresa al ciclo del ácido cítrico, generando NADH y FADH2, que son transportadores de electrones utilizados en la cadena de transporte de electrones. Se llama así porque el carbono beta de la cadena de ácidos grasos se oxida y se convierte en un grupo carbonilo para comenzar el ciclo de nuevo. La beta-oxidación es facilitada principalmente por la proteína trifuncional mitocondrial, un complejo enzimático asociado con la membrana mitocondrial interna, aunque los ácidos grasos de cadena muy larga se oxidan en los peroxisomas.
La reacción general de un ciclo de oxidación beta es:
- Cn-acyl-CoA + FAD + NAD+ + H2O + CoA → Cn-2-acyl-CoA + FADH2 + NADH + H+ + acetil-CoA
Activación y transporte de membrana
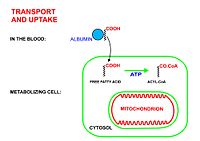
Los ácidos grasos libres no pueden atravesar ninguna membrana biológica debido a su carga negativa. Los ácidos grasos libres deben atravesar la membrana celular a través de proteínas de transporte específicas, como la proteína de transporte de ácidos grasos de la familia SLC27. Una vez en el citosol, los siguientes procesos llevan los ácidos grasos a la matriz mitocondrial para que pueda tener lugar la beta-oxidación.
- El ligaso de cadena larga cataliza la reacción entre un ácido graso con ATP para dar un adenilato de acil graso, más pirofosfato inorgánico, que luego reacciona con la coenzima libre A para dar un acil-CoA ester y AMP grasos.
- Si el gordo acyl-CoA tiene una cadena larga, entonces el transbordador de carnitina debe ser utilizado (shown in the table below):
- Acyl-CoA se transfiere al grupo hidroxil de carnitina por carnitina palmitoyltransferase I, ubicado en las caras citosólicas de las membranas mitocondriales externas e internas.
- Acyl-carnitine es transferido por un translocase carnitina-acylcarnitina, ya que un carnitina es lanzada afuera.
- El acyl-carnitina se convierte de nuevo en acyl-CoA por carnitina palmitoyltransferase II, situada en la cara interior de la membrana mitocondrial interior. La carnitina liberada es lanzada de vuelta al citosol, ya que se lanza un acil-carnitina en la matriz.
- Si el acyl-CoA grasa contiene una cadena corta, estos ácidos grasos de cadena corta pueden simplemente difundir a través de la membrana mitocondrial interna.
Mecanismo general de la beta oxidación

Una vez que el ácido graso está dentro de la matriz mitocondrial, se produce la beta-oxidación al escindir dos carbonos en cada ciclo para formar acetil-CoA. El proceso consta de 4 pasos.
- Un ácido graso de cadena larga está deshidratado para crear un vínculo doble trans entre C2 y C3. Esto es catalizado por acyl CoA dehydrogenase para producir trans-delta 2-enoyl CoA. Utiliza FAD como receptor de electrones y se reduce a FADH2.
- Trans-delta 2-enoyl CoA se hidrata en el doble enlace para producir L-3-hidroxiacyl CoA por enoyl-CoA hidratatase.
- L-3-hidroxiacilo CoA está deshidratado de nuevo para crear 3-ketoacyl CoA por 3-hidroxiacyl CoA deshidrogenasa. Esta enzima utiliza el NAD como receptor de electrones.
- La tiolisis ocurre entre C2 y C3 (carbonos de alfa y beta) de 3-ketoacyl CoA. La enzima tiolasa cataliza la reacción cuando una nueva molécula de coenzima A rompe el vínculo por ataque nucleófilo contra C3. Esto libera las dos primeras unidades de carbono, como acetil CoA, y un graso acyl CoA menos dos carbonos. El proceso continúa hasta que todos los carbonos del ácido graso se conviertan en Acetil CoA.
Este acetil-CoA luego ingresa al ciclo del ácido tricarboxílico mitocondrial (ciclo TCA). Tanto la betaoxidación de los ácidos grasos como el ciclo del TCA producen NADH y FADH2, que son utilizados por la cadena de transporte de electrones para generar ATP.
Los ácidos grasos son oxidados por la mayoría de los tejidos del cuerpo. Sin embargo, algunos tejidos como los glóbulos rojos de los mamíferos (que no contienen mitocondrias) y las células del sistema nervioso central no utilizan ácidos grasos para sus necesidades energéticas, sino que utilizan carbohidratos (glóbulos rojos y neuronas) o cuerpos cetónicos. (solo neuronas).
Debido a que muchos ácidos grasos no están completamente saturados o no tienen un número par de carbonos, han evolucionado varios mecanismos diferentes, que se describen a continuación.
Ácidos grasos saturados pares
Una vez dentro de las mitocondrias, cada ciclo de β-oxidación, que libera una unidad de dos carbonos (acetil-CoA), ocurre en una secuencia de cuatro reacciones:
Este proceso continúa hasta que toda la cadena se escinde en unidades de acetil CoA. El ciclo final produce dos acetil CoA separados, en lugar de un acil CoA y un acetil CoA. Para cada ciclo, la unidad de acil CoA se acorta en dos átomos de carbono. Al mismo tiempo se forman una molécula de FADH2, NADH y acetil CoA.
Ácidos grasos saturados impares

Los ácidos grasos con un número impar de carbonos se encuentran en los lípidos de las plantas y de algunos organismos marinos. Muchos animales rumiantes forman una gran cantidad de propionato de 3 carbonos durante la fermentación de los carbohidratos en el rumen. Los ácidos grasos de cadena larga con un número impar de átomos de carbono se encuentran particularmente en la grasa y la leche de los rumiantes.
Las cadenas con un número impar de carbonos se oxidan de la misma manera que las cadenas pares, pero los productos finales son propionil-CoA y acetil-CoA.
Primero se carboxila propionil-CoA utilizando un ion bicarbonato en un estereoisómero D de metilmalonil-CoA. Esta reacción involucra un cofactor de biotina, ATP y la enzima propionil-CoA carboxilasa. El carbono del ion bicarbonato se añade al carbono medio del propionil-CoA, formando una D-metilmalonil-CoA. Sin embargo, la conformación D se convierte enzimáticamente en la conformación L mediante la metilmalonil-CoA epimerasa. Luego sufre un reordenamiento intramolecular, que es catalizado por la metilmalonil-CoA mutasa (que requiere B12 como coenzima) para formar succinil-CoA. La succinil-CoA formada entra entonces en el ciclo del ácido cítrico.
Sin embargo, mientras que el acetil-CoA ingresa al ciclo del ácido cítrico al condensarse con una molécula existente de oxalacetato, la succinil-CoA ingresa al ciclo como un principio por derecho propio. Por lo tanto, el succinato simplemente aumenta la población de moléculas circulantes en el ciclo y no sufre ninguna metabolización neta mientras está en él. Cuando esta infusión de intermediarios del ciclo del ácido cítrico excede la demanda cataplerótica (como para la síntesis de aspartato o glutamato), algunos de ellos pueden extraerse a la vía de la gluconeogénesis, en el hígado y los riñones, a través de la fosfoenolpiruvato carboxiquinasa, y convertirse en glucosa libre.
Ácidos grasos insaturados
La β-oxidación de ácidos grasos insaturados plantea un problema ya que la ubicación de un enlace cis puede impedir la formación de un enlace trans-Δ2 que es esencial para la continuación de la β-oxidación, ya que esta La conformación es ideal para la catálisis enzimática. Esto lo manejan dos enzimas adicionales, la enoil CoA isomerasa y la 2,4 dienoil CoA reductasa.

La β-oxidación ocurre normalmente hasta que la acil CoA (debido a la presencia de un doble enlace) no es un sustrato apropiado para la acil CoA deshidrogenasa o la enoil CoA hidratasa:
- Si el acyl CoA contiene un cis-Δ3 bonoEntonces cis-Δ3-Enoyl CoA isomerase convertirá el vínculo a un trans-Δ2 vínculo, que es un sustrato regular.
- Si el acyl CoA contiene un cis-Δ4 doble vínculo, entonces su deshidrogenación produce un intermedio de 2,4-dienoilo, que no es un sustrato para enoyl CoA hidrataatase. Sin embargo, la enzima 2,4 Dienoyl CoA reductase reduce el intermedio, utilizando NADPH, en trans-Δ3-enoyl CoA. Este compuesto se convierte en un intermedio adecuado por 3,2-Enoyl CoA isomerasa y β-Oxidación continúa.
Beta-oxidación peroxisomal
La oxidación de ácidos grasos también ocurre en los peroxisomas cuando las cadenas de ácidos grasos son demasiado largas para ser procesadas por las mitocondrias. En los peroxisomas se utilizan las mismas enzimas que en la matriz mitocondrial y se genera acetil-CoA. Los ácidos grasos de cadena muy larga (mayores que C-22), los ácidos grasos ramificados, algunas prostaglandinas y leucotrienos sufren una oxidación inicial en los peroxisomas hasta que se forma octanoil-CoA, momento en el cual sufre oxidación mitocondrial.
Una diferencia significativa es que la oxidación en los peroxisomas no está acoplada a la síntesis de ATP. En cambio, los electrones de alto potencial se transfieren al O2, lo que produce peróxido de hidrógeno. La enzima catalasa, que se encuentra principalmente en los peroxisomas y el citosol de los eritrocitos (y a veces en las mitocondrias), convierte el peróxido de hidrógeno en agua y oxígeno.
La β-oxidación peroxisomal también requiere enzimas específicas del peroxisoma y de ácidos grasos muy largos. Existen cuatro diferencias clave entre las enzimas utilizadas para la β-oxidación mitocondrial y peroxisomal:
- La NADH formada en el tercer paso oxidativo no puede ser reoxidizada en el peróxido, por lo que reducir los equivalentes se exportan al citosol.
- β-oxidación en el peroxioma requiere el uso de una carnitina peroxisomal acyltransferase (en lugar de carnitina acyltransferase I y II utilizada por la mitocondria) para el transporte del grupo acyl activado en la mitocondria para mayor desintegración.
- El primer paso de oxidación en el peróxido es catalizado por la enzima acyl-CoA oxidase.
- La β-ketotilase utilizada en la β-oxidación peroxisomal tiene una especificidad alterada del sustrato, diferente de la mitocondrial β-ketothiolase.
La oxidación peroxisomal es inducida por una dieta rica en grasas y la administración de fármacos hipolipidemiantes como el clofibrato.
Rendimiento energético
Ácidos grasos saturados pares
Teóricamente, el rendimiento de ATP para cada ciclo de oxidación donde se descomponen dos carbonos a la vez es 17, ya que cada NADH produce 3 ATP, FADH2 produce 2 ATP y una rotación completa de Acetil- La CoA en el ciclo del ácido cítrico produce 12 ATP. En la práctica, está más cerca de 14 ATP para un ciclo de oxidación completo, ya que se producen 2,5 ATP por molécula de NADH, 1,5 ATP por cada molécula de FADH2 y Acetil-CoA produce 10 ATP por rotación del ciclo de oxidación completo. ciclo del ácido cítrico (según la relación P/O). Este desglose es el siguiente:
| Fuente | ATP | Total |
|---|---|---|
| 1 FADH2 | x 1,5 ATP | = 1,5 ATP (Teóricamente 2 ATP) |
| 1 NADH | x 2,5 ATP | = 2.5 ATP (Teóricamente 3 ATP) |
| 1 Acetyl CoA | x 10 ATP | = 10 ATP (Teóricamente 12 ATP) |
| 1 Succinyl CoA | x 4 ATP | = 4 ATP |
| Total | = 14 ATP |
Para una grasa saturada par (Cn), son necesarias 0,5 * n - 1 oxidaciones y el proceso final produce acetil CoA adicional. Además, durante la activación del ácido graso se pierden dos equivalentes de ATP. Por tanto, la producción total de ATP se puede expresar como:
- ()0.5× × n− − 1)× × 14+10− − 2=ATP{displaystyle (0.5times n-1)times 14+10-2=ATP}
o
- 7n− − 6{displaystyle 7n-6}
Por ejemplo, el rendimiento de ATP del palmitato (C16, n = 16) es:
- 7× × 16− − 6=106ATP{displaystyle 7times 16-6=106ATP}
Representado en forma de tabla:
| Fuente | ATP | Total |
|---|---|---|
| 7 FADH2 | x 1,5 ATP | = 10,5 ATP |
| 7 NADH | x 2,5 ATP | = 17,5 ATP |
| 8 Acetyl CoA | x 10 ATP | = 80 ATP |
| Activación | = 2 ATP | |
| Total | 106 ATP |
Ácidos grasos saturados impares

Para una grasa saturada impar (Cn), son necesarias 0,5 * n - 1,5 oxidaciones y el proceso final produce 8 acetil CoA y 1 propionil CoA. Luego se convierte en succinil CoA mediante una reacción de carboxilación y genera 5 ATP adicionales (se consume 1 ATP en el proceso de carboxilación generando un neto de 4 ATP). Además, durante la activación del ácido graso se pierden dos equivalentes de ATP. Por tanto, la producción total de ATP se puede expresar como:
- ()0.5× × n− − 1,5)× × 14+4− − 2=ATP{displaystyle (0.5times n-1.5)times 14+4-2=ATP}
o
- 7n− − 19{displaystyle 7n-19}
Por ejemplo, el rendimiento de ATP del ácido nonadecílico (C19, n = 19) es:
- 7× × 19− − 19=114ATP{displaystyle 7times 19-19=114ATP}
Representado en forma de tabla:
| Fuente | ATP | Total |
|---|---|---|
| 8 FADH2 | x 1,5 ATP | = 12 ATP |
| 8 NADH | x 2,5 ATP | = 20 ATP |
| 8 Acetyl CoA | x 10 ATP | = 80 ATP |
| 1 Succinyl CoA | x 4 ATP | = 4 ATP |
| Activación | = 2 ATP | |
| Total | = 114 ATP |
Importancia clínica
Hay al menos 25 enzimas y proteínas de transporte específicas en la vía de β-oxidación. De ellos, 18 se han asociado con enfermedades humanas como errores innatos del metabolismo.
Además, los estudios indican que los trastornos de los lípidos están implicados en diversos aspectos de la tumorigénesis, y el metabolismo de los ácidos grasos hace que las células malignas sean más resistentes a un entorno hipóxico. En consecuencia, las células cancerosas pueden mostrar un metabolismo lipídico irregular con respecto tanto a la síntesis de ácidos grasos como a la oxidación de ácidos grasos mitocondriales (FAO), que están implicados en diversos aspectos de la tumorigénesis y el crecimiento celular. Se han identificado varios trastornos específicos de la β-oxidación.
Deficiencia de acilcoenzima A deshidrogenasa de cadena media (MCAD)
La deficiencia de acilcoenzima A deshidrogenasa de cadena media (MCAD) es el trastorno de β-oxidación de ácidos grasos más común y un error congénito metabólico prevalente. A menudo se identifica mediante pruebas de detección en recién nacidos. Aunque los niños son normales al nacer, los síntomas suelen aparecer entre los tres meses y los dos años de edad, apareciendo algunos casos en la edad adulta.
La acil-CoA deshidrogenasa de cadena media (MCAD) desempeña un papel crucial en la β-oxidación de ácidos grasos mitocondriales, un proceso vital para generar energía durante períodos de ayuno prolongado o de alta demanda de energía. Este proceso, especialmente importante cuando se agota el glucógeno hepático, favorece la cetogénesis hepática. El paso específico catalizado por MCAD implica la deshidrogenación de acil-CoA. Este paso convierte la acil-CoA de cadena media en trans-2-enoil-CoA, que luego se metaboliza aún más para producir energía en forma de ATP.
Síntomas
- Los niños afectados, que parecen saludables inicialmente, pueden experimentar síntomas como azúcar en sangre baja sin cetonas (hipoketotic hipoglucemia) y vómitos
- Puede escalar a letargo, convulsiones y coma, normalmente provocado por la enfermedad
- Los episodios agudos también pueden implicar el hígado agrandado (hepatomegalia) y problemas hepáticos
- Muerte repentina
Tratamientos
- Administrar carbohidratos simples
- Evitar el ayuno
- Alimentación frecuente para bebés
- Para los niños pequeños, una dieta con menos del 30% de energía total de grasa
- Administrar 2 g/kg de almidón de maíz no cocido a la hora de dormir para suficiente glucosa durante la noche
- Prevenir la hipoglucemia, especialmente debido al ayuno excesivo.
- Evitar fórmulas infantiles con triglicéridos de cadena media como principal fuente de grasa

Deficiencia de hidroxiacil-CoA deshidrogenasa de cadena larga (LCHAD)
La deficiencia de hidroxiacil-CoA deshidrogenasa de cadena larga (LCHAD) es un efecto mitocondrial de la función enzimática alterada.
LCHAD realiza la deshidrogenación de derivados de hidroxiacil-CoA, facilitando la eliminación de hidrógeno y la formación de un grupo ceto. Esta reacción es esencial para los pasos posteriores de la beta oxidación que conducen a la producción de acetil-CoA, NADH y FADH2, que son importantes para generar ATP, la moneda energética de la célula.
La deficiencia de hidroxiacil-CoA deshidrogenasa de cadena larga (LCHAD) es una afección que afecta la función mitocondrial debido a alteraciones enzimáticas. La deficiencia de LCHAD es causada específicamente por una deficiencia de la enzima 3-hidroxiacil-CoA deshidrogenasa de cadena larga. Esto conduce a la incapacidad del cuerpo para transformar grasas específicas en energía, especialmente durante los períodos de ayuno.
Síntomas
- Fenotipo grave: los síntomas aparecen poco después del nacimiento e incluyen hipoglicemia, hepatomegalia, disfunción cerebral (encefalopatía) y a menudo cardiomiopatía
- Fenotipo intermedio: caracterizado por hipoglicemia hipoquetótica y desencadenado por infección o ayuno durante la infancia
- Fenotipo leve (comunicación tardía): presenta como debilidad muscular (miopatía) y enfermedad nerviosa (neuropatía)
- Complicaciones a largo plazo: pueden incluir neuropatía periférica y daño ocular (retinopatía)
Tratamientos
- Alimentación regular para evitar el ayuno
- Uso de triglicéridos de cadena media (MCT) o suplementos de triheptanoína y suplementos de carnitina
- Dieta baja en grasa
- Hospitalización con fluidos intravenosos que contienen al menos un 10% de dextrosis
- Terapia bicarbonato para acidosis metabólica severa
- Gestión de altos niveles de amoníaco y descomposición muscular
- Gestión de la cardiomiopatía
- Monitoreo regular de nutrición, análisis de sangre y hígado con perfil de ácido graso anual
- Crecimiento, desarrollo, evaluaciones cardíacas y neurológicas y evaluaciones de los ojos
Deficiencia de acil-coenzima A deshidrogenasa de cadena muy larga (VLCAD)
La deficiencia de acilcoenzima A deshidrogenasa de cadena muy larga (deficiencia de VLCAD) es un trastorno genético que afecta la capacidad del cuerpo para descomponer ciertas grasas. En el ciclo de β-oxidación, la función de VLCAD implica la eliminación de dos átomos de hidrógeno de la molécula de acil-CoA, formando un doble enlace y convirtiéndolo en trans-2-enoil-CoA. Este primer paso crucial en el ciclo es esencial para que el ácido graso se someta a un mayor procesamiento y producción de energía. Cuando hay una deficiencia de VLCAD, el cuerpo lucha por descomponer eficazmente los ácidos grasos de cadena larga. Esto puede provocar una acumulación de estas grasas y una escasez de energía, especialmente durante los períodos de ayuno o de mayor actividad física.
Síntomas
- Forma de insuficiencia cardiaca y multiorgan: los síntomas aparecen dentro de los días de nacimiento e incluyen miocardiopatía hipertrófica/dilatada, líquido alrededor del corazón (efusión pericardial), problemas de ritmo cardíaco (arritmias), hepatomegalia y hipoglicemia intermitente ocasional
- Forma hipoglucémica hepática o hipogótica: normalmente aparece en la primera infancia con hipoglicemia hipogótica
- Forma miopática episódica posterior: presenta con descomposición muscular después del ejercicio (rehabdomiolisis intermitente), calambres musculares y dolor, intolerancia al ejercicio y bajo azúcar en la sangre
Tratamientos
- Dieta baja en grasa
- Uso de suplementos de triglicéridos de cadena media
- Alimentación regular y frecuente, especialmente para bebés y niños
- Snacks alto en carbohidratos complejos antes de acostarse
- Ejercicio guiado y limitado para las personas mayores
- Administración de líquidos de alta energía intravenosa
- Evitar las grasas L-carnitina y IV
- Un montón de líquidos y alcalización de orina para el colapso muscular