Nucleótido
Los nucleótidos son moléculas orgánicas formadas por un nucleósido y un fosfato. Sirven como unidades monoméricas de los polímeros de ácido nucleico: ácido desoxirribonucleico (ADN) y ácido ribonucleico (ARN), los cuales son biomoléculas esenciales dentro de todas las formas de vida en la Tierra. Los nucleótidos se obtienen en la dieta y también se sintetizan a partir de nutrientes comunes en el hígado.
Los nucleótidos se componen de tres moléculas de subunidades: una nucleobase, un azúcar de cinco carbonos (ribosa o desoxirribosa) y un grupo fosfato que consta de uno a tres fosfatos. Las cuatro bases nitrogenadas del ADN son guanina, adenina, citosina y timina; en el ARN, se usa uracilo en lugar de timina.
Los nucleótidos también juegan un papel central en el metabolismo a un nivel celular fundamental. Proporcionan energía química, en forma de trifosfato de nucleósido, trifosfato de adenosina (ATP), trifosfato de guanosina (GTP), trifosfato de citidina (CTP) y trifosfato de uridina (UTP), a través de la célula para muchas funciones celulares que demandan energía, incluyendo : síntesis de aminoácidos, proteínas y membrana celular, movimiento de la célula y partes de la célula (tanto interna como intercelularmente), división celular, etc. Además, los nucleótidos participan en la señalización celular (guanosina monofosfato cíclica o cGMP y adenosina monofosfato cíclica o cAMP), y se incorporan a importantes cofactores de reacciones enzimáticas (p. ej., coenzima A, FAD, FMN, NAD y NADP).
En bioquímica experimental, los nucleótidos se pueden radiomarcar usando radionúclidos para producir radionucleótidos.
Los 5 nucleótidos también se utilizan en potenciadores del sabor como aditivos alimentarios para potenciar el sabor umami, a menudo en forma de extracto de levadura.
Estructura
Un nucleótido se compone de tres subunidades químicas distintivas: una molécula de azúcar de cinco carbonos, una nucleobase (los dos juntos se denominan nucleósido) y un grupo fosfato. Con los tres unidos, un nucleótido también se denomina " monofosfato de nucleósido", "difosfato de nucleósido " o "trifosfato de nucleósido ", según la cantidad de fosfatos que componen el grupo fosfato .
En los ácidos nucleicos, los nucleótidos contienen una base de purina o pirimidina, es decir, la molécula de base nitrogenada, también conocida como base nitrogenada, y se denominan ribonucleótidos si el azúcar es ribosa, o desoxirribonucleótidos si el azúcar es desoxirribosa. Las moléculas de fosfato individuales conectan repetidamente las moléculas del anillo de azúcar en dos monómeros de nucleótidos adyacentes, conectando así los monómeros de nucleótidos de un ácido nucleico de extremo a extremo en una cadena larga. Estas uniones en cadena de moléculas de azúcar y fosfato crean una hebra de "columna vertebral" para una hélice simple o doble. En cualquier hebra, la orientación química (direccionalidad) de las uniones de la cadena va desde el extremo 5' hasta el extremo 3' ( léase: 5 prime-end a 3 prime-end)—refiriéndose a los cinco sitios de carbono en las moléculas de azúcar en nucleótidos adyacentes. En una doble hélice, las dos cadenas están orientadas en direcciones opuestas, lo que permite el emparejamiento de bases y la complementariedad entre los pares de bases, todo lo cual es esencial para replicar o transcribir la información codificada que se encuentra en el ADN.
Los ácidos nucleicos son entonces macromoléculas poliméricas ensambladas a partir de nucleótidos, las unidades monoméricas de los ácidos nucleicos. Las bases de purina adenina y guanina y la base de pirimidina citosina se encuentran tanto en el ADN como en el ARN, mientras que las bases de pirimidina timina (en el ADN) y uracilo (en el ARN) se encuentran en uno solo. La adenina forma un par de bases con la timina con dos enlaces de hidrógeno, mientras que la guanina se empareja con la citosina con tres enlaces de hidrógeno.
Además de ser componentes básicos para la construcción de polímeros de ácido nucleico, los nucleótidos singulares desempeñan funciones en el almacenamiento y suministro de energía celular, la señalización celular, como fuente de grupos fosfato utilizados para modular la actividad de las proteínas y otras moléculas de señalización, y como cofactores enzimáticos., a menudo llevando a cabo reacciones redox. Los nucleótidos cíclicos de señalización se forman uniendo el grupo fosfato dos veces a la misma molécula de azúcar, uniendo los grupos hidroxilo 5' y 3' del azúcar. Algunos nucleótidos de señalización difieren de la configuración estándar de un solo grupo fosfato, ya que tienen múltiples grupos fosfato unidos a diferentes posiciones en el azúcar. Los cofactores de nucleótidos incluyen una gama más amplia de grupos químicos unidos al azúcar a través del enlace glucosídico, incluidos la nicotinamida y la flavina, y en el último caso, el azúcar ribosa es lineal en lugar de formar el anillo que se ve en otros nucleótidos.
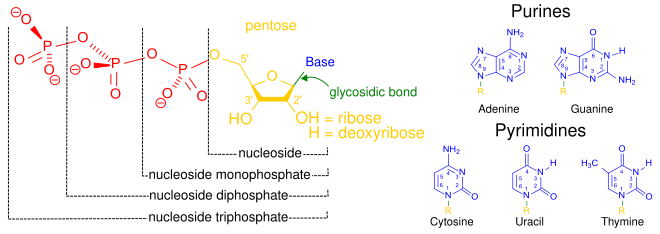 Elementos estructurales de tres nucleótidos
Elementos estructurales de tres nucleótidos
, donde uno, dos o tres fosfatos están unidos al nucleósido
( en amarillo, azul, verde) en el centro: primero, el nucleótido denominado monofosfato
de nucleósido se forma al agregar un fosfato (en rojo); 2º, la adición de un segundo fosfato forma un
nucleósido difosfato ; En tercer lugar, la adición de un tercer fosfato da como resultado un
nucleósido trifosfato. + La base nitrogenada (base nitrogenada) se indica mediante "Base" y "enlace glucosídico" (enlace de azúcar). Las cinco bases primarias o canónicas, las purinas y las pirimidinas, están dibujadas a la derecha (en azul).Ejemplos de nucleótidos que no son ácidos nucleicos
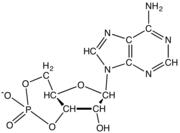 cAMP, una molécula de señalización de nucleótidos cíclicos con un solo fosfato unido a las posiciones 5 y 3.
cAMP, una molécula de señalización de nucleótidos cíclicos con un solo fosfato unido a las posiciones 5 y 3.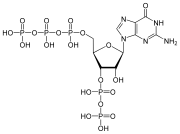 pppGpp, una molécula de señalización de nucleótidos con fosfatos 5' y 3'.
pppGpp, una molécula de señalización de nucleótidos con fosfatos 5' y 3'.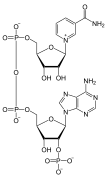 NADP, un cofactor enzimático dinucleótido.
NADP, un cofactor enzimático dinucleótido.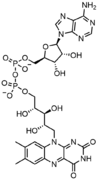 FAD, un cofactor enzimático de dinucleótido en el que uno de los azúcares ribosa adopta una configuración lineal en lugar de un anillo.
FAD, un cofactor enzimático de dinucleótido en el que uno de los azúcares ribosa adopta una configuración lineal en lugar de un anillo.
Síntesis
Los nucleótidos se pueden sintetizar por una variedad de medios tanto in vitro como in vivo.
Los grupos protectores in vitro pueden usarse durante la producción de nucleótidos en el laboratorio. Un nucleósido purificado se protege para crear una fosforamidita, que luego se puede usar para obtener análogos que no se encuentran en la naturaleza y/o para sintetizar un oligonucleótido.
In vivo, los nucleótidos pueden sintetizarse de novo o reciclarse a través de vías de recuperación.Los componentes utilizados en la síntesis de nucleótidos de novo se derivan de precursores biosintéticos del metabolismo de carbohidratos y aminoácidos, y de amoníaco y dióxido de carbono. El hígado es el órgano principal de la síntesis de novo de los cuatro nucleótidos. La síntesis de novo de pirimidinas y purinas sigue dos vías diferentes. Las pirimidinas se sintetizan primero a partir de aspartato y carbamoil-fosfato en el citoplasma hasta el ácido orótico de estructura de anillo precursor común, al que se une covalentemente una unidad de ribosilo fosforilada. Sin embargo, las purinas se sintetizan primero a partir de la plantilla de azúcar en la que se produce la síntesis del anillo. Como referencia, las síntesis de los nucleótidos de purina y pirimidina son realizadas por varias enzimas en el citoplasma de la célula, no dentro de un orgánulo específico.
Síntesis de ribonucleótidos de pirimidina
La síntesis de las pirimidinas CTP y UTP ocurre en el citoplasma y comienza con la formación de carbamoil fosfato a partir de glutamina y CO 2. A continuación, la aspartato carbamoiltransferasa cataliza una reacción de condensación entre el aspartato y el carbamoil fosfato para formar ácido carbamoil aspártico, que es ciclado en ácido 4,5-dihidroorótico por la dihidroorotasa. Este último se convierte en orotato por la dihidroorotato oxidasa. La reacción neta es:( S )-Dihidroorotato + O 2 → Orotato + H 2 O 2
El orotato está unido covalentemente con una unidad de ribosilo fosforilada. El enlace covalente entre la ribosa y la pirimidina ocurre en la posición C 1 de la unidad de ribosa, que contiene un pirofosfato, y N 1 del anillo de pirimidina. La orotato fosforribosiltransferasa (PRPP transferasa) cataliza la reacción neta que produce monofosfato de orotidina (OMP):Orotato + 5-fosfo-α-D-ribosa 1-difosfato (PRPP) → Orotidina 5'-fosfato + pirofosfato
El 5'-monofosfato de orotidina es descarboxilado por la descarboxilasa de 5'-fosfato de orotidina para formar monofosfato de uridina (UMP). PRPP transferasa cataliza las reacciones de ribosilación y descarboxilación, formando UMP a partir de ácido orótico en presencia de PRPP. Es de UMP que se derivan otros nucleótidos de pirimidina. UMP es fosforilado por dos quinasas a trifosfato de uridina (UTP) a través de dos reacciones secuenciales con ATP. Primero, se produce el difosfato de UDP, que a su vez se fosforila a UTP. Ambos pasos son alimentados por hidrólisis de ATP:ATP + UDP → ADP + UDPUDP + ATP → UTP + ADP
Posteriormente, CTP se forma por la aminación de UTP por la actividad catalítica de la CTP sintetasa. La glutamina es el donante de NH 3 y la reacción también es impulsada por la hidrólisis de ATP:UTP + Glutamina + ATP + H 2 O → CTP + ADP + P i
El monofosfato de citidina (CMP) se deriva del trifosfato de citidina (CTP) con la consiguiente pérdida de dos fosfatos.
Síntesis de ribonucleótidos de purina
Los átomos que se utilizan para construir los nucleótidos de purina provienen de una variedad de fuentes:
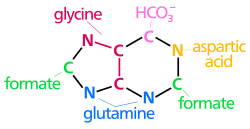 | Los orígenes biosintéticos de los átomos del anillo de purina N 1 surgen del grupo amina de Asp C 2 y C 8 se originan del formiato N 3 y N 9 son aportados por el grupo amida de Gln C 4, C 5 y N 7 se derivan de Gly C 6 proviene de HCO 3 (CO 2 ) |
La síntesis de novo de los nucleótidos de purina mediante la cual estos precursores se incorporan al anillo de purina procede por una vía de 10 pasos hasta el intermedio IMP del punto de ramificación, el nucleótido de la base hipoxantina. El AMP y el GMP se sintetizan posteriormente a partir de este intermedio a través de vías separadas de dos pasos. Por lo tanto, los restos de purina se forman inicialmente como parte de los ribonucleótidos en lugar de como bases libres.
Seis enzimas participan en la síntesis de IMP. Tres de ellos son multifuncionales:
- GART (reacciones 2, 3 y 5)
- PAICS (reacciones 6 y 7)
- ATIC (reacciones 9 y 10)
El camino comienza con la formación de PRPP. PRPS1 es la enzima que activa R5P, que se forma principalmente por la vía de las pentosas fosfato, a PRPP al reaccionar con ATP. La reacción es inusual porque un grupo pirofosforilo se transfiere directamente del ATP al C 1 de R5P y el producto tiene la configuración α alrededor de C1. Esta reacción también se comparte con las vías para la síntesis de Trp, His y los nucleótidos de pirimidina. Al estar en una importante encrucijada metabólica y requerir mucha energía, esta reacción está altamente regulada.
En la primera reacción exclusiva de la biosíntesis de nucleótidos de purina, PPAT cataliza el desplazamiento del grupo pirofosfato de PRPP (PP i ) por un nitrógeno de amida donado de glutamina (N), glicina (N&C), aspartato (N), ácido fólico (C 1 ) o CO2 . Este es el paso comprometido en la síntesis de purinas. La reacción ocurre con la inversión de la configuración alrededor de la ribosa C 1, formando así β -5-fosforibosilamina (5-PRA) y estableciendo la forma anomérica del futuro nucleótido.
A continuación, se incorpora una glicina impulsada por la hidrólisis de ATP, y el grupo carboxilo forma un enlace amina con el NH 2 previamente introducido. A continuación, se añade una unidad de un carbono procedente de la coenzima N10 -formil-THF del ácido fólico al grupo amino de la glicina sustituida, seguido del cierre del anillo de imidazol. A continuación, se transfiere un segundo grupo NH 2 de la glutamina al primer carbono de la unidad de glicina. Se añade concomitantemente una carboxilación del segundo carbono de la unidad de glicina. Este nuevo carbono se modifica mediante la adición de un tercer NH 2unidad, esta vez transferida de un residuo de aspartato. Finalmente, se agrega una segunda unidad de un carbono de formil-THF al grupo de nitrógeno y el anillo se cierra covalentemente para formar el monofosfato de inosina precursor común de purina (IMP).
El monofosfato de inosina se convierte en monofosfato de adenosina en dos pasos. Primero, la hidrólisis de GTP alimenta la adición de aspartato a IMP por la adenilosuccinato sintasa, sustituyendo el oxígeno del carbonilo por nitrógeno y formando el adenilosuccinato intermedio. A continuación, el fumarato se escinde formando monofosfato de adenosina. Este paso es catalizado por la adenilosuccinato liasa.
El monofosfato de inosina se convierte en monofosfato de guanosina mediante la oxidación de IMP formando xantilato, seguido de la inserción de un grupo amino en C2 . NAD es el aceptor de electrones en la reacción de oxidación. La transferencia del grupo amida de la glutamina es impulsada por la hidrólisis de ATP.
Degradación de pirimidinas y purinas
En humanos, los anillos de pirimidina (C, T, U) pueden degradarse completamente a CO 2 y NH 3 (excreción de urea). Dicho esto, los anillos de purina (G, A) no pueden. En cambio, se degradan al ácido úrico metabólicamente inerte que luego se excreta del cuerpo. El ácido úrico se forma cuando el GMP se divide en la base guanina y ribosa. La guanina se desamina a xantina, que a su vez se oxida a ácido úrico. Esta última reacción es irreversible. De manera similar, el ácido úrico se puede formar cuando el AMP se desamina a IMP, del cual se elimina la unidad de ribosa para formar hipoxantina. La hipoxantina se oxida a xantina y finalmente a ácido úrico. En lugar de la secreción de ácido úrico, la guanina y el IMP se pueden utilizar con fines de reciclaje y síntesis de ácidos nucleicos en presencia de PRPP y aspartato (NH 3donante).
Síntesis prebiótica de nucleótidos
Las teorías sobre cómo surgió la vida requieren el conocimiento de las vías químicas que permiten la formación de los componentes básicos de la vida en condiciones prebióticas plausibles. La hipótesis del mundo del ARN sostiene que en la sopa primordial existían ribonucleótidos flotantes, las moléculas fundamentales que se combinan en serie para formar el ARN. Las moléculas complejas como el ARN debieron surgir de moléculas pequeñas cuya reactividad estaba gobernada por procesos físico-químicos. El ARN está compuesto de nucleótidos de purina y pirimidina, los cuales son necesarios para la transferencia confiable de información y, por lo tanto, para la evolución darwiniana. Becker et al. mostró cómo los nucleósidos de pirimidina se pueden sintetizar a partir de moléculas pequeñas y ribosa, impulsados únicamente por ciclos húmedo-seco. Los nucleósidos de purina se pueden sintetizar por una vía similar. Los 5'-mono- y di-fosfatos también se forman selectivamente a partir de minerales que contienen fosfato, lo que permite la formación simultánea de polirribonucleótidos con las bases de purina y pirimidina. Por lo tanto, se puede establecer una red de reacción hacia los bloques de construcción de ARN de purina y pirimidina a partir de moléculas volcánicas o atmosféricas simples.
Par de bases no naturales (UBP)
Un par de bases no naturales (UBP) es una subunidad diseñada (o nucleobase) de ADN que se crea en un laboratorio y no ocurre en la naturaleza. Los ejemplos incluyen d5SICS y dNaM. Estos nucleótidos artificiales que contienen nucleobases hidrofóbicas presentan dos anillos aromáticos fusionados que forman un complejo (d5SICS–dNaM) o un par de bases en el ADN. Se ha inducido a E. coli a replicar un plásmido que contiene UBP a lo largo de varias generaciones. Este es el primer ejemplo conocido de un organismo vivo que transmite un código genético ampliado a las generaciones posteriores.
Aplicaciones médicas de los nucleótidos sintéticos
Varios derivados de nucleótidos se han utilizado como antivirales contra la hepatitis y el VIH. Tenofovir disoproxil, Tenofovir alafenamide y Sofosbuvir son ejemplos de NRTI utilizados contra la hepatitis. Mientras que ciertos medicamentos como Mericitabina, Lamivudina, Entecavir y Telbivudina, por ejemplo, son nucleósidos, pero se metabolizan en sus formas de nucleótidos bioactivos a través de la fosforilación.
Unidad de longitud
El nucleótido (abreviado "nt") es una unidad común de longitud para los ácidos nucleicos monocatenarios, similar a cómo el par de bases es una unidad de longitud para los ácidos nucleicos bicatenarios.
Códigos de abreviaturas para bases degeneradas
La IUPAC ha designado los símbolos de los nucleótidos. Además de las cinco bases (A, G, C, T/U), a menudo se utilizan bases degeneradas especialmente para diseñar cebadores de PCR. Estos códigos de nucleótidos se enumeran aquí. Algunas secuencias de cebadores también pueden incluir el carácter "I", que codifica el nucleótido inosina no estándar. La inosina se produce en los ARNt y se emparejará con adenina, citosina o timina. Sin embargo, este carácter no aparece en la siguiente tabla porque no representa una degeneración. Si bien la inosina puede cumplir una función similar a la degeneración "D", es un nucleótido real, en lugar de una representación de una mezcla de nucleótidos que cubre cada posible emparejamiento necesario.
| Símbolo | Descripción | Bases representadas | ||||
|---|---|---|---|---|---|---|
| UN | una denina | UN | 1 | |||
| C | citosina _ | C | ||||
| GRAMO | Guanina _ | GRAMO | ||||
| T | t himina | T | ||||
| tu | eres racil | tu | ||||
| W | débil _ | UN | T | 2 | ||
| S | fuerte _ | C | GRAMO | |||
| METRO | un niño _ | UN | C | |||
| k | k eto | GRAMO | T | |||
| R | pu r ina | UN | GRAMO | |||
| Y | pirimidina _ _ | C | T | |||
| B | no A ( B viene después de A) | C | GRAMO | T | 3 | |
| D | no C ( D viene después de C) | UN | GRAMO | T | ||
| H | no G ( H viene después de G) | UN | C | T | ||
| V | no T ( V viene después de T y U) | UN | C | GRAMO | ||
| norte | una base n y (no un espacio) | UN | C | GRAMO | T | 4 |
Contenido relacionado
Solanum
Cisne
Cronología de la agricultura y la tecnología alimentaria