Norma interna
En un análisis químico, el método del estándar interno implica agregar la misma cantidad de una sustancia química a cada muestra y solución de calibración. El estándar interno responde proporcionalmente a los cambios en el analito y proporciona una señal de medición similar, pero no idéntica. También debe estar ausente de la matriz de la muestra para garantizar que no haya otra fuente del estándar interno presente. Tomando la relación entre la señal del analito y la señal del estándar interno y graficandola contra las concentraciones del analito en las soluciones de calibración se obtendrá una curva de calibración. La curva de calibración se puede utilizar luego para calcular la concentración del analito en una muestra desconocida.
La selección de un estándar interno adecuado tiene en cuenta las fuentes aleatorias y sistemáticas de incertidumbre que surgen durante la preparación de la muestra o la fluctuación del instrumento. Esto se debe a que la relación entre el analito y la cantidad de estándar interno es independiente de estas variaciones. Si el valor medido del analito se desplaza por error por encima o por debajo del valor real, las mediciones del estándar interno deberían desplazarse en la misma dirección.
El gráfico de proporción proporciona una buena manera de compensar la variación de la sensibilidad del detector, pero puede estar sesgado y debe reemplazarse por cálculos de concentración relativa/calibración relativa si la razón de la variabilidad de la respuesta es una masa diferente de la muestra analizada y la curva de calibración tradicional (no la del estándar interno) de cualquier analito no es lineal a través del origen.
Historia
El primer uso registrado del método del patrón interno se remonta al trabajo de Gouy sobre espectroscopia de llama en 1877, donde utilizó un patrón interno para determinar si la excitación en su llama era constante. Su procedimiento experimental se reintrodujo más tarde en la década de 1940, cuando los fotómetros de llama con registro se hicieron fácilmente disponibles. El uso de patrones internos continuó creciendo y se aplicó a una amplia gama de técnicas analíticas, incluida la espectroscopia de resonancia magnética nuclear (RMN), la cromatografía y la espectroscopia de plasma acoplado inductivamente.
Aplicaciones
Espectroscopia de resonancia magnética nuclear
En la espectroscopia de RMN, por ejemplo, de los núcleos 1H, 13C y 29Si, las frecuencias dependen del campo magnético, que no es el mismo en todos los experimentos. Por lo tanto, las frecuencias se informan como diferencias relativas al tetrametilsilano (TMS), un estándar interno que George Tiers propuso en 1958 y que la Unión Internacional de Química Pura y Aplicada ha respaldado desde entonces. La diferencia relativa con el TMS se denomina desplazamiento químico.
El TMS funciona como un estándar ideal porque es relativamente inerte y sus protones de metilo idénticos producen una señal fuerte en el campo, aislada de la mayoría de los demás protones. Es soluble en la mayoría de los solventes orgánicos y se puede eliminar por destilación debido a su bajo punto de ebullición.
En la práctica, se conoce la diferencia entre las señales de los disolventes comunes y las de TMS. Por lo tanto, no es necesario añadir TMS a los disolventes deuterados comerciales, ya que los instrumentos modernos son capaces de detectar las pequeñas cantidades de disolvente protonado presentes. Al especificar el disolvente de bloqueo que se utilizará, los espectrómetros modernos pueden referenciar correctamente la muestra; de hecho, el propio disolvente sirve como estándar interno.
Cromatografía
En cromatografía, los estándares internos se utilizan para determinar la concentración de otros analitos mediante el cálculo del factor de respuesta. El estándar interno seleccionado debe tener un tiempo de retención y derivatización similar. Debe ser estable y no interferir con los componentes de la muestra. Esto mitiga la incertidumbre que puede producirse en los pasos preparatorios, como la inyección de la muestra.
En la cromatografía de gases-espectrometría de masas (GC-MS), los compuestos deuterados con estructuras similares a las del analito actúan habitualmente como estándares internos eficaces. Sin embargo, existen estándares internos no deuterados, como la norleucina, que es popular en el análisis de aminoácidos porque se puede separar de los picos que la acompañan.
La selección de un estándar interno para cromatografía líquida-espectrometría de masas (LC-MS) depende del método de ionización empleado. El estándar interno necesita una respuesta de ionización y un patrón de fragmentación comparables a los del analito. Los estándares internos de LC-MS suelen ser isotópicamente análogos a la estructura del analito, y utilizan isótopos como el deuterio (2H), 13C, 15N y 18O.
plasma acoplado inductivamente
Seleccionar un estándar interno en la espectroscopia de plasma acoplado inductivamente puede ser difícil, porque las señales de la matriz de la muestra pueden superponerse con las que pertenecen al analito. El itrio es un estándar interno común que está naturalmente ausente en la mayoría de las muestras. Tiene una masa de rango medio y líneas de emisión que no interfieren con muchos analitos. La intensidad de la señal de itrio es con lo que se compara la señal del analito.
En la espectrometría de masas con plasma acoplado inductivamente (ICP-MS), las especies con una masa similar a la del analito suelen servir como buenos estándares internos, aunque no en todos los casos. Los factores que también contribuyen a la eficacia de un estándar interno en la ICP-MS incluyen la proximidad de su potencial de ionización, el cambio de entalpía y el cambio de entropía con el analito.
Los estándares internos de la espectroscopia de emisión óptica con plasma acoplado inductivamente (ICP-OES) se pueden seleccionar observando cómo cambian las señales del analito y del estándar interno con distintas condiciones experimentales. Esto incluye realizar ajustes en la matriz de muestra o en la configuración de la instrumentación y evaluar si el estándar interno seleccionado está reaccionando de la misma manera que el analito.
Ejemplo del método estándar interno
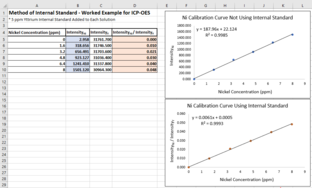
Una forma de visualizar el método de estándar interno es crear una curva de calibración que no utilice el método y una curva de calibración que sí lo utilice. Supongamos que existen concentraciones conocidas de níquel en un conjunto de soluciones de calibración: 0 ppm, 1,6 ppm, 3,2 ppm, 4,8 ppm, 6,4 ppm y 8 ppm. Cada solución también tiene 5 ppm de itrio para actuar como estándar interno. Si estas soluciones se miden utilizando ICP-OES, la intensidad de la señal de itrio debería ser constante en todas las soluciones. De lo contrario, es probable que la intensidad de la señal de níquel también sea imprecisa.
La curva de calibración que no utiliza el método de patrón interno ignora la incertidumbre entre mediciones. El coeficiente de determinación (R2) para esta gráfica es 0,9985.
En la curva de calibración que utiliza el estándar interno, el eje y es la relación entre la señal de níquel y la señal de itrio. Esta relación no se ve afectada por la incertidumbre en las mediciones de níquel, como debería afectar a las mediciones de itrio de la misma manera. Esto da como resultado un R2 más alto, 0,9993.
Referencias
- ^ a b c d e f Skoog, Douglas A. (2018). Principios de análisis instrumental. F. James Holler, Stanley R. Crouch (7th ed.). Australia: Cengage Learning. ISBN 978-1-305-57721-3. OCLC 986919158.
- ^ Kalambet, Yuri; Kozmin, Yuri (18 de diciembre de 2018). "Aritmética estándar interna implementada como concentración relativa/calibración relativa". Journal of Chemometrics. 33 (6): 1–7. doi:10.1002/cem.3106.
- ^ a b Burns, D. Thorburn; Walker, Michael J. (2019-05-01). "Originas del método de adiciones estándar y del uso de un estándar interno en análisis químicos instrumental cuantitativos". Química analítica y bioanalítica. 411 (13): 2749–2753. doi:10.1007/s00216-019-01754-w. ISSN 1618-2650. PMC 6522454. PMID 30941480.
- ^ Gouy, M. (1880). "Recherches photométriques sur les flammes colorée". Journal de Physique Théorique et Appliquée (en francés). 9 (1): 19–27. doi:10.1051/jphystap:01880009001901. ISSN 0368-3893. S2CID 178492346.
- ^ Tiers, George Van Dyke (1958-09-01). "Resonancia nuclear confiable Valores de Escudo por "Referencia Interna" con Tetrametil-silano". El Diario de Química Física. 62 (9): 1151–1152. doi:10.1021/j150567a041. ISSN 0022-3654.
- ^ Harris, Robin K.; Becker, Edwin D.; Cabral de Menezes, Sonia M.; Goodfellow, Robin; Granger, Pierre (2001-01-01). "Nomenclatura NMR. Propiedades y convenciones de giro nuclear para cambios químicos (Recomendaciones IUPAC 2001)". Química pura y aplicada. 73 (11): 1795–1818. doi:10.1351/pac200173111795. ISSN 1365-3075. S2CID 95765050.
- ^ a b Guzman, Alexander L.; Hoye, Thomas R. (2022-01-21). "TMS es superior a residual C H Cl 3 para uso como referencia interna para la rutina 1 H NMR Spectra grabado en CDCl 3". The Journal of Organic Chemistry. 87 (2): 905-909. doi:10.1021/acs.joc.1c02590. ISSN 0022-3263. S2CID 245651135.
- ^ Unice, Kenneth M.; Kreider, Marisa L.; Panko, Julie M. (2012-11-08). "Uso de un Estándar Interno Deuterado con Pyrolysis-GC/MS Dimeric Marker Analysis to Quantify Tire Tread Particles in the Environment". International Journal of Environmental Research and Public Health. 9 (11): 4033–4055. doi:10.3390/ijerph9114033. ISSN 1660-4601. PMC 3524611. PMID 23202830.
- ^ Fico, D.; Margapoti, E.; Pennetta, A.; De Benedetto, G. E. (2018-04-01). "Procedimiento de GC/MS mejorado para la identificación de proteínas en microsamplos de pintura". Journal of Analytical Methods in Chemistry. 2018: e6032084. doi:10.1155/2018/6032084. ISSN 2090-8865. PMC 5902064. PMID 29805835.
- ^ Pons, Alexandre; Richet, Colette; Robbe, Catherine; Herrmann, Annkatrin; Timmerman, Philippe; Huet, Guillemette; Leroy, Yves; Carlstedt, Ingemar; Capon, Calliope; Zanetta, Jean-Pierre (2003-07-01). "Sequential GC/MS Analysis of Sialic Acids, Monosaccharides, and Amino Acids of Glycoproteins on a Single Sample as Heptafluorobutyrate Derivatives". Bioquímica. 42 (27): 8342–8353. doi:10.1021/bi034250e. ISSN 0006-2960.
- ^ Harduf, Z.; Bielorai, R.; Alumot, E. (1977-09-11). "Norleucine —un estándar interno para la columna básica utilizada en el análisis de aminoácidos fisiológicos". Journal of Chromatography A. 139 (1): 215–217. doi:10.1016/S0021-9673(01)84148-0. ISSN 0021-9673. PMID 893614.
- ^ "Internal Standard an Important Analyte Use in Drug Analysis by Liquid Chromatography Mass Spectrometry- An Article". International Journal of Pharmaceutical and Bio Medical Science2022-01-13. doi:10.47191/ijpbms/v2-i1-02. S2CID 245957199.
- ^ Grocholska, Paulina; Bąchor, Remigiusz (2021-05-18). "Trends in the Hydrogen−Deuterium Exchange at the Carbon Centers. Preparación de Normas Internas para Análisis Cuantitativo por LC-MS". Molecules. 26 (10): 2989. doi:10.3390/molecules26102989. ISSN 1420-3049. PMC 8157363. PMID 34069879.
- ^ Zachariadis, G. A.; Vogiatzis, C. (2010-05-17). "Una visión general del uso de Yttrium para la estandarización interna en la Espectrometría de Emisión Atómica de Plasma". Reseñas de espectroscopia aplicadas. 45 (3): 220–239. Código:2010ApSRv..45..220Z. doi:10.1080/05704921003719122. ISSN 0570-4928. S2CID 98458774.
- ^ Finley-Jones, Haley J.; Molloy, John L.; Holcombe, James A. (2008-08-06). "Eligiendo estándares internos basados en un enfoque de análisis multivariado con ICP(TOF)MS". Journal of Analytical Atomic Spectrometry. 23 (9): 1214–1222. doi:10.1039/B804048F. ISSN 1364-5544.
- ^ Sedcole, J. R.; Lee, J.; Pritchard, M. W. (1986-01-01). "Selección interna estándar en presencia de interacciones matriz en un plasma argón inductivamente unido optimizado para el análisis multielemento simultáneo por espectrometría de emisión atómica". Spectrochimica Acta Parte B: Espectroscopia atómica. 41 (3): 227–235.Bibcode:1986AcSpe..41..227S. doi:10.1016/0584-8547(86)80162-8. ISSN 0584-8547.