Nitruro de boro
El nitruro de boro es un compuesto refractario de boro y nitrógeno resistente térmica y químicamente con la fórmula química BN. Existe en varias formas cristalinas que son isoelectrónicas a una red de carbono de estructura similar. La forma hexagonal correspondiente al grafito es la más estable y blanda de los polimorfos BN, por lo que se utiliza como lubricante y aditivo en productos cosméticos. La variedad cúbica (zincblenda, también conocida como estructura de esfalerita) análoga al diamante se llama c-BN; es más blando que el diamante, pero su estabilidad térmica y química es superior. La rara modificación BN de wurtzita es similar a la lonsdaleita pero ligeramente más suave que la forma cúbica.
Debido a su excelente estabilidad térmica y química, las cerámicas de nitruro de boro se utilizan en equipos de alta temperatura y fundición de metales. El nitruro de boro tiene un uso potencial en nanotecnología.
Estructura
El nitruro de boro existe en múltiples formas que difieren en la disposición de los átomos de boro y nitrógeno, lo que da lugar a diferentes propiedades a granel del material.
Forma amorfa (a-BN)
La forma amorfa del nitruro de boro (a-BN) no es cristalina y carece de regularidad a larga distancia en la disposición de sus átomos. Es análogo al carbono amorfo.
Todas las demás formas de nitruro de boro son cristalinas.
Forma hexagonal (h-BN)
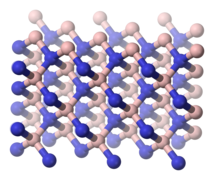
La forma cristalina más estable es la hexagonal, también denominada h-BN, α-BN, g-BN y nitruro de boro grafítico. El nitruro de boro hexagonal (grupo puntual = D6h; grupo espacial = P63/mmc) tiene una estructura en capas similar al grafito. Dentro de cada capa, los átomos de boro y nitrógeno están unidos por fuertes enlaces covalentes, mientras que las capas se mantienen unidas por fuerzas débiles de van der Waals. La capa intermedia "registro" de estas láminas difiere, sin embargo, del patrón visto para el grafito, porque los átomos están eclipsados, con átomos de boro que se encuentran por encima de los átomos de nitrógeno. Este registro refleja la polaridad local de los enlaces B-N, así como las características del donante de N/aceptor de B entre capas. Del mismo modo, existen muchas formas metaestables que consisten en politipos apilados de manera diferente. Por lo tanto, h-BN y el grafito son vecinos muy cercanos, y el material puede acomodar el carbono como elemento sustituyente para formar BNC. Se han sintetizado híbridos BC6N, donde el carbono sustituye a algunos átomos de B y N.
Forma cúbica (c-BN)
El nitruro de boro cúbico tiene una estructura cristalina análoga a la del diamante. De acuerdo con que el diamante es menos estable que el grafito, la forma cúbica es menos estable que la forma hexagonal, pero la tasa de conversión entre las dos es insignificante a temperatura ambiente, como lo es para el diamante. La forma cúbica tiene la estructura cristalina de esfalerita, la misma que la del diamante (con átomos de B y N ordenados), y también se denomina β-BN o c-BN.
Forma wurtzita (w-BN)
La forma de wurtzita del nitruro de boro (w-BN; grupo puntual = C6v; grupo espacial = P63mc) tiene la misma estructura que la lonsdaleita, una rara polimorfo hexagonal del carbono. Como en la forma cúbica, los átomos de boro y nitrógeno se agrupan en tetraedros. En la forma de wurtzita, los átomos de boro y nitrógeno se agrupan en anillos de 6 miembros. En la forma cúbica todos los anillos están en configuración de silla, mientras que en w-BN los anillos entre 'capas' están en configuración de barco. Informes optimistas anteriores predijeron que la forma de wurtzita era muy fuerte, y una simulación estimó que potencialmente tenía una fuerza un 18% más fuerte que la del diamante. Dado que solo existen pequeñas cantidades del mineral en la naturaleza, esto aún no se ha verificado experimentalmente. Su dureza es de 46 GPa, ligeramente más dura que los boruros comerciales pero más blanda que la forma cúbica del nitruro de boro.
Propiedades
Física
(feminine)| Material | Nitruro de hierro (BN) | Gráfico | Diamante | |||
|---|---|---|---|---|---|---|
| a- | h- | c- | w- | |||
| Densidad (g/cm3) | 2.28 | ~2.1 | 3.45 | 3.49 | ~2.1 | 3.515 |
| Dureza Knoop (GPa) | 10 | 45 | 34 | 100 | ||
| Bulk modulus (GPa) | 100 | 36,5 | 400 | 400 | 34 | 440 |
| Conductividad térmica (W/m·K) | 3 | 600 ∥, 30 ⟂ | 740 | 200-2000 ∥, 2-800 ⟂ | 600 a 2000 | |
| Expansión térmica (10)−6/K) | −2.7 ∥, 38 ⟂ | 1.2 | 2.7 | −1.5 ∥, 25 ⟂ | 0,8 | |
| Distancia de banda (eV) | 5.05 | 5.9-6.4 | 6.4 | 4.5–5.5 | 0 | 5,5 |
| Índice de referencia | 1.7 | 1.8 | 2.1 | 2.05 | 2.4 | |
| Susceptibilidad magnética (μemu/g) | −0.48 ∥, −17.3 ⟂ | −0.2 – −2.7 ∥, −20 - −28 ⟂ | −1.6 | |||
La estructura parcialmente iónica de las capas de BN en h-BN reduce la covalencia y la conductividad eléctrica, mientras que la interacción entre capas aumenta, lo que da como resultado una mayor dureza de h-BN en relación con el grafito. La deslocalización de electrones reducida en hexagonal-BN también se indica por su ausencia de color y una gran brecha de banda. Enlaces muy diferentes (covalente fuerte dentro de los planos basales (planos donde los átomos de boro y nitrógeno están unidos covalentemente) y débil entre ellos) provoca una anisotropía alta de la mayoría de las propiedades de h-BN.
Por ejemplo, la dureza, la conductividad eléctrica y térmica son mucho más altas dentro de los planos que perpendiculares a ellos. Por el contrario, las propiedades de c-BN y w-BN son más homogéneas e isotrópicas.
Esos materiales son extremadamente duros; la dureza del c-BN a granel es ligeramente menor y la del w-BN es incluso mayor que la del diamante. También se informa que el c-BN policristalino con tamaños de grano del orden de 10 nm tiene una dureza Vickers comparable o superior a la del diamante. Debido a una estabilidad mucho mejor al calor y a los metales de transición, el c-BN supera al diamante en aplicaciones mecánicas, como el mecanizado de acero. La conductividad térmica de BN se encuentra entre las más altas de todos los aisladores eléctricos (ver tabla).
El nitruro de boro se puede dopar tipo p con berilio y tipo n con boro, azufre, silicio o si se co-dopa con carbono y nitrógeno. Tanto el BN hexagonal como el cúbico son semiconductores de brecha amplia con una energía de brecha correspondiente a la región UV. Si se aplica voltaje a h-BN o c-BN, emite luz ultravioleta en el rango de 215 a 250 nm y, por lo tanto, puede usarse potencialmente como diodos emisores de luz (LED) o láser.
Se sabe poco sobre el comportamiento de fusión del nitruro de boro. Se sublima a 2973 °C a presión normal liberando gas nitrógeno y boro, pero se funde a presión elevada.
Estabilidad térmica
BN hexagonal y cúbico (y probablemente w-BN) muestran notables estabilidades químicas y térmicas. Por ejemplo, h-BN es estable a la descomposición a temperaturas de hasta 1000 °C en el aire, 1400 °C en el vacío y 2800 °C en una atmósfera inerte. La reactividad de h-BN y c-BN es relativamente similar, y los datos para c-BN se resumen en la siguiente tabla.
| Sólido | Ambient | Medida | Temperatura Umbral (°C) |
|---|---|---|---|
| Mo | 10−2Pa vacío | Reacción | 1360 |
| Ni | 10−2Pa vacío | Wetting | 1360 |
| Fe, Ni, Co | Argon | Reacción | 1400-1500 |
| Al | 10−2Pa vacío | Sentimiento y reacción | 1050 |
| Si | 10−3Pa vacío | Wetting | 1500 |
| Cu, Ag, Au, Ga, In, Ge, Sn | 10−3Pa vacío | No mojar | 1100 |
| B | No mojar | 2200 | |
| Al2O3 + B2O3 | 10−2Pa vacío | No hay reacción | 1360 |
La estabilidad térmica de c-BN se puede resumir de la siguiente manera:
- En el aire o el oxígeno: B2O3 capa protectora evita una mayor oxidación a ~1300 °C; ninguna conversión a forma hexagonal a 1400 °C.
- En nitrógeno: cierta conversión a h-BN a 1525 °C después de 12 h.
- En vacío10; 5 -Pa): conversión a h-BN a 1550–1600 °C.
Estabilidad química
El nitruro de boro es insoluble en los ácidos habituales, pero es soluble en sales fundidas alcalinas y nitruros, como LiOH, KOH, NaOH-Na2CO3, NaNO3, Li3N, Mg3N2, Sr3N2, Ba3N2 o Li3BN2, por lo que se utilizan para grabar BN.
Conductividad térmica
La conductividad térmica teórica de las nanocintas de nitruro de boro hexagonal (BNNR) puede acercarse a 1700-2000 W/(m⋅K), que tiene el mismo orden de magnitud que el valor experimental medido para el grafeno y puede ser comparable al teórico Cálculos para nanocintas de grafeno. Además, el transporte térmico en las BNNR es anisotrópico. La conductividad térmica de los BNNR con bordes en zigzag es aproximadamente un 20 % mayor que la de las nanocintas con bordes de sillón a temperatura ambiente.
Ocurrencia natural
En 2009, se informó sobre un mineral de nitruro de boro natural en forma cúbica (c-BN) en el Tíbet, y se propuso el nombre de qingsongita. La sustancia se encontró en inclusiones dispersas de tamaño micrométrico en rocas ricas en cromo. En 2013, la Asociación Mineralógica Internacional afirmó el mineral y el nombre.
Síntesis
Preparación y reactividad de BN hexagonal
El nitruro de boro se produce sintéticamente. El nitruro de boro hexagonal se obtiene mediante la reacción del trióxido de boro (B2O3) o ácido bórico (H3BO3) con amoniaco (NH3) o urea (CO(NH2)2 ) en una atmósfera de nitrógeno:
- B2O3 + 2 NH3 → 2 BN + 3 H2O ()T = 900 °C)
- B(OH)3 + NH3 → BN + 3 H2O ()T = 900 °C)
- B2O3 + CO(NH)2)2 → 2 BN + CO2 + 2 H2O ()T Ø 1000 °C)
- B2O3 + 3 CaB6 + 10 N2 → 20 BN + 3 CaO ()T √ 1500 °C)
El nitruro de boro desordenado (amorfo) resultante contiene 92–95 % de BN y 5–8 % de B2O 3. Los restantes B2O3 puede evaporarse en un segundo paso a temperaturas > 1500 °C para lograr una concentración de BN >98%. Tal recocido también cristaliza BN, aumentando el tamaño de los cristalitos con la temperatura de recocido.
Las piezas h-BN se pueden fabricar de forma económica mediante prensado en caliente con mecanizado posterior. Las piezas están fabricadas con polvos de nitruro de boro añadiendo óxido de boro para una mejor compresibilidad. Se pueden obtener películas delgadas de nitruro de boro por deposición química de vapor a partir de precursores de tricloruro de boro y nitrógeno. La combustión de polvo de boro en plasma de nitrógeno a 5500 °C produce nitruro de boro ultrafino que se utiliza para lubricantes y tóneres.
El nitruro de boro reacciona con el fluoruro de yodo en el triclorofluorometano a -30 °C para producir un explosivo de contacto extremadamente sensible, NI3, en bajo rendimiento. El nitruro de boro reacciona con nitruros de litio, metales alcalinotérreos y lantánidos para formar compuestos de nitruroborato. Por ejemplo:
- Li3N + BN → Li3BN2
Intercalación de BN hexagonales
Al igual que el grafito, se pueden intercalar varias moléculas, como NH3 o metales alcalinos en nitruro de boro hexagonal, que se inserta entre sus capas. Tanto el experimento como la teoría sugieren que la intercalación es mucho más difícil para el BN que para el grafito.
Preparación de BN cúbico
La síntesis de c-BN utiliza los mismos métodos que la del diamante: el nitruro de boro cúbico se produce mediante el tratamiento del nitruro de boro hexagonal a alta presión y temperatura, al igual que el diamante sintético se produce a partir del grafito. Se ha observado conversión directa de nitruro de boro hexagonal a la forma cúbica a presiones entre 5 y 18 GPa y temperaturas entre 1730 y 3230 °C, que son parámetros similares a los de la conversión directa de grafito-diamante. La adición de una pequeña cantidad de óxido de boro puede reducir la presión requerida a 4–7 GPa y la temperatura a 1500 °C. Al igual que en la síntesis de diamantes, para reducir aún más las presiones y temperaturas de conversión, se añade un catalizador, como el litio, el potasio o el magnesio, sus nitruros, sus fluoronitruros, agua con compuestos amónicos o hidrazina. Otros métodos de síntesis industrial, nuevamente tomados del crecimiento de diamantes, utilizan el crecimiento de cristales en un gradiente de temperatura u onda de choque explosiva. El método de ondas de choque se utiliza para producir un material llamado heterodiamante, un compuesto superduro de boro, carbono y nitrógeno.
Es posible la deposición a baja presión de películas delgadas de nitruro de boro cúbico. Como en el crecimiento del diamante, el principal problema es suprimir el crecimiento de las fases hexagonales (h-BN o grafito, respectivamente). Mientras que en el crecimiento de diamantes esto se logra agregando gas hidrógeno, el trifluoruro de boro se usa para c-BN. También se utilizan la deposición de haz de iones, la deposición de vapor químico mejorada con plasma, la deposición de láser pulsado, la pulverización catódica reactiva y otros métodos físicos de deposición de vapor.
Preparación de wurtzita BN
La wurtzita BN se puede obtener mediante métodos estáticos de alta presión o de choque dinámico. Los límites de su estabilidad no están bien definidos. Tanto c-BN como w-BN se forman comprimiendo h-BN, pero la formación de w-BN se produce a temperaturas mucho más bajas, cercanas a los 1700 °C.
Estadísticas de producción
Mientras que las cifras de producción y consumo de las materias primas utilizadas para la síntesis de BN, a saber, ácido bórico y trióxido de boro, son bien conocidas (ver boro), las cifras correspondientes para el nitruro de boro no se incluyen en los informes estadísticos. Una estimación para la producción mundial de 1999 es de 300 a 350 toneladas métricas. Los principales productores y consumidores de BN se encuentran en Estados Unidos, Japón, China y Alemania. En 2000, los precios variaron entre $75 y $120/kg para el h-BN de calidad industrial estándar y hasta $200-400/kg para los grados de BN de alta pureza.
Aplicaciones
BN hexagonal
El BN hexagonal (h-BN) es el polimorfo más utilizado. Es un buen lubricante tanto a bajas como a altas temperaturas (hasta 900 °C, incluso en atmósfera oxidante). El lubricante h-BN es particularmente útil cuando la conductividad eléctrica o la reactividad química del grafito (lubricante alternativo) serían problemáticas. En los motores de combustión interna, donde el grafito podría oxidarse y convertirse en lodo de carbón, se puede agregar h-BN con su estabilidad térmica superior al lubricante del motor; sin embargo, con todas las suspensiones de nanopartículas, el asentamiento del movimiento browniano es un problema y asentamiento clave. puede obstruir los filtros de aceite del motor, lo que limita la aplicación de lubricantes sólidos en un motor de combustión solo a configuraciones de carreras automotrices, donde la reconstrucción del motor es una práctica común. Dado que el carbono tiene una solubilidad apreciable en ciertas aleaciones (como los aceros), lo que puede conducir a la degradación de las propiedades, el BN suele ser superior para aplicaciones de alta temperatura y/o alta presión. Otra ventaja del h-BN sobre el grafito es que su lubricidad no requiere moléculas de agua o gas atrapadas entre las capas. Por lo tanto, los lubricantes h-BN se pueden usar incluso en vacío, p. en aplicaciones espaciales. Las propiedades lubricantes del h-BN de grano fino se utilizan en cosméticos, pinturas, cementos dentales y minas de lápices.
El BN hexagonal se utilizó por primera vez en cosmética alrededor de 1940 en Japón. Sin embargo, debido a su alto precio, pronto se abandonó el h-BN para esta aplicación. Su uso se revitalizó a fines de la década de 1990 con la optimización de los procesos de producción de h-BN, y actualmente h-BN es utilizado por casi todos los principales productores de productos cosméticos para bases, maquillaje, sombras de ojos, rubores, lápices kohl, lápices labiales y otros. Productos para el cuidado de la piel.
Debido a su excelente estabilidad térmica y química, la cerámica de nitruro de boro se usa tradicionalmente como parte de equipos de alta temperatura. h-BN se puede incluir en cerámicas, aleaciones, resinas, plásticos, cauchos y otros materiales, otorgándoles propiedades autolubricantes. Dichos materiales son adecuados para la construcción de, p. rodamientos y en la fabricación de acero. Los plásticos rellenos con BN tienen una menor expansión térmica, así como una mayor conductividad térmica y resistividad eléctrica. Debido a sus excelentes propiedades dieléctricas y térmicas, el BN se utiliza en electrónica, p. como sustrato para semiconductores, ventanas transparentes a las microondas, como relleno conductor del calor pero eléctricamente aislante en pastas térmicas y como material estructural para sellos. Muchos dispositivos cuánticos utilizan h-BN multicapa como material de sustrato. También se puede utilizar como dieléctrico en memorias resistivas de acceso aleatorio.
El BN hexagonal se utiliza en procesos xerográficos e impresoras láser como capa de barrera contra fugas de carga del tambor fotográfico. En la industria automotriz, el h-BN mezclado con un aglutinante (óxido de boro) se usa para sellar sensores de oxígeno, que brindan retroalimentación para ajustar el flujo de combustible. El aglutinante utiliza la estabilidad de temperatura única y las propiedades aislantes de h-BN.
Las piezas se pueden fabricar mediante prensado en caliente a partir de cuatro grados comerciales de h-BN. El grado HBN contiene un aglutinante de óxido de boro; se puede utilizar hasta 550–850 °C en atmósfera oxidante y hasta 1600 °C en vacío, pero debido al contenido de óxido de boro es sensible al agua. El grado HBR utiliza un aglutinante de borato de calcio y se puede utilizar a 1600 °C. Los grados HBC y HBT no contienen aglutinante y se pueden utilizar hasta 3000 °C.
Las nanoláminas de nitruro de boro (h-BN) se pueden depositar mediante descomposición catalítica de borazina a una temperatura de ~1100 °C en una configuración de deposición química de vapor, en áreas de hasta unos 10 cm2. Debido a su estructura atómica hexagonal, pequeño desajuste de red con el grafeno (~ 2%) y alta uniformidad, se utilizan como sustratos para dispositivos basados en grafeno. Las nanoláminas de BN también son excelentes conductoras de protones. Su alta tasa de transporte de protones, combinada con la alta resistencia eléctrica, puede dar lugar a aplicaciones en pilas de combustible y electrólisis de agua.
h-BN se ha utilizado desde mediados de la década de 2000 como lubricante para balas y ánimas en aplicaciones de rifle de precisión como alternativa al recubrimiento de disulfuro de molibdeno, comúnmente conocido como "moly". Se afirma que aumenta la vida útil efectiva del cañón, aumenta los intervalos entre la limpieza del orificio y disminuye la desviación en el punto de impacto entre los primeros disparos limpios y los disparos posteriores.
BN cúbico
El nitruro de boro cúbico (CBN o c-BN) se usa mucho como abrasivo. Su utilidad surge de su insolubilidad en hierro, níquel y aleaciones relacionadas a altas temperaturas, mientras que el diamante es soluble en estos metales. Por lo tanto, los abrasivos policristalinos c-BN (PCBN) se utilizan para mecanizar acero, mientras que los abrasivos de diamante son los preferidos para aleaciones de aluminio, cerámica y piedra. Cuando entra en contacto con el oxígeno a altas temperaturas, el BN forma una capa de pasivación de óxido de boro. El nitruro de boro se une bien a los metales, debido a la formación de capas intermedias de boruros o nitruros metálicos. Los materiales con cristales de nitruro de boro cúbico se utilizan a menudo en las brocas de las herramientas de corte. Para aplicaciones de esmerilado, aglutinantes más blandos, p. Se utilizan resinas, cerámicas porosas y metales blandos. También se pueden utilizar aglutinantes cerámicos. Los productos comerciales se conocen con los nombres "Borazon" (por Hyperion Materials & Technologies) y "Elbor" o "Cubonita" (por proveedores rusos).
A diferencia del diamante, los gránulos grandes de c-BN se pueden producir en un proceso simple (llamado sinterización) de recocido de polvos de c-BN en flujo de nitrógeno a temperaturas ligeramente por debajo de la temperatura de descomposición del BN. Esta capacidad de fusión de los polvos c-BN y h-BN permite la producción económica de piezas grandes de BN.
Al igual que el diamante, la combinación en c-BN de la más alta conductividad térmica y resistividad eléctrica es ideal para disipadores de calor.
Como el nitruro de boro cúbico consta de átomos ligeros y es muy resistente química y mecánicamente, es uno de los materiales populares para las membranas de rayos X: la baja masa da como resultado una pequeña absorción de rayos X y las buenas propiedades mecánicas permiten el uso de membranas delgadas membranas, reduciendo así aún más la absorción.
BN amorfa
(feminine)Las capas de nitruro de boro amorfo (a-BN) se utilizan en algunos dispositivos semiconductores, p. MOSFET. Se pueden preparar por descomposición química de tricloroborazina con cesio, o por métodos de deposición química térmica de vapor. La CVD térmica también se puede utilizar para la deposición de capas de h-BN, oa altas temperaturas, c-BN.
Otras formas de nitruro de boro
Nitruro de boro atómicamente delgado
El nitruro de boro hexagonal se puede exfoliar en láminas de una o pocas capas atómicas. Debido a su estructura análoga a la del grafeno, el nitruro de boro atómicamente delgado a veces se denomina grafeno blanco.
Propiedades mecánicas
El nitruro de boro atómicamente delgado es uno de los materiales aislantes eléctricos más resistentes. El nitruro de boro monocapa tiene un módulo de Young promedio de 0,865 TPa y una resistencia a la fractura de 70,5 GPa y, a diferencia del grafeno, cuya resistencia disminuye drásticamente con el aumento del espesor, las láminas de nitruro de boro de pocas capas tienen una resistencia similar a la de las monocapas. nitruro de boro.
Conductividad térmica
El nitruro de boro atómicamente delgado tiene uno de los coeficientes de conductividad térmica más altos (751 W/mK a temperatura ambiente) entre los semiconductores y aislantes eléctricos, y su conductividad térmica aumenta con un espesor reducido debido a un menor acoplamiento intracapa.
Estabilidad térmica
La estabilidad del aire del grafeno muestra una clara dependencia del espesor: el grafeno monocapa es reactivo al oxígeno a 250 °C, fuertemente dopado a 300 °C y grabado a 450 °C; por el contrario, el grafito a granel no se oxida hasta los 800 °C. El nitruro de boro atómicamente delgado tiene una resistencia a la oxidación mucho mejor que el grafeno. El nitruro de boro monocapa no se oxida hasta los 700 °C y puede soportar hasta 850 °C en el aire; Las nanoláminas de nitruro de boro bicapa y tricapa tienen temperaturas iniciales de oxidación ligeramente más altas. La excelente estabilidad térmica, la alta impermeabilidad a los gases y líquidos, y el aislamiento eléctrico hacen que el nitruro de boro sea atómicamente delgado como material de recubrimiento potencial para prevenir la oxidación y corrosión superficial de metales y otros materiales bidimensionales (2D), como el fósforo negro.
Mejor adsorción superficial
Se ha descubierto que el nitruro de boro atómicamente delgado tiene mejores capacidades de adsorción superficial que el nitruro de boro hexagonal a granel. De acuerdo con estudios teóricos y experimentales, el nitruro de boro atómicamente delgado como adsorbente experimenta cambios conformacionales en la adsorción de moléculas en la superficie, lo que aumenta la energía y la eficiencia de adsorción. El efecto sinérgico del espesor atómico, la alta flexibilidad, la mayor capacidad de adsorción de la superficie, el aislamiento eléctrico, la impermeabilidad, la alta estabilidad térmica y química de las nanoláminas de BN pueden aumentar la sensibilidad Raman hasta en dos órdenes y, mientras tanto, lograr estabilidad a largo plazo y reutilización extraordinaria que no se puede lograr con otros materiales.
Propiedades dieléctricas
El nitruro de boro hexagonal atómicamente delgado es un sustrato dieléctrico excelente para el grafeno, el disulfuro de molibdeno (MoS2), y muchos otros dispositivos electrónicos y fotónicos basados en materiales 2D. Como lo muestran los estudios de microscopía de fuerza eléctrica (EFM), la detección del campo eléctrico en el nitruro de boro atómicamente delgado muestra una débil dependencia del espesor, lo que está en línea con la disminución suave del campo eléctrico dentro del nitruro de boro de pocas capas revelado por los primeros principios. calculos
Características Raman
La espectroscopia Raman ha sido una herramienta útil para estudiar una variedad de materiales 2D, y la firma Raman de nitruro de boro atómicamente delgado de alta calidad fue reportada por primera vez por Gorbachev et al. en 2011. y Li et al. Sin embargo, los dos resultados Raman informados de nitruro de boro monocapa no coincidieron entre sí. Cai et al., por lo tanto, realizaron estudios teóricos y experimentales sistemáticos para revelar el espectro Raman intrínseco del nitruro de boro atómicamente delgado. Revela que el nitruro de boro atómicamente delgado sin interacción con un sustrato tiene una frecuencia de banda G similar a la del nitruro de boro hexagonal a granel, pero la tensión inducida por el sustrato puede causar cambios de Raman. Sin embargo, la intensidad Raman de la banda G de nitruro de boro atómicamente delgado se puede utilizar para estimar el espesor de la capa y la calidad de la muestra.
Nanomalla de nitruro de boro
La nanomalla de nitruro de boro es un material bidimensional nanoestructurado. Consiste en una sola capa de BN, que forma por autoensamblaje una malla muy regular después de la exposición a alta temperatura de una superficie limpia de rodio o rutenio a la borazina en un vacío ultraalto. La nanomalla parece un conjunto de poros hexagonales. La distancia entre los centros de dos poros es de 3,2 nm y el diámetro de los poros es de ~2 nm. Otros términos para este material son boroitreno o grafeno blanco.
La nanomalla de nitruro de boro no solo es estable a la descomposición en vacío, aire y algunos líquidos, sino también a temperaturas de hasta 800 °C. Además, muestra la extraordinaria capacidad de atrapar moléculas y grupos metálicos que tienen tamaños similares a los poros de la nanomalla, formando una matriz bien ordenada. Estas características prometen aplicaciones interesantes de la nanomalla en áreas como catálisis, funcionalización de superficies, espintrónica, computación cuántica y medios de almacenamiento de datos como discos duros.
Nanotubos de nitruro de boro
Los túbulos de nitruro de boro fueron fabricados por primera vez en 1989 por Shore y Dolan Este trabajo fue patentado en 1989 y publicado en 1989 tesis (Dolan) y luego en 1993 Science. El trabajo de 1989 fue también la primera preparación de BN amorfo por B-tricloroborazina y cesio metálico.
Los nanotubos de nitruro de boro se predijeron en 1994 y se descubrieron experimentalmente en 1995. Pueden imaginarse como una lámina enrollada de nitruro de h-boro. Estructuralmente, es un análogo cercano del nanotubo de carbono, es decir, un cilindro largo con un diámetro de varios a cientos de nanómetros y una longitud de muchos micrómetros, excepto que los átomos de carbono se sustituyen alternativamente por átomos de nitrógeno y boro. Sin embargo, las propiedades de los nanotubos BN son muy diferentes: mientras que los nanotubos de carbono pueden ser metálicos o semiconductores según la dirección y el radio de rodadura, un nanotubo BN es un aislante eléctrico con una banda prohibida de ~5,5 eV, básicamente independiente de la quiralidad y morfología del tubo. Además, una estructura de BN en capas es mucho más estable térmica y químicamente que una estructura de carbono grafítico.
Aerogel de nitruro de boro
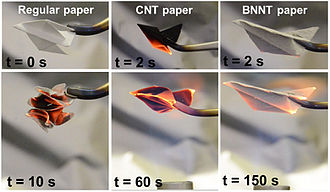
El aerogel de nitruro de boro es un aerogel hecho de BN altamente poroso. Por lo general, consiste en una mezcla de nanotubos y nanoláminas de BN deformados. Puede tener una densidad tan baja como 0,6 mg/cm3 y un área de superficie específica tan alta como 1050 m2/g y, por lo tanto, tiene aplicaciones potenciales como absorbente, soporte de catalizador y medio de almacenamiento de gas. Los aerogeles BN son altamente hidrofóbicos y pueden absorber hasta 160 veces su peso en aceite. Son resistentes a la oxidación en el aire a temperaturas de hasta 1200 °C y, por lo tanto, se pueden reutilizar después de que el aceite absorbido se haya quemado con la llama. Los aerogeles BN se pueden preparar mediante deposición de vapor químico asistida por plantilla utilizando borazina como gas de alimentación.
Composites que contienen BN
La adición de nitruro de boro a la cerámica de nitruro de silicio mejora la resistencia al choque térmico del material resultante. Con el mismo fin, el BN se añade también a las cerámicas de nitruro de silicio-alúmina y de nitruro de titanio-alúmina. Otros materiales que se refuerzan con BN incluyen alúmina y zirconia, vidrios de borosilicato, vitrocerámicas, esmaltes y compuestos cerámicos con boruro de titanio-nitruro de boro, boruro de titanio-nitruro de aluminio-nitruro de boro y composición de carburo de silicio-nitruro de boro.
Problemas de salud
Nitruro de boro (junto con Si3N4, NbN y BNC) muestran actividad fibrogénica débil y causan neumoconiosis cuando se inhalan en forma de partículas. La concentración máxima recomendada para nitruros de no metales es de 10 mg/m3 para BN y 4 para AlN o ZrN.
Contenido relacionado
Desaminación
Reactivo de Benedict
Grupo acilo