Neuropsicofarmacología
Neuropsicofarmacología, una ciencia interdisciplinaria relacionada con la psicofarmacología (estudio de los efectos de las drogas en la mente) y la neurociencia fundamental, es el estudio de los mecanismos neuronales sobre los que actúan las drogas para influir en el comportamiento. Implica la investigación de mecanismos de neuropatología, farmacodinámica (acción de los fármacos), enfermedades psiquiátricas y estados de conciencia. Estos estudios se inician a un nivel detallado que involucra la actividad de neurotransmisión/receptor, procesos bioquímicos y circuitos neuronales. La neuropsicofarmacología reemplaza a la psicofarmacología en las áreas de "cómo" y "por qué", y además aborda otras cuestiones de la función cerebral. En consecuencia, el aspecto clínico del campo incluye tratamientos basados en farmacología tanto psiquiátricos (psicoactivos) como neurológicos (no psicoactivos). Los avances en neuropsicofarmacología pueden afectar directamente los estudios de los trastornos de ansiedad, los trastornos afectivos, los trastornos psicóticos, los trastornos degenerativos, la conducta alimentaria y la conducta del sueño.
Historia
Drogas como el opio, el alcohol y ciertas plantas han sido utilizadas por los seres humanos durante milenios para aliviar el sufrimiento o cambiar la conciencia, pero hasta la era científica moderna el conocimiento sobre cómo funcionaban estas sustancias era bastante limitado. , siendo la mayor parte del conocimiento farmacológico más una serie de observaciones que un modelo coherente. La primera mitad del siglo XX consideró que la psicología y la psiquiatría eran en gran medida fenomenológicas, en el sentido de que los comportamientos o temas que se observaban en los pacientes a menudo podían correlacionarse con una variedad limitada de factores, como experiencias infantiles, tendencias heredadas o lesiones en áreas cerebrales específicas. Los modelos de función y disfunción mental se basaron en tales observaciones. De hecho, la rama conductual de la psicología prescindió por completo de lo que realmente sucedía dentro del cerebro, considerando la mayoría de las disfunciones mentales como lo que podría denominarse "software" errores. En la misma época, el sistema nervioso se estudiaba progresivamente a nivel microscópico y químico, pero prácticamente no había ningún beneficio mutuo con los campos clínicos, hasta que varios acontecimientos después de la Segunda Guerra Mundial comenzaron a unirlos. Se puede considerar que la neuropsicofarmacología comenzó a principios de la década de 1950 con el descubrimiento de fármacos como los inhibidores de la MAO, los antidepresivos tricíclicos, la torazina y el litio, que mostraron cierta especificidad clínica para enfermedades mentales como la depresión y la esquizofrenia. Hasta ese momento, los tratamientos dirigidos realmente a estas complejas enfermedades eran prácticamente inexistentes. Los métodos destacados que podrían afectar directamente los circuitos cerebrales y los niveles de neurotransmisores fueron la lobotomía prefrontal y la terapia electroconvulsiva, la última de las cuales se llevó a cabo sin relajantes musculares y ambas causaron a menudo al paciente grandes daños físicos y psicológicos. .
El campo ahora conocido como neuropsicofarmacología es el resultado del crecimiento y extensión de muchos campos previamente aislados que se han reunido en el centro de la medicina psiquiátrica e involucra a una amplia gama de profesionales, desde psiquiatras hasta investigadores en genética y química. El uso del término ha ganado popularidad desde 1990 con la fundación de varias revistas e instituciones como el Colegio Húngaro de Neuropsicofarmacología.[1 ] Este campo de rápida maduración muestra cierto grado de cambio, ya que las hipótesis de investigación a menudo se reestructuran en función de nueva información.
Descripción general
Una premisa implícita en la neuropsicofarmacología con respecto a los aspectos psicológicos es que todos los estados mentales, incluidos los estados alterados tanto normales como inducidos por drogas, y las enfermedades que implican disfunción mental o cognitiva, tienen una base neuroquímica en el nivel fundamental, y ciertas vías del circuito en el sistema nervioso central a un nivel superior. (Ver también: Doctrina de las neuronas) Por lo tanto, la comprensión de las células nerviosas o neuronas del cerebro es fundamental para comprender la mente. Se razona que los mecanismos involucrados pueden dilucidarse a través de métodos clínicos y de investigación modernos, como la manipulación genética en sujetos animales, técnicas de imagen como la imagen por resonancia magnética funcional (fMRI) e in vitro estudios que utilizan agentes aglutinantes selectivos en cultivos de tejidos vivos. Estos permiten monitorear y medir la actividad neuronal en respuesta a una variedad de condiciones de prueba. Otras herramientas de observación importantes incluyen imágenes radiológicas[2], como la tomografía por emisión de positrones (PET) y la tomografía por emisión de positrones (PET). tomografía computarizada por emisión de fotones (SPECT). Estas técnicas de imagen son extremadamente sensibles y pueden obtener imágenes de pequeñas concentraciones moleculares del orden de 10−10 M, como las que se encuentran con el receptor extraestriatal D1 para la dopamina.
Uno de los objetivos finales es idear y desarrollar recetas de tratamiento para una variedad de afecciones neuropatológicas y trastornos psiquiátricos. Más profundamente, sin embargo, el conocimiento adquirido puede proporcionar una visión de la naturaleza misma del pensamiento humano, de capacidades mentales como el aprendizaje y la memoria, y tal vez de la conciencia misma. Un producto directo de la investigación neuropsicofarmacológica es la base de conocimientos necesaria para desarrollar fármacos que actúen sobre receptores muy específicos dentro de un sistema de neurotransmisores. Estas "acción hiperselectiva" Los fármacos permitirían dirigirse directamente a sitios específicos de actividad neuronal relevante, maximizando así la eficacia (o técnicamente la potencia) del fármaco dentro del objetivo clínico y minimizando los efectos adversos. Sin embargo, hay algunos casos en los que cierto grado de promiscuidad farmacológica es tolerable e incluso deseable, produciendo resultados más deseables que los que produciría un agente más selectivo. Un ejemplo de esto es la vortioxetina, un fármaco que no es particularmente selectivo como inhibidor de la recaptación de serotonina y que tiene un grado significativo de actividad moduladora de la serotonina, pero que ha demostrado una reducción de los síntomas de interrupción (y una menor probabilidad de recaída) y una incidencia muy reducida de disfunción sexual. , sin pérdida de eficacia antidepresiva.
Actualmente se están sentando las bases para la próxima generación de tratamientos farmacológicos, que mejorarán la calidad de vida con una eficiencia cada vez mayor. Por ejemplo, contrariamente a lo que se pensaba anteriormente, ahora se sabe que en el cerebro adulto, hasta cierto punto, crecen nuevas neuronas, cuyo estudio, además de los factores neurotróficos, puede ofrecer esperanzas para enfermedades neurodegenerativas como el Alzheimer y el Parkinson. 39;s, ELA y tipos de corea. Todas las proteínas implicadas en la neurotransmisión son una pequeña fracción de las más de 100.000 proteínas del cerebro. Por tanto, hay muchas proteínas que ni siquiera se encuentran en el camino directo de la transducción de señales, y cualquiera de las cuales aún puede ser un objetivo para una terapia específica. En la actualidad, se informa de nuevos enfoques farmacológicos para enfermedades o afecciones a un ritmo de casi uno por semana.[3]
Neurotransmisión
Hasta donde sabemos, todo lo que percibimos, sentimos, pensamos, sabemos y hacemos es el resultado de la activación y el reinicio de las neuronas. Cuando una célula del cerebro se activa, pequeñas oscilaciones químicas y eléctricas llamadas potencial de acción pueden afectar la activación de hasta mil otras neuronas en un proceso llamado neurotransmisión. De esta manera, las señales se generan y transportan a través de redes de neuronas, cuyo efecto eléctrico general puede medirse directamente en el cuero cabelludo mediante un dispositivo EEG.
En la última década del siglo XX, se había adquirido el conocimiento esencial de todas las características centrales de la neurotransmisión.[4] Estas características son:
- La síntesis y almacenamiento de sustancias neurotransmisoras,
- El transporte de vesículas sinápticas y posterior liberación en la sinapsis,
- Función de activación y cascada del receptor,
- Mecanismos de transporte (recaptación) y/o degradación de enzimas
Los avances más recientes implican la comprensión a nivel molecular orgánico; acción bioquímica de los ligandos endógenos, enzimas, proteínas receptoras, etc. Los cambios críticos que afectan la activación celular ocurren cuando los neurotransmisores de señalización de una neurona, que actúan como ligandos, se unen a los receptores de otra neurona. Muchos sistemas de neurotransmisores y receptores son bien conocidos, y continúa la investigación hacia la identificación y caracterización de una gran cantidad de subtipos de receptores muy específicos. Para los seis neurotransmisores más importantes Glu, GABA, Ach, NE, DA y 5HT (enumerados en neurotransmisor) existen al menos 29 subtipos principales de receptores. Otros "subsubtipos" Existen junto con variantes, que suman cientos para solo estos 6 transmisores. - (ver receptor de serotonina, por ejemplo.) A menudo se descubre que los subtipos de receptores tienen funciones diferenciadas, lo que en principio abre la posibilidad de un control intencional refinado sobre la función cerebral.
Se sabía anteriormente que el control final sobre el voltaje o potencial de membrana de una célula nerviosa y, por tanto, sobre la activación de la célula, reside en los canales iónicos transmembrana que controlan las corrientes de membrana a través de los iones K+. , Na+ y Ca++, y en menor importancia Mg++ y Cl−. Las diferencias de concentración entre el interior y el exterior de la célula determinan el voltaje de la membrana.
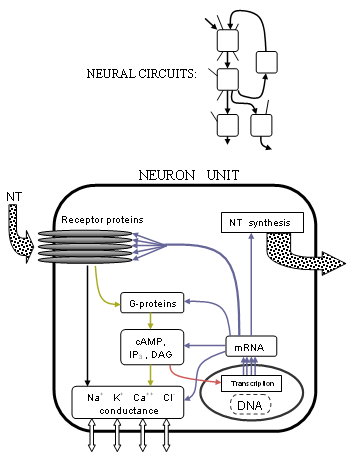
Precisamente cómo se controlan estas corrientes se ha vuelto mucho más claro con los avances en la estructura del receptor y los procesos acoplados a la proteína G. Se ha descubierto que muchos receptores son grupos pentaméricos de cinco proteínas transmembrana (no necesariamente iguales) o subunidades receptoras, cada una de las cuales es una cadena de muchos aminoácidos. Los transmisores suelen unirse en la unión entre dos de estas proteínas, en las partes que sobresalen de la membrana celular. Si el receptor es del tipo ionotrópico, se moverá mecánicamente un poro o canal central en el medio de las proteínas para permitir que ciertos iones fluyan a través de él, alterando así la diferencia de concentración de iones. Si el receptor es del tipo metabotrópico, las proteínas G provocarán un metabolismo dentro de la célula que eventualmente puede cambiar otros canales iónicos. Los investigadores comprenden mejor con precisión cómo se producen estos cambios en función de las formas de la estructura de las proteínas y las propiedades químicas.
El alcance de esta actividad se ha ampliado aún más, hasta llegar al mismísimo modelo de la vida, desde que se esclareció el mecanismo subyacente a la transcripción genética. La síntesis de proteínas celulares a partir del ADN nuclear tiene la misma maquinaria fundamental[5] para todas las células; cuya exploración tiene ahora una base sólida gracias al Proyecto Genoma Humano, que ha enumerado toda la secuencia del ADN humano, aunque muchos de los 35.000 genes estimados aún quedan por identificar. El proceso completo de neurotransmisión se extiende al nivel genético. La expresión génica determina las estructuras de las proteínas a través de la ARN polimerasa de tipo II. Por lo tanto, las enzimas que sintetizan o descomponen neurotransmisores, receptores y canales iónicos se elaboran a partir de ARNm mediante la transcripción de ADN de su gen o genes respectivos. Pero la neurotransmisión, además de controlar los canales iónicos, ya sea directamente o mediante procesos metabotrópicos, también modula la expresión genética. Esto se logra principalmente mediante la modificación del proceso de inicio de la transcripción mediante una variedad de factores de transcripción producidos a partir de la actividad del receptor.
Aparte de las importantes posibilidades farmacológicas de las vías de expresión génica, la correspondencia de un gen con su proteína permite la importante herramienta analítica de la desactivación genética. Se pueden crear especímenes vivos mediante recombinación homóloga en la que no se puede expresar un gen específico. El organismo tendrá entonces una deficiencia de la proteína asociada, que puede ser un receptor específico. Este método evita el bloqueo químico que puede producir efectos secundarios confusos o ambiguos, de modo que los efectos de la falta de receptor pueden estudiarse en un sentido más puro.
Drogas
El inicio de muchas clases de fármacos es, en principio, sencillo: cualquier sustancia química que pueda mejorar o disminuir la acción de una proteína objetivo podría investigarse más a fondo para tal uso. El truco consiste en encontrar una sustancia química que sea específica del receptor (cf. "droga sucia") y que sea segura para consumir. El informe Médicos' Desk Reference enumera el doble de medicamentos recetados que la versión de 1990.[6] Muchas personas ya están familiarizadas con " ;inhibidores selectivos de la recaptación de serotonina", o ISRS, que ejemplifican los productos farmacéuticos modernos. Estos fármacos antidepresivos ISRS, como Paxil y Prozac, inhiben selectivamente y, por tanto, principalmente, el transporte de serotonina, lo que prolonga la actividad en la sinapsis. Existen numerosas categorías de fármacos selectivos y el bloqueo del transporte es sólo un modo de acción. La FDA ha aprobado medicamentos que actúan selectivamente sobre cada uno de los neurotransmisores principales, como los antidepresivos inhibidores de la recaptación de NE, los antipsicóticos bloqueadores de DA y los tranquilizantes agonistas de GABA (benzodiazepinas).
Continuamente se identifican nuevas sustancias químicas endógenas. Se han encontrado receptores específicos para las drogas THC (cannabis) y GHB,[7] con transmisores endógenos anandamida y GHB. Otro importante descubrimiento reciente se produjo en 1999, cuando se descubrió que la orexina, o hipocretina, desempeñaba un papel en la excitación, ya que la falta de receptores de orexina refleja la condición de la narcolepsia. El agonismo de la orexina puede explicar la acción antinarcoléptica del fármaco modafinilo que ya se utilizaba sólo un año antes.
El siguiente paso, en el que las principales compañías farmacéuticas están trabajando arduamente para desarrollar, son los fármacos de subtipos de receptores específicos y otros agentes específicos. Un ejemplo es la búsqueda de mejores agentes ansiolíticos (ansiolíticos) basados en agonistas GABAA(α2), antagonistas CRF1 y 5HT2c antagonistas.[8] Otra es la propuesta de nuevas rutas de exploración para antipsicóticos como los inhibidores de la recaptación de glicina.[9] Aunque existen capacidades para fármacos con receptores específicos, una deficiencia de la terapia farmacológica es la falta de capacidad para proporcionar características anatómicas especificidad. Al alterar la función del receptor en una parte del cerebro, se puede inducir una actividad anormal en otras partes del cerebro debido al mismo tipo de cambios en los receptores. Un ejemplo común es el efecto de los fármacos que alteran el D2 (neurolépticos) que pueden ayudar en la esquizofrenia, pero causan una variedad de discinesias por su acción sobre la corteza motora.
Los estudios modernos están revelando detalles de los mecanismos de daño al sistema nervioso, como la apoptosis (muerte celular programada) y la alteración de los radicales libres. Se ha descubierto que la fenciclidina causa muerte celular en células estriatopalidas y vacuolización anormal en el hipocampo y otras neuronas. El trastorno de percepción persistente de alucinógenos (HPPD), también conocido como trastorno de percepción post-psicodélico, se ha observado en pacientes hasta 26 años después del uso de LSD. La posible causa del HPPD es el daño al circuito inhibidor de GABA en la vía visual (los agonistas de GABA como el midazolam pueden disminuir algunos efectos de la intoxicación por LSD). El daño puede ser el resultado de una respuesta excitotóxica de las interneuronas 5HT2. [Nota: la gran mayoría de los consumidores de LSD no experimentan HPPD. Su manifestación puede depender igualmente de la química cerebral individual como del uso de la droga en sí.] En cuanto a la MDMA, aparte de las pérdidas persistentes de 5HT y SERT, se encuentra una reducción duradera de los axones y terminales serotoninérgicos debido al uso a corto plazo y un nuevo crecimiento. puede tener una función comprometida.
Circuitos neuronales
Muchas funciones del cerebro están de alguna manera localizadas en áreas asociadas, como la capacidad motora y del habla. Las asociaciones funcionales de la anatomía del cerebro ahora se complementan con correlatos clínicos, conductuales y genéticos de la acción del receptor, completando el conocimiento de la señalización neuronal (ver también: Human Cognome Project). Las rutas de señales de las neuronas están hiperorganizadas más allá de la escala celular en rutas de circuitos neuronales a menudo complejas. El conocimiento de estas vías es quizás el más fácil de interpretar, siendo más reconocible desde el punto de vista del análisis de sistemas, como se puede ver en los siguientes resúmenes.
Se ha descubierto que casi todas las drogas con potencial conocido de abuso modulan la actividad (directa o indirectamente) en el sistema de dopamina mesolímbico, que incluye y conecta el área tegmental ventral del mesencéfalo con el hipocampo, la corteza prefrontal medial y la amígdala. en el prosencéfalo; así como el núcleo accumbens en el estriado ventral de los ganglios basales. En particular, el núcleo accumbens (NAc) juega un papel importante en la integración de la memoria experiencial del hipocampo, la emoción de la amígdala y la información contextual del PFC para ayudar a asociar estímulos o comportamientos particulares con sentimientos de placer y recompensa; La activación continua de este sistema indicador de recompensa por una droga adictiva también puede hacer que estímulos previamente neutrales se codifiquen como señales de que el cerebro está a punto de recibir una recompensa. Esto sucede mediante la liberación selectiva de dopamina, un neurotransmisor responsable de los sentimientos de euforia y placer. El uso de fármacos dopaminérgicos altera la cantidad de dopamina liberada en todo el sistema mesolímbico, y el uso regular o excesivo del fármaco puede provocar una regulación negativa a largo plazo de la señalización de la dopamina, incluso después de que un individuo deja de ingerir el fármaco. Esto puede llevar al individuo a adoptar conductas de búsqueda de drogas de leves a extremas, ya que el cerebro comienza a esperar regularmente una mayor presencia de dopamina y los sentimientos de euforia que la acompañan, pero cuán problemático sea esto depende en gran medida de la droga y la situación.
Se han logrado avances significativos en los mecanismos centrales de ciertas drogas alucinógenas. A estas alturas se sabe con relativa certeza que los principales efectos compartidos de un amplio grupo farmacológico de alucinógenos, a veces llamados "psiquedélicos clásicos", pueden atribuirse en gran medida al agonismo de los receptores de serotonina. El receptor 5HT2A, que parece ser el receptor más crítico para la actividad psicodélica, y el receptor 5HT2C, que es un objetivo importante de la mayoría de los psicodélicos pero que no tiene una respuesta clara. papel en la alucinogénesis, participan liberando glutamato en la corteza frontal, mientras que simultáneamente en el locus coeruleus se promueve la información sensorial y disminuye la actividad espontánea. La actividad 5HT2A tiene un efecto prodopaminérgico neto, mientras que el agonismo del receptor 5HT2C tiene un efecto inhibidor sobre la actividad dopaminérgica, particularmente en la corteza prefrontal. Una hipótesis sugiere que en la corteza frontal, 5HT2A promueve potenciales postsinápticos excitadores asincrónicos tardíos, un proceso antagonizado por la propia serotonina a través de los receptores 5HT1, lo que puede explicar por qué los ISRS y otros Los fármacos que afectan la serotonina normalmente no provocan alucinaciones en el paciente. Sin embargo, el hecho de que muchos psicodélicos clásicos tengan de hecho una afinidad significativa por los receptores 5HT1 pone en duda esta afirmación. La respuesta de contracción de la cabeza, una prueba utilizada para evaluar la actividad psicodélica clásica en roedores, es producida por la propia serotonina sólo en presencia de beta-arrestinas, pero es desencadenada por psicodélicos clásicos independientemente del reclutamiento de beta-arrestinas. Esto puede explicar mejor la diferencia entre la farmacología de la neurotransmisión serotoninérgica (incluso si es promovida por fármacos como los ISRS) y la de los psicodélicos clásicos. Sin embargo, hallazgos más recientes indican que la unión al heterodímero 5HT2A-mGlu2 también es necesaria para la actividad psicodélica clásica. Esto también puede ser relevante para las diferencias farmacológicas entre los dos. Si bien en los inicios de la historia de la investigación sobre drogas psicodélicas se suponía que estas alucinaciones eran comparables a las producidas por la psicosis y, por lo tanto, que los psicodélicos clásicos podían servir como modelo de psicosis, es importante señalar que el conocimiento neuropsicofarmacológico moderno de la psicosis ha progresado significativamente desde entonces. Entonces, y ahora sabemos que la psicosis muestra poca similitud con los efectos de los psicodélicos clásicos en el mecanismo, la experiencia reportada o en la mayoría de los demás aspectos, aparte de la similitud superficial de la "alucinación".

El ritmo circadiano, o ciclo de sueño/vigilia, se centra en el núcleo supraquiasmático (SCN) dentro del hipotálamo y se caracteriza por niveles de melatonina entre un 2.000% y un 4.000% más altos durante el sueño que durante el día. Se sabe que un circuito comienza con células de melanopsina en el ojo que estimulan el SCN a través de neuronas de glutamato del tracto hipotalámico. Las neuronas GABAérgicas del SCN inhiben el núcleo paraventricular, que envía señales al ganglio cervical superior (SCG) a través de fibras simpáticas. La producción del SCG estimula los receptores NE (β) en la glándula pineal, que produce N-acetiltransferasa, lo que provoca la producción de melatonina a partir de serotonina. Los receptores inhibidores de melatonina en el SCN proporcionan una vía de retroalimentación positiva. Por tanto, la luz inhibe la producción de melatonina, que "arrastra" el ciclo de 24 horas de actividad de SCN.[10][11] El SCN también recibe señales de otras partes del cerebro, y su ciclo (aproximadamente) de 24 horas no depende solo de los patrones de luz. De hecho, el tejido seccionado del SCN exhibirá un ciclo diario in vitro durante muchos días. Además, (no se muestra en el diagrama), el núcleo basal proporciona una entrada inhibidora GABAérgica al hipotálamo anterior preóptico (PAH). Cuando la adenosina se acumula a partir del metabolismo del ATP a lo largo del día, se une a los receptores de adenosina, inhibiendo el núcleo basal. Luego se activa la PAH, generando una actividad de sueño de ondas lentas. Se sabe que la cafeína bloquea los receptores de adenosina, inhibiendo así el sueño, entre otras cosas.
Investigación
La investigación en el campo de la neuropsicofarmacología abarca una amplia gama de objetivos. Estos podrían incluir el estudio de un nuevo compuesto químico para detectar efectos cognitivos o conductuales potencialmente beneficiosos, o el estudio de un compuesto químico antiguo para comprender mejor su mecanismo de acción a nivel celular y del circuito neuronal. Por ejemplo, se sabe desde hace mucho tiempo que la cocaína, una droga estimulante adictiva, actúa sobre el sistema de recompensa del cerebro, aumentando los niveles de dopamina y norepinefrina e induciendo euforia por un corto tiempo. Sin embargo, estudios publicados más recientemente han ido más allá del nivel del circuito y han descubierto que un complejo receptor acoplado a proteína G particular llamado A2AR-D2R-Sigma1R se forma en la NAc después del consumo de cocaína; este complejo reduce la señalización D2R en la vía mesolímbica y puede ser un factor que contribuye a la adicción a la cocaína. Otros estudios de vanguardia se han centrado en la genética para identificar biomarcadores específicos que puedan predecir las reacciones específicas de un individuo o su grado de respuesta a una droga o su tendencia a desarrollar adicciones en el futuro. Estos hallazgos son importantes porque proporcionan información detallada sobre los circuitos neuronales involucrados en el uso de drogas y ayudan a refinar métodos de tratamiento antiguos y nuevos para trastornos o adicciones. Diferentes estudios relacionados con el tratamiento están investigando el papel potencial de los ácidos peptídicos nucleicos en el tratamiento de la enfermedad de Parkinson y la esquizofrenia, mientras que otros intentan establecer correlatos neuronales previamente desconocidos que subyacen a ciertos fenómenos.
La investigación en neuropsicofarmacología proviene de una amplia gama de actividades en neurociencia e investigación clínica. Esto ha motivado a organizaciones como el Colegio Americano de Neuropsicofarmacología (ACNP), el Colegio Europeo de Neuropsicofarmacología (ECNP) y el Collegium Internationale Neuro-psychopharmacologicum (CINP) a establecerse como medida de enfoque. El ECNP publica Neuropsicofarmacología y, como parte del Grupo Reed Elsevier, el ACNP publica la revista Neuropsicofarmacología y el CINP publica la revista International Journal of Neuropsychopharmacology con Cambridge University Press. En 2002, una reciente y exhaustiva obra recopilada del ACNP, "Neuropsicofarmacología: la quinta generación del progreso" fue compilado. Es una medida del estado de los conocimientos en 2002 y podría decirse que representa un hito en el objetivo de un siglo de establecer los principios neurobiológicos básicos que gobiernan las acciones del cerebro.
Existen muchas otras revistas que contienen información relevante como Neurociencia. Algunos de ellos figuran en la biblioteca de la Universidad de Brown.
Contenido relacionado
Ley de Fick
Triglicéridos
Memoria
Herman Boerhaave
Agente bacteriostático