Modelo de mosaico fluido
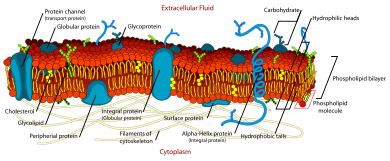
El modelo de mosaico fluido explica varias observaciones sobre la estructura de las membranas celulares funcionales. De acuerdo con este modelo biológico, hay una bicapa lipídica (una capa gruesa de dos moléculas que consiste principalmente en fosfolípidos anfipáticos) en la que están incrustadas las moléculas de proteína. La bicapa de fosfolípidos da fluidez y elasticidad a la membrana. Pequeñas cantidades de carbohidratos también se encuentran en la membrana celular. El modelo biológico, ideado por Seymour Jonathan Singer y Garth L. Nicolson en 1972, describe la membrana celular como un líquido bidimensional que restringe la difusión lateral de los componentes de la membrana. Dichos dominios están definidos por la existencia de regiones dentro de la membrana con un capullo especial de lípidos y proteínas que promueven la formación de balsas lipídicas o complejos de proteínas y glicoproteínas. Además, se adelantó al otro modelo que introdujo la primera bicapa. Otra forma de definir los dominios de membrana es la asociación de la membrana lipídica con los filamentos del citoesqueleto y la matriz extracelular a través de proteínas de membrana. El modelo actual describe características importantes relevantes para muchos procesos celulares, que incluyen: señalización celular, apoptosis, división celular, gemación de membranas y fusión celular. El modelo de mosaico fluido es el modelo más aceptable de la membrana plasmática. Su función principal es separar el contenido de la celda del exterior.
Composición química
| Componentes | Ubicación | Funciones |
|---|---|---|
| fosfolípido | El tejido principal de la membrana plasmática | Proporciona permeabilidad selectiva a la membrana celular. |
| Carbohidratos | Acoplado a proteínas en capas de membrana externas | Ayuda en el reconocimiento celular a célula. |
| Colesterol | Entre fosfolípidos y bicapas fosfolípidos | Ayuda a la membrana plasmática a conservar su fluidez. |
| Proteínas | Embedded in or on the surface of phospholipid layers | Estos canales de forma permiten el movimiento de moléculas. |
Evidencia experimental
La propiedad fluida de las membranas biológicas funcionales se ha determinado mediante experimentos de etiquetado, difracción de rayos X y calorimetría. Estos estudios mostraron que las proteínas integrales de la membrana se difunden a velocidades afectadas por la viscosidad de la bicapa lipídica en la que estaban incrustadas y demostraron que las moléculas dentro de la membrana celular son dinámicas en lugar de estáticas.
Los modelos anteriores de membranas biológicas incluían el modelo de membrana unitaria de Robertson y el modelo de tres capas de Davson-Danielli. Estos modelos tenían proteínas presentes como láminas vecinas a una capa de lípidos, en lugar de incorporarse a la bicapa de fosfolípidos. Otros modelos describieron unidades regulares y repetitivas de proteínas y lípidos. Estos modelos no estaban bien respaldados por microscopía y datos termodinámicos, y no acomodaron evidencia de propiedades dinámicas de membrana.

Frye y Edidin realizaron un experimento importante que proporcionó evidencia que respalda la biología fluida y dinámica. Usaron el virus Sendai para obligar a las células humanas y de ratón a fusionarse y formar un heterocarión. Usando la tinción de anticuerpos, pudieron demostrar que las proteínas de ratón y humanas permanecieron separadas en mitades separadas del heterocarión poco tiempo después de la fusión celular. Sin embargo, las proteínas eventualmente se difundieron y con el tiempo se perdió el borde entre las dos mitades. Bajar la temperatura ralentizó la velocidad de esta difusión haciendo que los fosfolípidos de la membrana pasaran de una fase fluida a una de gel. Singer y Nicolson racionalizaron los resultados de estos experimentos utilizando su modelo de mosaico fluido.
El modelo de mosaico fluido explica los cambios en la estructura y el comportamiento de las membranas celulares bajo diferentes temperaturas, así como la asociación de proteínas de membrana con las membranas. Si bien Singer y Nicolson obtuvieron evidencia sustancial extraída de múltiples subcampos para respaldar su modelo, los avances recientes en microscopía de fluorescencia y biología estructural han validado la naturaleza de mosaico fluido de las membranas celulares.
Desarrollos posteriores
Asimetría de membrana
Además, las dos láminas de las membranas biológicas son asimétricas y están divididas en subdominios compuestos por proteínas o lípidos específicos, lo que permite la segregación espacial de los procesos biológicos asociados con las membranas. El colesterol y las proteínas que interactúan con el colesterol pueden concentrarse en balsas de lípidos y restringir los procesos de señalización celular solo a estas balsas. Otra forma de asimetría fue mostrada por el trabajo de Mouritsen y Bloom en 1984, donde propusieron un modelo de colchón de interacciones lípido-proteína para abordar la evidencia biofísica de que la membrana puede variar en grosor e hidrofobicidad de las proteínas.
Membranas no bicapa
La existencia de formaciones lipídicas sin bicapa con funciones biológicas importantes se confirmó después de la publicación del modelo de mosaico fluido. Estas estructuras de membrana pueden ser útiles cuando la célula necesita propagar una forma no bicapa, lo que ocurre durante la división celular y la formación de una unión comunicante.
Curvatura de la membrana
La bicapa de la membrana no siempre es plana. La curvatura local de la membrana puede ser causada por la asimetría y la organización no bicapa de los lípidos como se discutió anteriormente. Se logra una curvatura más dramática y funcional a través de los dominios BAR, que se unen al fosfatidilinositol en la superficie de la membrana, lo que ayuda en la formación de vesículas, la formación de orgánulos y la división celular. El desarrollo de la curvatura está en constante flujo y contribuye a la naturaleza dinámica de las membranas biológicas.
Movimiento de lípidos dentro de la membrana
Durante la década de 1970, se reconoció que las moléculas lipídicas individuales experimentan una difusión lateral libre dentro de cada una de las capas de la membrana lipídica. La difusión ocurre a alta velocidad, con una molécula de lípido promedio que se difunde ~2 µm, aproximadamente la longitud de una célula bacteriana grande, en aproximadamente 1 segundo. También se ha observado que las moléculas de lípidos individuales giran rápidamente alrededor de su propio eje. Además, las moléculas de fosfolípidos pueden, aunque rara vez lo hacen, migrar de un lado de la bicapa lipídica al otro (un proceso conocido como flip-flop). Sin embargo, el flip-flop podría mejorarse con las enzimas flipasa. Los procesos descritos anteriormente influyen en la naturaleza desordenada de las moléculas lipídicas y las proteínas que interactúan en las membranas lipídicas, con consecuencias para la fluidez, la señalización, el tráfico y la función de la membrana.
Restricciones a la fluidez bicapa
Existen restricciones a la movilidad lateral de los componentes lipídicos y proteicos en la membrana líquida impuestas por la formación de subdominios dentro de la bicapa lipídica. Estos subdominios surgen por varios procesos p. ej. la unión de los componentes de la membrana a la matriz extracelular, regiones nanométricas de la membrana con una composición bioquímica particular que promueven la formación de balsas lipídicas y complejos proteicos mediados por interacciones proteína-proteína. Además, las asociaciones proteína-citoesqueleto median la formación de “vallas citoesqueléticas”, corrales en los que los lípidos y las proteínas de membrana pueden difundirse libremente, pero rara vez pueden salir. La restricción de las tasas de difusión lateral de los componentes de la membrana es muy importante porque permite la especialización funcional de regiones particulares dentro de las membranas celulares.
Balsas lipídicas
Las balsas lipídicas son plataformas nanométricas de membrana con una composición particular de lípidos y proteínas que se difunden lateralmente, navegando en la capa bilipídica líquida. Los esfingolípidos y el colesterol son componentes importantes de las balsas lipídicas.
Complejos proteicos
Las proteínas y glicoproteínas de la membrana celular no existen como elementos únicos de la membrana lipídica, como propusieron por primera vez Singer y Nicolson en 1972. Más bien, se presentan como complejos de difusión dentro de la membrana. El ensamblaje de moléculas individuales en estos complejos macromoleculares tiene importantes consecuencias funcionales para la célula; como transporte de iones y metabolitos, señalización, adhesión celular y migración.
Cercas citoesqueléticas (corrales) y unión a la matriz extracelular
Algunas proteínas incrustadas en la capa bilipídica interactúan con la matriz extracelular fuera de la célula, los filamentos del citoesqueleto dentro de la célula y estructuras similares a anillos de septina. Estas interacciones tienen una fuerte influencia en la forma y la estructura, así como en la compartimentación. Además, imponen restricciones físicas que restringen la difusión lateral libre de proteínas y al menos algunos lípidos dentro de la capa bilipídica.
Cuando las proteínas integrales de la bicapa lipídica están unidas a la matriz extracelular, no pueden difundirse libremente. Las proteínas con un dominio intracelular largo pueden chocar con una valla formada por filamentos del citoesqueleto. Ambos procesos restringen la difusión de proteínas y lípidos directamente involucrados, así como de otros componentes interactuantes de las membranas celulares.

Las estructuras tipo anillo setin (en verde) pueden pellizcar las membranas celulares y dividirlas en subdominios.
Las septinas son una familia de proteínas de unión a GTP altamente conservadas entre los eucariotas. Los procariotas tienen proteínas similares llamadas paraseptinas. Forman estructuras compartimentadas en forma de anillo fuertemente asociadas con las membranas celulares. Los septinos están involucrados en la formación de estructuras tales como cilios y flagelos, espinas dendríticas y brotes de levadura.
Cronología histórica
- 1895 – Ernest Overton hipotetizó que las membranas celulares están hechas de lípidos.
- 1925 – Evert Gorter y François Grendel encontraron que las membranas de glóbulos rojos están formadas por una capa grasa dos moléculas de espesor, i.e. describen la naturaleza bilipida de la membrana celular.
- 1935 – Hugh Davson y James Danielli propusieron que las membranas lipídicas son capas compuestas por proteínas y lípidos con estructuras similares a los poros que permiten una permeabilidad específica para ciertas moléculas. Luego, sugirieron un modelo para la membrana celular, consistente en una capa de lípido rodeada de capas de proteínas a ambos lados de ella.
- 1957 – J. David Robertson, basado en estudios de microscopía de electrones, establece la "Hipotesis Unit Membrane". Esto, afirma que todas las membranas de la célula, i.e. Las membranas de plasma y organela tienen la misma estructura: una bicapa de fosfolípidos con monocapas de proteínas a ambos lados.
- 1972 – SJ Singer y GL Nicolson propusieron el modelo de mosaico de fluidos como una explicación para los datos y las últimas evidencias sobre la estructura y la termodinámica de las membranas celulares.
Notas y referencias
- ^ a b c d Singer SJ, Nicolson GL (Feb 1972). "El modelo de mosaico fluido de la estructura de las membranas celulares". Ciencia. 175 (4023): 720–31. doi:10.1126/ciencia.175.4023.720. PMID 43397. S2CID 83851531.
- ^ a b c d e f g h Nicolson GL (2014). "El Modelo Fluid-Mosaico de la Estructura Membrana: sigue siendo relevante para comprender la estructura, función y dinámica de las membranas biológicas después de más de 40 años". Biochimica et Biophysica Acta (BBA) - Biomembranes. 1838 (6): 1451–146. doi:10.1016/j.bbamem.2013.10.019. PMID 24189436.
- ^ Frye LD, Edidin M (1970). "La rápida mezcla de antígenos de superficie celular después de la formación de heterokaryones humanos del ratón". J Cell Sci. 7 (2): 319–35. doi:10.1242/jcs.7.2.319. PMID 4098863.
- ^ Silvius JR (2005). "Partición de moléculas de membrana entre los dominios de balsa y no-robo: Insights from model-membrane studies". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1746 (3): 193–202. doi:10.1016/j.bbamcr.2005.09.003. PMID 16271405.
- ^ Mouritsen OG, Bloom M (1984). "Mattress model of lipid-protein interactions in membranas". Biophys J. 46 (2): 141–153 doi:10.1016/S0006-3495(84)84007-2. PMC1435039. PMID 6478029.
- ^ van den Brink-van der Laan E; et al. (2004). "Los lípidos nonbilayer afectan las proteínas de membrana periférica e integral mediante cambios en el perfil de presión lateral". Biochim Biophys Acta. 1666 (1–2): 275–88. doi:10.1016/j.bbamem.2004.06.010. PMID 15519321.
- ^ Frost A; et al. (2009). "El dominio BAR superfamilia: macromoléculas moldeadoras de membrana". Celular. 137 (2): 191–6. doi:10.1016/j.cell.2009.04.010. PMC4832598. PMID 19379681.
- ^ Rodríguez-García R; et al. (2009). "Especto bimodal para las fluctuaciones de curvatura de vesículas bilayer: doblado puro más modos híbridos de curvatura-dilatación". Phys Rev Lett. 102 (12): 128101. doi:10.1103/PhysRevLett.102.128101. PMID 19392326.
- ^ a b c Alberts B, Johnson A, Lewis J, et al. (2008). Biología molecular de la célula (5a edición). Nueva York: Garland Science. pp. 621–622. ISBN 978-0-8153-4105-5.
- ^ Lingwood D, Simons K (2010). "Rafts líquidos como principio de organización de membrana". Ciencia. 327 (5961): 46–50. doi:10.1126/science.1174621. PMID 20044567. S2CID 35095032.
- ^ G. Vereb; et al. (2003). "Dinámica, pero estructurada: La membrana celular tres décadas después del modelo Singer-Nicolson". PNAS. 100 (14): 8053–8058. doi:10.1073/pnas.1332550100. PMC166180. PMID 12832616.
- ^ Juha Saarikangas; Yves Barral (2011). "Las funciones emergentes de las septinas en metazoos". EMBO Informes. 12 11): 1118–1126. doi:10.1038/embor.2011.193. PMC3207108. PMID 21997296.
- ^ Overton, E (1895). "Uberdie osmotischen Eigenshafter der Lebenden Pflanzen und tierzelle". VJSCHR Naturf Ges Zurich. 40: 159–201.
- ^ E. Gorter; F. Grendel (1925). "Sobre las Capas Biomoleculares de Lipoides en los Cromocitos de la Sangre". Journal of Experimental Medicine. 41 (4): 439–443. doi:10.1084/jem.41.439. PMC2130960. PMID 19868999.
- ^ James Danielli; Hugh Davson (1935). "Una contribución a la teoría de la permeabilidad de las películas delgadas". Journal of Cellular and Comparative Physiology. 5 (4): 495–508. doi:10.1002/jcp.1030050409.
- ^ John E. Heuser (1995). "En memoria de J. David Robertson" (PDF). Boletín de la Sociedad Americana de Biología Celular.
Contenido relacionado
OMG (desambiguación)
Alcoholismo
Aracnofobia