Miastenia gravis
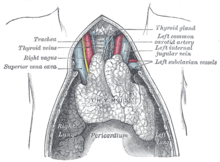
La miastenia gravis (MG) es una enfermedad de la unión neuromuscular a largo plazo que conduce a diversos grados de debilidad del músculo esquelético. Los músculos más comúnmente afectados son los de los ojos, la cara y la deglución. Puede resultar en visión doble, párpados caídos, dificultad para hablar y dificultad para caminar. El inicio puede ser repentino. Los afectados a menudo tienen un timo grande o desarrollan un timoma.
La miastenia gravis es una enfermedad autoinmune de la unión neuromuscular que resulta de anticuerpos que bloquean o destruyen los receptores nicotínicos de acetilcolina (AChR) en la unión entre el nervio y el músculo. Esto evita que los impulsos nerviosos desencadenen contracciones musculares. La mayoría de los casos se deben a anticuerpos de inmunoglobulina G1 (IgG1) e IgG3 que atacan a AChR en la membrana postsináptica, causando daño mediado por complemento y debilidad muscular. En raras ocasiones, un defecto genético heredado en la unión neuromuscular da como resultado una condición similar conocida como miastenia congénita. Los bebés de madres con miastenia pueden tener síntomas durante los primeros meses de vida, lo que se conoce como miastenia neonatal. El diagnóstico puede respaldarse con análisis de sangre para anticuerpos específicos, la prueba de edrofonio o un estudio de conducción nerviosa.
La MG generalmente se trata con medicamentos conocidos como inhibidores de la acetilcolinesterasa, como la neostigmina y la piridostigmina. También se pueden usar inmunosupresores, como la prednisona o la azatioprina. La extirpación quirúrgica del timo puede mejorar los síntomas en ciertos casos. La plasmaféresis y la inmunoglobulina intravenosa en dosis altas pueden usarse durante los brotes repentinos de la afección. Si los músculos respiratorios se debilitan significativamente, es posible que se requiera ventilación mecánica. Una vez intubados, los inhibidores de la acetilcolinesterasa pueden suspenderse temporalmente para reducir las secreciones de las vías respiratorias.
MG afecta de 50 a 200 por millón de personas. Se diagnostica recientemente en tres a 30 por millón de personas cada año. El diagnóstico se ha vuelto más común debido a una mayor conciencia. La MG ocurre con mayor frecuencia en mujeres menores de 40 años y en hombres mayores de 60 años. Es poco común en niños. Con tratamiento, la mayoría de los afectados llevan una vida relativamente normal y tienen una esperanza de vida normal. La palabra proviene del griego mys, "músculo" y astheneia "debilidad", y el latín gravis, "grave".
Signos y síntomas
El síntoma principal inicial de la MG es la debilidad indolora de músculos específicos, no la fatiga. La debilidad muscular empeora progresivamente durante los períodos de actividad física y mejora después de los períodos de descanso. Por lo general, la debilidad y la fatiga empeoran hacia el final del día. La MG generalmente comienza con debilidad ocular (del ojo); luego podría progresar a una forma generalizada más grave, caracterizada por debilidad en las extremidades o en los músculos que controlan las funciones básicas de la vida.
Ojos
En alrededor de dos tercios de las personas, el síntoma inicial de la MG está relacionado con los músculos que rodean el ojo. Caída del párpado (puede ocurrir ptosis debido a la debilidad del músculo elevador del párpado superior) y visión doble (diplopía, debido a la debilidad de los músculos extraoculares). Los síntomas oculares tienden a empeorar cuando mira televisión, lee o conduce, particularmente en condiciones de mucha luz. En consecuencia, algunas personas afectadas optan por usar gafas de sol. El término "miastenia gravis ocular" describe un subtipo de MG donde la debilidad muscular se limita a los ojos, es decir, músculos extraoculares, m. elevador del párpado superior y m. orbicularis oculi. Por lo general, este subtipo evoluciona a MG generalizada, generalmente después de algunos años.
Comer
La debilidad de los músculos implicados en la deglución puede provocar dificultad para tragar (disfagia). Por lo general, esto significa que es posible que quede algo de comida en la boca después de intentar tragar, o que la comida y los líquidos regurgiten en la nariz en lugar de pasar por la garganta (insuficiencia velofaríngea). La debilidad de los músculos que mueven la mandíbula (músculos de la masticación) puede causar dificultad para masticar. En las personas con MG, la masticación tiende a volverse más agotadora cuando se mastican alimentos duros y fibrosos. La dificultad para tragar, masticar y hablar es el primer síntoma en alrededor de una sexta parte de las personas.
Hablar
La debilidad de los músculos implicados en el habla puede provocar disartria e hipofonía. El habla puede ser lenta y arrastrada, o tener una cualidad nasal. En algunos casos, se debe abandonar una afición o profesión de canto.
Cabeza y cuello
Debido a la debilidad de los músculos de la expresión facial y los músculos de la masticación, la debilidad facial puede manifestarse como la incapacidad para mantener la boca cerrada (el "signo de la mandíbula colgante") y como una expresión de gruñido cuando se intenta sonrisa. Con los párpados caídos, la debilidad facial puede hacer que el individuo parezca somnoliento o triste. Puede haber dificultad para mantener la cabeza erguida.
Otro
Los músculos que controlan la respiración y los movimientos de las extremidades también pueden verse afectados; rara vez se presentan como los primeros síntomas de la MG, pero se desarrollan a lo largo de meses o años. En una crisis miasténica, se produce una parálisis de los músculos respiratorios, lo que requiere ventilación asistida para mantener la vida. Las crisis pueden ser desencadenadas por diversos factores estresantes biológicos, como infecciones, fiebre, una reacción adversa a un medicamento o estrés emocional.
Fisiopatología
MG es una sinaptopatía autoinmune. El trastorno ocurre cuando el sistema inmunológico funciona mal y genera anticuerpos que atacan los tejidos del cuerpo. Los anticuerpos en MG atacan una proteína humana normal, el receptor nicotínico de acetilcolina, o una proteína relacionada llamada MuSK, una cinasa específica de músculo. Otros anticuerpos menos frecuentes se encuentran contra las proteínas LRP4, agrina y titina.
Los haplotipos de antígenos leucocitarios humanos están asociados con una mayor susceptibilidad a la miastenia gravis y otros trastornos autoinmunes. Los familiares de personas con miastenia grave tienen un mayor porcentaje de otros trastornos inmunológicos.
Las células de la glándula timo forman parte del sistema inmunológico del cuerpo. En aquellos con miastenia gravis, la glándula del timo es grande y anormal. A veces contiene grupos de células inmunitarias que indican hiperplasia linfoide, y la glándula timo puede dar instrucciones incorrectas a las células inmunitarias.
En el embarazo
Para las mujeres que están embarazadas y ya tienen MG, en un tercio de los casos, se sabe que experimentan una exacerbación de sus síntomas y, en esos casos, generalmente ocurre en el primer trimestre del embarazo. Los signos y síntomas en las madres embarazadas tienden a mejorar durante el segundo y tercer trimestre. La remisión completa puede ocurrir en algunas madres. La terapia inmunosupresora debe mantenerse durante todo el embarazo, ya que reduce la posibilidad de debilidad muscular neonatal y controla la miastenia de la madre.
Alrededor del 10 al 20 % de los bebés de madres afectadas por la afección nacen con miastenia neonatal transitoria (TNM), que generalmente produce dificultades respiratorias y de alimentación que se desarrollan entre 12 horas y varios días después del nacimiento. Un niño con TNM suele responder muy bien a los inhibidores de la acetilcolinesterasa y, por lo general, la afección se resuelve en un período de tres semanas, a medida que disminuyen los anticuerpos, y por lo general no genera complicaciones. En muy raras ocasiones, un bebé puede nacer con artrogriposis múltiple congénita, secundaria a una debilidad intrauterina profunda. Esto se debe a los anticuerpos maternos que se dirigen a los receptores de acetilcolina del bebé. En algunos casos, la madre permanece asintomática.
Diagnóstico
La MG puede ser difícil de diagnosticar, ya que los síntomas pueden ser sutiles y difíciles de distinguir tanto de las variantes normales como de otros trastornos neurológicos.
Se pueden distinguir tres tipos de síntomas miasténicos en niños:
- La miastenia neonatal transitoria ocurre en el 10 al 15% de los bebés nacidos de madres afligidas con el trastorno, y desaparece después de unas semanas.
- La miastenia congénita, la forma más rara, ocurre cuando los genes están presentes de ambos padres.
- La miastenia juvenil gravis es más común en las mujeres.
Las miastenias congénitas causan debilidad muscular y fatigabilidad similares a las de la MG. Los signos de la miastenia congénita suelen estar presentes en los primeros años de la infancia, aunque es posible que no se reconozcan hasta la edad adulta.
Clasificación
| Clase | Descripción |
|---|---|
| I | Cualquier debilidad muscular ocular, posible ptosis, ninguna otra evidencia de debilidad muscular en otro lugar |
| II | Debilidad muscular del ojo de cualquier gravedad, debilidad leve de otros músculos |
| IIa | Extremidad predominante o músculos axiales |
| IIb | Predominantemente bulbar y/o músculos respiratorios |
| III | Debilidad muscular del ojo de cualquier gravedad, debilidad moderada de otros músculos |
| IIIa | Extremidad predominante o músculos axiales |
| IIIb | Predominantemente bulbar y/o músculos respiratorios |
| IV | Debilidad muscular del ojo de cualquier gravedad, debilidad severa de otros músculos |
| IVa | Extremidad predominante o músculos axiales |
| IVb | Predominantemente bulbar y/o músculos respiratorios |
| V | Intubación necesaria para mantener la vía aérea |
Cuando se diagnostica MG, se evalúa el estado neurológico de la persona y se establece el nivel de la enfermedad. Esto generalmente se hace usando la escala de Clasificación Clínica de la Miastenia Gravis Foundation of America aceptada.
Examen físico
Durante un examen físico para detectar MG, el médico puede pedirle a la persona que realice movimientos repetitivos. Por ejemplo, el médico puede pedirle que mire a un punto fijo durante 30 segundos y que relaje los músculos de la frente, porque una persona con MG y ptosis de los ojos podría estar usando involuntariamente los músculos de la frente para compensar la debilidad en los ojos. párpados El examinador clínico también podría tratar de obtener el "signo de la cortina" en una persona manteniendo uno de los ojos de la persona abierto, lo que en el caso de MG hará que el otro ojo se cierre.
Análisis de sangre
Si se sospecha el diagnóstico, se puede realizar una serología:
- Una prueba es para anticuerpos contra el receptor de acetilcolina; la prueba tiene una sensibilidad razonable del 80-96%, pero en la miastenia ocular, la sensibilidad cae al 50%.
- Una proporción de personas sin anticuerpos contra el receptor de acetilcolina tienen anticuerpos contra la proteína MuSK.
- En situaciones específicas, se realizan pruebas para el síndrome de Lambert-Eaton.
Electrodiagnóstico
Las fibras musculares de las personas con MG se fatigan con facilidad, lo que la prueba de estimulación nerviosa repetitiva puede ayudar a diagnosticar. En la electromiografía de fibra única, que se considera la prueba más sensible (aunque no la más específica) para la MG, se inserta un electrodo de aguja delgada en diferentes áreas de un músculo en particular para registrar los potenciales de acción de varias muestras de diferentes músculos individuales. fibras Se identifican dos fibras musculares pertenecientes a la misma unidad motora y se mide la variabilidad temporal en sus patrones de activación. La frecuencia y la proporción de patrones de potencial de acción anormales particulares, llamados "jitter" y "bloqueo", son de diagnóstico. Jitter se refiere a la variación anormal en el intervalo de tiempo entre los potenciales de acción de las fibras musculares adyacentes en la misma unidad motora. El bloqueo se refiere a la falla de los impulsos nerviosos para provocar potenciales de acción en las fibras musculares adyacentes de la misma unidad motora.
Prueba de hielo
La aplicación de hielo durante 2 a 5 minutos en los músculos tiene una sensibilidad y una especificidad del 76,9 % y del 98,3 %, respectivamente, para la identificación de la MG. Se cree que la acetilcolinesterasa se inhibe a la temperatura más baja, que es la base de esta prueba de diagnóstico. Esto generalmente se realiza en los párpados cuando hay ptosis y se considera positivo si se produce un aumento de ≥2 mm en el párpado después de retirar el hielo.
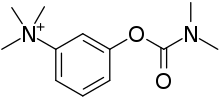
Prueba de edrofonio
Esta prueba requiere la administración intravenosa de cloruro de edrofonio o neostigmina, fármacos que bloquean la descomposición de la acetilcolina por la colinesterasa (inhibidores de la acetilcolinesterasa). Esta prueba ya no se realiza normalmente, ya que su uso puede provocar bradicardia (frecuencia cardíaca lenta) potencialmente mortal que requiere atención de emergencia inmediata. La producción de edrofonio se suspendió en 2008.
Imágenes
Una radiografía de tórax puede identificar un ensanchamiento del mediastino que sugiere un timoma, pero la tomografía computarizada o la resonancia magnética nuclear (RMN) son formas más sensibles de identificar los timomas y generalmente se realizan por este motivo. También se puede realizar una resonancia magnética del cráneo y las órbitas para descartar lesiones compresivas e inflamatorias de los nervios craneales y los músculos oculares.
Prueba de función pulmonar
La capacidad vital forzada puede controlarse a intervalos para detectar una debilidad muscular creciente. En forma aguda, se puede usar la fuerza inspiratoria negativa para determinar la idoneidad de la ventilación; se realiza en aquellas personas con MG.
Administración
El tratamiento es con medicación y/o cirugía. La medicación consiste principalmente en inhibidores de la acetilcolinesterasa para mejorar directamente la función muscular y fármacos inmunosupresores para reducir el proceso autoinmune. La timectomía es un método quirúrgico para tratar la MG.
Medicación
Puede empeorar con medicamentos como fluoroquinolonas, aminoglucósidos y magnesio. Alrededor del 10 % de las personas con MG generalizada se consideran refractarias al tratamiento. El trasplante autólogo de células madre hematopoyéticas (HSCT, por sus siglas en inglés) a veces se usa en la MG grave refractaria al tratamiento. Los datos disponibles proporcionan evidencia preliminar de que el HSCT puede ser una opción terapéutica eficaz en casos cuidadosamente seleccionados.
Efgartigimod alfa fue aprobado para uso médico en los Estados Unidos en diciembre de 2021.
Inhibidores de la acetilcolinesterasa
Los inhibidores de la acetilcolinesterasa pueden proporcionar un beneficio sintomático y es posible que no eliminen por completo la debilidad de la MG en una persona. Si bien es posible que no eliminen por completo todos los síntomas de la MG, aún pueden permitir que una persona realice sus actividades diarias normales. Por lo general, los inhibidores de la acetilcolinesterasa se inician con una dosis baja y se aumentan hasta lograr el resultado deseado. Si se toma 30 minutos antes de una comida, los síntomas serán leves durante la comida, lo que es útil para quienes tienen dificultad para tragar debido a su enfermedad. Otro medicamento utilizado para la MG, la atropina, puede reducir los efectos secundarios muscarínicos de los inhibidores de la acetilcolinesterasa. La piridostigmina es un fármaco de acción relativamente prolongada (en comparación con otros agonistas colinérgicos), con una vida media de alrededor de cuatro horas y relativamente pocos efectos secundarios. Generalmente, se suspende en aquellos que están siendo ventilados mecánicamente, ya que se sabe que aumenta la cantidad de secreciones salivales. Unos pocos estudios de alta calidad compararon directamente los inhibidores de la colinesterasa con otros tratamientos (o placebo); su beneficio práctico puede ser tal que sería difícil realizar estudios en los que se les negarían a algunas personas.
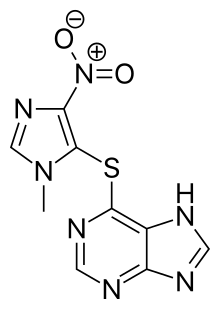
Supresores inmunológicos
El esteroide prednisona también se puede usar para lograr un mejor resultado, pero puede provocar el empeoramiento de los síntomas y lleva semanas lograr su máxima eficacia. Debido a la miríada de síntomas que pueden causar los tratamientos con esteroides, no es el método de tratamiento preferido. También se pueden usar otros medicamentos inmunosupresores, incluidos rituximab o azatioprina.
Plasmaféresis e IVIG
Si la miastenia es grave (crisis miasténica), se puede utilizar la plasmaféresis para eliminar los supuestos anticuerpos de la circulación. Además, se pueden usar inmunoglobulinas intravenosas (IGIV) para unir los anticuerpos circulantes. Ambos tratamientos tienen beneficios de duración relativamente corta, generalmente medidos en semanas, y a menudo están asociados con costos altos, lo que los hace prohibitivos; generalmente se reservan para cuando la MG requiere hospitalización.
Cirugía
Como los timomas se observan en el 10 % de todas las personas con MG, a menudo se les realiza una radiografía de tórax y una tomografía computarizada para evaluar la necesidad de extirpar quirúrgicamente las glándulas del timo y cualquier tejido canceroso que pueda estar presente. Incluso si se realiza una cirugía para extirpar un timoma, generalmente no conduce a la remisión de la MG. La cirugía en el caso de la MG consiste en la extirpación del timo, aunque en 2013 no se indicaba un claro beneficio salvo en presencia de un timoma. Sin embargo, un ensayo aleatorizado y controlado de 2016 encontró algunos beneficios.
Medidas físicas
Se debe educar a las personas con MG sobre la naturaleza fluctuante de sus síntomas, incluida la debilidad y la fatiga inducida por el ejercicio. Se debe alentar la participación en el ejercicio con descansos frecuentes. En personas con MG generalizada, alguna evidencia indica que un programa casero parcial que incluya entrenamiento en respiración diafragmática, respiración con los labios fruncidos y terapia muscular basada en intervalos puede mejorar la fuerza de los músculos respiratorios, la movilidad de la pared torácica, el patrón respiratorio y la resistencia respiratoria.
Imágenes médicas
En las personas con miastenia grave, las formas más antiguas de contraste yodado utilizadas para imágenes médicas han causado un mayor riesgo de exacerbación de la enfermedad, pero las formas modernas no tienen un mayor riesgo inmediato.
Pronóstico
El pronóstico de las personas con MG generalmente es bueno, al igual que la calidad de vida, con un tratamiento muy bueno. El seguimiento de una persona con MG es muy importante, ya que al menos el 20% de las personas diagnosticadas experimentarán una crisis miasténica dentro de los dos años posteriores a su diagnóstico, lo que requerirá una intervención médica rápida. En general, el período más incapacitante de la MG puede ser años después del diagnóstico inicial. A principios del siglo XX, el 70 % de los casos detectados morían por problemas pulmonares; ahora, se estima que ese número es de alrededor del 3% al 5%, lo que se atribuye a una mayor conciencia y medicamentos para controlar los síntomas.
Epidemiología
MG ocurre en todos los grupos étnicos y en ambos sexos. Afecta más comúnmente a mujeres menores de 40 años y personas de 50 a 70 años de cualquier sexo, pero se sabe que ocurre a cualquier edad. Las personas más jóvenes rara vez tienen timoma. La prevalencia en los Estados Unidos se estima entre 0,5 y 20,4 casos por 100 000, con un estimado de 60 000 estadounidenses afectados. Dentro del Reino Unido, se estima que ocurren 15 casos de MG por cada 100 000 personas.
Historia
Los primeros en escribir sobre MG fueron Thomas Willis, Samuel Wilks, Erb y Goldflam. El término "miastenia grave pseudoparalítica" fue propuesto en 1895 por Jolly, un médico alemán. Mary Walker trató a una persona con MG con fisostigmina en 1934. Simpson y Nastuck detallaron la naturaleza autoinmune de la condición. En 1973, Patrick y Lindstrom usaron conejos para demostrar que la inmunización con receptores de acetilcolina similares a músculos purificados provocaba el desarrollo de síntomas similares a los de la MG.
Investigación
Actualmente se están investigando sustancias inmunomoduladoras, como fármacos que impiden la modulación del receptor de acetilcolina por parte del sistema inmunitario. Algunas investigaciones recientes se han centrado en los inhibidores anti-c5 para la investigación de tratamientos, ya que son seguros y se usan en el tratamiento de otras enfermedades. La efedrina parece beneficiar a algunas personas más que a otros medicamentos, pero no se ha estudiado adecuadamente hasta 2014. En el laboratorio, la MG se estudia principalmente en organismos modelo, como roedores. Además, en 2015, los científicos desarrollaron un ensayo de unión neuromuscular totalmente humano funcional in vitro a partir de células madre embrionarias humanas y células madre de músculo somático. Después de la adición de anticuerpos patógenos contra el receptor de acetilcolina y la activación del sistema del complemento, el cocultivo neuromuscular muestra síntomas como contracciones musculares más débiles.
Contenido relacionado
Enfermedad de Von Hippel-Lindau
Labios menores
Cólera