Método Kjeldahl
El método Kjeldahl o digestión Kjeldahl (pronunciación danesa: IPA nowrap" lang="da-Latn-fonipa">[ˈkʰelˌtɛˀl]) en química analítica es un método para la determinación cuantitativa del nitrógeno orgánico más amoníaco/amonio de una muestra (NH3/NH4+). Sin modificación, otras formas de nitrógeno inorgánico, por ejemplo, el nitrato, no se incluyen en esta medición. Utilizando una relación empírica entre el nitrógeno Kjeldahl y la proteína, es un método importante para cuantificar indirectamente el contenido de proteína de una muestra. Este método fue desarrollado por Johan Kjeldahl en 1883.
Método
El método consiste en calentar una muestra a 360–410 °C con ácido sulfúrico concentrado (H2SO4), que descompone ("digiere" o "destruye") la muestra orgánica por oxidación para liberar el nitrógeno reducido como sulfato de amonio. El ácido sulfúrico concentrado caliente oxida el carbono (como el carbón bituminoso) y el azufre (ver reacciones del ácido sulfúrico con el carbono):
- C + 2 H2Así que...4 → CO2 + 2 SO2 + 2 H2O
- S + 2 H2Así que...4 → 3 SO2 + 2 H2O
A menudo se añaden catalizadores como selenio, Hg2SO4 o CuSO4 para acelerar la digestión. También se añade Na2SO4 o K2SO4 para aumentar el punto de ebullición del H2SO4. La digestión se completa cuando el licor se clarifica con la liberación de vapores. A continuación se muestra un sistema de destilación.
 | 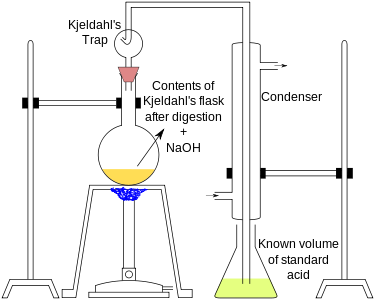 |
El extremo del condensador se sumerge en un volumen conocido de ácido estándar (es decir, ácido de concentración conocida). A menudo se utiliza un ácido débil como el ácido bórico (H3BO3) en exceso de amoníaco. En su lugar, se puede utilizar HCl estandarizado, H2SO4 o algún otro ácido fuerte, pero esto es menos habitual. A continuación, la solución de muestra se destila con una pequeña cantidad de hidróxido de sodio (NaOH). También se puede añadir NaOH con un embudo de goteo. El NaOH hace reaccionar el amonio (NH4+) a amoníaco (NH3), que evapora la solución de muestra. El amoníaco burbujea a través de la solución de ácido estándar y reacciona de nuevo en sales de amonio con el ácido débil o fuerte.
La concentración de iones de amonio en la solución ácida y, por lo tanto, la cantidad de nitrógeno en la muestra, se mide mediante titulación. Si se utilizó ácido bórico (o algún otro ácido débil), se realiza una titulación directa ácido-base con un ácido fuerte de concentración conocida. Se puede utilizar HCl o H2SO4. En cambio, si se utilizaron ácidos fuertes para preparar la solución ácida estándar, se utiliza una titulación indirecta por retroceso: se utiliza una base fuerte de concentración conocida (como NaOH) para neutralizar la solución. En este caso, la cantidad de amoníaco se calcula como la diferencia entre la cantidad de HCl y NaOH. En el caso de la titulación directa, no es necesario saber la cantidad exacta de ácido débil (p. ej., ácido bórico) porque no interfiere con la titulación (tiene que ser en exceso de amoníaco para atraparlo de manera eficiente). Por lo tanto, se necesita una solución estándar (p. ej. HCl) en la titulación directa, mientras que se necesitan dos (p. ej. HCl y NaOH) en la titulación por retroceso. Uno de los indicadores adecuados para estas reacciones de titulación es el indicador de Tashiro.
En la práctica, este análisis está en gran medida automatizado; los catalizadores específicos aceleran la descomposición. Originalmente, el catalizador de elección era el óxido de mercurio. Sin embargo, aunque era muy eficaz, los problemas de salud hicieron que se lo sustituyera por el sulfato cúprico. El sulfato cúprico no era tan eficaz como el óxido de mercurio y arrojaba resultados de proteínas más bajos. Pronto se complementó con dióxido de titanio, que actualmente es el catalizador aprobado en todos los métodos de análisis de proteínas en los Métodos Oficiales y Prácticas Recomendadas de la AOAC International.
Aplicaciones
La universalidad, precisión y reproducibilidad del método Kjeldahl lo han convertido en el método internacionalmente reconocido para estimar el contenido de proteínas en los alimentos y es el método estándar con el que se comparan todos los demás métodos. También se utiliza para analizar suelos, aguas residuales, fertilizantes y otros materiales. Sin embargo, no proporciona una medida del contenido real de proteínas, ya que mide el nitrógeno no proteico además del nitrógeno presente en las proteínas. Esto se evidencia en el incidente de los alimentos para mascotas de 2007 y el escándalo de la leche en polvo china de 2008, cuando se añadió melamina, una sustancia química rica en nitrógeno, a las materias primas para simular un alto contenido de proteínas. Además, se necesitan diferentes factores de corrección para diferentes proteínas a fin de tener en cuenta las diferentes secuencias de aminoácidos. Otras desventajas, como la necesidad de utilizar ácido sulfúrico concentrado a alta temperatura y el tiempo de prueba relativamente largo (una hora o más), lo comparan desfavorablemente con el método Dumas para medir el contenido de proteína cruda.
Total Kjeldahl nitrogen
El nitrógeno total Kjeldahl o TKN es la suma del nitrógeno ligado a sustancias orgánicas, nitrógeno en amoniaco (NH3-N) y en amonio (NH4+-N) en el análisis químico del suelo, el agua o las aguas residuales (por ejemplo, los efluentes de las plantas de tratamiento de aguas residuales).
En la actualidad, el TKN es un parámetro obligatorio para la presentación de informes reglamentarios en muchas plantas de tratamiento y como medio para supervisar las operaciones de la planta.
Factores de conversión
El TKN se utiliza a menudo como sustituto de las proteínas en las muestras de alimentos. La conversión de TKN a proteína depende del tipo de proteína presente en la muestra y de qué fracción de la proteína está compuesta de aminoácidos nitrogenados, como la arginina y la histidina. Sin embargo, el rango de factores de conversión es relativamente estrecho. Los factores de conversión de ejemplo, conocidos como factores N, para los alimentos varían de 6,38 para los productos lácteos y 6,25 para la carne, los huevos, el maíz y el sorgo a 5,83 para la mayoría de los cereales; 5,95 para el arroz, 5,70 para la harina de trigo y 5,46 para los cacahuetes. En la práctica, se utiliza 6,25 para casi todos los alimentos y piensos, independientemente de su aplicabilidad. El factor 6,25 es un requisito específico de las normas de las etiquetas nutricionales de los EE. UU. en ausencia de otro factor publicado.
| Origen animal | Factor | semillas de hierbas | Factor | Alubias y cacahuetes | Factor |
|---|---|---|---|---|---|
| huevos | 6.25 | Barley | 5.83 | Castor bean | 5.30 |
| Carne | 6.25 | Corn (maíz) | 6.25 | Jack Bean | 6.25 |
| Milk | 6.38 | Millets | 5.83 | Lima bean | 6.25 |
| Oats | 5.83 | Marine bean | 6.25 | ||
| Rice | 5.95 | Mung bean | 6.25 | ||
| Rye | 5.83 | Soybean | 5.71 | ||
| Sorghum | 6.25 | Velvet bean | 6.25 | ||
| Trigo: núcleo completo | 5.83 | Maní | 5.46 | ||
| Trigo: latón | 6.31 | ||||
| Trigo: Endosperm | 5.70 |
Sensibilidad
El método Kjeldahl es poco sensible en su versión original. Se han utilizado otros métodos de detección para cuantificar el NH4+ tras la mineralización y la destilación, consiguiendo una sensibilidad mejorada: generador en línea de hidruro acoplado a un espectrómetro de emisión atómica de plasma (ICP-AES-HG, 10–25 mg/L), titulación potenciométrica (>0,1 mg de nitrógeno), electroforesis capilar en zona (1,5 μg/mL de nitrógeno) y cromatografía iónica (0,5 μg/mL).
Limitaciones
El método Kjeldahl no es aplicable a compuestos que contienen nitrógeno en grupos nitro y azo y nitrógeno presente en anillos (por ejemplo, piridina, quinolina, isoquinolina) ya que el nitrógeno de estos compuestos no se convierte en sulfato de amonio en las condiciones de este método.
Véase también
- Método Dumas, otro método de análisis de nitrógeno
- Aleación de Devarda, un poderoso agente de reducción para análisis de nitratos
- Ensayo de ácido bicinconinico, un ensayo colorimétrico para proteína-nitrógeno
- Análisis de combustión otro método de análisis de carbono, hidrógeno y nitrógeno
Referencias
- ^ Kjeldahl, J. (1883) "Neue Methode zur Bestimmung des Stickstoffs in organischen Körpern" (Nuevo método para la determinación del nitrógeno en sustancias orgánicas), Zeitschrift für analytische Chemie, 22 (1): 366-383.
- ^ Julius B. Cohen Química Orgánica Práctica 1910 Enlace al texto en línea
- ^ a b c d e Michałowski, T; Asuero, AG; Wybraniec, S (2013-02-12). "La Titación en el Método Kjeldahl de Determinación de Nitrógeno: Base o Ácido como Titrant?". Journal of Chemical Education. 90 (2): 191–197. Código:2013JChEd...90..191M. doi:10.1021/ed200863p. ISSN 0021-9584.
- ^ "Internacional Starch: ISI 24 Determination of Protein by Kjeldahl". www.starch.dk. Retrieved 2019-03-21.
- ^ AOAC Internacional
- ^ D. Julian McClements. "Análisis de Proteínas". University of Massachusetts Amherst. Retrieved 2007-04-27.
- ^ "Capítulo 2: MÉTODOS DE ANALISIS FOOD". Fao.org. Retrieved 30 de diciembre 2017.
- ^ "21 CFR 101.9 c)(7)".
- ^ "Capítulo 2: métodos de análisis de alimentos". www.fao.org2020-11-14. Archivado desde el original el 21 de septiembre de 2012. Retrieved 2021-02-05.
- ^ A.M.Y. Jaber; N.A. Mehanna; S.M. Sultan (2009). "Determinación de amonio y nitrógeno orgánico ligado por espectroscopia de emisión de plasma inductivamente acoplada". Talanta. 78 (4–5): 1298–1302. doi:10.1016/j.talanta.2009.01.060. PMID 19362191.
- ^ "Intérêt de l'ECZ pour le dosage de l'azote total (méthode de Kjeldahl) - Blog Pharma Physic". Blog.pharmaphysic.fr5 de abril de 2012. Retrieved 30 de diciembre 2017.
- ^ "Peut-on éviter l'étape de distillation dans la méthode Kjeldahl"? - Blog Pharma Physic". Blog.pharmaphysic.fr26 de abril de 2012. Retrieved 30 de diciembre 2017.
Bibliografía
- Ingeniería de aguas residuales: Tratamiento y Reutilización, Metcalf ' Eddy, McGraw-Hill Higher Education; 4th edition, 1 May 2002, ISBN 978-0071241403
Enlaces externos
- Soluciones para la automatización del método Kjeldahl
- Kjeldahl Proficiency guide