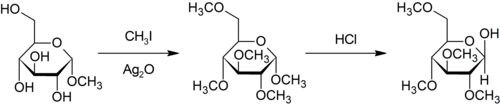Metilación
En las ciencias químicas, metilación denota la adición de un grupo metilo en un sustrato, o la sustitución de un átomo (o grupo) por un grupo metilo. La metilación es una forma de alquilación, con un grupo metilo reemplazando un átomo de hidrógeno. Estos términos se usan comúnmente en química, bioquímica, ciencia del suelo y ciencias biológicas.
En los sistemas biológicos, la metilación es catalizada por enzimas; dicha metilación puede estar involucrada en la modificación de metales pesados, la regulación de la expresión génica, la regulación de la función de las proteínas y el procesamiento del ARN. La metilación in vitro de muestras de tejido también es un método para reducir ciertos artefactos de tinción histológica. Lo contrario de la metilación es la desmetilación.
En biología
En los sistemas biológicos, la metilación se lleva a cabo mediante enzimas. La metilación puede modificar los metales pesados, regular la expresión génica, el procesamiento del ARN y la función de las proteínas. Se ha reconocido como un proceso clave subyacente a la epigenética.
Metanogénesis
La metanogénesis, el proceso que genera metano a partir de CO2, implica una serie de reacciones de metilación. Estas reacciones son efectuadas por un conjunto de enzimas albergadas por una familia de microbios anaerobios.
En la metanogénesis inversa, el metano sirve como agente de metilación.
O-metiltransferasas
Una amplia variedad de fenoles se someten a O-metilación para dar derivados de anisol. Este proceso, catalizado por enzimas como la cafeoil-CoA O-metiltransferasa, es una reacción clave en la biosíntesis de lignoles, precursores de la lignina, un componente estructural importante de las plantas.
Las plantas producen flavonoides e isoflavonas con metilaciones en los grupos hidroxilo, es decir, enlaces metoxi. Esta 5-O-metilación afecta la solubilidad en agua de los flavonoides. Los ejemplos son 5-O-metilgenisteína, 5-O-metilmiricetina o 5-O-metilquercetina, también conocida como azaleatina.
Proteínas
Junto con la ubiquitina y la fosforilación, la metilación es un proceso bioquímico importante para modificar la función de las proteínas. Las metilaciones de proteínas más prevalentes afectan a los residuos de arginina y lisina de histonas específicas. De lo contrario, la histidina, el glutamato, la asparagina y la cisteína son susceptibles de metilación. Algunos de estos productos incluyen S-metilcisteína, dos isómeros de N-metilhistidina y dos isómeros de N-metilarginina.
Metionina sintasa
La metionina sintasa regenera la metionina (Met) a partir de la homocisteína (Hcy). La reacción general transforma el 5-metiltetrahidrofolato (N5-MeTHF) en tetrahidrofolato (THF) mientras transfiere un grupo metilo a Hcy para formar Met. Las metionina sintasas pueden ser dependientes de cobalamina e independientes de cobalamina: las plantas tienen ambas, los animales dependen de la forma dependiente de metilcobalamina.
En las formas de la enzima dependientes de metilcobalamina, la reacción se desarrolla en dos pasos en una reacción de ping-pong. La enzima se prepara inicialmente a un estado reactivo mediante la transferencia de un grupo metilo de N5-MeTHF a Co(I) en la cobalamina unida a la enzima (Cob), formando metil-cobalamina (Me-Cob) que ahora contiene Me-Co(III) y activando la enzima. Luego, una Hcy que se ha coordinado con un zinc unido a una enzima para formar un tiolato reactivo reacciona con el Me-Cob. El grupo metilo activado se transfiere de Me-Cob al tiolato de Hcy, que regenera Co(I) en Cob, y Met se libera de la enzima.
Metales pesados: arsénico, mercurio, cadmio
La biometilación es la vía para convertir algunos elementos pesados en derivados más móviles o más letales que pueden entrar en la cadena alimentaria. La biometilación de los compuestos de arsénico comienza con la formación de metanoarsonatos. Por lo tanto, los compuestos de arsénico inorgánico trivalente se metilan para dar metanoarsonato. S-adenosilmetionina es el donante de metilo. Los metanoarsonatos son los precursores de los dimetilarsonatos, nuevamente por el ciclo de reducción (a ácido metilarsonoso) seguido de una segunda metilación. Vías relacionadas se aplican a la biosíntesis de metilmercurio.
Metilación epigenética
Metilación de ADN/ARN
La metilación del ADN en los vertebrados generalmente ocurre en los sitios CpG (sitios de citosina-fosfato-guanina, es decir, donde una citosina es seguida directamente por una guanina en la secuencia de ADN). Esta metilación da como resultado la conversión de la citosina en 5-metilcitosina. La formación de Me-CpG es catalizada por la enzima ADN metiltransferasa. En los mamíferos, la metilación del ADN es común en las células del cuerpo y la metilación de los sitios CpG parece ser la predeterminada. El ADN humano tiene alrededor del 80-90 % de los sitios CpG metilados, pero hay ciertas áreas, conocidas como islas CpG, que son ricas en CG (alto contenido de citosina y guanina, compuesto por alrededor del 65 % de residuos de CG), en las que ninguno está metilado. Estos están asociados con los promotores del 56% de los genes de mamíferos, incluidos todos los genes expresados de forma ubicua. Entre uno y dos por ciento del genoma humano son grupos de CpG y existe una relación inversa entre la metilación de CpG y la actividad transcripcional. La metilación que contribuye a la herencia epigenética puede ocurrir a través de la metilación del ADN o la metilación de proteínas. Las metilaciones inadecuadas de los genes humanos pueden conducir al desarrollo de enfermedades, incluido el cáncer. De manera similar, la metilación del ARN ocurre en diferentes especies de ARN, a saber. tRNA, rRNA, mRNA, tmRNA, snRNA, snoRNA, miRNA y RNA viral. Se emplean diferentes estrategias catalíticas para la metilación del ARN por una variedad de ARN-metiltransferasas. Se cree que la metilación del ARN existió antes que la metilación del ADN en las primeras formas de vida que evolucionaron en la Tierra.
N6-metiladenosina (m6A) es la modificación de metilación más común y abundante en las moléculas de ARN (ARNm) presente en eucariotas. La 5-metilcitosina (5-mC) también se encuentra comúnmente en varias moléculas de ARN. Datos recientes sugieren fuertemente que la metilación del ARN m6A y 5-mC afecta la regulación de varios procesos biológicos, como la estabilidad del ARN y la traducción del ARNm, y que la metilación anormal del ARN contribuye a la etiología de las enfermedades humanas.
Metilación de proteínas
La metilación de proteínas generalmente tiene lugar en los residuos de aminoácidos de arginina o lisina en la secuencia de la proteína. La arginina se puede metilar una vez (arginina monometilada) o dos veces, con ambos grupos metilo en un nitrógeno terminal (dimetilarginina asimétrica) o uno en ambos nitrógenos (dimetilarginina simétrica), por proteínas arginina metiltransferasas (PRMT). La lisina puede ser metilada una, dos o tres veces por metiltransferasas de lisina. La metilación de proteínas ha sido más estudiada en las histonas. La transferencia de grupos metilo de la S-adenosil metionina a las histonas está catalizada por enzimas conocidas como histona metiltransferasas. Las histonas que están metiladas en ciertos residuos pueden actuar epigenéticamente para reprimir o activar la expresión génica. La metilación de proteínas es un tipo de modificación postraduccional.
Evolución
El metabolismo de metilo es muy antiguo y se puede encontrar en todos los organismos de la tierra, desde bacterias hasta humanos, lo que indica la importancia del metabolismo de metilo para la fisiología. De hecho, la inhibición farmacológica de la metilación global en especies que van desde humanos, ratones, peces, moscas, gusanos redondos, plantas, algas y cianobacterias provoca los mismos efectos en sus ritmos biológicos, lo que demuestra funciones fisiológicas conservadas de la metilación durante la evolución.
En química
El término metilación en química orgánica se refiere al proceso de alquilación utilizado para describir la entrega de un CH3 grupo.
Metilación electrofílica
Las metilaciones se suelen realizar con fuentes de metilo electrofílicas, como yodometano, sulfato de dimetilo, carbonato de dimetilo o cloruro de tetrametilamonio. Los reactivos de metilación menos comunes pero más potentes (y más peligrosos) incluyen triflato de metilo, diazometano y fluorosulfonato de metilo (metilo mágico). Todos estos reactivos reaccionan a través de sustituciones nucleofílicas SN2. Por ejemplo, un carboxilato se puede metilar en oxígeno para dar un éster metílico; una sal de alcóxido RO− también puede metilarse para dar un éter, ROCH3; o un enolato de cetona puede metilarse sobre carbono para producir una nueva cetona.
La metilación de Purdie es específica para la metilación en oxígeno de carbohidratos utilizando yodometano y óxido de plata.
Metilación de Eschweiler-Clarke
La reacción de Eschweiler-Clarke es un método para la metilación de aminas. Este método evita el riesgo de cuaternización, que ocurre cuando las aminas se metilan con haluros de metilo.
Diazometano y trimetilsilildiazometano
Diazometano y el análogo más seguro trimetilsilildiazometano metilato de ácidos carboxílicos, fenoles e incluso alcoholes:
- RCO2CH3 + CH3Otms + N2}}}" xmlns="http://www.w3.org/1998/Math/MathML">RCO2H+tmsCHN2+CH3Oh.restablecimiento restablecimiento RCO2CH3+CH3Otms+N2{displaystyle {ce {RCO2H + tmsCHN2 + CH3OH - titulada RCO2CH3 + CH3Otms + N2}}}
RCO2CH3 + CH3Otms + N2}}}" aria-hidden="true" class="mwe-math-fallback-image-inline" src="https://wikimedia.org/api/rest_v1/media/math/render/svg/99e6a069dc908747dac07cd0714c61760f4b816a" style="vertical-align: -1.005ex; width:66.018ex; height:2.843ex;"/>
El método ofrece la ventaja de que los productos secundarios se eliminan fácilmente de la mezcla de productos.
Metilación nucleófila
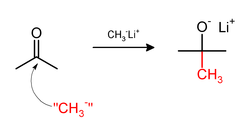
La metilación a veces implica el uso de reactivos de metilo nucleofílico. Los agentes de metilación fuertemente nucleofílicos incluyen metillitio (CH3Li) o reactivos de Grignard como bromuro de metilmagnesio (CH3MgX). Por ejemplo, CH3Li agregará grupos metilo al carbonilo (C=O) de las cetonas y aldehído.:
Los agentes de metilación más suaves incluyen tetrametilestaño, dimetilzinc y trimetilaluminio.
Contenido relacionado
Quiralidad (desambiguación)
Tiamina
Petroquímica