Metformina
La metformina, vendida bajo la marca Glucophage, entre otros, es el principal medicamento de primera línea para el tratamiento de la diabetes tipo 2, especialmente en personas con sobrepeso.. También se utiliza en el tratamiento del síndrome de ovario poliquístico. A veces se usa como complemento no indicado en la etiqueta para disminuir el riesgo de síndrome metabólico en personas que toman antipsicóticos. La metformina no está asociada con el aumento de peso y se toma por vía oral.
La metformina generalmente se tolera bien. Los efectos adversos comunes incluyen diarrea, náuseas y dolor abdominal. Tiene un pequeño riesgo de causar niveles bajos de azúcar en la sangre. El nivel alto de ácido láctico en la sangre es una preocupación si el medicamento se usa en dosis demasiado grandes o se receta a personas con problemas renales graves.
La metformina es un agente antihiperglucémico biguanida. Actúa disminuyendo la producción de glucosa en el hígado, aumentando la sensibilidad a la insulina de los tejidos corporales y aumentando la secreción de GDF15, lo que reduce el apetito y la ingesta calórica.
La metformina fue descrita por primera vez en la literatura científica en 1922 por Emil Werner y James Bell. El médico francés Jean Sterne comenzó el estudio en humanos en la década de 1950. Se introdujo como medicamento en Francia en 1957 y en los Estados Unidos en 1995. La metformina se encuentra en la Lista de medicamentos esenciales de la Organización Mundial de la Salud y es el medicamento oral más utilizado para la diabetes. Está disponible como medicamento genérico. En 2020, fue el tercer medicamento recetado con más frecuencia en los Estados Unidos, con más de 92 millones de recetas.
Usos médicos
La metformina se usa para reducir la glucosa en sangre en personas con diabetes tipo 2. También se usa como agente de segunda línea para la infertilidad en personas con síndrome de ovario poliquístico.
Diabetes tipo 2
La Asociación Estadounidense de Diabetes y el Colegio Estadounidense de Médicos recomiendan la metformina como agente de primera línea para tratar la diabetes tipo 2. Es tan efectivo como la repaglinida y más efectivo que todos los demás medicamentos orales para la diabetes tipo 2.
Eficacia
Las pautas de tratamiento de las principales asociaciones profesionales, incluida la Asociación Europea para el Estudio de la Diabetes, la Sociedad Europea de Cardiología y la Asociación Estadounidense de Diabetes, describen la evidencia de los beneficios cardiovasculares de la metformina como equívoca. Una revisión sistemática Cochrane de 2020 no encontró suficiente evidencia de reducción de la mortalidad cardiovascular, infarto de miocardio no fatal o accidente cerebrovascular no fatal al comparar la monoterapia con metformina con otros medicamentos para reducir la glucosa, intervenciones de cambio de comportamiento, placebo o ninguna intervención.
El uso de metformina reduce el peso corporal en personas con diabetes tipo 2 en contraste con las sulfonilureas, que se asocian con el aumento de peso. Cierta evidencia muestra que la metformina está asociada con la pérdida de peso en la obesidad en ausencia de diabetes. La metformina tiene un menor riesgo de hipoglucemia que las sulfonilureas, aunque la hipoglucemia se ha producido con poca frecuencia durante el ejercicio intenso, el déficit de calorías o cuando se usa con otros agentes para reducir la glucosa en sangre. La metformina reduce modestamente las lipoproteínas de baja densidad y los niveles de triglicéridos.
En personas con prediabetes, una revisión sistemática de 2019 que comparó los efectos de la metformina con otras intervenciones en la reducción del riesgo de desarrollar diabetes tipo 2 encontró evidencia de calidad moderada de que la metformina redujo el riesgo de desarrollar diabetes tipo 2 en comparación con la dieta y el ejercicio o un placebo. Sin embargo, cuando se comparó la metformina con una dieta intensiva o ejercicio, se encontró evidencia de calidad moderada de que la metformina no redujo el riesgo de desarrollar diabetes tipo 2 y se encontró evidencia de calidad muy baja de que agregar metformina a una dieta o ejercicio intensivos no mostró ninguna ventaja o desventaja en la reducción del riesgo de diabetes tipo 2 en comparación con el ejercicio intensivo y la dieta solos. La misma revisión también encontró un ensayo adecuado que comparó los efectos de la metformina y la sulfonilurea en la reducción del riesgo de desarrollar diabetes tipo 2 en personas prediabéticas; sin embargo, este ensayo no informó ningún resultado relevante para los pacientes.
Síndrome de ovario poliquístico
En aquellas con síndrome de ovario poliquístico (SOP), la evidencia provisional muestra que el uso de metformina aumenta la tasa de nacidos vivos. Esto incluye a aquellas que no han podido quedar embarazadas con clomifeno. La metformina no parece cambiar el riesgo de aborto espontáneo. También se han encontrado otros beneficios tanto durante el embarazo como en mujeres no embarazadas con SOP. En una revisión Cochrane (2020) actualizada sobre metformina versus placebo/ningún tratamiento antes o durante la FIV/ICSI en mujeres con SOP, no se encontró evidencia concluyente de mejores tasas de nacidos vivos. En los protocolos prolongados de agonistas de la GnRH hubo incertidumbre en la evidencia de mejores tasas de nacidos vivos, pero podría haber aumentos en la tasa de embarazo clínico. En protocolos breves de antagonistas de GnRH, la metformina puede reducir las tasas de nacidos vivos con incertidumbre sobre su efecto en la tasa de embarazo clínico. La metformina puede resultar en una reducción del SHO, pero podría tener una mayor frecuencia de efectos secundarios. Hubo incertidumbre en cuanto al impacto de la metformina en el aborto espontáneo. La evidencia no respalda el uso general durante el embarazo para mejorar los resultados maternos e infantiles en mujeres obesas.
El Instituto Nacional para la Salud y la Excelencia Clínica del Reino Unido recomendó en 2004 que las mujeres con síndrome de ovario poliquístico y un índice de masa corporal superior a 25 recibieran metformina para la anovulación y la infertilidad cuando otras terapias no dieran resultados. Las guías de práctica clínica del Reino Unido e internacionales no recomiendan la metformina como tratamiento de primera línea o no la recomiendan en absoluto, excepto para las mujeres con intolerancia a la glucosa. Las pautas sugieren el clomifeno como la primera opción de medicación y enfatizan la modificación del estilo de vida independientemente del tratamiento médico. El tratamiento con metformina reduce el riesgo de desarrollar diabetes tipo 2 en mujeres con SOP que presentaban intolerancia a la glucosa al inicio del estudio.
Diabetes y embarazo
Una revisión total del uso de metformina durante el embarazo en comparación con la insulina sola encontró una buena seguridad a corto plazo tanto para la madre como para el bebé, pero una seguridad poco clara a largo plazo. Varios estudios observacionales y ensayos controlados aleatorios encontraron que la metformina es tan efectiva y segura como la insulina para el control de la diabetes gestacional. No obstante, se han planteado varias preocupaciones y falta evidencia sobre la seguridad a largo plazo de la metformina tanto para la madre como para el niño. En comparación con la insulina, las mujeres con diabetes gestacional tratadas con metformina aumentan menos de peso y tienen menos probabilidades de desarrollar preeclampsia durante el embarazo. Los bebés nacidos de mujeres tratadas con metformina tienen menos grasa visceral y esto puede hacerlos menos propensos a la resistencia a la insulina en el futuro. El uso de metformina para la diabetes gestacional resultó en bebés más pequeños en comparación con el tratamiento con insulina. Sin embargo, a pesar de un peso inicial más bajo al nacer, los niños expuestos a la metformina durante el embarazo tuvieron un crecimiento acelerado después del nacimiento y pesaban más a mediados de la infancia que los expuestos a la insulina durante el embarazo. Este patrón de bajo peso inicial al nacer seguido de un crecimiento compensatorio que supera a los niños de comparación se ha asociado con enfermedad cardiometabólica a largo plazo.
Cambio de peso
El uso de metformina generalmente se asocia con la pérdida de peso. Parece ser seguro y efectivo para contrarrestar el aumento de peso causado por los medicamentos antipsicóticos olanzapina y clozapina. Aunque se encuentra una modesta reversión del aumento de peso asociado con la clozapina con metformina, la prevención primaria del aumento de peso es más valiosa.
Uso con insulina
La metformina puede reducir el requerimiento de insulina en la diabetes tipo 1, aunque con un mayor riesgo de hipoglucemia.
Extensión de vida
Existe alguna evidencia de que la metformina puede ser útil para prolongar la esperanza de vida, incluso en personas sanas. Ha recibido un interés sustancial como agente que retrasa el envejecimiento, posiblemente a través de mecanismos similares a los de su tratamiento de la diabetes (regulación de la insulina y los carbohidratos).
Un estudio utilizó datos observacionales retrospectivos del Clinical Practice Research Datalink (CPRD) del Reino Unido de 2000. Sujetos con diabetes tipo 2 que progresaron al tratamiento de primera línea con metformina o sulfonilurea monoterapia fueron seleccionados y emparejados con personas sin diabetes. El estudio involucró a más de 180 000 sujetos y mostró que los pacientes con diabetes tipo 2 que comenzaron con monoterapia con metformina tenían una vida útil más larga que sus contrapartes no diabéticos, mientras que aquellos tratados con sulfonilureas tenían una supervivencia notablemente menor en comparación con controles emparejados y aquellos que recibieron monoterapia con metformina.
Enfermedad de Alzheimer
Se está investigando la posibilidad de que la metformina pueda retrasar el inicio o la progresión de la enfermedad de Alzheimer, o incluso prevenirla. Se ha publicado una variedad de investigaciones en este campo en un esfuerzo por establecer una correlación entre la diabetes tipo 2 y la enfermedad de Alzheimer. La investigación incluye estudios con participantes no diagnosticados con diabetes.
Contraindicaciones
La metformina está contraindicada en personas con:
- Afecto renal grave (tasa de filtración glomerular estimada (eGFR) inferior a 30 mL/min/1,73 m2)
- Hipersensibilidad conocida para metformin
- acidosis metabólica aguda o crónica, incluyendo cetoacidosis diabética (de diabetes incontrolada), con o sin coma
Efectos adversos
El efecto adverso más común de la metformina es la irritación gastrointestinal, que incluye diarrea, calambres, náuseas, vómitos y aumento de las flatulencias; la metformina se asocia más comúnmente con efectos adversos gastrointestinales que la mayoría de los otros medicamentos antidiabéticos. El efecto adverso potencial más grave de la metformina es la acidosis láctica; esta complicación es rara y parece estar relacionada con la función hepática o renal alterada. La metformina no está aprobada para su uso en personas con enfermedad renal grave, pero aún se puede usar en dosis más bajas en personas con problemas renales.
Aparato digestivo
El malestar gastrointestinal puede causar molestias graves; es más común cuando se administra metformina por primera vez o cuando se aumenta la dosis. La incomodidad a menudo se puede evitar comenzando con una dosis baja (1,0 a 1,7 g/día) y aumentando la dosis gradualmente, pero incluso con dosis bajas, el 5 % de las personas pueden no tolerar la metformina. El uso de preparaciones de liberación lenta o prolongada puede mejorar la tolerabilidad.
El uso a largo plazo de metformina se ha asociado con niveles elevados de homocisteína y malabsorción de vitamina B12. Las dosis más altas y el uso prolongado están asociados con una mayor incidencia de deficiencia de vitamina B12, y algunos investigadores recomiendan estrategias de detección o prevención.
Acidosis láctica
La acidosis láctica casi nunca ocurre con la exposición a la metformina durante la atención médica de rutina. Las tasas de acidosis láctica asociada a metformina son de aproximadamente nueve por cada 100 000 personas/año, que es similar a la tasa de fondo de acidosis láctica en la población general. Una revisión sistemática concluyó que no existen datos para vincular definitivamente la metformina con la acidosis láctica.
La metformina generalmente es segura en personas con enfermedad renal crónica de leve a moderada, con una reducción proporcional de la dosis de metformina según la gravedad de la tasa de filtración glomerular estimada (TFGe) y con evaluación periódica de la función renal (p. ej., medición periódica de creatinina plasmática). La Administración de Drogas y Alimentos de los EE. UU. (FDA) recomienda evitar el uso de metformina en la enfermedad renal crónica más grave, por debajo del límite de eGFR de 30 ml/minuto/1,73 m2. La captación de lactato por el hígado disminuye con el uso de metformina porque el lactato es un sustrato para la gluconeogénesis hepática, un proceso que inhibe la metformina. En individuos sanos, este ligero exceso se elimina por otros mecanismos (incluida la absorción por riñones sanos) y no se produce una elevación significativa de los niveles de lactato en sangre. Dada la insuficiencia renal grave, la depuración de metformina y lactato se reduce, aumentando los niveles de ambos y posiblemente provocando una acumulación de ácido láctico. Debido a que la metformina disminuye la captación hepática de lactato, cualquier condición que pueda precipitar la acidosis láctica es una contraindicación. Las causas comunes incluyen alcoholismo (debido al agotamiento de las reservas de NAD+), insuficiencia cardíaca y enfermedad respiratoria (debido a la oxigenación inadecuada de los tejidos); la causa más común es la enfermedad renal.
La producción de lactato asociada a la metformina también puede tener lugar en el intestino grueso, lo que podría contribuir potencialmente a la acidosis láctica en personas con factores de riesgo. Sin embargo, se desconoce la importancia clínica de esto, y el riesgo de acidosis láctica asociada con la metformina se atribuye más comúnmente a la disminución de la captación hepática en lugar del aumento de la producción intestinal.
Sobredosis
Los síntomas más comunes después de una sobredosis incluyen vómitos, diarrea, dolor abdominal, taquicardia, somnolencia y, en raras ocasiones, hipoglucemia o hiperglucemia. El tratamiento de la sobredosis de metformina generalmente es de apoyo, ya que no se conoce un antídoto específico. Se recomiendan tratamientos extracorpóreos en sobredosis graves. Debido al bajo peso molecular de la metformina y la falta de unión a proteínas plasmáticas, estas técnicas tienen la ventaja de eliminar la metformina del plasma sanguíneo, evitando una mayor sobreproducción de lactato.
La metformina se puede cuantificar en sangre, plasma o suero para monitorear la terapia, confirmar un diagnóstico de envenenamiento o ayudar en una investigación forense de muerte. Las concentraciones de metformina en sangre o plasma generalmente están en un rango de 1 a 4 mg/L en personas que reciben dosis terapéuticas, 40 a 120 mg/L en víctimas de sobredosis aguda y 80 a 200 mg/L en muertes. Comúnmente se emplean técnicas cromatográficas.
El riesgo de acidosis láctica asociada con la metformina también aumenta con una sobredosis masiva de metformina, aunque incluso las dosis bastante altas a menudo no son fatales.
Interacciones
El antagonista del receptor H2, cimetidina, provoca un aumento en la concentración plasmática de metformina al reducir la eliminación de metformina por los riñones; tanto la metformina como la cimetidina se eliminan del cuerpo por secreción tubular y ambas, en particular la forma catiónica (con carga positiva) de la cimetidina, pueden competir por el mismo mecanismo de transporte. Un pequeño estudio aleatorio doble ciego encontró que el antibiótico cefalexina también aumenta las concentraciones de metformina por un mecanismo similar; en teoría, otros medicamentos catiónicos pueden producir el mismo efecto.
La metformina también interactúa con los medicamentos anticolinérgicos debido a su efecto sobre la motilidad gástrica. Los fármacos anticolinérgicos reducen la motilidad gástrica, lo que prolonga el tiempo que pasan los fármacos en el tracto gastrointestinal. Este deterioro puede hacer que se absorba más metformina que sin la presencia de un fármaco anticolinérgico, lo que aumenta la concentración de metformina en el plasma y aumenta el riesgo de efectos adversos.
Farmacología
Mecanismo de acción
El mecanismo molecular de la metformina no se comprende por completo. Se han propuesto múltiples mecanismos de acción potenciales: inhibición de la cadena respiratoria mitocondrial (complejo I), activación de la proteína quinasa activada por AMP (AMPK), inhibición de la elevación del monofosfato de adenosina cíclico (AMPc) inducida por glucagón con activación reducida de la proteína quinasa A (PKA), inhibición mediada por el complejo IV de la variante GPD2 de la glicerol-3-fosfato deshidrogenasa mitocondrial (reduciendo así la gluconeogénesis hepática derivada del glicerol) y un efecto sobre la microbiota intestinal.
La metformina ejerce un efecto anorexígeno en la mayoría de las personas, disminuyendo la ingesta calórica. La metformina disminuye la gluconeogénesis (producción de glucosa) en el hígado. La metformina inhibe la secreción basal de la glándula pituitaria de la hormona del crecimiento, la hormona adrenocorticotrópica, la hormona estimulante del folículo y la expresión de la propiomelanocortina, que en parte explica su efecto sensibilizador a la insulina con múltiples acciones en los tejidos, incluido el hígado, el músculo esquelético, el endotelio y el tejido adiposo., y los ovarios. El paciente promedio con diabetes tipo 2 tiene una tasa de gluconeogénesis tres veces mayor que la normal; el tratamiento con metformina reduce esto en más de un tercio.
Se requería la activación de AMPK para el efecto inhibitorio de la metformina sobre la producción de glucosa en el hígado. AMPK es una enzima que desempeña un papel importante en la señalización de la insulina, el equilibrio energético de todo el cuerpo y el metabolismo de la glucosa y las grasas. La activación de AMPK es necesaria para un aumento en la expresión del compañero heterodímero pequeño, que a su vez inhibe la expresión de los genes gluconeogénicos hepáticos fosfoenolpiruvato carboxicinasa y glucosa 6-fosfatasa. La metformina se usa con frecuencia en la investigación junto con el ribonucleótido AICA como agonista de AMPK. El mecanismo por el cual las biguanidas aumentan la actividad de AMPK sigue siendo incierto: la metformina aumenta la concentración de monofosfato de adenosina (AMP) citosólico (a diferencia de un cambio en AMP total o AMP total/trifosfato de adenosina) que podría activar AMPK alostéricamente a niveles altos; una teoría más nueva implica la unión a PEN-2. La metformina inhibe la producción de AMP cíclico, bloqueando la acción del glucagón y, por lo tanto, reduciendo los niveles de glucosa en ayunas. La metformina también induce un cambio profundo en el perfil de la comunidad microbiana fecal en ratones diabéticos, y esto puede contribuir a su modo de acción, posiblemente a través de un efecto sobre la secreción del péptido 1 similar al glucagón.
Además de suprimir la producción de glucosa hepática, la metformina aumenta la sensibilidad a la insulina, mejora la captación de glucosa periférica (induciendo la fosforilación del factor potenciador de GLUT4), disminuye la supresión de la oxidación de ácidos grasos inducida por la insulina y disminuye la absorción de glucosa del tracto gastrointestinal. tracto. El aumento del uso periférico de glucosa puede deberse a una mejor unión de la insulina a los receptores de insulina. El aumento de la unión a la insulina después del tratamiento con metformina también se ha demostrado en pacientes con diabetes tipo 2.
Es probable que la AMPK también desempeñe un papel en el aumento de la sensibilidad periférica a la insulina, ya que la administración de metformina aumenta la actividad de la AMPK en el músculo esquelético. Se sabe que AMPK causa el despliegue de GLUT4 en la membrana plasmática, lo que da como resultado una captación de glucosa independiente de la insulina. Algunas acciones metabólicas de la metformina parecen ocurrir por mecanismos independientes de la AMPK; sin embargo, es probable que la AMPK tenga un efecto general modesto y no es probable que su actividad reduzca directamente la gluconeogénesis en el hígado.
La metformina tiene efectos antiandrogénicos indirectos en mujeres con resistencia a la insulina, como aquellas con SOP, debido a sus efectos beneficiosos sobre la sensibilidad a la insulina. Puede reducir los niveles de testosterona en estas mujeres hasta en un 50%. Sin embargo, una revisión de Cochrane encontró que la metformina fue solo ligeramente efectiva para disminuir los niveles de andrógenos en mujeres con SOP.
La metformina también tiene efectos significativos en el microbioma intestinal, como su efecto sobre el aumento de la producción de agmatina por parte de las bacterias intestinales, pero la importancia relativa de este mecanismo en comparación con otros mecanismos es incierta.
Farmacocinética
La metformina tiene una biodisponibilidad oral del 50 al 60 % en ayunas y se absorbe lentamente. Las concentraciones plasmáticas máximas (Cmax) se alcanzan entre 1 y 3 horas después de tomar metformina de liberación inmediata y entre 4 y 8 horas con formulaciones de liberación prolongada. La unión a proteínas plasmáticas de la metformina es insignificante, como se refleja en su volumen aparente de distribución muy alto (300-1000 l después de una dosis única). El estado estacionario generalmente se alcanza en 1 a 2 días.
La metformina tiene valores constantes de disociación ácida (pKa) de 2,8 y 11,5, por lo que existe en gran medida como especie catiónica hidrófila a valores de pH fisiológicos. Los valores de metformina pKa la convierten en una base más fuerte que la mayoría de los otros medicamentos básicos con menos del 0,01 % de no ionizado en la sangre. Además, la solubilidad en lípidos de las especies no ionizadas es leve, como lo muestra su bajo valor logP (log(10) del coeficiente de distribución de la forma no ionizada entre octanol y agua) de -1,43. Estos parámetros químicos indican baja lipofilicidad y, en consecuencia, es improbable una rápida difusión pasiva de metformina a través de las membranas celulares. Como resultado de su baja liposolubilidad, requiere el transportador SLC22A1 para poder ingresar a las células. El logP de la metformina es menor que el de la fenformina (-0,84) porque dos sustituyentes metilo en la metformina imparten menor lipofilicidad que la cadena lateral más grande de feniletilo en la fenformina. Actualmente se están investigando más derivados lipófilos de la metformina con el objetivo de producir profármacos con una absorción oral superior a la de la metformina.
La metformina no se metaboliza. Se elimina del cuerpo por secreción tubular y se excreta sin cambios en la orina; es indetectable en el plasma sanguíneo dentro de las 24 horas posteriores a una dosis oral única. La vida media de eliminación promedio en plasma es de 6,2 horas. La metformina se distribuye (y parece acumularse) en los glóbulos rojos, con una vida media de eliminación mucho más larga: 17,6 horas (se informó que varió de 18,5 a 31,5 horas en un estudio de dosis única de no diabéticos).
Alguna evidencia indica que las concentraciones hepáticas de metformina en humanos pueden ser de dos a tres veces más altas que las concentraciones plasmáticas, debido a la absorción de la vena porta y la captación de primer paso por el hígado en la administración oral.
Química
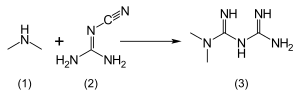
El clorhidrato de metformina (clorhidrato de 1,1-dimetilbiguanida) es completamente soluble en agua, ligeramente soluble en etanol, pero casi insoluble en acetona, éter o cloroformo. El pKa de la metformina es 12,4. La síntesis habitual de metformina, descrita originalmente en 1922, implica la reacción en un solo recipiente de clorhidrato de dimetilamina y 2-cianoguanidina sobre calor.
Según el procedimiento descrito en la patente de Aron de 1975 y la Enciclopedia de fabricación farmacéutica, se disuelven cantidades equimolares de dimetilamina y 2-cianoguanidina en tolueno con enfriamiento para formar una solución concentrada y una se añade lentamente una cantidad de cloruro de hidrógeno. La mezcla comienza a hervir por sí sola y, después de enfriar, precipita el clorhidrato de metformina con un rendimiento del 96%.
Derivados
Un nuevo derivado HL156A, también conocido como IM156, es un nuevo fármaco potencial para uso médico.
Historia
La clase de biguanida de medicamentos antidiabéticos, que también incluye los agentes retirados fenformina y buformina, tiene su origen en la lila francesa o ruda de cabra (Galega officinalis), una planta utilizada en la medicina popular. durante varios siglos. G. officinalis en sí no contiene ninguno de estos medicamentos, pero sí isoamileno guanidina; La fenformina, la buformina y la metformina son compuestos sintetizados químicamente compuestos por dos moléculas de guanidina y son más lipófilos que el compuesto original derivado de plantas.
La metformina fue descrita por primera vez en la literatura científica en 1922 por Emil Werner y James Bell, como un producto en la síntesis de N,N-dimetilguanidina. En 1929, Slotta y Tschesche descubrieron su acción reductora de azúcar en conejos y lo encontraron el análogo de biguanida más potente que estudiaron. Este resultado fue ignorado, ya que otros análogos de guanidina, como las sintalinas, se hicieron cargo y pronto fueron eclipsados por la insulina.
El interés por la metformina se reanudó a fines de la década de 1940. En 1950, se descubrió que la metformina, a diferencia de otros compuestos similares, no disminuía la presión arterial ni la frecuencia cardíaca en los animales. Ese año, el médico filipino Eusebio Y. García usó metformina (la llamó Fluamine) para tratar la influenza; señaló que el medicamento "bajó el nivel de azúcar en la sangre al límite fisiológico mínimo" y no era tóxico. García creía que la metformina tenía acciones bacteriostáticas, antivirales, antipalúdicas, antipiréticas y analgésicas. En una serie de artículos de 1954, el farmacólogo polaco Janusz Supniewski no pudo confirmar la mayoría de estos efectos, incluida la disminución del azúcar en la sangre. En cambio, observó efectos antivirales en humanos.
El diabetólogo francés Jean Sterne estudió las propiedades antihiperglucemiantes de la galegina, un alcaloide aislado de G. officinalis, cuya estructura está relacionada con la metformina, y se había utilizado brevemente como antidiabético antes de que se desarrollaran las sintalinas. Más tarde, trabajando en Laboratoires Aron en París, el informe de García lo incitó a volver a investigar la actividad reductora del azúcar en la sangre de la metformina y varios análogos de biguanida. Sterne fue el primero en probar la metformina en humanos para el tratamiento de la diabetes; acuñó el nombre "Glucophage" (devorador de glucosa) para la medicación y publicó sus resultados en 1957.
La metformina estuvo disponible en el Formulario Nacional Británico en 1958. Fue vendida en el Reino Unido por una pequeña subsidiaria de Aron llamada Rona.
El amplio interés en la metformina no se reavivó hasta que se retiraron las demás biguanidas en la década de 1970. La metformina se aprobó en Canadá en 1972, pero no recibió la aprobación de la Administración de Drogas y Alimentos de los EE. UU. (FDA) para la diabetes tipo 2 hasta 1994. Producida bajo licencia por Bristol-Myers Squibb, Glucophage fue la primera formulación de marca de metformina que se comercializó en los EE. UU., a partir del 3 de marzo de 1995. Las formulaciones genéricas están disponibles en varios países, y se cree que la metformina se ha convertido en el medicamento antidiabético más recetado en el mundo.
Sociedad y cultura
Ambiental
La metformina y su principal producto de transformación, la guanilurea, están presentes en los efluentes de las plantas de tratamiento de aguas residuales y se detectan periódicamente en las aguas superficiales. Se han medido concentraciones de guanilurea superiores a 200 μg/L en el río alemán Erpe, que se encuentran entre las más altas reportadas para productos de transformación farmacéutica en ambientes acuáticos.
Formulaciones
El nombre "metformina" es la BAN, USAN e INN de este medicamento y se vende con varios nombres comerciales. Las marcas comunes incluyen Glucophage, Riomet, Fortamet y Glumetza en los EE. UU. En otras zonas del mundo también están Obimet, Gluformin, Dianben, Diabex, Diaformin, Metsol, Siofor, Metfogamma y Glifor. Hay varias formulaciones de metformina disponibles en el mercado, y todas excepto la forma líquida tienen equivalentes genéricos. Metformin IR (liberación inmediata) está disponible en tabletas de 500, 850 y 1000 mg, mientras que Metformin XR (liberación prolongada) está disponible en concentraciones de 500, 750 y 1000 mg (también se vende como Fortamet, Glumetza, y Glucophage XR en los EE. UU.). También está disponible la metformina líquida (vendida como Riomet en los EE. UU.), donde 5 ml de solución contienen la misma cantidad de medicamento que una tableta de 500 mg.
Combinación con otros medicamentos
Cuando se usa para la diabetes tipo 2, la metformina a menudo se receta en combinación con otros medicamentos.
Varios están disponibles como combinaciones de dosis fijas, con el potencial de reducir la carga de píldoras, disminuir el costo y simplificar la administración.
Tiazolidinedionas (glitazonas)
Rosiglitazona
Una combinación de metformina y rosiglitazona se lanzó en 2002 y GlaxoSmithKline la vendió como Avandamet o como medicamento genérico. Las formulaciones son 500/1, 500/2, 500/4, 1000/2 y 1000 mg/4 mg de metformina/rosiglitazona.
Para 2009, se había convertido en la combinación de metformina más popular.
En 2005, el stock de Avandamet fue retirado del mercado, luego de que las inspecciones demostraron que la fábrica donde se producía estaba violando las buenas prácticas de fabricación. El par de medicamentos se siguió recetando por separado y Avandamet volvió a estar disponible a fines de ese año. Una formulación genérica de metformina/rosiglitazona de Teva recibió la aprobación provisional de la FDA y llegó al mercado a principios de 2012.
Sin embargo, luego de un metanálisis en 2007 que vinculó el uso del medicamento con un mayor riesgo de ataque cardíaco, surgieron preocupaciones sobre la seguridad de los medicamentos que contienen rosiglitazona. En septiembre de 2010, la Agencia Europea de Medicamentos recomendó que se suspendiera el medicamento del mercado europeo porque los beneficios de la rosiglitazona ya no superaban los riesgos.
Se retiró del mercado en el Reino Unido e India en 2010, y en Nueva Zelanda y Sudáfrica en 2011. Desde noviembre de 2011 hasta noviembre de 2013, la FDA no permitió la venta sin receta de rosiglitazona o metformina/rosiglitazona; además, los fabricantes debían notificar a los pacientes sobre los riesgos asociados con su uso, y el medicamento debía comprarse por correo a través de farmacias específicas."Estrategia actualizada de evaluación y mitigación de riesgos (REMS)". Estados Unidos Administración de Alimentos y Medicamentos (FDA). 1 de julio de 2021. Consultado el 6 de marzo de 2023.</ref>
En noviembre de 2013, la FDA levantó sus restricciones anteriores sobre la rosiglitazona después de revisar los resultados del ensayo clínico RECORD de 2009 (un ensayo de control aleatorio abierto de seis años), que no demostró un riesgo elevado de ataque cardíaco o muerte. asociado con el medicamento.
Pioglitazona
La combinación de metformina y pioglitazona (Actoplus Met, Piomet, Politor, Glubrava) está disponible en EE. UU. y la Unión Europea.
Inhibidores de la DPP-4
Los inhibidores de la dipeptidil peptidasa-4 inhiben la dipeptidil peptidasa-4 y, por lo tanto, reducen los niveles de glucagón y glucosa en sangre.
Los inhibidores de DPP-4 combinados con metformina incluyen una combinación de sitagliptina/metformina (Janumet), una combinación de saxagliptina/metformina (Kombiglyze XR, Komboglyze) y una combinación de alogliptina/metformina (Kazano, Vipdomet).
La linagliptina combinada con clorhidrato de metformina se vende bajo la marca Jentadueto. A partir de agosto de 2021, la linagliptina/metformina está disponible como medicamento genérico en los EE. UU.
Inhibidores de SGLT-2
Existen combinaciones de metformina con dapagliflozina, empagliflozina y canagliflozina.
Sulfonilureas
Las sulfonilureas actúan aumentando la liberación de insulina de las células beta del páncreas.
Una revisión sistemática de 2019 sugirió que hay pruebas limitadas de si el uso combinado de metformina con sulfonilurea en comparación con la combinación de metformina más otra intervención para reducir la glucosa proporciona beneficios o daños en la mortalidad, los eventos adversos graves y las complicaciones macrovasculares y microvasculares. La terapia combinada de metformina y sulfonilureas pareció conducir a un mayor riesgo de hipoglucemia.
La metformina está disponible combinada con las sulfonilureas glipizida (Metaglip) y glibenclamida (EE. UU.: gliburida) (Glucovance). Están disponibles formulaciones genéricas de metformina/glipizida y metformina/glibenclamida (la última es más popular).
Meglitinida
Las meglitinidas son similares a las sulfonilureas, ya que se unen a las células beta del páncreas, pero se diferencian por el sitio de unión al receptor previsto y los fármacos' afinidades por el receptor. Como resultado, tienen una duración de acción más corta en comparación con las sulfonilureas y requieren niveles más altos de glucosa en sangre para comenzar a secretar insulina. Ambas meglitinidas, conocidas como nateglinida y repanglinida, se venden en formulaciones combinadas con metformina. Una combinación de repaglinida/metformina se vende como Prandimet o su equivalente genérico.
Combinación triple
La combinación de metformina con dapagliflozen y saxagliptina está disponible en los Estados Unidos como Qternmet XR.
La combinación de metformina con pioglitazona y glibenclamida está disponible en India como Accuglim-MP, Adglim MP y Alnamet-GP, junto con Filipinas como Tri-Senza.
La combinación de metformina con pioglitazona y ácido lipoico está disponible en Turquía como Pional.
Impurezas
En diciembre de 2019, la FDA de EE. UU. anunció que se enteró de que algunos medicamentos de metformina fabricados fuera de los Estados Unidos podrían contener una impureza de nitrosamina llamada N-nitrosodimetilamina (NDMA), clasificada como probable carcinógeno humano, en niveles bajos. Health Canada anunció que estaba evaluando los niveles de NDMA en la metformina.
En febrero de 2020, la FDA encontró niveles de NDMA en algunas muestras de metformina analizadas que no superaban la ingesta diaria aceptable.
En febrero de 2020, Health Canada anunció un retiro del mercado de metformina de liberación inmediata Apotex, seguido en marzo por retiros de metformina Ranbaxy y en marzo por metformina Jamp.
En mayo de 2020, la FDA solicitó a cinco empresas que retiraran voluntariamente sus productos de metformina de liberación sostenida. Las cinco compañías no fueron nombradas, pero se reveló que eran Amneal Pharmaceuticals, Actavis Pharma, Apotex Corp, Lupin Pharma y Marksans Pharma Limited en una carta enviada a Valisure, la farmacia que primero alertó a la FDA sobre este contaminante en la metformina a través de una petición ciudadana.
En junio de 2020, la FDA publicó los resultados de su laboratorio que mostraban las cantidades de NDMA en los productos de metformina que probó. Encontró NDMA en ciertos lotes de metformina ER y recomienda a las empresas que retiren los lotes con niveles de NDMA por encima del límite de ingesta aceptable de 96 nanogramos por día. La FDA también está colaborando con reguladores internacionales para compartir los resultados de las pruebas de metformina.
En julio de 2020, Lupin Pharmaceuticals retiró todos los lotes (lotes) de metformina después de descubrir niveles inaceptablemente altos de NDMA en las muestras analizadas.
En agosto de 2020, Bayshore Pharmaceuticals retiró dos lotes de tabletas.
Investigación
La metformina se ha estudiado por sus efectos en muchas otras afecciones, entre ellas:
- Enfermedad hepática grasa no alcohólica
- pubertad prematura
- Cáncer
- Enfermedad cardiovascular en personas con diabetes
- Envejecimiento
Si bien la metformina puede reducir el peso corporal en personas con síndrome X frágil, no se sabe si mejora los síntomas neurológicos o psiquiátricos. La metformina se ha estudiado in vivo (C. elegans y grillos) por sus efectos sobre el envejecimiento. Una revisión de 2017 encontró que las personas con diabetes que tomaban metformina tenían una mortalidad por todas las causas más baja. También habían reducido el cáncer y las enfermedades cardiovasculares en comparación con los de otras terapias.
También hay algunas investigaciones que sugieren que, aunque la metformina previene la diabetes, no reduce el riesgo de cáncer ni de enfermedades cardiovasculares y, por lo tanto, no prolonga la esperanza de vida en personas no diabéticas. Además, algunos estudios sugieren que el uso crónico a largo plazo de metformina por parte de individuos sanos puede desarrollar deficiencia de vitamina B12.
Contenido relacionado
Ley de Fick
Ácido pícrico
Trimix (respiración de gas)
Georg Ernst Stahl
Cuerpos cetónicos