Metástasis
La metástasis es la propagación de un agente patógeno desde un sitio inicial o primario a un sitio diferente o secundario dentro del cuerpo del huésped; el término se usa típicamente cuando se hace referencia a la metástasis de un tumor canceroso. Los nuevos sitios patológicos, entonces, son metástasis (mets). Generalmente se distingue de la invasión del cáncer, que es la extensión y penetración directa de las células cancerosas en los tejidos vecinos.
El cáncer se produce después de que las células se alteran genéticamente para que proliferen de forma rápida e indefinida. Esta proliferación descontrolada por mitosis produce un tumor heterogéneo primario. Las células que constituyen el tumor finalmente sufren metaplasia, seguida de displasia y luego anaplasia, lo que da como resultado un fenotipo maligno. Esta malignidad permite la invasión de la circulación, seguida de la invasión de un segundo sitio para la tumorigénesis.
Algunas células cancerosas conocidas como células tumorales circulantes adquieren la capacidad de penetrar las paredes de los vasos linfáticos o sanguíneos, luego de lo cual pueden circular a través del torrente sanguíneo hacia otros sitios y tejidos del cuerpo. Este proceso se conoce (respectivamente) como diseminación linfática o hematógena. Después de que las células tumorales descansan en otro sitio, vuelven a penetrar en el vaso o las paredes y continúan multiplicándose, formando finalmente otro tumor clínicamente detectable. Este nuevo tumor se conoce como tumor metastásico (o secundario). La metástasis es una de las características del cáncer, que lo distingue de los tumores benignos.La mayoría de los cánceres pueden hacer metástasis, aunque en diversos grados. El carcinoma de células basales, por ejemplo, rara vez hace metástasis.
Cuando las células tumorales hacen metástasis, el nuevo tumor se denomina tumor secundario o metastásico, y sus células son similares a las del tumor original o primario. Esto significa que si el cáncer de mama hace metástasis a los pulmones, el tumor secundario está formado por células mamarias anormales, no por células pulmonares anormales. El tumor en el pulmón entonces se llama cáncer de mama metastásico, no cáncer de pulmón. La metástasis es un elemento clave en los sistemas de estadificación del cáncer como el sistema de estadificación TNM, donde representa la "M". En la agrupación general de estadios, la metástasis coloca al cáncer en el estadio IV. Las posibilidades de un tratamiento curativo se reducen considerablemente o, a menudo, se eliminan por completo cuando un cáncer ha hecho metástasis.
Signos y síntomas
Inicialmente, los ganglios linfáticos cercanos se golpean temprano. Los pulmones, el hígado, el cerebro y los huesos son los lugares de metástasis más comunes de los tumores sólidos.
- En las metástasis de los ganglios linfáticos, un síntoma común es la linfadenopatía
- Metástasis pulmonar: tos, hemoptisis y disnea (dificultad para respirar)
- Metástasis hepáticas: hepatomegalia (hígado agrandado), náuseas e ictericia
- Metástasis ósea: dolor óseo, fractura de huesos afectados
- Metástasis cerebral: síntomas neurológicos como dolores de cabeza, convulsiones y vértigo
Aunque el cáncer avanzado puede causar dolor, a menudo no es el primer síntoma.
Algunos pacientes, sin embargo, no muestran ningún síntoma. Cuando el órgano tiene una enfermedad metastásica, comienza a encogerse hasta que sus ganglios linfáticos revientan o sufren lisis.
Fisiopatología
Los tumores metastásicos son muy comunes en las últimas etapas del cáncer. La diseminación de la metástasis puede ocurrir por vía sanguínea o linfática o por ambas vías. Los sitios más comunes de metástasis son los pulmones, el hígado, el cerebro y los huesos.
Actualmente, se han propuesto tres teorías principales para explicar la vía metastásica del cáncer: la hipótesis de la transición epitelial-mesenquimatosa (EMT) y la transición mesenquimatosa-epitelial (MET) (1), la hipótesis de las células madre del cáncer (2) y la teoría de los macrófagos. hipótesis híbrida de fusión de células cancerosas (3). También se sugirieron algunas hipótesis nuevas, es decir, bajo el efecto de factores estresantes bioquímicos y/o físicos particulares, las células cancerosas pueden sufrir una expulsión nuclear con la subsiguiente absorción y fusión de macrófagos, con la formación de células de fusión cancerosas (CFC).
Factores involucrados
La metástasis implica una serie compleja de pasos en los que las células cancerosas abandonan el sitio del tumor original y migran a otras partes del cuerpo a través del torrente sanguíneo, el sistema linfático o por extensión directa. Para hacerlo, las células malignas se separan del tumor primario y se unen a las proteínas que componen la matriz extracelular (MEC) que lo rodea, y las degradan, lo que separa el tumor de los tejidos adyacentes. Al degradar estas proteínas, las células cancerosas pueden romper la MEC y escapar. La ubicación de las metástasis no siempre es aleatoria, con diferentes tipos de cáncer que tienden a diseminarse a órganos y tejidos particulares a un ritmo más alto de lo esperado solo por casualidad estadística.El cáncer de mama, por ejemplo, tiende a hacer metástasis en los huesos y los pulmones. Esta especificidad parece estar mediada por moléculas señalizadoras solubles como las quimiocinas y el factor de crecimiento transformante beta. El cuerpo resiste la metástasis por una variedad de mecanismos a través de las acciones de una clase de proteínas conocidas como supresores de metástasis, de las cuales se conocen alrededor de una docena.
Las células humanas exhiben diferentes tipos de movimiento: motilidad colectiva, movimiento de tipo mesenquimatoso y movimiento ameboide. Las células cancerosas a menudo cambian de manera oportunista entre diferentes tipos de movimiento. Algunos investigadores del cáncer esperan encontrar tratamientos que puedan detener o al menos retrasar la propagación del cáncer al bloquear de alguna manera algún paso necesario en uno o más tipos de movimiento.
Todos los pasos de la cascada metastásica implican una serie de procesos físicos. La migración celular requiere la generación de fuerzas, y cuando las células cancerosas transmigran a través de la vasculatura, esto requiere que se formen espacios físicos en los vasos sanguíneos. Además de las fuerzas, la regulación de varios tipos de adherencias célula-célula y célula-matriz es crucial durante la metástasis.
Los pasos metastásicos están críticamente regulados por varios tipos de células, incluidas las células de los vasos sanguíneos (células endoteliales), las células inmunitarias o las células del estroma. El crecimiento de una nueva red de vasos sanguíneos, llamada angiogénesis tumoral, es un sello distintivo crucial del cáncer. Por lo tanto, se ha sugerido que los inhibidores de la angiogénesis evitarían el crecimiento de metástasis. Se ha demostrado que las células progenitoras endoteliales tienen una fuerte influencia en la metástasis y la angiogénesis.Las células progenitoras endoteliales son importantes en el crecimiento tumoral, la angiogénesis y la metástasis, y se pueden marcar con el inhibidor de unión al ADN 1 (ID1). Este nuevo hallazgo significó que los investigadores obtuvieron la capacidad de rastrear las células progenitoras endoteliales desde la médula ósea hasta la sangre y el estroma del tumor e incluso incorporarlas en la vasculatura del tumor. Las células progenitoras endoteliales incorporadas en la vasculatura tumoral sugieren que este tipo de células en el desarrollo de los vasos sanguíneos es importante en un entorno tumoral y metástasis. Además, la ablación de las células progenitoras endoteliales en la médula ósea puede conducir a una disminución significativa del crecimiento del tumor y del desarrollo de la vasculatura. Por lo tanto, las células progenitoras endoteliales son importantes en la biología tumoral y presentan nuevas dianas terapéuticas.El sistema inmunitario generalmente está desregulado en el cáncer y afecta muchas etapas de la progresión del tumor, incluida la metástasis.
La regulación epigenética también juega un papel importante en el crecimiento metastásico de células tumorales diseminadas. Las metástasis muestran alteraciones en las modificaciones de las histonas, como la metilación de H3K4 y la metilación de H3K9, en comparación con los tumores primarios correspondientes. Estas modificaciones epigenéticas en las metástasis pueden permitir la proliferación y supervivencia de células tumorales diseminadas en órganos distantes.
Un estudio reciente muestra que PKC-iota promueve la invasión de células de melanoma al activar la vimentina durante la EMT. La inhibición o eliminación de PKC-iota dio como resultado un aumento en los niveles de E-cadherina y RhoA mientras disminuía la vimentina total, la vimentina fosforilada (S39) y Par6 en las células de melanoma metastásico. Estos resultados sugirieron que PKC-ι está involucrada en las vías de señalización que regulan al alza la EMT en el melanoma, por lo que estimula directamente la metástasis.
Recientemente, una serie de experimentos de alto perfil sugiere que la cooptación de la diafonía intercelular mediada por vesículas de exosomas es un factor crítico involucrado en todos los pasos de la cascada de invasión-metástasis.
Rutas
La metástasis ocurre por las siguientes cuatro rutas:
Transcelómico
La diseminación de una neoplasia maligna hacia las cavidades corporales puede ocurrir a través de la penetración en la superficie de los espacios peritoneal, pleural, pericárdico o subaracnoideo. Por ejemplo, los tumores de ovario pueden diseminarse transperitonealmente a la superficie del hígado.
Propagación linfática
La diseminación linfática permite el transporte de células tumorales a los ganglios linfáticos regionales cerca del tumor primario y, en última instancia, a otras partes del cuerpo. Esto se denomina afectación ganglionar, ganglios positivos o enfermedad regional. "Nodos positivos" es un término que utilizarían los especialistas médicos para describir los ganglios linfáticos regionales que dieron positivo para malignidad. Es una práctica médica común analizar mediante biopsia al menos un ganglio linfático cerca del sitio del tumor cuando se realiza una cirugía para examinar o extirpar un tumor. Este ganglio linfático se denomina ganglio linfático centinela. La diseminación linfática es la ruta más común de metástasis inicial para los carcinomas.Por el contrario, es poco común que un sarcoma haga metástasis a través de esta ruta. La diseminación localizada a los ganglios linfáticos regionales cerca del tumor primario normalmente no se considera una metástasis, aunque esto es un signo de un peor resultado. El sistema linfático finalmente drena desde el conducto torácico y el conducto linfático derecho hacia el sistema venoso sistémico en el ángulo venoso y hacia las venas braquiocefálicas y, por lo tanto, estas células metastásicas también pueden eventualmente diseminarse por vía hematógena.
Propagación hematógena
Esta es la ruta típica de metástasis para los sarcomas, pero también es la ruta preferida para ciertos tipos de carcinoma, como el carcinoma de células renales que se origina en el riñón y los carcinomas foliculares de la tiroides. Debido a sus paredes más delgadas, las venas son invadidas con más frecuencia que las arterias y las metástasis tienden a seguir el patrón del flujo venoso. Es decir, la diseminación hematógena a menudo sigue patrones distintos según la ubicación del tumor primario. Por ejemplo, el cáncer colorrectal se disemina principalmente a través de la vena porta hacia el hígado.
Propagación canalicular
Algunos tumores, especialmente los carcinomas, pueden hacer metástasis a lo largo de los espacios canaliculares anatómicos. Estos espacios incluyen, por ejemplo, los conductos biliares, el sistema urinario, las vías respiratorias y el espacio subaracnoideo. El proceso es similar al de la diseminación transcelómica. Sin embargo, a menudo no está claro si los tumores de un sistema canalicular diagnosticados simultáneamente son un proceso metastásico o, de hecho, tumores independientes causados por el mismo agente (cancerización de campo).
Objetivos específicos de órganos
Hay una propensión a que ciertos tumores se propaguen en órganos particulares. Esto fue discutido por primera vez como la teoría de "semilla y suelo" por Stephen Paget en 1889. La propensión de una célula metastásica a propagarse a un órgano en particular se denomina "organotropismo". Por ejemplo, el cáncer de próstata suele hacer metástasis en los huesos. De manera similar, el cáncer de colon tiene tendencia a hacer metástasis en el hígado. El cáncer de estómago a menudo hace metástasis al ovario en las mujeres, cuando se le llama tumor de Krukenberg.
Según la teoría de la "semilla y el suelo", es difícil que las células cancerosas sobrevivan fuera de su región de origen, por lo que para metastatizar deben encontrar un lugar con características similares. Por ejemplo, las células tumorales del seno, que recolectan iones de calcio de la leche materna, hacen metástasis al tejido óseo, donde pueden recolectar iones de calcio de los huesos. El melanoma maligno se disemina al cerebro, presumiblemente porque el tejido neural y los melanocitos surgen de la misma línea celular en el embrión.
En 1928, James Ewing desafió la teoría de la "semilla y el suelo" y propuso que la metástasis ocurre puramente por vías anatómicas y mecánicas. Esta hipótesis se ha utilizado recientemente para sugerir varias hipótesis sobre el ciclo de vida de las células tumorales circulantes (CTC) y para postular que los patrones de propagación podrían entenderse mejor a través de una perspectiva de "filtro y flujo". Sin embargo, las evidencias contemporáneas indican que el tumor primario puede dictar metástasis organotrópicas al inducir la formación de nichos premetastásicos en sitios distantes, donde las células metastásicas entrantes pueden injertarse y colonizarse.Específicamente, se ha demostrado que las vesículas de exosomas secretadas por los tumores se alojan en sitios premetastásicos, donde activan procesos prometastásicos como la angiogénesis y modifican la contextura inmunitaria, a fin de fomentar un microambiente favorable para el crecimiento tumoral secundario.
Metástasis y cáncer primario
Se teoriza que la metástasis siempre coincide con un cáncer primario y, como tal, es un tumor que se originó a partir de una célula o células cancerosas en otra parte del cuerpo. Sin embargo, más del 10% de los pacientes que acuden a las unidades de oncología tendrán metástasis sin que se encuentre un tumor primario. En estos casos, los médicos se refieren al tumor primario como "desconocido" u "oculto", y se dice que el paciente tiene cáncer de origen primario desconocido (CUP) o tumores primarios desconocidos (UPT). Se estima que el 3% de todos los cánceres son de origen primario desconocido. Los estudios han demostrado que, si un simple interrogatorio no revela el origen del cáncer (toser sangre, "probablemente pulmón", orinar sangre, "probablemente vejiga"), las imágenes complejas tampoco lo harán. En algunos de estos casos, un tumor primario puede aparecer más tarde.
El uso de la inmunohistoquímica ha permitido a los patólogos dar una identidad a muchas de estas metástasis. Sin embargo, las imágenes del área indicada solo ocasionalmente revelan un tumor primario. En casos raros (p. ej., de melanoma), no se encuentra un tumor primario, ni siquiera en la autopsia. Por lo tanto, se piensa que algunos tumores primarios pueden retroceder por completo, pero dejar atrás sus metástasis. En otros casos, el tumor podría ser demasiado pequeño y/o estar en una ubicación inusual para ser diagnosticado.
Diagnóstico
Las células de un tumor metastásico se parecen a las del tumor primario. Una vez que el tejido canceroso se examina bajo un microscopio para determinar el tipo de célula, el médico generalmente puede determinar si ese tipo de célula se encuentra normalmente en la parte del cuerpo de la que se tomó la muestra de tejido.
Por ejemplo, las células de cáncer de mama se ven iguales ya sea que se encuentren en el seno o se hayan propagado a otra parte del cuerpo. Por lo tanto, si una muestra de tejido extraída de un tumor en el pulmón contiene células que parecen células mamarias, el médico determina que el tumor pulmonar es un tumor secundario. Aún así, la determinación del tumor primario a menudo puede ser muy difícil y el patólogo puede tener que usar varias técnicas adyuvantes, como inmunohistoquímica, FISH (hibridación fluorescente in situ) y otras. A pesar del uso de técnicas, en algunos casos el tumor primario permanece sin identificar.
Los cánceres metastásicos se pueden encontrar al mismo tiempo que el tumor primario, o meses o años después. Cuando se encuentra un segundo tumor en un paciente que ha sido tratado por cáncer en el pasado, es más frecuente que se trate de una metástasis que de otro tumor primario.
Anteriormente se pensaba que la mayoría de las células cancerosas tienen un potencial metastásico bajo y que hay células raras que desarrollan la capacidad de hacer metástasis a través del desarrollo de mutaciones somáticas. De acuerdo con esta teoría, el diagnóstico de cánceres metastásicos solo es posible después del evento de metástasis. Los medios tradicionales de diagnóstico del cáncer (por ejemplo, una biopsia) solo investigarían una subpoblación de células cancerosas y muy probablemente no tomarían muestras de la subpoblación con potencial metastásico.
La teoría de la mutación somática del desarrollo de metástasis no se ha comprobado en los cánceres humanos. Más bien, parece que el estado genético del tumor primario refleja la capacidad de ese cáncer para hacer metástasis. La investigación que comparó la expresión génica entre adenocarcinomas primarios y metastásicos identificó un subconjunto de genes cuya expresión podría distinguir los tumores primarios de los tumores metastásicos, denominado "firma metastásica". Los genes regulados al alza en la firma incluyen: SNRPF, HNRPAB, DHPS y securin. La regulación negativa de actina, miosina y MHC clase II también se asoció con la firma. Además, la expresión asociada a la metástasis de estos genes también se observó en algunos tumores primarios, lo que indica que las células con potencial para metastatizar podrían identificarse simultáneamente con el diagnóstico del tumor primario. Un trabajo reciente identificó una forma de inestabilidad genética en el cáncer llamada inestabilidad cromosómica (CIN) como impulsor de la metástasis. En las células cancerosas agresivas, los fragmentos de ADN sueltos de los cromosomas inestables se derraman en el citosol, lo que conduce a la activación crónica de las vías inmunitarias innatas, que son secuestradas por las células cancerosas para propagarse a órganos distantes.
La expresión de esta firma metastásica se ha correlacionado con un mal pronóstico y se ha demostrado que es consistente en varios tipos de cáncer. Se demostró que el pronóstico era peor para las personas cuyos tumores primarios expresaban la firma metastásica. Además, se demostró que la expresión de estos genes asociados con metástasis se aplica a otros tipos de cáncer además del adenocarcinoma. Las metástasis de cáncer de mama, meduloblastoma y cáncer de próstata tenían patrones de expresión similares de estos genes asociados a metástasis.
La identificación de esta firma asociada a la metástasis ofrece la promesa de identificar células con potencial metastásico dentro del tumor primario y la esperanza de mejorar el pronóstico de estos cánceres asociados con la metástasis. Además, identificar los genes cuya expresión cambia en la metástasis ofrece objetivos potenciales para inhibir la metástasis.
 Corte de la superficie de un húmero aserrado a lo largo, que muestra una gran metástasis cancerosa (el tumor blanquecino entre la cabeza y el eje del hueso)
Corte de la superficie de un húmero aserrado a lo largo, que muestra una gran metástasis cancerosa (el tumor blanquecino entre la cabeza y el eje del hueso) Micrografía de cáncer de tiroides (carcinoma papilar de tiroides) en un ganglio linfático del cuello. tinción H&E
Micrografía de cáncer de tiroides (carcinoma papilar de tiroides) en un ganglio linfático del cuello. tinción H&E Imagen de TC de metástasis hepáticas múltiples
Imagen de TC de metástasis hepáticas múltiples Imagen de TC de una metástasis pulmonar
Imagen de TC de una metástasis pulmonar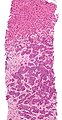 Metástasis demostrada por biopsia de hígado (tumor (adenocarcinoma): dos tercios inferiores de la imagen). Tinción H&E.
Metástasis demostrada por biopsia de hígado (tumor (adenocarcinoma): dos tercios inferiores de la imagen). Tinción H&E.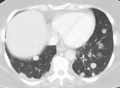 Cáncer metastásico en los pulmones
Cáncer metastásico en los pulmones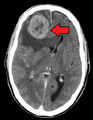 Metástasis de los pulmones al cerebro.
Metástasis de los pulmones al cerebro. Metástasis de los pulmones al páncreas
Metástasis de los pulmones al páncreas
Administración
El tratamiento y la supervivencia están determinados, en gran medida, por si un cáncer permanece o no localizado o se propaga a otros lugares del cuerpo. Si el cáncer hace metástasis a otros tejidos u órganos, generalmente aumenta drásticamente la probabilidad de muerte del paciente. Algunos tipos de cáncer, como algunas formas de leucemia, un cáncer de la sangre o tumores malignos en el cerebro, pueden causar la muerte sin propagarse en absoluto.
Una vez que el cáncer ha hecho metástasis, aún se puede tratar con radiocirugía, quimioterapia, radioterapia, terapia biológica, terapia hormonal, cirugía o una combinación de estas intervenciones ("terapia multimodal"). La elección del tratamiento depende de muchos factores, incluido el tipo de cáncer primario, el tamaño y la ubicación de las metástasis, la edad y el estado general de salud del paciente, y los tipos de tratamientos utilizados anteriormente. En pacientes diagnosticados con CUP, a menudo todavía es posible tratar la enfermedad incluso cuando no se puede localizar el tumor primario.
Los tratamientos actuales rara vez pueden curar el cáncer metastásico, aunque algunos tumores, como el cáncer testicular y el cáncer de tiroides, suelen ser curables.
Los cuidados paliativos, cuidados destinados a mejorar la calidad de vida de las personas con enfermedades graves, se han recomendado como parte de los programas de manejo de la metástasis. Los resultados de una revisión sistemática de la literatura sobre la radioterapia para las metástasis cerebrales encontraron que hay poca evidencia para informar la efectividad comparativa y los resultados centrados en el paciente sobre la calidad de vida, el estado funcional y los efectos cognitivos.
Investigar
Aunque se acepta ampliamente que la metástasis es el resultado de la migración de células tumorales, existe una hipótesis que dice que algunas metástasis son el resultado de procesos inflamatorios por parte de células inmunitarias anormales. La existencia de cánceres metastásicos en ausencia de tumores primarios también sugiere que la metástasis no siempre es causada por células malignas que dejan los tumores primarios.
La investigación realizada por el equipo de Sarna demostró que las células de melanoma muy pigmentadas tienen un módulo de Young de alrededor de 4,93, cuando en las no pigmentadas era de solo 0,98. En otro experimento encontraron que la elasticidad de las células de melanoma es importante para su metástasis y crecimiento: los tumores no pigmentados eran más grandes que los pigmentados y les era mucho más fácil propagarse. Demostraron que hay células pigmentadas y no pigmentadas en los tumores de melanoma, por lo que pueden ser resistentes a los medicamentos y metastásicos.
Historia
En marzo de 2014, los investigadores descubrieron el ejemplo completo más antiguo de un ser humano con cáncer metastásico. Los tumores se habían desarrollado en un esqueleto de 3.000 años encontrado en 2013 en una tumba en Sudán que data del 1200 a. El esqueleto se analizó mediante radiografía y un microscopio electrónico de barrido. Estos hallazgos fueron publicados en la revista Public Library of Science.
Etimología
Metástasis es una palabra griega que significa "desplazamiento", de μετά, meta, "siguiente", y στάσις, estasis, "colocación".
Contenido relacionado
Gen supresor tumoral
Hidrocefalia
Telofase