Metabolismo de drogas
Metabolismo de fármacos es la descomposición metabólica de fármacos por parte de organismos vivos, generalmente a través de sistemas enzimáticos especializados. De manera más general, el metabolismo xenobiótico (del griego xenos "extraño" y biótico "relacionado con los seres vivos") es el conjunto de vías metabólicas que modifican la estructura química de xenobióticos, que son compuestos extraños a la bioquímica normal de un organismo, como cualquier droga o veneno. Estas vías son una forma de biotransformación presente en todos los grupos principales de organismos y se consideran de origen antiguo. Estas reacciones a menudo actúan para desintoxicar compuestos venenosos (aunque en algunos casos los intermediarios del metabolismo xenobiótico pueden causar por sí mismos efectos tóxicos). El estudio del metabolismo de los fármacos se llama farmacocinética.
El metabolismo de los fármacos es un aspecto importante de la farmacología y la medicina. Por ejemplo, la tasa de metabolismo determina la duración y la intensidad de la acción farmacológica de un fármaco. El metabolismo de los fármacos también afecta la resistencia a múltiples fármacos en enfermedades infecciosas y en la quimioterapia para el cáncer, y las acciones de algunos fármacos como sustratos o inhibidores de enzimas implicadas en el metabolismo xenobiótico son una razón común para las interacciones farmacológicas peligrosas. Estas vías también son importantes en las ciencias ambientales, ya que el metabolismo xenobiótico de los microorganismos determina si un contaminante se descompondrá durante la biorremediación o persistirá en el medio ambiente. Las enzimas del metabolismo xenobiótico, particularmente las glutatión S-transferasas, también son importantes en la agricultura, ya que pueden producir resistencia a pesticidas y herbicidas.
El metabolismo de los fármacos se divide en tres fases. En la fase I, enzimas como las oxidasas del citocromo P450 introducen grupos reactivos o polares en los xenobióticos. Estos compuestos modificados luego se conjugan con compuestos polares en reacciones de fase II. Estas reacciones son catalizadas por enzimas transferasas como las glutatión S-transferasas. Finalmente, en la fase III, los xenobióticos conjugados pueden procesarse aún más, antes de ser reconocidos por los transportadores de eflujo y bombeados fuera de las células. El metabolismo de los fármacos a menudo convierte los compuestos lipófilos en productos hidrófilos que se excretan más fácilmente.
Barreras de permeabilidad y desintoxicación
Los compuestos exactos a los que está expuesto un organismo serán en gran medida impredecibles y pueden diferir mucho con el tiempo; Estas son las principales características del estrés tóxico xenobiótico. El principal desafío al que se enfrentan los sistemas de desintoxicación xenobióticos es que deben poder eliminar el número casi ilimitado de compuestos xenobióticos de la compleja mezcla de sustancias químicas implicadas en el metabolismo normal. La solución que ha evolucionado para abordar este problema es una combinación elegante de barreras físicas y sistemas enzimáticos de baja especificidad.
Todos los organismos utilizan membranas celulares como barreras de permeabilidad hidrófobas para controlar el acceso a su entorno interno. Los compuestos polares no pueden difundirse a través de estas membranas celulares y la captación de moléculas útiles está mediada por proteínas de transporte que seleccionan específicamente sustratos de la mezcla extracelular. Esta absorción selectiva significa que la mayoría de las moléculas hidrófilas no pueden entrar en las células, ya que no son reconocidas por ningún transportador específico. Por el contrario, la difusión de compuestos hidrófobos a través de estas barreras no se puede controlar y, por lo tanto, los organismos no pueden excluir los xenobióticos solubles en lípidos que utilizan barreras de membrana.
Sin embargo, la existencia de una barrera de permeabilidad significa que los organismos pudieron desarrollar sistemas de desintoxicación que explotan la hidrofobicidad común a los xenobióticos permeables a la membrana. Por lo tanto, estos sistemas resuelven el problema de la especificidad al poseer especificidades de sustrato tan amplias que metabolizan casi cualquier compuesto no polar. Los metabolitos útiles se excluyen porque son polares y, en general, contienen uno o más grupos cargados.
La desintoxicación de los subproductos reactivos del metabolismo normal no se puede lograr mediante los sistemas descritos anteriormente, porque estas especies se derivan de constituyentes celulares normales y generalmente comparten sus características polares. Sin embargo, dado que estos compuestos son pocos, enzimas específicas pueden reconocerlos y eliminarlos. Ejemplos de estos sistemas de desintoxicación específicos son el sistema glioxalasa, que elimina el aldehído reactivo metilglioxal, y los diversos sistemas antioxidantes que eliminan especies reactivas de oxígeno.
Fases de la desintoxicación
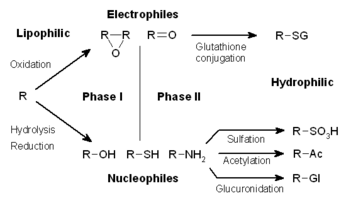
El metabolismo de los xenobióticos a menudo se divide en tres fases: modificación, conjugación y excreción. Estas reacciones actúan en conjunto para desintoxicar los xenobióticos y eliminarlos de las células.
Fase I – modificación
En la fase I, una variedad de enzimas actúan para introducir grupos reactivos y polares en sus sustratos. Una de las modificaciones más comunes es la hidroxilación catalizada por el sistema oxidasa de función mixta dependiente del citocromo P-450. Estos complejos enzimáticos actúan para incorporar un átomo de oxígeno en hidrocarburos no activados, lo que puede resultar en la introducción de grupos hidroxilo o en la desalquilación N, O y S de sustratos. El mecanismo de reacción de las oxidasas P-450 se produce mediante la reducción del oxígeno unido al citocromo y la generación de una especie de oxiferril altamente reactiva, según el siguiente esquema:
- O2 + NADPH + H+ + RH → NADP+ + H2O + ROH
Las reacciones de fase I (también denominadas reacciones no sintéticas) pueden ocurrir por oxidación, reducción, hidrólisis, ciclación, deciclización y adición de oxígeno o eliminación de hidrógeno, llevadas a cabo por oxidasas de función mixta, a menudo en el hígado. Estas reacciones oxidativas suelen implicar una monooxigenasa del citocromo P450 (a menudo abreviada CYP), NADPH y oxígeno. Las clases de fármacos que utilizan este método para su metabolismo incluyen fenotiazinas, paracetamol y esteroides. Si los metabolitos de las reacciones de la fase I son suficientemente polares, pueden excretarse fácilmente en este punto. Sin embargo, muchos productos de la fase I no se eliminan rápidamente y sufren una reacción posterior en la que un sustrato endógeno se combina con el grupo funcional recién incorporado para formar un conjugado altamente polar.
Un común La oxidación de fase I implica la conversión de un vínculo C-H a un C-OH. Esta reacción a veces convierte un compuesto farmacológicamente inactivo (un medicamento prodrug) a uno farmacológicomente activo. De la misma manera, Fase I puede convertir una molécula no tóxica en venenosa (toxificación). La hidrólisis simple en el estómago es normalmente una reacción inocua, sin embargo hay excepciones. Por ejemplo, el metabolismo fase I convierte acetonitrile a HOCH2CN, que se disocia rápidamente en formaldehído y cianuro de hidrógeno.
El metabolismo de fase I de los fármacos candidatos se puede simular en el laboratorio utilizando catalizadores no enzimáticos. Este ejemplo de reacción biomimética tiende a generar productos que a menudo contienen los metabolitos de la Fase I. Como ejemplo, el principal metabolito de la trimebutina farmacéutica, la desmetiltrimebutina (nor-trimebutina), puede producirse eficazmente mediante oxidación in vitro del fármaco disponible comercialmente. La hidroxilación de un grupo N-metilo conduce a la expulsión de una molécula de formaldehído, mientras que la oxidación de los grupos O-metilo se produce en menor medida.
Oxidación
- Sistema de monooxigenasa P450 Cytochrome
- Sistema de monooxigenasa que contiene Flavin
- Alcohol deshidrogenasa y aldehido deshidrogenasa
- Monoamina oxidase
- Co-oxidación por peróxidos
Reducción
- NADPH-cytochrome P450 reductase
La citocromo P450 reductasa, también conocida como NADPH:ferrihemoproteína oxidorreductasa, NADPH:hemoproteína oxidorreductasa, NADPH:P450 oxidorreductasa, P450 reductasa, POR, CPR, CYPOR, es una enzima unida a membrana necesaria para la transferencia de electrones al citocromo P450 en el microsoma. de la célula eucariota a partir de una enzima que contiene FAD y FMN NADPH:citocromo P450 reductasa El esquema general de flujo de electrones en el sistema POR/P450 es: NADPH → MODA → FMN → P450 → O2
- Reducido (ferroso) citocromo P450
Durante las reacciones de reducción, una sustancia química puede entrar en un ciclo inútil, en el que gana un electrón de radical libre y luego rápidamente lo pierde en oxígeno (para formar un anión superóxido).
Hidrólisis
- Esterases y amidase
- Epoxide hydrolase
Fase II – conjugación
En reacciones posteriores de fase II, estos metabolitos xenobióticos activados se conjugan con especies cargadas como el glutatión (GSH), el sulfato, la glicina o el ácido glucurónico. Los sitios de los fármacos donde se producen reacciones de conjugación incluyen grupos carboxi (-COOH), hidroxi (-OH), amino (NH2) y tiol (-SH). Los productos de las reacciones de conjugación tienen un mayor peso molecular y tienden a ser menos activos que sus sustratos, a diferencia de las reacciones de Fase I que a menudo producen metabolitos activos. La adición de grandes grupos aniónicos (como el GSH) desintoxica los electrófilos reactivos y produce metabolitos más polares que no pueden difundirse a través de las membranas y, por lo tanto, pueden transportarse activamente.
Estas reacciones son catalizadas por un gran grupo de transferasas de amplia especificidad, que en combinación pueden metabolizar casi cualquier compuesto hidrófobo que contenga grupos nucleofílicos o electrófilos. Una de las clases más importantes de este grupo es la de las glutatión S-transferasas (GST).
| Mecanismo | Enzima rotatoria | Co-factor | Ubicación | Fuentes |
|---|---|---|---|---|
| Metilación | metiltransferas | S-adenosyl-L-methionine | hígado, riñón, pulmón, SNC | |
| sulfato | sulfotransferas | 3'-phosphoadenosine-5'-phosulfate | hígado, riñón, intestino | |
| acetilación |
| acetyl coenzyme A | hígado, pulmón, bazo, mucosa gástrica, RBCs, linfocitos | |
| glucuronidación | UDP-glucuronosyltransferases | UDP-glucuronic acid | hígado, riñón, intestino, pulmón, piel, próstata, cerebro | |
| Conjugación de glutatión | glutathione S-transferases | glutatióne | hígado, riñón | |
| glicina conjugación | Proceso de dos pasos:
| glicina | hígado, riñón |
Fase III – modificación y excreción adicionales
Después de las reacciones de fase II, los conjugados xenobióticos pueden metabolizarse aún más. Un ejemplo común es el procesamiento de conjugados de glutatión en conjugados de acetilcisteína (ácido mercaptúrico). Aquí, la gamma-glutamil transpeptidasa y las dipeptidasas eliminan los residuos de γ-glutamato y glicina en la molécula de glutatión. En el paso final, se acetila el residuo de cisteína del conjugado.
Los conjugados y sus metabolitos pueden ser excretados de las células en la fase III de su metabolismo, con los grupos aniónicos actuando como etiquetas de afinidad para una variedad de transportadores de membrana de la familia de la proteína de resistencia multidroga. Estas proteínas son miembros de la familia de transportadores de cassettes combinados con ATP y pueden catalizar el transporte dependiente de ATP de una gran variedad de aniones hidrofóbicos, y así actuar para eliminar los productos de fase II al medio extracelular, donde pueden ser metabolizados o excretados más.
Toxinas endógenas
La desintoxicación de metabolitos reactivos endógenos, como peróxidos y aldehídos reactivos, a menudo no se puede lograr mediante el sistema descrito anteriormente. Este es el resultado de la acción de estas especies. derivan de constituyentes celulares normales y generalmente comparten sus características polares. Sin embargo, dado que estos compuestos son pocos, es posible que los sistemas enzimáticos utilicen un reconocimiento molecular específico para reconocerlos y eliminarlos. Por lo tanto, la similitud de estas moléculas con metabolitos útiles significa que normalmente se requieren diferentes enzimas de desintoxicación para el metabolismo de cada grupo de toxinas endógenas. Ejemplos de estos sistemas de desintoxicación específicos son el sistema glioxalasa, que actúa para eliminar el aldehído reactivo metilglioxal, y los diversos sistemas antioxidantes que eliminan las especies reactivas de oxígeno.
Sitios
Cuantitativamente, el retículo endoplásmico liso de la célula hepática es el principal órgano del metabolismo de los fármacos, aunque cada tejido biológico tiene cierta capacidad para metabolizar fármacos. Los factores responsables de la contribución del hígado al metabolismo de los fármacos incluyen que es un órgano grande, que es el primer órgano perfundido por sustancias químicas absorbidas en el intestino y que existen concentraciones muy altas de la mayoría de los sistemas enzimáticos que metabolizan los fármacos en relación con el hígado. a otros órganos. Si un fármaco se introduce en el tracto gastrointestinal, donde ingresa a la circulación hepática a través de la vena porta, se metaboliza bien y se dice que muestra el efecto de primer paso.
Otros sitios del metabolismo de los fármacos incluyen las células epiteliales del tracto gastrointestinal, los pulmones, los riñones y la piel. Estos sitios suelen ser responsables de reacciones de toxicidad localizadas.
Factores que afectan el metabolismo de los medicamentos
La duración y la intensidad de la acción farmacológica de la mayoría de los fármacos lipófilos están determinadas por la velocidad a la que se metabolizan en productos inactivos. El sistema monooxigenasa del citocromo P450 es una vía crucial a este respecto. En general, cualquier cosa que aumente la tasa de metabolismo (p. ej., inducción enzimática) de un metabolito farmacológicamente activo disminuirá la duración y la intensidad de la acción del fármaco. Lo contrario también es cierto, como en la inhibición enzimática. Sin embargo, en los casos en que una enzima es responsable de metabolizar un profármaco en un fármaco, la inducción enzimática puede acelerar esta conversión y aumentar los niveles del fármaco, lo que puede provocar toxicidad.
Varios factores fisiológicos y patológicos también pueden afectar el metabolismo de los fármacos. Los factores fisiológicos que pueden influir en el metabolismo de los fármacos incluyen la edad, la variación individual (p. ej., farmacogenética), la circulación enterohepática, la nutrición, las diferencias sexuales o la microbiota intestinal. Este último factor tiene importancia porque los microorganismos intestinales son capaces de modificar químicamente la estructura de los fármacos mediante procesos de degradación y biotransformación, alterando así la actividad y toxicidad de los fármacos. Estos procesos pueden disminuir la eficacia de los fármacos, como es el caso de la digoxina ante la presencia de Eggerthella lenta en la microbiota. La variación genética (polimorfismo) explica parte de la variabilidad en el efecto de las drogas.
En general, las drogas se metabolizan más lentamente en humanos y animales fetales, neonatales y ancianos que en adultos. Con N-acetilransferases (involucrado en Fase II reacciones), la variación individual crea un grupo de personas que acetilan lentamente (acetiladores lentos) y los que acetilan rápidamente, se dividieron aproximadamente 50:50 en la población de Canadá. Esta variación puede tener consecuencias dramáticas, ya que los acetiladores lentos son más propensos a la toxicidad dependiente de la dosis.
La dosis, la frecuencia, la vía de administración, la distribución tisular y la unión a proteínas del fármaco afectan su metabolismo. Los factores patológicos también pueden influir en el metabolismo de los fármacos, incluidas las enfermedades hepáticas, renales o cardíacas.
Los métodos de simulación y modelado in silico permiten predecir el metabolismo de los fármacos en poblaciones virtuales de pacientes antes de realizar estudios clínicos en seres humanos. Esto se puede utilizar para identificar a las personas con mayor riesgo de sufrir una reacción adversa.Historia
Los estudios sobre cómo las personas transforman las sustancias que ingieren comenzaron a mediados del siglo XIX, cuando los químicos descubrieron que las sustancias químicas orgánicas como el benzaldehído podían oxidarse y conjugarse con aminoácidos en el cuerpo humano. Durante el resto del siglo XIX, se descubrieron otras reacciones básicas de desintoxicación, como la metilación, la acetilación y la sulfonación.
A principios del siglo XX, el trabajo pasó a la investigación de las enzimas y las vías responsables de la producción de estos metabolitos. Este campo quedó definido como un área de estudio separada con la publicación por Richard Williams del libro Mecanismos de detoxicación en 1947. Esta investigación bioquímica moderna dio como resultado la identificación del glutatión S- transferasas en 1961, seguido por el descubrimiento del citocromo P450 en 1962, y la comprensión de su papel central en el metabolismo xenobiótico en 1963.