Mesitileno
Mesitileno o 1,3,5-trimetilbenceno es un derivado del benceno con tres sustituyentes metilo colocados simétricamente alrededor del anillo. Los otros dos trimetilbencenos isoméricos son 1,2,4-trimetilbenceno (pseudocumeno) y 1,2,3-trimetilbenceno (hemimeliteno). Los tres compuestos tienen la fórmula C6H3(CH3)3, que comúnmente se abrevia C6H3Yo3. El mesitileno es un líquido incoloro con un olor aromático dulce. Es un componente del alquitrán de hulla, que es su fuente tradicional. Es un precursor de diversas sustancias químicas finas. El grupo mesitilo (Mes) es un sustituyente con la fórmula C6H2Me3 y se encuentra en varios otros compuestos.
Preparación
El mesitileno se prepara mediante transalquilación de xileno sobre un catalizador ácido sólido:
- 2 C6H4(CH3)2 ⇌ C6H3(CH)3)3+ C6H5CH3
- C6H4(CH)3)2+ CH3OH → C6H3(CH)3)3+ H2O
Aunque no es práctico, podría prepararse mediante trimerización de propino, que también requiere un catalizador ácido y produce una mezcla de 1,3,5- y 1,2,4-trimetilbencenos.
La trimerización de acetona mediante condensación aldólica, que es catalizada y deshidratada por ácido sulfúrico, es otro método para sintetizar mesitileno.
Reacciones
La oxidación del mesitileno con ácido nítrico produce ácido trimésico, C6H3(COOH)3. Utilizando dióxido de manganeso, un agente oxidante más suave, se forma 3,5-dimetilbenzaldehído. El mesitileno se oxida con ácido trifluoroperacético para producir mesitol (2,4,6-trimetilfenol). La bromación se produce fácilmente, dando bromuro de mesitilo:
- (CH)3)3C6H3 + Br2 →3)3C6H2Br + HBr
El mesitileno es un ligando en la química organometálica, un ejemplo es el complejo de organomolibdeno [(η6-C6H3Me3)Mo(CO)3] que se puede preparar a partir de hexacarbonilo de molibdeno.
Aplicaciones
El mesitileno se utiliza principalmente como precursor de la 2,4,6-trimetilanilina, un precursor de los colorantes. Este derivado se prepara mediante mononitración selectiva de mesitileno, evitando la oxidación de los grupos metilo.
Usos especializados
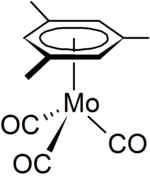
El mesitileno se utiliza en el laboratorio como disolvente especial. En la industria electrónica, el mesitileno se ha utilizado como revelador de siliconas fotopatternables debido a sus propiedades disolventes.
Los tres átomos de hidrógeno aromáticos del mesitileno se encuentran en entornos de cambio químico idénticos. Por lo tanto, solo dan un pico único cerca de 6,8 ppm en el espectro de RMN 1H; Lo mismo ocurre con los nueve protones de metilo, que dan un singlete cercano a 2,3 ppm. Por esta razón, el mesitileno a veces se utiliza como estándar interno en muestras de RMN que contienen protones aromáticos.
El ácido uvítico se obtiene oxidando mesitileno o condensando ácido pirúvico con agua baritada.
La reacción de Gattermann se puede simplificar reemplazando la combinación HCN/AlCl3 por cianuro de zinc (Zn(CN)2). Aunque es altamente tóxico, el Zn(CN)2 es un sólido, lo que hace que trabajar con él sea más seguro que el cianuro de hidrógeno gaseoso (HCN). El Zn(CN)2 reacciona con el HCl para formar el reactivo clave HCN y ZnCl2 que sirve como catalizador de ácido de Lewis in situ. Un ejemplo del método Zn(CN)2 es la síntesis de mesitaldehído a partir de mesitileno.
Historia
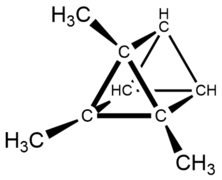
El mesitileno fue preparado por primera vez en 1837 por Robert Kane, un químico irlandés, calentando acetona con ácido sulfúrico concentrado. Llamó a su nueva sustancia "mesitileno" porque el químico alemán Carl Reichenbach había llamado a la acetona "mesit" (del griego μεσίτης, el mediador), y Kane creía que su reacción había deshidratado al mesit, convirtiéndolo en un alqueno, "mesitileno". Sin embargo, la determinación de Kane de la composición química ("fórmula empírica") del mesitileno fue incorrecta. La fórmula empírica correcta fue proporcionada por August W. von Hofmann en 1849. En 1866, Adolf von Baeyer dio una fórmula empírica correcta del mesitileno; sin embargo, con una estructura incorrecta del tetraciclo[3.1.1.11,3.13,5]nonano. Albert Ladenburg proporcionó una prueba concluyente de que el mesitileno era trimetilbenceno en 1874; sin embargo, suponiendo una estructura de benceno incorrecta del prismano.
- Estructuras históricas del mesitylene
Mesitylene by Adolf von Baeyer (tetracyclo[3.1.1.11,3.13,5No.
Mesitylene by Albert Ladenburg (1,2,6-trimetilprismane)
Grupo mesitilo
El grupo (CH3)3C6H2- se llama mesityl (símbolo de grupo orgánico: Mes). Derivados de mesitilo, p.e. tetramesitildiiron, normalmente se preparan a partir del reactivo de Grignard (CH3)3C6H2MgBr. Debido a su gran demanda estérica, el grupo mesitilo se utiliza como un gran grupo bloqueador en catálisis asimétrica (para mejorar la diastereo o enantioselectividad) y en la química organometálica (para estabilizar centros metálicos con estados de oxidación bajos o números de coordinación bajos). Análogos más grandes con una demanda estérica aún mayor, por ejemplo 2,6-diisopropilfenil (Dipp) y el nombre análogo Tripp ((iPr)3C6H2, Is) y supermesityl ((t Bu)3C6H2, Mes*), pueden ser incluso más eficaces para lograr estos objetivos.
Seguridad y medio ambiente
El mesitileno también es un importante compuesto orgánico volátil (COV) urbano que resulta de la combustión. Desempeña un papel importante en la formación de aerosoles y ozono troposférico, así como en otras reacciones de la química atmosférica.
Contenido relacionado
Permanganato de potasio
Char (química)
Efecto de ion común
![Mesitylene by Adolf von Baeyer (tetracyclo[3.1.1.11,3.13,5]nonane)](https://upload.wikimedia.org/wikipedia/commons/thumb/0/0e/Mesitylen_by_Adolf_von_Baeyer.png/260px-Mesitylen_by_Adolf_von_Baeyer.png)