Máquina térmica
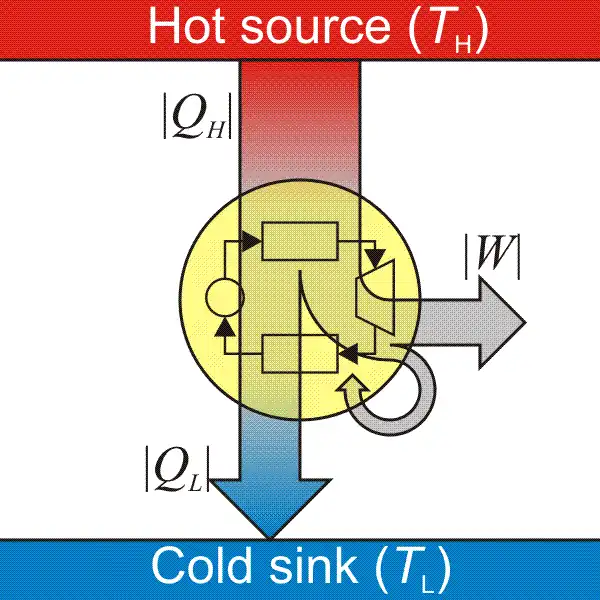
En termodinámica e ingeniería, una máquina térmica es un sistema que convierte el calor en energía mecánica, que luego se puede utilizar para realizar un trabajo mecánico.Lo hace al llevar una sustancia de trabajo de una temperatura de estado más alta a una temperatura de estado más baja. Una fuente de calor genera energía térmica que lleva la sustancia de trabajo al estado de alta temperatura. La sustancia de trabajo genera trabajo en el cuerpo de trabajo del motor mientras transfiere calor al disipador más frío hasta que alcanza un estado de baja temperatura. Durante este proceso, parte de la energía térmica se convierte en trabajo aprovechando las propiedades de la sustancia de trabajo. La sustancia de trabajo puede ser cualquier sistema con una capacidad calorífica distinta de cero, pero por lo general es un gas o un líquido. Durante este proceso, normalmente se pierde algo de calor hacia el entorno y no se convierte en trabajo. Además, parte de la energía es inutilizable debido a la fricción y el arrastre.
En general, un motor es cualquier máquina que convierte energía en trabajo mecánico. Los motores térmicos se distinguen de otros tipos de motores por el hecho de que su eficiencia está fundamentalmente limitada por el teorema de Carnot. Aunque esta limitación de eficiencia puede ser un inconveniente, una ventaja de los motores térmicos es que la mayoría de las formas de energía se pueden convertir fácilmente en calor mediante procesos como reacciones exotérmicas (como la combustión), fisión nuclear, absorción de luz o partículas energéticas, fricción, disipación y resistencia Dado que la fuente de calor que suministra energía térmica al motor puede alimentarse prácticamente con cualquier tipo de energía, los motores térmicos cubren una amplia gama de aplicaciones.
Los motores térmicos a menudo se confunden con los ciclos que intentan implementar. Por lo general, el término "motor" se usa para un dispositivo físico y "ciclo" para los modelos.
Visión de conjunto
En termodinámica, los motores térmicos a menudo se modelan utilizando un modelo de ingeniería estándar como el ciclo de Otto. El modelo teórico se puede refinar y aumentar con datos reales de un motor en funcionamiento, utilizando herramientas como un diagrama indicador. Dado que muy pocas implementaciones reales de motores térmicos coinciden exactamente con sus ciclos termodinámicos subyacentes, se podría decir que un ciclo termodinámico es un caso ideal de un motor mecánico. En cualquier caso, comprender completamente un motor y su eficiencia requiere una buena comprensión del modelo teórico (posiblemente simplificado o idealizado), los matices prácticos de un motor mecánico real y las discrepancias entre los dos.
En términos generales, cuanto mayor sea la diferencia de temperatura entre la fuente caliente y el sumidero frío, mayor será la eficiencia térmica potencial del ciclo. En la Tierra, el lado frío de cualquier motor térmico se limita a estar cerca de la temperatura ambiente del medio ambiente, o no muy por debajo de los 300 kelvin, por lo que la mayoría de los esfuerzos para mejorar las eficiencias termodinámicas de varios motores térmicos se centran en aumentar la temperatura del medio ambiente. fuente, dentro de los límites materiales. La eficiencia teórica máxima de un motor térmico (que ningún motor alcanza nunca) es igual a la diferencia de temperatura entre los extremos caliente y frío dividida por la temperatura en el extremo caliente, cada uno expresado en temperatura absoluta.
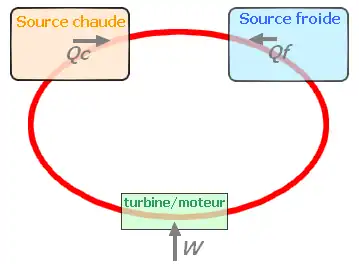
La eficiencia de varios motores térmicos propuestos o utilizados hoy en día tiene un amplio rango:
- 3% (97 por ciento de calor residual usando calor de baja calidad) para la propuesta de energía oceánica de conversión de energía térmica oceánica (OTEC)
- 25% para la mayoría de los motores de gasolina de automóviles
- 49% para una central eléctrica de carbón supercrítico como la central eléctrica de Avedøre
- 60% para una turbina de gas de ciclo combinado
La eficiencia de estos procesos es aproximadamente proporcional a la caída de temperatura a través de ellos. Los equipos auxiliares, como las bombas, pueden consumir una cantidad significativa de energía, lo que reduce efectivamente la eficiencia.
Ejemplos
Es importante señalar que aunque algunos ciclos tienen una ubicación de combustión típica (interna o externa), a menudo se pueden implementar con la otra. Por ejemplo, John Ericsson desarrolló un motor con calefacción externa que funcionaba en un ciclo muy parecido al ciclo diésel anterior. Además, los motores con calefacción externa a menudo se pueden implementar en ciclos abiertos o cerrados. En un ciclo cerrado, el fluido de trabajo se retiene dentro del motor al finalizar el ciclo, mientras que en un ciclo abierto, el fluido de trabajo se intercambia con el medio ambiente junto con los productos de la combustión en el caso del motor de combustión interna o simplemente se ventila hacia el exterior. el medio ambiente en el caso de los motores de combustión externa como las máquinas de vapor y las turbinas.
Ejemplos cotidianos
Los ejemplos cotidianos de motores térmicos incluyen la central térmica, el motor de combustión interna, las armas de fuego, los refrigeradores y las bombas de calor. Las centrales eléctricas son ejemplos de motores térmicos que funcionan hacia adelante en los que el calor fluye desde un depósito caliente y fluye hacia un depósito frío para producir trabajo como el producto deseado. Los refrigeradores, acondicionadores de aire y bombas de calor son ejemplos de máquinas térmicas que funcionan a la inversa, es decir, usan trabajo para tomar energía térmica a baja temperatura y elevar su temperatura de una manera más eficiente que la simple conversión de trabajo en calor (ya sea a través de fricción o resistencia eléctrica). Los refrigeradores eliminan el calor del interior de una cámara sellada térmicamente a baja temperatura y ventilan el calor residual a una temperatura más alta hacia el ambiente y las bombas de calor toman el calor del ambiente a baja temperatura y lo "ventilan".
En general, los motores térmicos aprovechan las propiedades térmicas asociadas con la expansión y compresión de los gases según las leyes de los gases o las propiedades asociadas con los cambios de fase entre los estados gaseoso y líquido.
El motor térmico de la Tierra
La atmósfera y la hidrosfera de la Tierra, el motor térmico de la Tierra, son procesos acoplados que equilibran constantemente los desequilibrios del calentamiento solar a través de la evaporación del agua superficial, la convección, la lluvia, los vientos y la circulación oceánica, al distribuir el calor por todo el mundo.
Una celda de Hadley es un ejemplo de un motor térmico. Implica el ascenso de aire cálido y húmedo en la región ecuatorial de la tierra y el descenso de aire más frío en los subtrópicos creando una circulación directa impulsada térmicamente, con la consiguiente producción neta de energía cinética.
Ciclos de cambio de fase
En estos ciclos y motores, los fluidos de trabajo son gases y líquidos. El motor convierte el fluido de trabajo de gas a líquido, de líquido a gas, o ambos, generando trabajo a partir de la expansión o compresión del fluido.
- Ciclo Rankine (máquina de vapor clásica)
- Ciclo regenerativo (máquina de vapor más eficiente que el ciclo Rankine)
- Ciclo orgánico de Rankine (fase de cambio de refrigerante en rangos de temperatura de hielo y agua líquida caliente)
- Ciclo de vapor a líquido (pájaro bebedor, inyector, rueda Minto)
- Ciclo de líquido a sólido (elevación de escarcha: el agua que cambia de hielo a líquido y viceversa puede levantar rocas hasta 60 cm).
- Ciclo de sólido a gas (armas de fuego: los propulsores sólidos se queman en gases calientes).
Ciclos solo de gas
En estos ciclos y motores el fluido de trabajo es siempre un gas (es decir, no hay cambio de fase):
- Ciclo de Carnot (máquina térmica de Carnot)
- Ciclo de Ericsson (Nave Calórica John Ericsson)
- Ciclo Stirling (motor Stirling, dispositivos termoacústicos)
- Motor de combustión interna (ICE):
- Ciclo Otto (por ejemplo, gasolina/motor de gasolina)
- Ciclo diésel (por ejemplo, motor diésel)
- Ciclo Atkinson (motor Atkinson)
- Ciclo Brayton o ciclo Joule originalmente ciclo Ericsson (turbina de gas)
- Ciclo Lenoir (p. ej., motor a reacción pulsante)
- Ciclo Miller (motor Miller)
Ciclos de solo líquido
En estos ciclos y motores el fluido de trabajo es siempre como líquido:
- Ciclo Stirling (motor Malone)
- Ciclón regenerativo de calor
Ciclos de electrones
- Convertidor de energía termoeléctrica Johnson
- Termoeléctrico (efecto Peltier-Seebeck)
- Celda termogalvánica
- Emisión termoiónica
- Refrigeración por termotúnel
Ciclos magnéticos
- Motor termomagnético (Tesla)
Ciclos utilizados para refrigeración
Un frigorífico doméstico es un ejemplo de bomba de calor: un motor térmico al revés. El trabajo se utiliza para crear un diferencial de calor. Muchos ciclos pueden funcionar a la inversa para mover el calor del lado frío al lado caliente, haciendo que el lado frío se enfríe y el lado caliente se caliente más. Las versiones de motor de combustión interna de estos ciclos son, por su naturaleza, no reversibles.
Los ciclos de refrigeración incluyen:
- máquina de ciclo de aire
- Frigorífico de absorción de gas
- refrigeración magnética
- Refrigerador criogénico Stirling
- Refrigeración por compresión de vapor
- Ciclo de Vuilleumier
Motores de calor evaporativo
El motor de evaporación de Barton es un motor térmico basado en un ciclo que produce energía y aire húmedo enfriado a partir de la evaporación del agua en aire seco y caliente.
Motores térmicos mesoscópicos
Los motores térmicos mesoscópicos son dispositivos a nanoescala que pueden cumplir el objetivo de procesar flujos de calor y realizar un trabajo útil a pequeña escala. Las aplicaciones potenciales incluyen, por ejemplo, dispositivos de refrigeración eléctricos. En estos motores térmicos mesoscópicos, el trabajo por ciclo de operación fluctúa debido al ruido térmico. Existe una igualdad exacta que relaciona el promedio de los exponentes del trabajo realizado por cualquier motor térmico y la transferencia de calor del baño de calor más caliente. Esta relación transforma la desigualdad de Carnot en igualdad exacta. Esta relación es también una igualdad del ciclo de Carnot
Eficiencia
La eficiencia de una máquina térmica relaciona la cantidad de trabajo útil que se produce para una cantidad determinada de entrada de energía térmica.
De las leyes de la termodinámica, después de un ciclo completo:{displaystyle W+Q=Delta_{ciclo}U=0}



En otras palabras, una máquina térmica absorbe energía térmica de la fuente de calor de alta temperatura, convirtiendo parte de ella en trabajo útil y emitiendo el resto como calor residual al disipador de calor de temperatura fría.
En general, la eficiencia de un proceso de transferencia de calor dado se define por la relación entre "lo que se saca" y "lo que se pone". (Para un refrigerador o una bomba de calor, que se puede considerar como un motor térmico que funciona a la inversa, este es el coeficiente de rendimiento y es ≥ 1). En el caso de un motor, se desea extraer trabajo y se debe poner calor{ estilo de visualización Q_ {h}}
La eficiencia es inferior al 100% debido al calor residual.{displaystyle Q_{c}<0}<img src="https://wikimedia.org/api/rest_v1/media/math/render/svg/bc70a08660c1452f860a5bfb1b594d03f72c1634" alt="{displaystyle Q_{c}se pierde inevitablemente en el disipador de frío (y se aplica el trabajo de compresión correspondiente) durante la recompresión requerida a la temperatura fría antes de que vuelva a producirse la carrera de potencia del motor.
La eficiencia máxima teórica de cualquier motor térmico depende únicamente de las temperaturas entre las que opera. Esta eficiencia generalmente se obtiene utilizando un motor térmico imaginario ideal como el motor térmico de Carnot, aunque otros motores que utilizan diferentes ciclos también pueden alcanzar la máxima eficiencia. Matemáticamente, después de un ciclo completo, el cambio total de entropía es cero:
{displaystyle Delta S_{h}+Delta S_{c}=Delta _{ciclo}S=0}
Tenga en cuenta que{ estilo de visualización Delta S_ {h}}



{displaystyle Q_{h}/T_{h}+Q_{c}/T_{c}=0}
lo que da{displaystyle Q_{c}/Q_{h}=-T_{c}/T_{h}}
donde{displaystyle T_{h}}

El razonamiento detrás de esto, siendo la eficiencia máxima, es el siguiente. Primero se supone que si es posible un motor térmico más eficiente que un motor de Carnot, entonces podría funcionar en reversa como una bomba de calor. El análisis matemático se puede utilizar para mostrar que esta supuesta combinación daría como resultado una disminución neta de la entropía. Dado que, según la segunda ley de la termodinámica, esto es estadísticamente improbable hasta el punto de la exclusión, la eficiencia de Carnot es un límite superior teórico de la eficiencia confiable de cualquier ciclo termodinámico.
Empíricamente, nunca se ha demostrado que una máquina térmica funcione con mayor eficiencia que una máquina térmica de ciclo de Carnot.
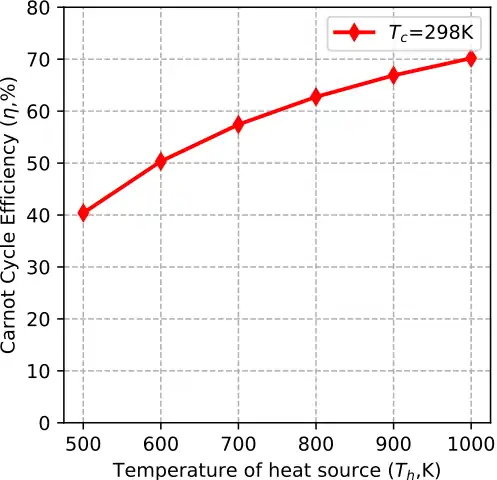
La Figura 2 y la Figura 3 muestran variaciones en la eficiencia del ciclo de Carnot con la temperatura. La Figura 2 indica cómo cambia la eficiencia con un aumento en la temperatura de adición de calor para una temperatura de entrada del compresor constante. La Figura 3 indica cómo cambia la eficiencia con un aumento en la temperatura de rechazo de calor para una temperatura de entrada de turbina constante.
 Figura 2: Eficiencia del ciclo de Carnot con cambios en la temperatura de adición de calor. Figura 2: Eficiencia del ciclo de Carnot con cambios en la temperatura de adición de calor. | 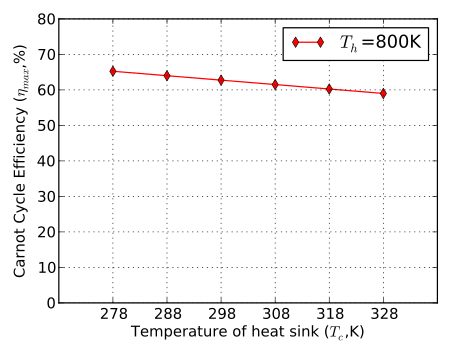 Figura 3: Eficiencia del ciclo de Carnot con temperatura de rechazo de calor cambiante. Figura 3: Eficiencia del ciclo de Carnot con temperatura de rechazo de calor cambiante. |
Motores térmicos endo-reversibles
Por su naturaleza, cualquier ciclo de Carnot de máxima eficiencia debe operar con un gradiente de temperatura infinitesimal; esto se debe a que cualquier transferencia de calor entre dos cuerpos de diferentes temperaturas es irreversible, por lo tanto, la expresión de eficiencia de Carnot se aplica solo al límite infinitesimal. El principal problema es que el objetivo de la mayoría de los motores térmicos es generar potencia, y rara vez se desea una potencia infinitesimal.
Las consideraciones de la termodinámica endorreversible dan una medida diferente de la eficiencia ideal del motor térmico, donde el sistema se divide en subsistemas reversibles, pero con interacciones no reversibles entre ellos. Un ejemplo clásico es el motor de Curzon-Ahlborn, muy similar al motor de Carnot, pero donde los depósitos térmicos a temperatura{displaystyle T_{h}}






pero al precio de una potencia de salida que se desvanece. Si, por el contrario, se elige operar el motor a su máxima potencia de salida, la eficiencia se vuelve{displaystyle eta =1-{sqrt {frac {T_{c}}{T_{h}}}}}
Este modelo hace un mejor trabajo al predecir qué tan bien pueden funcionar los motores térmicos del mundo real (Callen 1985, ver también termodinámica endorreversible):
| Central eléctrica | {displaystyle T_{c}} (°C) (°C) | {displaystyle T_{h}} (°C) (°C) | { estilo de visualización eta} (Carnot) (Carnot) | { estilo de visualización eta} (Endoreversible) (Endoreversible) | { estilo de visualización eta} (Observado) (Observado) |
|---|---|---|---|---|---|
| Central eléctrica de carbón de West Thurrock (Reino Unido) | 25 | 565 | 0,64 | 0.40 | 0.36 |
| Central nuclear CANDU (Canadá) | 25 | 300 | 0.48 | 0.28 | 0.30 |
| Central geotérmica de Larderello (Italia) | 80 | 250 | 0.33 | 0.178 | 0.16 |
Como se muestra, la eficiencia de Curzon-Ahlborn modela mucho más de cerca lo observado.
Historia
Los motores térmicos se conocen desde la antigüedad, pero solo se convirtieron en dispositivos útiles en el momento de la revolución industrial en el siglo XVIII. Continúan desarrollándose en la actualidad.
Mejoras
Los ingenieros han estudiado los diversos ciclos de los motores térmicos para mejorar la cantidad de trabajo utilizable que podrían extraer de una fuente de energía determinada. El límite del ciclo de Carnot no se puede alcanzar con ningún ciclo basado en gas, pero los ingenieros han encontrado al menos dos formas de eludir ese límite y una forma de obtener una mayor eficiencia sin infringir ninguna regla:
- Aumentar la diferencia de temperatura en el motor térmico. La forma más sencilla de hacer esto es aumentar la temperatura del lado caliente, que es el enfoque utilizado en las modernas turbinas de gas de ciclo combinado. Desafortunadamente, los límites físicos (como el punto de fusión de los materiales utilizados para construir el motor) y las preocupaciones ambientales con respecto a la producción de NOx ( si la fuente de calor es la combustión con aire ambiental) restringen la temperatura máxima en los motores térmicos que funcionan. Las turbinas de gas modernas funcionan a temperaturas lo más altas posible dentro del rango de temperaturas necesario para mantener una producción aceptable de NO x. Otra forma de aumentar la eficiencia es reducir la temperatura de salida. Un nuevo método para hacerlo es usar fluidos de trabajo químicos mixtos y luego explotar el comportamiento cambiante de las mezclas. Uno de los más famosos es el llamado ciclo Kalina, que utiliza una mezcla 70/30 de amoníaco y agua como fluido de trabajo. Esta mezcla permite que el ciclo genere energía útil a temperaturas considerablemente más bajas que la mayoría de los otros procesos.
- Explotar las propiedades físicas del fluido de trabajo. La explotación más común es el uso de agua por encima del punto crítico (agua supercrítica). El comportamiento de los fluidos por encima de su punto crítico cambia radicalmente, y con materiales como el agua y el dióxido de carbono es posible aprovechar esos cambios de comportamiento para extraer una mayor eficiencia termodinámica del motor térmico, incluso si se utiliza un Brayton o un Rankine bastante convencionales. ciclo. Un material más nuevo y muy prometedor para tales aplicaciones es el CO2 supercrítico . TAN 2y el xenón también se han considerado para tales aplicaciones. Las desventajas incluyen problemas de corrosión y erosión, el diferente comportamiento químico por encima y por debajo del punto crítico, las altas presiones necesarias y, en el caso del dióxido de azufre y, en menor medida, la toxicidad del dióxido de carbono. Entre los compuestos mencionados, el xenón es menos adecuado para su uso en un reactor nuclear debido a la alta sección transversal de absorción de neutrones de casi todos los isótopos de xenón, mientras que el dióxido de carbono y el agua también pueden funcionar como moderadores de neutrones para un reactor de espectro térmico.
- Explotar las propiedades químicas del fluido de trabajo. Una hazaña bastante nueva y novedosa es utilizar fluidos de trabajo exóticos con propiedades químicas ventajosas. Uno de ellos es el dióxido de nitrógeno (NO 2), un componente tóxico del smog, que tiene un dímero natural como tetraóxido de dinitrógeno (N 2 O 4). A baja temperatura, el N 2 O 4 se comprime y luego se calienta. El aumento de la temperatura hace que cada N 2 O 4 se separe en dos moléculas de NO 2. Esto reduce el peso molecular del fluido de trabajo, lo que aumenta drásticamente la eficiencia del ciclo. Una vez que el NO 2se ha expandido a través de la turbina, es enfriado por el disipador de calor, que lo hace recombinar en N 2 O 4. Esto luego es retroalimentado por el compresor para otro ciclo. Se han investigado especies como el bromuro de aluminio (Al 2 Br 6), NOCl y Ga 2 I 6 para tales usos. Hasta la fecha, sus inconvenientes no han justificado su uso, a pesar de las ganancias de eficiencia que se pueden obtener.
Procesos de motores térmicos
| Ciclo | Compresión, 1→2 | Adición de calor, 2→3 | Expansión, 3→4 | Rechazo de calor, 4→1 | notas |
|---|---|---|---|---|---|
| Ciclos de energía normalmente con combustión externa o ciclos de bomba de calor: | |||||
| campana coleman | adiabático | isobárico | adiabático | isobárico | Un ciclo Brayton invertido |
| Carnot | isentrópico | isotérmico | isentrópico | isotérmico | Máquina térmica de Carnot |
| Ericsson | isotérmico | isobárico | isotérmico | isobárico | El segundo ciclo de Ericsson de 1853 |
| Ranking | adiabático | isobárico | adiabático | isobárico | Máquinas de vapor |
| Higroscópico | adiabático | isobárico | adiabático | isobárico | |
| Scuderi | adiabático | presióny volumen variables | adiabático | isocorico | |
| Stirling | isotérmico | isocorico | isotérmico | isocorico | motores Stirling |
| Manson | isotérmico | isocorico | isotérmico | isocórico luego adiabático | Motores Manson y Manson-Guise |
| Stoddard | adiabático | isobárico | adiabático | isobárico | |
| Ciclos de energía normalmente con combustión interna: | |||||
| Atkinson | isentrópico | isocorico | isentrópico | isocorico | Difiere del ciclo de Otto en que V 1 < V 4. |
| Brayton | adiabático | isobárico | adiabático | isobárico | Estatorreactores, turborreactores, puntales y ejes. Originalmente desarrollado para su uso en motores alternativos. La versión de combustión externa de este ciclo se conoce como el primer ciclo Ericsson de 1833. |
| Diesel | adiabático | isobárico | adiabático | isocorico | Motor diesel |
| Humphrey | isentrópico | isocorico | isentrópico | isobárico | Shcramjets, motores de detonación pulsada y continua |
| Lenoir | isocorico | adiabático | isobárico | Chorros de pulso. Tenga en cuenta que 1→2 logra tanto el rechazo de calor como la compresión. Originalmente desarrollado para su uso en motores alternativos. | |
| Otón | isentrópico | isocorico | isentrópico | isocorico | Motores de gasolina / gasolina |
Cada proceso es uno de los siguientes:
- isotérmico (a temperatura constante, mantenido con calor agregado o eliminado de una fuente de calor o sumidero)
- isobárico (a presión constante)
- isométrico/isocórico (a volumen constante), también conocido como isovolumétrico
- adiabático (no se agrega ni elimina calor del sistema durante el proceso adiabático)
- isentrópico (proceso adiabático reversible, no se agrega ni elimina calor durante el proceso isentrópico)
Contenido relacionado
Infrasonido
Dispositivo de carga acoplada
Otto von Guericke


