Lothar Meyer
Julius Lothar Meyer (19 de agosto de 1830 – 11 de abril de 1895) fue un químico alemán. Fue uno de los pioneros en desarrollar las primeras versiones de la tabla periódica de elementos químicos. El químico ruso Dmitri Mendeleev (su principal rival) y él mismo habían trabajado con Robert Bunsen. Meyer nunca usó su primer nombre y fue conocido durante toda su vida simplemente como Lothar Meyer.
Carrera
Meyer nació en Varel, Alemania (entonces parte del Ducado de Oldenburg). Era hijo del médico Friedrich August Meyer y de Anna Biermann. Después de asistir al Altes Gymnasium de Oldenburg, estudió medicina en la Universidad de Zurich en 1851. Dos años más tarde, estudió patología en la Universidad de Würzburg como alumno de Rudolf Virchow. En Zurich, había estudiado con Carl Ludwig, lo que le impulsó a dedicar su atención a la química fisiológica. Después de graduarse como Doctor en Medicina en Würzburg en 1854, fue a la Universidad de Heidelberg, donde Robert Bunsen ocupaba la cátedra de química. En 1858, recibió un doctorado. en química por la Universidad de Breslau con una tesis sobre los efectos del monóxido de carbono en la sangre. Con este interés por la fisiología de la respiración, reconoció que el oxígeno se combina con la hemoglobina en la sangre.
Influenciado por la enseñanza matemática de Gustav Kirchhoff, comenzó a estudiar física matemática en la Universidad de Königsberg con Franz Ernst Neumann y en 1859, después de haber recibido su habilitation (certificado para la enseñanza universitaria), se convirtió en Privatdozent. en física y química en la Universidad de Breslau. En 1866, Meyer aceptó un puesto en la Academia Forestal de Eberswalde en Neustadt-Eberswalde, pero dos años más tarde fue nombrado profesor en el Politécnico de Karlsruhe.
En 1872, Meyer fue el primero en sugerir que los seis átomos de carbono en el anillo de benceno (que había sido propuesto unos años antes por August Kekulé) estaban interconectados únicamente por enlaces simples, estando dirigida la cuarta valencia de cada átomo de carbono. hacia el interior del anillo.
Durante la guerra franco-prusiana, el Politécnico se utilizó como hospital y Meyer participó activamente en el cuidado de los heridos. En 1876, Meyer se convirtió en profesor de química en la Universidad de Tubinga, donde ocupó hasta su muerte por un derrame cerebral el 11 de abril de 1895 a la edad de 64 años.
Tabla periódica
Meyer es mejor conocido por su papel en la clasificación periódica de los elementos. Observó, como lo hizo John A. R. Newlands en Inglaterra, que si los elementos se ordenaban según sus pesos atómicos, caían en grupos de propiedades químicas y físicas similares que se repetían a intervalos periódicos. Según él, si los pesos atómicos se representaban en ordenadas y los volúmenes atómicos en abscisas, la curva obtenía una serie de máximos y mínimos, y los elementos más electropositivos aparecían en los picos de la curva en el orden de sus pesos atómicos.

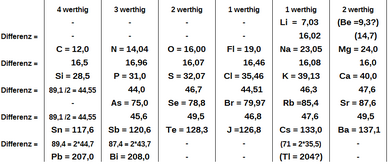
Su libro, Die modernen Theorien der Chemie, que comenzó a escribir en Breslau en 1862 y que se publicó dos años después, contenía una versión temprana de la tabla periódica que contenía 28 elementos, clasificados en seis familias por su valencia; por primera vez, los elementos se habían agrupado según su valencia. Los trabajos sobre organización de los elementos por peso atómico, hasta entonces, se habían visto obstaculizados por el uso generalizado de pesos equivalentes para los elementos, en lugar de pesos atómicos.
Publicó artículos sobre la tabla de clasificación de los elementos en forma horizontal (1864) y forma vertical (1870), en los que la serie de períodos termina propiamente con un elemento del grupo de los metales alcalinotérreos.
Mesa de Meyer, 1864
| Valence IV | Valence III | Valence II | Valence I | Valence I | Valence II | Diferencia masiva | |
| I row | Li | Be | ~16 | ||||
| II filas | C | N | O | F | Na | Mg | ~16 |
| III filas | Si | P | S | Cl | K | Ca | ~45 |
| IV. | As | Se | Br | Rb | Sr | ~45 | |
| V fila | Sn | Sb | Te | I | Cs | Ba | ~90 |
| VI fila | Pb | Bi | Tl | ~90 |
Mesa de Meyer, 1870
En 1869, Dmitri Mendeleev publicó una tabla periódica de todos los elementos conocidos en ese momento (más tarde predijo varios elementos nuevos para completar la tabla y corrigió algunos pesos atómicos). Unos meses más tarde, Meyer publicó un artículo que incluía una versión revisada de su tabla de 1864 que ahora incluía prácticamente todos los elementos conocidos, que era similar a la tabla publicada por Mendeleev:
| I | II | III | IV | V | VI | VII | VIII | IX |
| B | Al | ? In† † {displaystyle ^{dagger} | Tl | |||||
| C | Si | Ti | Zr | Sn | Pb | |||
| N | P | V | As | Nb | Sb | Ta | Bi | |
| O | S | Cr | Se | Mo | Те | W | ||
| F | Cl | Mn Fe Co Ni | Br | Ru Rh Pd | I | Os Ir Pt | ||
| Li | Na | K | Cu | Rb | Ag | Cs | Au | |
| ? Be† † {displaystyle ^{dagger} | Mg | Ca | Zn | Sr | Cd | Ba | Hg | |
| † † {displaystyle ^{dagger} Las marcas indican que los pesos atómicos fueron conjeturados sobre la base de los pesos equivalentes. | ||||||||
Meyer había desarrollado su tabla periódica completa de forma independiente, pero reconoció la prioridad de Mendeleev. En el artículo de Meyer se incluía un gráfico de líneas de volúmenes atómicos en función de los pesos atómicos, que mostraba gráficamente la periodicidad de los elementos. Al igual que Mendeleev, también incluyó predicciones de elementos futuros, pero a diferencia de Mendeleev no enfatizó estas predicciones ni sugirió detalles de las propiedades físicas y químicas de los elementos futuros.
En 1882, tanto Meyer como Mendeleev recibieron la Medalla Davy de la Royal Society en reconocimiento a su trabajo sobre la Ley Periódica.
El mineral lotermeyerita, CaZn2(AsO4)2 · 2H2O, fue descubierto en 1983 y nombrado en reconocimiento al trabajo de Meyer sobre la Ley Periódica. La localidad tipo es la mina Ojuela, Mapimí, Durango, México. Desde 1983 se han descrito cuatro minerales estrechamente relacionados: ferrilotarmeyerita (1992); cobaltolotarmeyerita (1997); níquellotarmeyerita (1999); y manganlotarmeyerita (2002).
Vida personal
Meyer se casó con Johanna Volkmann en 1866.
Homenaje
El 19 de agosto de 2020, Google celebró su 190.º cumpleaños con un Google Doodle.
Contenido relacionado
Selenocisteína
Estados de la materia
Svante Arrhenius
Plasma (física)
Materia
