Ley de Frank-Starling
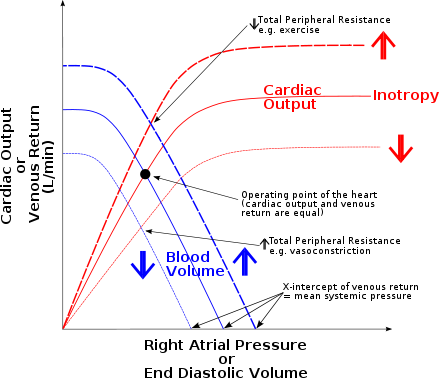
La ley de Frank-Starling del corazón (también conocida como ley de Starling y el mecanismo de Frank-Starling) representa la relación entre el volumen sistólico y el volumen diastólico final. La ley establece que el volumen sistólico del corazón aumenta en respuesta a un aumento en el volumen de sangre en los ventrículos, antes de la contracción (el volumen diastólico final), cuando todos los demás factores permanecen constantes. A medida que fluye un mayor volumen de sangre hacia el ventrículo, la sangre estira el músculo cardíaco, lo que provoca un aumento en la fuerza de contracción. El mecanismo de Frank-Starling permite sincronizar el gasto cardíaco con el retorno venoso, el riego sanguíneo arterial y la longitud humoral, sin depender de regulación externa para realizar alteraciones. La importancia fisiológica del mecanismo radica principalmente en mantener la igualdad del gasto ventricular izquierdo y derecho.
Fisiología
El mecanismo de Frank-Starling se produce como resultado de la relación longitud-tensión observada en el músculo estriado, incluidos, por ejemplo, los músculos esqueléticos, los músculos artrópodos y el músculo cardíaco (corazón). A medida que se estira el músculo estriado, se crea tensión activa al alterar la superposición de filamentos gruesos y delgados. La mayor tensión isométrica activa se desarrolla cuando un músculo tiene su longitud óptima. En la mayoría de las fibras del músculo esquelético relajadas, las propiedades elásticas pasivas mantienen la longitud de las fibras musculares cerca de la óptima, determinada generalmente por la distancia fija entre los puntos de unión de los tendones a los huesos (o el exoesqueleto de los artrópodos) en cada extremo del músculo. Por el contrario, la longitud relajada del sarcómero de las células del músculo cardíaco, en un ventrículo en reposo, es inferior a la longitud óptima para la contracción. No hay hueso para fijar la longitud del sarcómero en el corazón (de ningún animal), por lo que la longitud del sarcómero es muy variable y depende directamente del llenado de sangre y, por tanto, de la expansión de las cámaras del corazón. En el corazón humano, la fuerza máxima se genera con una longitud inicial del sarcómero de 2,2 micrómetros, una longitud que rara vez se supera en un corazón normal. Longitudes iniciales mayores o menores que este valor óptimo disminuirán la fuerza que el músculo puede alcanzar. Para longitudes de sarcómero más largas, esto es el resultado de que hay menos superposición de los filamentos finos y gruesos; para longitudes de sarcómero más cortas, la causa es la disminución de la sensibilidad al calcio por parte de los miofilamentos. Un aumento en el llenado del ventrículo aumenta la carga experimentada por cada célula del músculo cardíaco, estirando sus sarcómeros hacia su longitud óptima.
El estiramiento de los sarcómeros aumenta la contracción del músculo cardíaco al aumentar la sensibilidad al calcio de las miofibrillas, lo que provoca que se forme una mayor cantidad de puentes cruzados de actina-miosina dentro del músculo. Específicamente, la sensibilidad de la troponina para unirse al Ca2+ aumenta y hay una mayor liberación de Ca2+ desde el retículo sarcoplásmico. Además, el estiramiento de los miocitos cardíacos aumenta la capacidad de liberación de Ca2+ del almacén interno, el retículo sarcoplásmico, como lo demuestra un aumento en la velocidad de chispa de Ca2+ en el eje axial. tramo de miocitos cardíacos únicos. Finalmente, se cree que hay una disminución en el espacio entre los filamentos gruesos y delgados cuando se estira un músculo cardíaco, lo que permite que se forme un mayor número de puentes cruzados. La fuerza que genera cualquier célula del músculo cardíaco está relacionada con la longitud del sarcómero en el momento de la activación de las células musculares por el calcio. El estiramiento de cada célula, causado por el llenado ventricular, determina la longitud del sarcómero de las fibras. Por lo tanto, la fuerza (presión) generada por las fibras del músculo cardíaco está relacionada con el volumen telediastólico de los ventrículos izquierdo y derecho, según lo determinado por las complejidades de la relación fuerza-longitud del sarcómero.
Debido a la propiedad intrínseca del miocardio que es responsable del mecanismo de Frank-Starling, el corazón puede acomodar automáticamente un aumento en el retorno venoso, a cualquier frecuencia cardíaca. El mecanismo es de importancia funcional porque sirve para adaptar el gasto del ventrículo izquierdo al gasto del ventrículo derecho. Si este mecanismo no existiera y los gastos cardíacos derecho e izquierdo no fueran equivalentes, la sangre se acumularía en la circulación pulmonar (si el ventrículo derecho produjera más gasto que el izquierdo) o en la circulación sistémica (si el ventrículo izquierdo produjera más gasto que el izquierdo). bien).
Ejemplos clínicos
Contracción ventricular prematura
La contracción ventricular prematura provoca el vaciado temprano del ventrículo izquierdo (VI) hacia la aorta. Dado que la siguiente contracción ventricular ocurre en el momento habitual, el tiempo de llenado del VI aumenta, lo que provoca un aumento del volumen telediastólico del VI. Debido al mecanismo de Frank-Starling, la siguiente contracción ventricular es más intensa, lo que provoca la expulsión de un volumen de sangre mayor de lo normal y hace que el volumen telesistólico del VI vuelva al valor inicial.
Disfunción diastólica – insuficiencia cardíaca
La disfunción diastólica se asocia con una distensibilidad reducida o una mayor rigidez de la pared del ventrículo. Esta distensibilidad reducida da como resultado un llenado inadecuado del ventrículo y una disminución del volumen telediastólico. La disminución del volumen telediastólico conduce a una reducción del volumen sistólico debido al mecanismo de Frank-Starling.
Historia
La ley de Frank-Starling lleva el nombre de los dos fisiólogos, Otto Frank y Ernest Henry Starling. Sin embargo, ni Frank ni Starling fueron los primeros en describir la relación entre el volumen telediastólico y la regulación del gasto cardíaco. La primera formulación de la ley fue teorizada por el fisiólogo italiano Dario Maestrini, quien el 13 de diciembre de 1914 inició el primero de 19 experimentos que lo llevaron a formular la "legge del cuore" .
Las contribuciones de Otto Frank se derivan de sus experimentos de 1895 con corazones de rana. Para relacionar el trabajo del corazón con la mecánica del músculo esquelético, Frank observó cambios en la presión diastólica con volúmenes variables del ventrículo de rana. Sus datos fueron analizados en un diagrama de presión-volumen, lo que resultó en su descripción de la presión isovolumétrica máxima y sus efectos sobre el volumen ventricular.
Starling experimentó con corazones intactos de mamíferos, como los de perros, para comprender por qué las variaciones en la presión arterial, la frecuencia cardíaca y la temperatura no afectan el gasto cardíaco relativamente constante. Más de 30 años antes del desarrollo del modelo de contracción muscular de filamentos deslizantes y de la comprensión de la relación entre la tensión activa y la longitud del sarcómero, Starling planteó la hipótesis en 1914: "la energía mecánica liberada en el paso del estado de reposo al estado de reposo" El estado activo es función de la longitud de la fibra." Starling utilizó un diagrama volumen-presión para construir un diagrama longitud-tensión a partir de sus datos. Los datos de Starling y los diagramas asociados proporcionaron evidencia de que la longitud de las fibras musculares y la tensión resultante alteraban la presión sistólica.