Klebsiella pneumoniae
klebsiella pneumoniae es una bacteria gramnegativa, no motil, encapsulada, fermentada de lactosa, anaeróbica facultativa, en forma de varilla. Aparece como un fermentador de lactosa mucoide en el agar MacConkey.
Aunque se encuentra en la flora normal de la boca, la piel y los intestinos, puede causar cambios destructivos en los pulmones humanos y animales si se aspiran, específicamente a los alvéolos, lo que da como resultado un esputo de gelatina de color sangriento, parduzco o amarillo. En el entorno clínico, es el miembro más significativo del género Klebsiella de las enterobacteriaceae. k. oxytoca y k. Rhinoscleromatis también se han demostrado en muestras clínicas humanas. En los últimos años, las especies Klebsiella se han convertido en patógenos importantes en las infecciones nosocomiales.
ocurre naturalmente en el suelo, y aproximadamente el 30% de las cepas pueden fijar el nitrógeno en condiciones anaeróbicas. Como diazótrofo de vida libre, su sistema de fijación de nitrógeno ha sido muy estudiado y es de interés agrícola, como k. Se ha demostrado que las pneumoniae aumentan los rendimientos de los cultivos en condiciones agrícolas.
Está estrechamente relacionado con K. oxytoca de la que se distingue por ser indol-negativo y por su capacidad de crecer sobre melecitosa pero no sobre 3-hidroxibutirato.
Historia
El género Klebsiella lleva el nombre del microbiólogo alemán Edwin Klebs (1834-1913). También se le conoce como bacilo de Friedlander en honor a Carl Friedländer, un patólogo alemán, quien propuso que esta bacteria era el factor etiológico de la neumonía que se observa especialmente en personas inmunocomprometidas, como personas con enfermedades crónicas o alcohólicos.
La neumonía adquirida en la comunidad causada por Klebsiella pneumoniae puede en ocasiones denominarse neumonía de Friedländer.
Epidemiología
Las enfermedades afectan más comúnmente a hombres de mediana edad y mayores que a mujeres con enfermedades debilitantes. Se cree que esta población de pacientes tiene deterioro de las defensas respiratorias del huésped, incluidas personas con diabetes, alcoholismo, enfermedades malignas, enfermedades hepáticas, enfermedades pulmonares obstructivas crónicas, terapia con glucocorticoides, insuficiencia renal y ciertas exposiciones ocupacionales (como los trabajadores de las fábricas de papel). Muchas de estas infecciones se contraen cuando una persona está en el hospital por algún otro motivo (una infección nosocomial).
Además de la neumonía, Klebsiella también puede causar infecciones en el tracto urinario, el tracto biliar inferior y los sitios de heridas quirúrgicas. El rango de enfermedades clínicas incluye neumonía, tromboflebitis, infección del tracto urinario, colecistitis, diarrea, infección del tracto respiratorio superior, infección por heridas, osteomielitis, meningitis y bacteriemia y sepsis. Para los pacientes con un dispositivo invasivo en sus cuerpos, la contaminación del dispositivo se convierte en un riesgo; Los dispositivos de barrio neonatal, el equipo de apoyo respiratorio y los catéteres urinarios ponen a los pacientes en mayor riesgo. Además, el uso de antibióticos puede ser un factor que aumenta el riesgo de infección nosocomial con Klebsiella bacterias. La sepsis y el shock séptico pueden seguir la entrada de la bacteria en la sangre.
Investigación realizada en King ' S College, Londres, ha implicado la mimetismo molecular entre HLA-B27 y dos Klebsiella moléculas de superficie como la causa de la espondilitis anquilosante.
klebsiella ocupa el segundo lugar en e. coli para infecciones del tracto urinario en personas mayores. También es un patógeno oportunista para pacientes con enfermedad pulmonar crónica, patogenicidad entérica, atrofia de mucosa nasal y rinoescleroma. Nuevas cepas resistentes a los antibióticos de k. Pneumoniae están apareciendo.
Klebsiella pneumonia
La afección más común causada por la bacteria Klebsiella fuera del hospital es la neumonía, generalmente en forma de bronconeumonía y también bronquitis. Estos pacientes tienen una mayor tendencia a desarrollar abscesos pulmonares, cavitación, empiema y adherencias pleurales. Tiene una tasa de mortalidad de alrededor del 50%, incluso con terapia antimicrobiana.
Fisiopatología
Por lo general, se debe a la aspiración y el alcoholismo puede ser un factor de riesgo, aunque también está comúnmente implicado en infecciones del tracto urinario adquiridas en el hospital y en personas con EPOC (enfermedad pulmonar obstructiva crónica). En términos de la fisiopatología de la neumonía por Klebsiella, la defensa mieloperoxidasa de los neutrófilos contra K. pneumoniae se observa a menudo. Está implicada la inactivación oxidativa de la elastasa, mientras que la LBP ayuda a transferir elementos de la pared celular de las bacterias a las células.
Signos y síntomas
Las personas con Klebsiella pneumoniae tienden a toser un esputo característico, además de tener fiebre, náuseas, taquicardia y vómitos. Klebsiella pneumoniae tiende a afectar a personas con enfermedades subyacentes, como el alcoholismo.
Diagnóstico
En términos del diagnóstico de Klebsiella pneumoniae, se puede hacer lo siguiente para determinar si el individuo tiene esta infección, además de pruebas de susceptibilidad para identificar organismos resistentes a los medicamentos:
- Cultura sanguínea
- CBC
- Sputum(cultura)
- Radiografía(estar)
- TC
Tratamiento
El tratamiento para Klebsiella pneumoniae consiste en antibióticos como aminoglucósidos, pipercilina, tazobactam y cefalosporinas; la elección depende de las pruebas de susceptibilidad a los antibióticos, el estado de salud de la persona, el historial médico y la gravedad de la enfermedad. enfermedad.

Klebsiella posee beta-lactamasa que le da resistencia a la ampicilina, muchas cepas han adquirido una beta-lactamasa de espectro extendido con resistencia adicional a la carbenicilina, amoxicilina y ceftazidima. Las bacterias siguen siendo susceptibles a los aminoglucósidos y algunas cefalosporinas, y se han informado diversos grados de inhibición de la beta-lactamasa con ácido clavulánico. Las infecciones debidas a patógenos gramnegativos resistentes a múltiples fármacos en la UCI han provocado el resurgimiento de la colistina. Sin embargo, las cepas de K. pneumoniae se han notificado en las UCI. En 2009, cepas de K. pneumoniae con un gen llamado metalobetalactamasa de Nueva Delhi (NDM-1), que incluso confiere resistencia al antibiótico intravenoso carbapenem, fueron descubiertos en India y Pakistán. Los casos de Klebsiella en Taiwán han mostrado una toxicidad anormal, causando abscesos hepáticos en personas con diabetes mellitus (DM); El tratamiento consiste en cefalosporinas de tercera generación.
Neumonía hipervirulenta por Klebsiella
La hipervirulenta (hvKp) es una variante de K pneumoniae bastante reciente que es significativamente más virulenta que la K clásica. pneumoniae (cKp). Si bien cKp es un patógeno oportunista responsable de infecciones nosocomiales que generalmente afectan a pacientes inmunocomprometidos, hvKp es clínicamente más preocupante ya que también causa enfermedades en individuos sanos y puede infectar prácticamente todas las partes del cuerpo. Los rasgos genéticos que conducen a este patotipo están incluidos en un plásmido de gran virulencia y potencialmente en elementos conjugativos adicionales.
Se describió que estas cepas recientemente identificadas producen en exceso componentes de la cápsula y sideróforos para la adquisición de hierro, entre otros factores. Aunque los estudios iniciales demostraron que hvKp es bastante susceptible al tratamiento con antibióticos, recientemente se ha demostrado que dichas cepas pueden adquirir plásmidos de resistencia y volverse multirresistentes a una variedad de antibióticos.
Es originaria de Asia, teniendo una alta tasa de mortalidad entre la población. A menudo se propaga al sistema nervioso central y a los ojos causando endoftalmitis, abscesos no hepáticos, neumonía, fascitis necrotizante y meningitis. Un rasgo visual de estas cepas es el fenotipo hipermucoviscoso y se puede utilizar una prueba de cuerda para ayudar al diagnóstico. Los exámenes y tratamientos adicionales se realizan caso por caso, ya que actualmente no existen directrices internacionales.
Transmisión
Para obtener una K. pneumoniae, la persona debe estar expuesta a la bacteria. En otras palabras, K. pneumoniae debe ingresar al tracto respiratorio para causar neumonía, o a la sangre para causar una infección del torrente sanguíneo. En entornos sanitarios, K. La bacteria pneumoniae se puede transmitir a través del contacto de persona a persona (por ejemplo, manos contaminadas del personal sanitario u otras personas, de paciente a paciente) o, menos comúnmente, por contaminación del medio ambiente; el papel de la transmisión directa del medio ambiente a los pacientes es controvertido y requiere más investigación. Sin embargo, las bacterias no se propagan por el aire. Los pacientes en entornos de atención médica también pueden estar expuestos al K. pneumoniae cuando están conectados a ventiladores, o tienen catéteres intravenosos o heridas. Estas herramientas y condiciones médicas pueden permitir que K. pneumoniae entre al cuerpo y cause infección.
Cepas resistentes
Klebsiella suelen ser resistentes a múltiples antibióticos. La evidencia actual implica a los plásmidos como la fuente principal de genes de resistencia. Las especies de Klebsiella con capacidad de producir betalactamasas de espectro extendido (BLEE) son resistentes a prácticamente todos los antibióticos betalactámicos, excepto a los carbapenémicos. Otros objetivos frecuentes de resistencia incluyen aminoglucósidos, fluoroquinolonas, tetraciclinas, cloranfenicol y trimetoprim/sulfametoxazol.

La infección por enterobacterias resistentes a carbapenems (CRE) o enterobacterias productoras de carbapenemasas está surgiendo como un desafío importante en los entornos de atención médica. Una de las muchas CRE es la Klebsiella pneumoniae resistente a los carbapenémicos (CRKP). Durante los últimos 10 años, se ha observado un aumento progresivo de CRKP en todo el mundo; sin embargo, este nuevo patógeno nosocomial emergente probablemente sea mejor conocido por un brote en Israel que comenzó alrededor de 2006 dentro del sistema de salud de ese país. En Estados Unidos, se describió por primera vez en Carolina del Norte en 1996; desde entonces, CRKP ha sido identificado en 41 estados; y se detecta de forma rutinaria en ciertos hospitales de Nueva York y Nueva Jersey. Ahora es la especie CRE más común que se encuentra en los Estados Unidos.
CRKP es resistente a casi todos los agentes antimicrobianos disponibles, y las infecciones por CRKP han causado altas tasas de morbilidad y mortalidad, en particular entre personas con hospitalizaciones prolongadas y aquellos críticamente enfermos y expuestos a dispositivos invasivos (p. ej., ventiladores o catéteres venosos centrales).). La preocupación es que el carbapenem se utiliza a menudo como fármaco de último recurso para combatir cepas bacterianas resistentes. Nuevas mutaciones leves podrían provocar infecciones para las cuales los profesionales de la salud pueden hacer muy poco o nada para tratar a los pacientes con organismos resistentes.
Varios mecanismos causan resistencia a los carbapenémicos en las enterobacterias. Estos incluyen hiperproducción de beta-lactamasa ampC con una mutación de porina de la membrana externa, beta-lactamasa de espectro extendido CTX-M con una mutación de porina o salida de fármaco y producción de carbapenemasas. El mecanismo de resistencia más importante de CRKP es la producción de una enzima carbapenemasa, blakpc. El gen que codifica la enzima blakpc se encuentra en una pieza móvil de material genético (un transposón; el transposón específico implicado se llama Tn4401), lo que aumenta el riesgo de diseminación. La CRE puede ser difícil de detectar porque algunas cepas que albergan blakpc tienen concentraciones inhibitorias mínimas elevadas, pero aún dentro del rango de susceptibilidad a los carbapenémicos. Debido a que estas cepas son susceptibles a los carbapenémicos, no se identifican como posibles riesgos clínicos o de control de infecciones mediante las pautas estándar de pruebas de susceptibilidad. Los pacientes con colonización CRKP no reconocida han sido reservorios de transmisión durante los brotes nosocomiales.
Actualmente se desconoce el alcance y la prevalencia de CRKP en el medio ambiente. La tasa de mortalidad también se desconoce, pero se ha observado que llega al 44%. Los Centros para el Control y la Prevención de Enfermedades publicaron una guía para un control agresivo de infecciones para combatir CRKP:
- Coloque todos los pacientes colonizados o infectados con Enterobacteriaceae productoras de carbapenemase en precauciones de contacto. Las instalaciones de atención aguda deben establecer un protocolo, junto con las directrices del Instituto de Normas Clínicas y Laboratorios, para detectar la no sostenibilidad y la producción de carbapenemasa en Enterobacteriaceae, en particular Klebsiella y Escherichia coli, y alertar inmediatamente a los funcionarios de epidemiología y control de infecciones si se identifica. Todas las instalaciones de atención aguda deben revisar los registros de microbiología correspondientes a los 6 a 12 meses anteriores para garantizar que no se hayan registrado casos de CRE previamente no reconocidos. Si identifican casos previamente no reconocidos, se necesita un estudio de prevalencia de puntos (una sola ronda de cultivos de vigilancia activa) en unidades con pacientes de alto riesgo (por ejemplo, unidades de cuidados intensivos, unidades en las que se han identificado casos anteriores, y unidades en las que muchos pacientes están expuestos a antimicrobianos de amplio espectro) para identificar pacientes adicionales colonizados con carbapenem resistentes o que producen carbapenemasa. Klebsiella y E. coli. Cuando se identifica un caso de CRE asociada al hospital, las instalaciones deben realizar una prueba de vigilancia activa de pacientes con vínculos epidemiológicos con el caso CRE (por ejemplo, aquellos pacientes de la misma unidad o pacientes atendidos por el mismo personal sanitario).
Brotes locales
Israel 2007-2008. Un brote nacional de CRE en Israel alcanzó su punto máximo en marzo de 2007 con 55,5 casos por 100.000 días-paciente y requirió un plan de tratamiento a nivel nacional. La intervención implicó la separación física de todos los transportistas de CRE y el nombramiento de un grupo de trabajo para supervisar la eficacia del aislamiento monitoreando de cerca los hospitales e interviniendo cuando fuera necesario. Después del plan de tratamiento (medido en mayo de 2008), el número de casos por 100.000 días-paciente disminuyó a 11,7. El plan fue efectivo debido al estricto cumplimiento hospitalario, en el que cada uno debía conservar documentación detallada de todos los transportistas de CRE. De hecho, por cada aumento del 10% en el cumplimiento, la incidencia de casos por 100.000 días-paciente disminuyó en 0,6. Por lo tanto, la contención a escala nacional requiere una intervención a nivel nacional.
Nevada 2016. A mediados de agosto de 2016, un residente del condado de Washoe fue hospitalizado en Reno debido a una infección por CRE (específicamente Klebsiella pneumoniae). A principios de septiembre del mismo año, sufrió un shock séptico y murió. En las pruebas realizadas por los CDC, se descubrió que un aislado del paciente era resistente a los 26 antibióticos disponibles en los EE. UU., incluido el fármaco de último recurso, la colistina. Se cree que pudo haber contraído el microbio mientras estuvo hospitalizada en la India durante dos años debido a una fractura del fémur derecho y posteriores infecciones de fémur y cadera.
Transferencia de genes de resistencia a los antimicrobianos
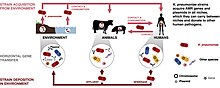
Klebsiella pneumoniae porta una gran cantidad de genes de resistencia a los antimicrobianos (genes AMR). Estos genes se transfieren a través de plásmidos desde y hacia otros patógenos humanos. Un patógeno humano que comúnmente adquiere genes de RAM de Klebsiella pneumoniae es Salmonella. Esto podría ayudar con el tratamiento de las infecciones por salmonella debido al conocimiento de posibles datos de resistencia a los antibióticos.
La mayoría de los genes de RAM en Klebsiella pneumoniae se transmiten por plásmidos. Un ejemplo de nicho sería el suelo, a menudo considerado un punto crítico para la transferencia de genes.
| Total de genes AMR por spp | Plasmides promedio | |
|---|---|---|
| Acinetobacter baumannii | 278 | 1,5 |
| Pseudomonas aeruginosa | 263 | 0 |
| Klebsiella pneumoniae | 410 | 2.5 |
| Enterobacter cloacae | 277 | 2.2 |
| Escherichia coli | 204 | 1 |
La tabla muestra el número de genes y plásmidos de RAM (por cepa o subespecie) en comparación con otras especies de bacterias comunes.
Prevención
Para evitar la propagación de infecciones por Klebsiella entre pacientes, el personal sanitario debe seguir precauciones específicas de control de infecciones, que pueden incluir un estricto cumplimiento de la higiene de manos (preferiblemente usar un desinfectante para manos a base de alcohol (60-90 %). o agua y jabón si las manos están visiblemente sucias (los desinfectantes para manos a base de alcohol son eficaces contra estos bacilos gramnegativos) y usar batas y guantes al ingresar a las habitaciones donde se alojan pacientes con enfermedades relacionadas con Klebsiella. Los centros sanitarios también deben seguir estrictos procedimientos de limpieza para evitar la propagación de Klebsiella.
Para prevenir la propagación de infecciones, los pacientes también deben lavarse las manos con mucha frecuencia, lo que incluye:
- Antes de preparar o comer alimentos
- Antes de tocar sus ojos, nariz o boca
- Antes y después de cambiar los vendajes o vendajes de la herida
- Después de usar el baño
- Después de soplar su nariz, tos o estornudos
- Después de tocar superficies hospitalarias como barandillas de cama, mesas de noche, porteros, controles remotos o el teléfono
Tratamiento
K. pneumoniae se puede tratar con antibióticos si las infecciones no son resistentes a los medicamentos. Infecciones por K. pneumoniae puede ser difícil de tratar porque hay menos antibióticos eficaces contra ellos. En tales casos, un laboratorio de microbiología debe realizar pruebas para determinar qué antibióticos tratarán la infección. En la sección anterior se proporcionan tratamientos más específicos de la neumonía por Klebsiella. Para las infecciones del tracto urinario por especies de Klebsiella resistentes a múltiples fármacos, se ha sugerido una terapia combinada con amikacina y meropenem.
Investigación
K. K resistente a múltiples fármacos. pneumoniae han sido eliminadas in vivo mediante la administración intraperitoneal, intravenosa o intranasal de fagos en pruebas de laboratorio. No es probable que la resistencia a los fagos sea tan problemática como a los antibióticos, ya que es probable que haya nuevos fagos infecciosos disponibles en los reservorios ambientales. La terapia con fagos se puede utilizar junto con antibióticos, para complementar su actividad en lugar de reemplazarla por completo.
Desarrollo de vacunas
Nuevas fuentes de datos que describen la carga global de K. pneumoniae y las formas resistentes a los medicamentos impulsen el desarrollo de vacunas profilácticas. El reciente estudio del IHME de 2022 mostró que en 2019 K. pneumoniae fue responsable de 790.000 muertes [571.000-1.060.000] en todos los grupos de edad en 11 síndromes infecciosos. Es importante destacar que en el África subsahariana K. pneumoniae fue responsable de 124.000 [89.000-167.000] muertes neonatales debido a infecciones del torrente sanguíneo. Con base en estos y otros datos, lo ideal sería diseñar una vacuna profiláctica recientemente desarrollada para prevenir la K invasiva. pneumoniae en personas vulnerables pero también como vacuna materna para prevenir la sepsis neonatal y se han publicado evaluaciones de la demanda global. A partir de junio de 2023, un único programa de desarrollo clínico para un K. pneumoniae [Kleb4V/GSK4429016A] estaba en un estudio de fase 1/2 en adultos sanos de 18 a 70 años (n=166) [Identificador de ensayos clínicos: NCT04959344]. La vacuna es un conjugado basado en antígeno O donde los antígenos O específicos de la vacuna no se revelan [Michael Kowarik, LimmaTech Biologics, World Vaccine Congress EU, 2022] aunque solo un número limitado de serotipos O puede representar una alta proporción de aislados clínicos.