Ketamina
Ketamina es un anestésico disociativo utilizado médicamente para la inducción y mantenimiento de la anestesia. También se utiliza como droga recreativa. La ketamina también es fácil de administrar y altamente tolerable en comparación con drogas con efectos similares que son inflamables, irritantes o incluso explosivas. La ketamina es un compuesto novedoso, derivado de PCP, creado en la búsqueda de un anestésico más seguro con características similares. La ketamina también se utiliza para el tratamiento del dolor agudo.
En dosis anestésicas, la ketamina induce un estado de "anestesia disociativa", un estado de trance que proporciona alivio del dolor, sedación y amnesia. Las características distintivas de la anestesia con ketamina son la respiración y los reflejos de las vías respiratorias preservados, la función cardíaca estimulada con aumento de la presión arterial y la broncodilatación moderada. En dosis subanestésicas más bajas, la ketamina es un agente prometedor para el dolor y la depresión resistente al tratamiento. Sin embargo, la acción antidepresiva de una sola administración de ketamina se desvanece con el tiempo. Los efectos a largo plazo del uso repetido son en gran parte desconocidos y son un área de investigación activa.
Se ha informado toxicidad hepática y urinaria entre usuarios habituales de altas dosis de ketamina con fines recreativos. La ketamina es un bloqueador de poros del receptor NMDA y eso explica la mayoría de sus acciones, excepto el efecto antidepresivo, cuyo mecanismo es un tema de mucha investigación y debate.
La ketamina se sintetizó por primera vez en 1962 y se aprobó para su uso en los Estados Unidos en 1970. Se ha utilizado regularmente en medicina veterinaria y se usó ampliamente para la anestesia quirúrgica en la Guerra de Vietnam. Cuando se usa como droga recreativa, se encuentra tanto en forma líquida como en polvo, y a menudo se la denomina "Special K" por sus efectos alucinógenos y disociativos. Junto con otras drogas psicotrópicas, se encuentra en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud. Está disponible como medicamento genérico.
Usos médicos
Anestesia
El uso de ketamina en anestesia refleja sus características. Es un fármaco de elección para procedimientos a corto plazo cuando no se requiere relajación muscular. El efecto de la ketamina en los sistemas respiratorio y circulatorio es diferente al de otros anestésicos. Suprime la respiración mucho menos que la mayoría de los otros anestésicos disponibles. Cuando se usa en dosis anestésicas, la ketamina generalmente estimula en lugar de deprimir el sistema circulatorio. Los reflejos protectores de las vías respiratorias se conservan y, en ocasiones, es posible administrar anestesia con ketamina sin medidas de protección de las vías respiratorias. Los efectos psicotomiméticos limitan la aceptación de la ketamina; sin embargo, la lamotrigina y la nimodipina disminuyen los efectos psicotomiméticos y pueden ser contrarrestados también por la administración de benzodiazepinas o propofol.
La ketamina se usa con frecuencia en personas gravemente heridas y parece ser segura en este grupo. Ha sido ampliamente utilizado para cirugía de emergencia en condiciones de campo en zonas de guerra, por ejemplo, durante la Guerra de Vietnam. Una guía de práctica clínica de 2011 respalda el uso de ketamina como sedante en medicina de emergencia, incluso durante procedimientos físicamente dolorosos. Es el fármaco de elección para las personas en shock traumático que corren riesgo de hipotensión. La presión arterial baja es peligrosa para las personas con lesiones graves en la cabeza y es poco probable que la ketamina disminuya la presión arterial; por el contrario, a menudo aumenta la presión arterial, por lo que a menudo es la más adecuada para las personas con lesiones graves en la cabeza.
La ketamina es una opción en niños, como único anestésico para procedimientos menores o como agente de inducción seguido de bloqueador neuromuscular e intubación traqueal. En particular, los niños con cardiopatía cianótica y trastornos neuromusculares son buenos candidatos para la anestesia con ketamina.
Debido a las propiedades broncodilatadoras de la ketamina, se puede usar para la anestesia en personas con asma, enfermedad obstructiva crónica de las vías respiratorias y enfermedad reactiva grave de las vías respiratorias, incluido el broncoespasmo activo.
Dolor
Las infusiones de ketamina se utilizan para el tratamiento del dolor agudo en los servicios de urgencias y en el período perioperatorio en personas con dolor refractario. Las dosis son más bajas que las utilizadas para la anestesia; por lo general se denominan dosis subanestésicas. Como complemento de la morfina o sola, la ketamina reduce el uso de morfina, el nivel de dolor, las náuseas y los vómitos después de la cirugía. Es probable que la ketamina sea más beneficiosa para los pacientes quirúrgicos cuando se espera un dolor posoperatorio intenso y para los pacientes tolerantes a los opioides.
La ketamina es especialmente útil en el ámbito prehospitalario, por su eficacia y bajo riesgo de depresión respiratoria. La ketamina tiene una eficacia similar a los opiáceos en un servicio de urgencias de un hospital para el tratamiento del dolor agudo y para el control del dolor relacionado con procedimientos. También puede prevenir la hiperalgesia inducida por opioides y los escalofríos posanestésicos.
Para el dolor crónico, la ketamina se usa como analgésico intravenoso, particularmente si el dolor es neuropático. Tiene el beneficio adicional de contrarrestar la sensibilización espinal o los fenómenos de cuerda que se experimentan con el dolor crónico. En múltiples ensayos clínicos, las infusiones de ketamina proporcionaron alivio del dolor a corto plazo en diagnósticos de dolor neuropático, dolor después de una lesión traumática de la columna, fibromialgia y síndrome de dolor regional complejo (SDRC). Sin embargo, las pautas de consenso de 2018 sobre el dolor crónico concluyeron que, en general, solo hay evidencia débil a favor del uso de ketamina en el dolor por lesiones espinales, evidencia moderada a favor de la ketamina para el SDRC y evidencia débil o nula a favor de la ketamina en el dolor neuropático mixto. fibromialgia y dolor por cáncer. En particular, solo para el SDRC hay evidencia de alivio del dolor a mediano y largo plazo.
Depresión
La ketamina es un antidepresivo robusto y de acción rápida, aunque su efecto es transitorio. La infusión intravenosa de ketamina en la depresión resistente al tratamiento puede mejorar el estado de ánimo en 4 horas y alcanzar el punto máximo a las 24 horas. Se ha demostrado que una dosis única de ketamina intravenosa da como resultado una tasa de respuesta superior al 60 % tan pronto como 4,5 horas después de la dosis (con un efecto sostenido después de 24 horas) y superior al 40 % después de 7 días. Aunque solo hay unos pocos estudios piloto que estudian la dosis óptima, la creciente evidencia sugiere que una dosis de 0,5 mg/kg inyectada durante 40 minutos brinda un resultado óptimo. El efecto antidepresivo de la ketamina disminuye a los 7 días y la mayoría de las personas recaen dentro de los 10 días, aunque para una minoría significativa la mejora puede durar 30 días o más. Uno de los principales desafíos del tratamiento con ketamina puede ser el tiempo que duran los efectos antidepresivos después de terminar un ciclo de tratamiento. Una posible opción puede ser la terapia de mantenimiento con ketamina, que generalmente se realiza de dos a una vez por semana. La ketamina puede disminuir los pensamientos suicidas hasta tres días después de la inyección.
Un enantiómero de ketamina, esketamina vendido comercialmente como Spravato, fue aprobado como antidepresivo por la Agencia Europea de Medicamentos en 2019. La esketamina fue aprobada como un aerosol nasal para el tratamiento -depresión resistente en los Estados Unidos y en otros lugares en 2019 (ver Esketamina y Depresión). La Red Canadiense de Tratamientos para el Estado de Ánimo y la Ansiedad (CANMAT) recomienda la esketamina como tratamiento de tercera línea para la depresión.
Una revisión Cochrane de ensayos controlados aleatorios en adultos con trastorno depresivo mayor unipolar encontró que, en comparación con el placebo, las personas tratadas con ketamina o esketamina experimentaron una reducción o remisión de los síntomas que duraron de 1 a 7 días. Hubo un 18,7 % (4,1 a 40,4 %) más de personas que informaron algún beneficio y un 9,6 % (0,2 a 39,4 %) más que lograron la remisión dentro de las 24 horas posteriores al tratamiento con ketamina. Entre las personas que recibieron esketamina, el 2,1 % (2,5 a 24,4 %) más experimentó algún alivio a las 24 horas y el 10,3 % (4,5 a 18,2 %) más tuvo pocos o ningún síntoma. Estos efectos no persistieron más allá de una semana, aunque una mayor tasa de abandonos en algunos estudios significa que la duración del beneficio aún no está clara.
La ketamina puede mejorar parcialmente los síntomas depresivos entre las personas con depresión bipolar, 24 horas después del tratamiento, pero no 3 o más días. Potencialmente, 10 personas más con depresión bipolar de cada 1000 pueden experimentar una breve mejoría, pero no el cese de los síntomas, un día después del tratamiento. Estas estimaciones se basan en investigaciones limitadas disponibles.
En febrero de 2022, la Administración de Alimentos y Medicamentos de EE. UU. emitió una alerta para los profesionales de la salud sobre los productos de aerosol nasal compuestos que contienen ketamina destinados a tratar la depresión: "No existe un producto de aerosol nasal de ketamina aprobado por la FDA. Los medicamentos compuestos no están aprobados por la FDA, lo que significa que la FDA no ha evaluado su seguridad, eficacia o calidad antes de su comercialización."
Experiencia cercana a la muerte
La mayoría de las personas que pudieron recordar sus sueños durante la anestesia con ketamina informan experiencias cercanas a la muerte (ECM) cuando se utiliza la definición más amplia posible de ECM. La ketamina puede reproducir características que comúnmente se han asociado con las ECM. Un estudio a gran escala de 2019 encontró que los informes escritos de experiencias con ketamina tenían un alto grado de similitud con los informes escritos de ECM en comparación con otros informes escritos de experiencias con drogas.
Convulsiones
La ketamina se usa para tratar el estado epiléptico que no ha respondido a los tratamientos estándar, pero solo los estudios de casos y ningún ensayo controlado aleatorio respaldan su uso.
Contraindicaciones
Principales contraindicaciones de la ketamina:
- Enfermedad cardiovascular severa como angina inestable o hipertensión mal controlada
- Aumento de la presión intracraneal o intraocular. Ambas contraindicaciones son polémicas
- Psicosis mal controlada
- Enfermedad hepática grave como la cirrosis
- Embarazo
- Trastorno de uso de sustancias activas (para inyecciones de ketamina en serie)
- Edad inferior a 3 meses
Efectos secundarios
Con dosis anestésicas, del 10 al 20 % de los adultos (1 al 2 % de los niños) experimentan reacciones psiquiátricas adversas que ocurren durante la salida de la anestesia, que van desde sueños y disforia hasta alucinaciones y delirio de emergencia. Los efectos psicotomiméticos disminuyen al agregar lamotrigina y nimodipina y pueden contrarrestarse con un pretratamiento con una benzodiazepina o propofol. La anestesia con ketamina comúnmente causa movimientos tónico-clónicos (más del 10% de las personas) y rara vez hipertonía. Se pueden esperar vómitos en 5 a 15% de los pacientes; el pretratamiento con propofol también lo mitiga. El laringoespasmo ocurre raramente con ketamina. La ketamina, por lo general, estimula la respiración; sin embargo, en los primeros 2 a 3 minutos de una inyección intravenosa rápida de dosis alta puede causar una depresión respiratoria transitoria.
A dosis subanestésicas más bajas, los efectos secundarios psiquiátricos son prominentes. La mayoría de las personas se sienten extrañas, aturdidas, mareadas o con una sensación de flotar, o tienen distorsiones visuales o entumecimiento. También son muy frecuentes (20-50%) la dificultad para hablar, la confusión, la euforia, la somnolencia y la dificultad para concentrarse. Los síntomas de la psicosis, como meterse en un agujero, desaparecer, sentirse como si se derritiera, experimentar colores y alucinaciones, son descritos por el 6-10% de las personas. Los efectos secundarios no psiquiátricos comunes (>10%) son mareos, visión borrosa, sequedad de boca, hipertensión, náuseas, aumento o disminución de la temperatura corporal o sensación de rubor. Todos estos efectos adversos son más pronunciados al final de la inyección, se reducen drásticamente 40 minutos después y desaparecen por completo dentro de las 4 horas posteriores a la inyección.
Toxicidad urinaria y hepática
La toxicidad urinaria ocurre principalmente en personas que consumen grandes cantidades de ketamina de manera rutinaria, y entre el 20 y el 30 % de los usuarios frecuentes tienen molestias en la vejiga. Incluye una variedad de trastornos, desde cistitis hasta hidronefrosis e insuficiencia renal. Los síntomas típicos de la cistitis inducida por ketamina son micción frecuente, disuria y urgencia urinaria, a veces acompañada de dolor al orinar y sangre en la orina. El daño a la pared de la vejiga tiene similitudes con la cistitis intersticial y eosinofílica. La pared está engrosada y la capacidad funcional de la vejiga es tan baja como 10 a 150 ml.
El tratamiento de la cistitis inducida por ketamina implica el cese de la ketamina como primer paso. Le siguen los AINE y los anticolinérgicos y, si la respuesta es insuficiente, el tramadol. Los tratamientos de segunda línea son los agentes protectores del epitelio, como el polisulfato de pentosano oral o la instilación intravesical (intravejiga) de ácido hialurónico. La toxina botulínica intravesical también es útil.
La toxicidad hepática de la ketamina implica dosis más altas y administración repetida. En un grupo de usuarios crónicos de altas dosis de ketamina, se informó que la frecuencia de daño hepático era de alrededor del 10 %. Hay informes de casos de aumento de las enzimas hepáticas que involucran el tratamiento con ketamina del dolor crónico.
Dependencia y tolerancia
Aunque se desconoce la incidencia de la dependencia a la ketamina, algunas personas que consumen ketamina regularmente desarrollan dependencia a la ketamina. Los experimentos con animales también confirman el riesgo de mal uso. Además, el rápido inicio de los efectos después de la insuflación puede aumentar el uso potencial como droga recreativa. La corta duración de los efectos promueve los atracones. La tolerancia a la ketamina se desarrolla rápidamente, incluso con el uso médico repetido, lo que lleva al uso de dosis más altas. Algunos usuarios diarios reportaron síntomas de abstinencia, principalmente ansiedad, temblores, sudoración y palpitaciones, luego de los intentos de parar. Se observaron déficits cognitivos, así como un aumento de los síntomas de disociación y delirio en los usuarios recreativos frecuentes de ketamina.
Interacciones
La ketamina potencia los efectos sedantes del propofol y el midazolam. La naltrexona potencia los efectos psicotomiméticos de una dosis baja de ketamina, mientras que la lamotrigina y la nimodipina los disminuyen. La clonidina reduce el aumento de la salivación, el ritmo cardíaco y la presión arterial durante la anestesia con ketamina y disminuye la incidencia de pesadillas.
Las observaciones clínicas sugieren que las benzodiazepinas pueden disminuir los efectos antidepresivos de la ketamina. Parece que la mayoría de los antidepresivos convencionales se pueden combinar de forma segura con la ketamina.
Farmacología
Farmacodinámica
Mecanismo de acción
El bloqueo de poros del receptor NMDA es responsable de los efectos anestésicos, analgésicos y psicotomiméticos de la ketamina. El bloqueo del receptor NMDA produce analgesia al prevenir la sensibilización central en las neuronas del asta dorsal; en otras palabras, las acciones de la ketamina interfieren con la transmisión del dolor en la médula espinal.
El mecanismo de acción de la ketamina para aliviar la depresión no se comprende bien y es un área de investigación activa. Los posibles mecanismos incluyen la acción directa sobre el receptor NMDA, los efectos posteriores sobre los reguladores como BDNF y mTOR, y los efectos de los metabolitos de la ketamina, como la hidroxinorketamina. No está claro si el receptor NMDA es el único responsable de esta acción o si también son necesarias las interacciones con otros receptores. Tampoco está claro si la ketamina sola es suficiente para la acción antidepresiva o si sus metabolitos también son importantes. En cualquier caso, se ha aclarado que el bloqueo agudo de los receptores NMDA en el cerebro resulta en una activación de los receptores del ácido α-amino-3-hidroxi-5-metil-4-isoxazolpropiónico (receptores AMPA), que a su vez modulan una variedad de las vías de señalización aguas abajo para influir en la neurotransmisión en el sistema límbico y mediar los efectos antidepresivos de los antagonistas de los receptores NMDA como la ketamina. Tales acciones aguas abajo de esta activación de los receptores AMPA incluyen la regulación positiva del factor neurotrófico derivado del cerebro (BDNF) y la activación de su receptor de señalización, el receptor de tropomiosina quinasa B (TrkB), la activación de la vía del objetivo de la rapamicina en mamíferos (mTOR), la desactivación de la glucógeno sintasa quinasa 3 (GSK-3), e inhibición de la fosforilación de la quinasa del factor de elongación eucariota 2 (eEF2). Además del bloqueo del receptor NMDA, el metabolito activo de la ketamina hidroxinorketamina, que no interactúa de manera importante con el receptor NMDA, pero que, sin embargo, activa indirectamente los receptores AMPA de manera similar, también puede o alternativamente estar involucrado en los efectos antidepresivos de inicio rápido de la ketamina. Investigaciones recientes han aclarado que una inhibición aguda de la habénula lateral, una parte del cerebro en el sistema límbico que se conoce como el "centro anti-recompensa" (proyectando e inhibiendo la vía de recompensa mesolímbica y modulando otras áreas límbicas), pueden estar involucrados en los efectos antidepresivos de la ketamina.
La ketamina es una mezcla de cantidades iguales de dos enantiómeros: esketamina y arketamina. La esketamina es un bloqueador de poros del receptor NMDA más potente y un alucinógeno disociativo que la arketamina. Debido a la hipótesis de que el antagonismo del receptor NMDA es la base de los efectos antidepresivos de la ketamina, se desarrolló la esketamina como antidepresivo. Sin embargo, muchos otros antagonistas de los receptores de NMDA, incluidos memantina, lanicemina, rislenemdaz, rapastinel y 4-cloroquinurenina, hasta el momento no han logrado demostrar suficiente eficacia para la depresión. Además, la investigación en animales indica que la arketamina, el enantiómero con un antagonismo más débil del receptor NMDA, así como la (2R,6R)-hidroxinorketamina, el metabolito con una afinidad insignificante por el receptor NMDA, pero un potente antagonista del receptor nicotínico alfa-7, pueden tener efectos antidepresivos. acción. Ahora se argumenta que el antagonismo del receptor NMDA puede no ser el principal responsable de los efectos antidepresivos de la ketamina.
Blancos moleculares
| Sitio | Valor (μM) | Tipo | Medida | Especies | Ref. |
|---|---|---|---|---|---|
| NMDA | 0,25–0,66 | Ki | Antagonista | Human | |
| MOR | 42 | Ki | Antagonista | Human | |
| MOR2 | 12.1 | Ki | Antagonista | Human | |
| KOR | 28 25 | Ki Ki | Antagonista Agonista | Human | |
| σ2 | 26 | Ki | ND | Rat | |
| D2 | 0.5 ■10 | Ki Ki | Agonista ND | Human | |
| M1 | 45 | Ki | ND | Human | |
| α2β2 | 92 | IC50 | Antagonista | Human | |
| α2β4 | 29 | IC50 | Antagonista | Human | |
| α3β2 | 50 | IC50 | Antagonista | Human | |
| α3β4 | 9.5 | IC50 | Antagonista | Human | |
| α4β2 | 72 | IC50 | Antagonista | Human | |
| α4β4 | 18 | IC50 | Antagonista | Human | |
| α7 | 3.1 | IC50 | Antagonista | Rat | |
| ERα | 0.34 | Ki | ND | Human | |
| NET | 82–291 | IC50 | Inhibidor | Human | |
| DAT | 63 | Ki | Inhibidor | Rat | |
| HCN1 | 8 a 16 | CE50 | Inhibidor | Mouse | |
| TRPV1 | 1-100 | Ki | Agonista | Rat | |
| Cuanto menor sea el valor, más fuerte será la interacción con el sitio. | |||||
La ketamina actúa principalmente como bloqueador de poros del receptor NMDA, un receptor de glutamato ionotrópico. Los estereoisómeros S(+) y R(–) de la ketamina se unen al sitio de dizocilpina del receptor NMDA con diferentes afinidades, mostrando el primero aproximadamente 3 a 4 veces mayor afinidad por el receptor que este último. Como resultado, el isómero S es un anestésico y analgésico más potente que su contraparte R.
La ketamina puede interactuar e inhibir el NMDAR a través de otro sitio alostérico en el receptor.
Con un par de excepciones, las acciones de la ketamina en otros receptores son mucho más débiles que el antagonismo de la ketamina del receptor NMDA (consulte la tabla de actividad a la derecha).
Aunque la ketamina es un ligando muy débil de los transportadores de monoamina (Ki > 60 μM), se ha sugerido que puede interactuar con los sitios alostéricos en los transportadores de monoamina para producir una inhibición de la recaptación de monoamina. Sin embargo, no se ha observado inhibición funcional (IC50) de los transportadores de monoamina humanos con ketamina o sus metabolitos en concentraciones de hasta 10 000 nM. Además, los estudios en animales y al menos tres informes de casos humanos no han encontrado interacción entre la ketamina y el inhibidor de la monoaminooxidasa (IMAO) tranilcipromina, lo cual es importante ya que la combinación de un inhibidor de la recaptación de monoamina con un IMAO puede producir una toxicidad grave, como el síndrome serotoninérgico. o crisis hipertensiva. En conjunto, estos hallazgos arrojan dudas sobre la participación de la inhibición de la recaptación de monoaminas en los efectos de la ketamina en humanos. Se ha descubierto que la ketamina aumenta la neurotransmisión dopaminérgica en el cerebro, pero en lugar de deberse a la inhibición de la recaptación de dopamina, esto puede ser a través de mecanismos indirectos, es decir, a través del antagonismo del receptor NMDA.
Es controvertido si la ketamina es un agonista de los receptores D2. Las primeras investigaciones realizadas por el grupo de Philip Seeman encontraron que la ketamina es un agonista parcial D2 con una potencia similar a la de su antagonismo del receptor NMDA. Sin embargo, estudios posteriores realizados por diferentes investigadores encontraron una afinidad de la ketamina de >10 μM por los receptores regulares D2 humanos y de rata, además, mientras que los agonistas de los receptores D2 como bromocriptina son capaces de suprimir rápida y poderosamente la secreción de prolactina, no se ha encontrado que las dosis subanestésicas de ketamina hagan esto en humanos y, de hecho, se ha encontrado que dependiente de la dosis aumentan los niveles de prolactina. Los estudios de imágenes han mostrado resultados mixtos sobre la inhibición de la unión de racloprida [11C] estriatal por la ketamina en humanos, con algunos estudios que encuentran una disminución significativa y otros que no encuentran tal efecto. Sin embargo, los cambios en la unión de [11C] racloprida pueden deberse a cambios en las concentraciones de dopamina inducidas por la ketamina en lugar de la unión de la ketamina al receptor D2.
Relaciones entre niveles y efectos
Se han notificado efectos psicotomiméticos y de disociación en personas tratadas con ketamina en concentraciones plasmáticas de aproximadamente 100 a 250 ng/mL (0,42–1,1 μM). La dosis típica de antidepresivo intravenoso de ketamina que se usa para tratar la depresión es baja y da como resultado concentraciones plasmáticas máximas de 70 a 200 ng/mL (0,29–0,84 μM). A concentraciones plasmáticas similares (70 a 160 ng/mL; 0,29–0,67 μM) también muestra efectos analgésicos. En 1 a 5 minutos después de inducir la anestesia mediante una inyección intravenosa rápida de ketamina, su concentración plasmática alcanza hasta 60 a 110 μM. Cuando se mantuvo la anestesia con óxido nitroso junto con inyección continua de ketamina, la concentración de ketamina se estabilizó en aproximadamente 9,3 μM. En un experimento con anestesia pura con ketamina, las personas comenzaron a despertarse una vez que el nivel plasmático de ketamina disminuyó a aproximadamente 2600 ng/mL (11 μM) y se orientaron en el lugar y el tiempo cuando el nivel bajó a 1000 ng/mL (4 μM). En un estudio de caso único, la concentración de ketamina en el líquido cefalorraquídeo, un indicador de la concentración cerebral, durante la anestesia varió entre 2,8 y 6,5 μM y fue aproximadamente un 40 % más baja que en el plasma.
Farmacocinética
La ketamina se puede absorber por muchas vías diferentes debido a su solubilidad tanto en agua como en lípidos. La biodisponibilidad de la ketamina intravenosa es del 100 % por definición, la biodisponibilidad de la inyección intramuscular es ligeramente inferior al 93 % y la biodisponibilidad epidural es del 77 %. Nunca se ha medido la biodisponibilidad subcutánea, pero se supone que es alta. Entre las vías menos invasivas, la vía intranasal tiene la biodisponibilidad más alta (45–50 %) y la oral, la más baja (16–20 %). Las biodisponibilidades sublingual y rectal son intermedias, de aproximadamente 25 a 50%.
Después de la absorción, la ketamina se distribuye rápidamente en el cerebro y otros tejidos. La unión a proteínas plasmáticas de la ketamina es variable del 23 al 47%.
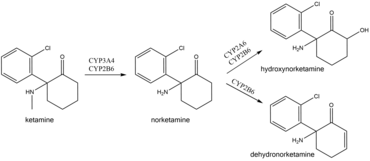
En el cuerpo, la ketamina sufre un extenso metabolismo. Es biotransformado por las isoenzimas CYP3A4 y CYP2B6 en norketamina, que, a su vez, es convertida por CYP2A6 y CYP2B6 en hidroxinorketamina y deshidronorketamina. La baja biodisponibilidad oral de la ketamina se debe al efecto de primer paso y, posiblemente, al metabolismo intestinal de la ketamina por CYP3A4. Como resultado, los niveles plasmáticos de norketamina son varias veces más altos que los de la ketamina después de la administración oral, y la norketamina puede desempeñar un papel en la acción anestésica y analgésica de la ketamina oral. Esto también explica por qué los niveles de ketamina por vía oral son independientes de la actividad de CYP2B6, a diferencia de los niveles de ketamina por vía subcutánea.
Después de una inyección intravenosa de ketamina marcada con tritio, el 91 % de la radiactividad se recupera de la orina y el 3 % de las heces. El medicamento se excreta principalmente en forma de metabolitos, y solo el 2% permanece sin cambios. Los derivados hidroxilados conjugados de la ketamina (80 %), seguidos de la deshidronorketamina (16 %), son los metabolitos más prevalentes detectados en la orina.
Química
Síntesis
El 2-clorobenzonitrilo se hace reaccionar con el bromuro de ciclopentilmagnesio reactivo de Grignard para dar (2-clorofenil)(ciclopentil)metanona. Luego se broma usando bromo para formar la bromocetona correspondiente, que luego se hace reaccionar con metilamina en una solución acuosa para formar el derivado de metilimino, 1-(2-cloro-N-metilbencimidoil)ciclopentanol, con hidrólisis del átomo de bromo terciario. Este intermedio final se calienta luego en decalina u otro solvente adecuado de alto punto de ebullición, sobre lo cual se produce un reordenamiento alfa-cetol que da como resultado una expansión del anillo y la formación de ketamina racémica.
Estructura
En estructura química, la ketamina es un derivado de la arilciclohexilamina. La ketamina es un compuesto quiral. El enantiómero más activo, esketamina (S-ketamina), también está disponible para uso médico bajo la marca Ketanest S, mientras que el enantiómero menos activo, arketamina (R-ketamina), nunca se ha comercializado como un fármaco enantiopuro para uso clínico. Mientras que la S-ketamina es más eficaz como analgésico y anestésico a través del antagonismo del receptor NMDA, la R-ketamina produce efectos más duraderos como antidepresivo.
La rotación óptica de un enantiómero dado de ketamina puede variar entre sus sales y su forma de base libre. La forma de base libre de (S)‑ketamina presenta dextrorotación y, por lo tanto, se denomina (S)‑(+)‑ketamina. Sin embargo, su sal de clorhidrato muestra levorotación y, por lo tanto, se etiqueta como clorhidrato de (S)‑(−)‑ketamina.
Detección
La ketamina se puede cuantificar en sangre o plasma para confirmar un diagnóstico de envenenamiento en personas hospitalizadas, proporcionar evidencia en un arresto por conducir bajo los efectos del alcohol o para ayudar en una investigación médico legal de muerte. Las concentraciones de ketamina en sangre o plasma suelen estar en un rango de 0.5 a 5.0 mg/L en personas que reciben el fármaco de forma terapéutica (durante la anestesia general), 1 a 2 mg/L en las personas arrestadas por conducir en estado de ebriedad y 3 a 20 mg/L en las víctimas de sobredosis mortal aguda. La orina es a menudo la muestra preferida para fines de seguimiento rutinario del consumo de drogas. La presencia de norketamina, un metabolito farmacológicamente activo, es útil para confirmar la ingestión de ketamina.
Historia
La ketamina fue sintetizada por primera vez en 1962 por Calvin L. Stevens, profesor de química en la Universidad Estatal de Wayne y consultor de Parke-Davis. Fue conocido por el nombre en clave de desarrollo CI-581. Después de una investigación preclínica prometedora en animales, la ketamina se probó en prisioneros humanos en 1964. Estas investigaciones demostraron que la corta duración de la acción de la ketamina y la toxicidad conductual reducida la convirtieron en una opción favorable sobre la fenciclidina (PCP) como anestésico. Los investigadores querían llamar al estado de anestesia con ketamina 'soñar', pero Parke-Davis no aprobó el nombre. Escuchar sobre este problema y sobre el "desconectado" apariencia de las personas tratadas, la Sra. Edward F. Domino, esposa de uno de los farmacólogos que trabajaban con la ketamina, sugirió "anestesia disociativa". Tras la aprobación de la FDA en 1970, la anestesia con ketamina se administró por primera vez a los soldados estadounidenses durante la Guerra de Vietnam.
El descubrimiento de la acción antidepresiva de la ketamina en el año 2000 se ha descrito como el avance más importante en el tratamiento de la depresión en más de 50 años. Ha despertado interés en los antagonistas de los receptores NMDA para la depresión y ha cambiado la dirección de la investigación y el desarrollo de antidepresivos.
Sociedad y cultura
Estado legal
Si bien la ketamina se comercializa legalmente en muchos países del mundo, también es una sustancia controlada en muchos países.
- En Australia, la ketamina figura como un programa de 8 medicamentos controlados bajo la Norma de Envenenamiento (octubre de 2015).
- En el Canadá, la ketamina se clasifica como narcóticos de la Lista I, desde 2005.
- En diciembre de 2013, el Gobierno de la India, en respuesta al aumento del uso recreativo y el uso de la ketamina como droga de violación de la fecha, lo ha añadido a la Lista X de la Ley de drogas y cosmética que exige una licencia especial para la venta y el mantenimiento de registros de todas las ventas durante dos años.
- In the United Kingdom, it became labeled a Class B drug on 12 February 2014.
- El aumento del uso recreativo dio lugar a la ketamina en la Lista III de la Ley de sustancias controladas por los Estados Unidos, en agosto de 1999.
Uso recreativo
A dosis subanestésicas, la ketamina produce un estado disociativo, caracterizado por una sensación de desapego del cuerpo físico y del mundo exterior que se conoce como despersonalización y desrealización. En dosis suficientemente altas, los usuarios pueden experimentar lo que se llama el 'agujero K', un estado de disociación con alucinaciones visuales y auditivas. John C. Lilly, Marcia Moore, D. M. Turner y David Woodard (entre otros) han escrito extensamente sobre sus propias experiencias enteogénicas y psiconáuticas con la ketamina. Turner murió prematuramente debido a que se ahogó durante el presunto uso de ketamina sin supervisión. En 2006, la edición rusa de Apocalypse Culture II de Adam Parfrey fue prohibida y destruida por las autoridades debido a la inclusión de un ensayo de Woodard sobre el uso enteogénico y las experiencias psiconáuticas con la ketamina. El uso recreativo de ketamina se ha relacionado con muertes en todo el mundo, con más de 90 muertes en Inglaterra y Gales en los años 2005-2013. Incluyen envenenamientos accidentales, ahogamientos, accidentes de tránsito y suicidios. La mayoría de las muertes se produjeron entre los jóvenes. Debido a su capacidad para causar confusión y amnesia, la ketamina se ha usado para violaciones en citas.
Investigación
La ketamina está bajo investigación por su potencial en el tratamiento de la depresión resistente al tratamiento. La ketamina es un psicoplastógeno conocido, que se refiere a un compuesto capaz de promover una neuroplasticidad rápida y sostenida.
Un estudio clínico de fase 2 demostró que la ketamina puede reducir de forma segura y eficaz la discinesia inducida por levodopa en pacientes con enfermedad de Parkinson. Se está realizando un ensayo clínico de fase II para probar el uso de ketamina como antidepresivo para pacientes con enfermedad de Parkinson.
Medicina veterinaria
En anestesia veterinaria, la ketamina se usa a menudo por sus efectos anestésicos y analgésicos en gatos, perros, conejos, ratas y otros animales pequeños. Se utiliza frecuentemente en la inducción y mantenimiento anestésico en equinos. Es una parte importante del 'cóctel de roedores', una mezcla de fármacos utilizados para anestesiar roedores. Los veterinarios a menudo usan ketamina con medicamentos sedantes para producir una anestesia y una analgesia equilibradas, y como una infusión de velocidad constante para ayudar a prevenir el dolor. La ketamina también se usa para controlar el dolor en animales grandes. Es el principal agente anestésico intravenoso utilizado en cirugía equina, a menudo junto con detomidina y tiopental, o algunas veces guaifenesina.
La ketamina parece no producir sedación ni anestesia en los caracoles. En cambio, parece tener un efecto excitatorio.
Contenido relacionado
Complejo respiratorio I
Bariatría
Clorpromazina