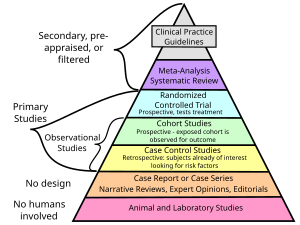
Jerarquía de evidencia
Una jerarquía de evidencia, que comprende niveles de evidencia (LOE), es decir, niveles de evidencia (EL), es una heurística utilizada para clasificar la solidez relativa de los resultados obtenidos a partir de la investigación experimental, especialmente la investigación médica. Existe un amplio consenso sobre la solidez relativa de los estudios epidemiológicos a gran escala. Se han propuesto más de 80 jerarquías diferentes para evaluar la evidencia médica. El diseño del estudio (como un informe de caso para un paciente individual o un ensayo controlado aleatorio ciego) y los puntos finales medidos (como la supervivencia o la calidad de vida) afectan la solidez de la evidencia. En la investigación clínica, la mejor evidencia de la eficacia del tratamiento proviene principalmente de los metanálisis de ensayos controlados aleatorios (ECA). Las revisiones sistemáticas de ensayos controlados aleatorios de alta calidad finalizados, como los publicados por la Colaboración Cochrane, tienen la misma clasificación que las revisiones sistemáticas de estudios observacionales de alta calidad finalizados en lo que respecta al estudio de los efectos secundarios. Las jerarquías de evidencia se aplican a menudo en las prácticas basadas en la evidencia y son parte integral de la medicina basada en la evidencia (MBE).
Definición
En 2014, Jacob Stegenga definió la jerarquía de la evidencia como "la clasificación de los tipos de métodos según el potencial de que ese método sufra de sesgo sistemático". En la cima de la jerarquía se encuentra el método con la mayor libertad de sesgo sistemático o la mejor validez interna en relación con la eficacia hipotética de la intervención médica probada. En 1997, Greenhalgh sugirió que era "el peso relativo que tienen los diferentes tipos de estudio primario al tomar decisiones sobre intervenciones clínicas".
El Instituto Nacional del Cáncer define los niveles de evidencia como "un sistema de clasificación utilizado para describir la solidez de los resultados medidos en un ensayo clínico o estudio de investigación. El diseño del estudio... y los criterios de valoración medidos... afectan la solidez de la evidencia".
Ejemplos
Se han propuesto numerosas jerarquías de evidencias. Todavía se están desarrollando protocolos similares para la evaluación de la calidad de la investigación. Hasta ahora, los protocolos disponibles prestan relativamente poca atención a si la investigación de resultados es relevante para la eficacia (el resultado de un tratamiento realizado en condiciones ideales) o para la efectividad (el resultado del tratamiento realizado en condiciones normales y esperables).
GRADE
El método GRADE (Grading of Recommendations Assessment, Development and Evaluation) es un método para evaluar la certeza de la evidencia (también conocida como calidad de la evidencia o confianza en las estimaciones de los efectos) y la solidez de las recomendaciones. GRADE comenzó en el año 2000 como una colaboración de metodólogos, desarrolladores de guías, bioestadísticos, médicos, científicos de salud pública y otros miembros interesados.
Más de 100 organizaciones (incluidas la Organización Mundial de la Salud, el Instituto Nacional para la Excelencia en la Salud y la Atención (NICE) del Reino Unido, el Grupo de Trabajo Canadiense para la Atención Sanitaria Preventiva y el Ministerio de Salud de Colombia, entre otras) han respaldado y/o están utilizando GRADE para evaluar la calidad de la evidencia y la solidez de las recomendaciones de atención sanitaria. (Vea ejemplos de guías de práctica clínica que utilizan GRADE en línea).
GRADES califica la calidad de la evidencia de la siguiente manera:
| Alto | Hay mucha confianza en que el efecto verdadero está cerca del efecto estimado. |
| Moderado | Existe una confianza moderada en el efecto estimado: Es probable que el efecto verdadero esté cerca del efecto estimado, pero existe la posibilidad de que sea sustancialmente diferente. |
| Baja | Hay poca confianza en el efecto estimado: El efecto verdadero podría ser sustancialmente diferente del efecto estimado. |
| Muy bajo | Hay muy poca confianza en el efecto estimado: Es probable que el efecto verdadero sea sustancialmente diferente del efecto estimado. |
Guyatt y Sackett
En 1995, Guyatt y Sackett publicaron la primera jerarquía de este tipo.
Greenhalgh ordenó los diferentes tipos de estudios primarios en el siguiente orden:
- Reseñas sistemáticas y metaanálisis de "RCTs con resultados definitivos".
- RCT con resultados definitivos (intervalos de confianza que no superponen el umbral efecto clínicamente significativo)
- RCT con resultados no definitivos (una estimación de puntos que sugiere un efecto clínicamente significativo pero con intervalos de confianza superando el umbral para este efecto)
- Estudios de cohortes
- Estudios de casos y control
- Encuestas transversales
- Informes de casos
Saunders et al.
Un protocolo sugerido por Saunders et al. asigna los informes de investigación a seis categorías, sobre la base del diseño de la investigación, los antecedentes teóricos, la evidencia de posibles daños y la aceptación general. Para ser clasificados bajo este protocolo, deben existir publicaciones descriptivas, incluido un manual o una descripción similar de la intervención. Este protocolo no considera la naturaleza de ningún grupo de comparación, el efecto de las variables de confusión, la naturaleza del análisis estadístico ni una serie de otros criterios. Las intervenciones se evalúan como pertenecientes a la Categoría 1, tratamientos eficaces y bien respaldados, si hay dos o más estudios de resultados controlados aleatorizados que comparan el tratamiento objetivo con un tratamiento alternativo apropiado y muestran una ventaja significativa para el tratamiento objetivo. Las intervenciones se asignan a la Categoría 2, tratamiento respaldado y probablemente eficaz, sobre la base de resultados positivos de diseños no aleatorios con alguna forma de control, que puede involucrar un grupo sin tratamiento. La Categoría 3, tratamiento respaldado y aceptable, incluye intervenciones respaldadas por un estudio controlado o no controlado, o por una serie de estudios de un solo sujeto, o por trabajo con una población diferente a la de interés. Categoría 4, tratamiento prometedor y aceptable, incluye intervenciones que no tienen respaldo excepto la aceptación general y la literatura clínica anecdótica; sin embargo, cualquier evidencia de posible daño excluye a los tratamientos de esta categoría. Categoría 5, tratamiento innovador y novedoso, incluye intervenciones que no se consideran dañinas, pero que no se usan ni se discuten ampliamente en la literatura. Categoría 6, relativa al tratamiento, es la clasificación para los tratamientos que tienen la posibilidad de hacer daño, así como también tienen fundamentos teóricos desconocidos o inadecuados.
Khan et al.
Un informe del Centro de Revisiones y Difusión, preparado por Khan et al. y concebido como un método general para evaluar intervenciones médicas y psicosociales, sugirió un protocolo para la evaluación de la calidad de la investigación. Si bien alentaba firmemente el uso de diseños aleatorios, este protocolo señalaba que dichos diseños eran útiles sólo si cumplían criterios exigentes, como la aleatorización verdadera y el ocultamiento del grupo de tratamiento asignado al cliente y a otras personas, incluidas las personas que evaluaban el resultado. El protocolo de Khan et al. enfatizaba la necesidad de hacer comparaciones sobre la base de la "intención de tratar" para evitar problemas relacionados con una mayor deserción en un grupo. El protocolo de Khan et al. también presentaba criterios exigentes para los estudios no aleatorios, que incluían la comparación de grupos en función de posibles variables de confusión y descripciones adecuadas de grupos y tratamientos en cada etapa, y el ocultamiento de la elección del tratamiento a las personas que evaluaban los resultados. Este protocolo no proporcionaba una clasificación de niveles de evidencia, pero incluía o excluía tratamientos de la clasificación como basados en evidencia dependiendo de si la investigación cumplía o no con los estándares establecidos.
Registro Nacional de prácticas y programas basados en pruebas
El Registro Nacional de Programas y Prácticas Basadas en la Evidencia (NREPP) de los Estados Unidos ha desarrollado un protocolo de evaluación. La evaluación según este protocolo se lleva a cabo únicamente si una intervención ya ha tenido uno o más resultados positivos, con una probabilidad de menos de 0,05, informados, si estos se han publicado en una revista revisada por pares o en un informe de evaluación, y si se ha puesto a disposición documentación como materiales de capacitación. La evaluación del NREPP, que asigna calificaciones de calidad de 0 a 4 a ciertos criterios, examina la confiabilidad y validez de las medidas de resultados utilizadas en la investigación, la evidencia de fidelidad de la intervención (uso predecible del tratamiento de la misma manera cada vez), los niveles de datos faltantes y deserción, las posibles variables de confusión y la idoneidad del manejo estadístico, incluido el tamaño de la muestra.
Historia
Canadá
El término se utilizó por primera vez en un informe de 1979 del «Grupo de trabajo canadiense sobre exámenes periódicos de salud» (CTF) para «calificar la eficacia de una intervención según la calidad de la evidencia obtenida». El grupo de trabajo utilizó tres niveles, subdividiendo el nivel II en:
- Nivel I: Evidencia de al menos un ensayo controlado aleatorizado,
- Nivel II1: Pruebas de al menos un estudio de cohortes bien diseñado o estudio de control de casos, preferiblemente de más de un centro o grupo de investigación.
- Nivel II2: Comparaciones entre tiempos y lugares con o sin intervención
- Nivel III: Opiniones de autoridades respetadas, basadas en la experiencia clínica, estudios descriptivos o informes de comités de expertos.
El CTF calificó sus recomendaciones en una escala de 5 puntos de la A a la E: A: Buen nivel de evidencia para la recomendación de considerar una afección, B: Nivel de evidencia aceptable para la recomendación de considerar una afección, C: Nivel de evidencia deficiente para la recomendación de considerar una afección, D: Nivel de evidencia aceptable para la recomendación de excluir la afección y E: Buen nivel de evidencia para la recomendación de excluir la afección de la consideración. El CTF actualizó su informe en 1984, 1986 y 1987.
Estados Unidos
En 1988, el Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF) publicó sus directrices basadas en el CTF utilizando los mismos tres niveles, subdividiendo aún más el nivel II.
- Nivel I: Evidencia obtenida de al menos un ensayo controlado debidamente diseñado.
- Nivel II-1: Evidencia obtenida de ensayos controlados bien diseñados sin aleatorización.
- Nivel II-2: Evidencia obtenida de estudios analíticos bien diseñados de cohorte o de control de casos, preferiblemente de más de un centro o grupo de investigación.
- Nivel II-3: Evidencia obtenida de múltiples diseños de series temporales con o sin la intervención. Los resultados dramáticos en juicios incontrolados también podrían considerarse como este tipo de pruebas.
- Nivel III: Opiniones de autoridades respetadas, basadas en la experiencia clínica, estudios descriptivos o informes de comités de expertos.
A lo largo de los años se han descrito muchos más sistemas de clasificación.
Reino Unido
En septiembre de 2000, el Centro de Medicina Basada en la Evidencia (CEBM) de Oxford (Reino Unido) publicó sus directrices sobre los "Niveles" de evidencia en relación con las afirmaciones sobre pronóstico, diagnóstico, beneficios del tratamiento, daños del tratamiento y detección. No solo abordaba la terapia y la prevención, sino también las pruebas diagnósticas, los marcadores de pronóstico o los daños. Los niveles originales del CEBM se publicaron por primera vez para la Medicina Basada en la Evidencia en el Momento para que el proceso de búsqueda de evidencia fuera factible y sus resultados explícitos. Tal como se publicaron en 2009, son:
- 1a: Reseñas sistemáticas (con homogeneidad) de ensayos controlados aleatorios
- 1b: Ensayos controlados aleatorizados individuales (con intervalo de confianza estrecho)
- 1c: Todos o ninguno (cuando todos los pacientes murieron antes de que el tratamiento estuviera disponible, pero algunos ahora sobreviven en él; o cuando algunos pacientes murieron antes de que el tratamiento estuviera disponible, pero ninguno muere ahora).
- 2a: Reseñas sistemáticas (con homogeneidad) de estudios de cohortes
- 2b: Estudio individual de cohortes o ensayos controlados aleatorizados de baja calidad (p.ej.
- 2c: "Explotación" Investigación; estudios ecológicos
- 3a: Revisión sistemática (con homogeneidad) de estudios de casos-control
- 3b: Estudio individual de control de casos
- 4: Serie de casos (y estudios de cohortes de mala calidad y control de casos)
- 5: Opinión de los expertos sin una evaluación crítica explícita, o basada en la fisiología, la investigación de los bancos o "primeros principios"
En 2011, un equipo internacional rediseñó los niveles de Oxford CEBM para que fueran más comprensibles y tuvieran en cuenta los avances recientes en los esquemas de clasificación de evidencia. Los niveles han sido utilizados por pacientes y médicos y también para desarrollar pautas clínicas que incluyen recomendaciones para el uso óptimo de la fototerapia y la terapia tópica en la psoriasis y pautas para el uso del sistema de estadificación BCLC para el diagnóstico y el seguimiento del carcinoma hepatocelular en Canadá.
Global
En 2007, el sistema de clasificación del Fondo Mundial para la Investigación del Cáncer describió cuatro niveles: evidencia convincente, probable, posible e insuficiente. Todos los estudios de la Carga Mundial de Enfermedades lo han utilizado para evaluar la evidencia epidemiológica que respalda las relaciones causales.
Proponents
En 1995, Wilson et al., en 1996, Hadorn et al. y en 1996, Atkins et al. describieron y defendieron varios tipos de sistemas de clasificación.
Crítica
En 2011, una revisión sistemática de la literatura crítica encontró tres tipos de críticas: aspectos procedimentales de la medicina basada en evidencia (especialmente de Cartwright, Worrall y Howick), falibilidad mayor de lo esperado de la medicina basada en evidencia (Ioaanidis y otros) y que la medicina basada en evidencia es incompleta como filosofía de la ciencia (Ashcroft y otros). Rawlins y Bluhm señalan que la medicina basada en evidencia limita la capacidad de los resultados de la investigación para informar la atención de pacientes individuales y que para comprender las causas de las enfermedades son necesarias investigaciones tanto a nivel poblacional como de laboratorio. La jerarquía de evidencia de la medicina basada en evidencia no tiene en cuenta la investigación sobre la seguridad y eficacia de las intervenciones médicas. Los RCT deben diseñarse "para dilucidar la variabilidad dentro del grupo, lo que sólo se puede hacer si la jerarquía de evidencia se reemplaza por una red que tenga en cuenta la relación entre la investigación epidemiológica y de laboratorio".
Se ha cuestionado la jerarquía de la evidencia producida por el diseño de un estudio, porque las pautas "no han logrado definir adecuadamente los términos clave, ponderar los méritos de ciertos ensayos controlados no aleatorios y emplear una lista completa de limitaciones del diseño de estudios".
Stegenga ha criticado específicamente que los metaanálisis se coloquen en la cima de tales jerarquías. La suposición de que los RCT deben estar necesariamente cerca de la cima de tales jerarquías ha sido criticada por Worrall y Cartwright.
En 2005, Ross Upshur afirmó que la medicina basada en evidencia afirma ser una guía normativa para ser un mejor médico, pero no es una doctrina filosófica.
Borgerson escribió en 2009 que las justificaciones de los niveles de jerarquía no son absolutas y no las justifican epistémicamente, pero que "los investigadores médicos deberían prestar más atención a los mecanismos sociales para gestionar los sesgos generalizados". La Caze señaló que la ciencia básica se encuentra en los niveles inferiores de la medicina basada en evidencia, aunque "juega un papel en la especificación de experimentos, pero también en el análisis e interpretación de los datos".
Concato dijo en 2004 que permitía a los RCTs demasiada autoridad y que no todas las preguntas de investigación podían ser respondidas a través de los RCTs, ya sea por cuestiones prácticas o éticas. Incluso cuando hay evidencia disponible de RCTs de alta calidad, la evidencia de otros tipos de estudios puede seguir siendo relevante. Stegenga opinó que los esquemas de evaluación de la evidencia son irrazonablemente restrictivos y menos informativos que otros esquemas disponibles en la actualidad.
En su tesis doctoral de 2015 dedicada al estudio de las diversas jerarquías de evidencia en medicina, Christopher J Blunt concluye que, aunque interpretaciones modestas como las que ofrece el modelo de La Caze, jerarquías condicionales como GRADE y enfoques heurísticos defendidos por Howick et al. sobreviven a críticas filosóficas anteriores, sostiene que las interpretaciones modestas son tan débiles que no son útiles para la práctica clínica. Por ejemplo, "GRADE y modelos condicionales similares omiten información clínicamente relevante, como información sobre la variación en los efectos de los tratamientos y las causas de las diferentes respuestas a la terapia; y que los enfoques heurísticos carecen del apoyo empírico necesario". Blunt concluye además que "las jerarquías son una base pobre para la aplicación de la evidencia en la práctica clínica", ya que los supuestos básicos detrás de las jerarquías de evidencia, de que "la información sobre los efectos promedio del tratamiento respaldada por evidencia de alta calidad puede justificar recomendaciones sólidas", es insostenible y, por lo tanto, la evidencia de los estudios individuales debe evaluarse de forma aislada.
Véase también
- Práctica basada en pruebas
- Medicina basada en pruebas
- Escala de Jadad
Referencias
- ^ Siegfried T (2017-11-13). "La crítica filosófica expone fallas en jerarquías de evidencia médica". Science News. Retrieved 2018-05-16.
- ^ Shafee, Thomas; Masukume, Gwinyai; Kipersztok, Lisa; Das, Diptanshu; Häggström, Mikael; Heilman, James (28 de agosto de 2017). "Evolución del contenido médico de Wikipedia: pasado, presente y futuro". Journal of Epidemiology and Community Health. 71 (11): jech–2016–208601. doi:10.1136/jech-2016-208601. ISSN 0143-005X. 5847101. PMID 28847845.
- ^ Straus SE, Richardson WS, Glasziou P, Haynes RB (2005). Medicina basada en pruebas: Cómo practicar y enseñar EBM (3a edición). Edimburgo: Churchill Livingstone. pp. 102–105. ISBN 978-0443074448.
- ^ Golder, Su; Loke, Yoon K.; Bland, Martin (2011-05-03). Vandenbroucke, Jan P. (ed.). "Meta-analyses of Adverse Effects Data Derived from Randomised Controlled Trials as Compared to Observational Studies: Methodological Overview". PLOS Medicina. 8 (5). Biblioteca Pública de Ciencias (PLoS): e1001026. doi:10.1371/journal.pmed.1001026. ISSN 1549-1676. PMC 3086872. PMID 21559325.
- ^ a b Stegenga J (octubre de 2014). "Abajo las jerarquías". Topoi. 33 (2): 313-322. doi:10.1007/s11245-013-9189-4. S2CID 109929514.
- ^ a b Greenhalgh T (julio de 1997). "Cómo leer un periódico. Conseguir sus rodamientos (decir de qué se trata el papel)". BMJ. 315 (7102): 243–246. doi:10.1136/bmj.315.7102.243. PMC 2127173. PMID 9253275.
- ^ National Cancer Institute (n.d.). "Diccionario Nacional de Cáncer Términos: Niveles de evidencia". US DHHS-National Institutes of Health. Retrieved 8 de diciembre 2014.
- ^ "Toma de decisiones basadas en la evidencia: Introducción y formulación de buenas preguntas clínicas ← Curso de educación continua Páginas de curso ← DentalCare.com". www.dentalcare.com. Archivado desde el original el 4 de marzo de 2016. Retrieved 2015-09-03.
- ^ "El Viaje de Investigación - Niveles de Evidencia vivieron CAPhO". www.capho.org. Archivado desde el original el 21 de febrero de 2016. Retrieved 2015-09-03.
- ^ Schünemann, HJ; Best, D; Vist, G; Oxman, AD (2003). "Cartas, números, símbolos y palabras: ¿Cómo mejor comunicar las calificaciones de evidencia y recomendaciones?". Canadian Medical Association Journal. 169 (7): 677-680.
- ^ "GRADEpro". Gradepro.org. Retrieved 16 de agosto 2019.
- ^ "Ministerio de Salud وزارة الدة". Archivado desde el original en 2016-02-25.
- ^ Balshem, H; Helfand, M; Schünemann, HJ; Oxman, AD; Kunz, R; Brozek, J; Vist, GE; Falck-Ytter, Y; Meerpohl, J; Norris, S; Guyatt, GH (abril 2011). "Directrices de GRADE 3: calificar la calidad de la evidencia – introducción". Journal of Clinical Epidemiology. 64 (4): 401–406. doi:10.1016/j.jclinepi.2010.07.015. PMID 21208779.
- ^ Reed Siemieniuk y Gordon Guyatt. "¿Qué es GRADE?". BMJ Buenas prácticas. Retrieved 2020-07-02.
- ^ Guyatt GH, Sackett DL, Sinclair JC, Hayward R, Cook DJ, Cook RJ (diciembre de 1995). "Guías de los usuarios a la literatura médica. IX. Un método para clasificar las recomendaciones de atención de la salud. Grupo de Trabajo sobre medicina basada en pruebas". JAMA. 274 (22): 1800–1804. doi:10.1001/jama.1995.03530220066035. PMID 7500513.
- ^ Saunders, B., Berliner, L., " Hanson, R. (2004). Abuso físico y sexual infantil: Directrices para tratamientos. Consultado el 15 de septiembre de 2006, en http://www.musc.edu/cvc.guidel.htm
- ^ Khan, K.S., et al. (2001). CRD Informe 4. Etapa II. Realización del examen. fase 5. Evaluación de la calidad del estudio. York, Reino Unido: Centro de Reseñas y Difusión, Universidad de York. Consultado el 20 de julio de 2007 en http://www.york.ac.uk/inst/crd/pdf/crd_4ph5.pdf
- ^ National Registry of Evidence-Based Practices and Programs (2007). Criterios de Revisión NREPP. Consultado el 10 de marzo de 2008 en http://www.nrepp.samsha.gov/review-criteria.htm
- ^ a b Canadian Task Force on the Periodic Health Examination (3 November 1979). "Task Force Report: The periodic health examination". Can Med Assoc J. 121 (9): 1193–1254. PMC 1704686. PMID 115569.
- ^ Canadian Task Force on the Periodic Health Examination (15 May 1984). "Task Force Report: The periodic health examination. 2. 1984 actualización". Can Med Assoc J. 130 (10): 1278–1285. PMC 1483525. PMID 6722691.
- ^ Canadian Task Force on the Periodic Health Examination (15 May 1986). "Task Force Report: The periodic health examination. 3. Actualización de 1986". Can Med Assoc J. 134 (10): 721-729.
- ^ Canadian Task Force on the Periodic Health Examination (1 April 1988). "Task Force Report: The periodic health examination. 2. 1987 actualización". Can Med Assoc J. 138 7): 618-626. PMC 1267740. PMID 3355931.
- ^ U.S. Preventive Services Task Force (1989). Guía para los servicios preventivos clínicos: informe del Grupo de Trabajo de Servicios Preventivos de los Estados Unidos. Diane Publishing. pp. 24–. ISBN 978-1568062976. Apéndice A
- ^ Welsh, Judith (enero de 2010). "Niveles de evidencia y análisis de la literatura". National Institutes of Health Library. Archivado desde el original el 31 de marzo de 2016. Retrieved 9 de septiembre 2015.
- ^ "Oxford Centre for Evidence-based Medicine – Levels of Evidence (March 2009)". Centre for Evidence-Based Medicine. 2009-06-11. Retrieved 25 de marzo 2015.
- ^ Burns el al 2011.
- ^ OCEBM Levels of Evidence Working Group (May 2016). "Los niveles de prueba de Oxford 2".
- ^ Paul, C.; Gallini, A.; Archier, E.; et al. (2012). "Recomendaciones basadas en la evidencia sobre el tratamiento tópico y la fototerapia de la psoriasis: Revisión sistemática y opinión experta de un panel de dermatólogos". Journal of the European Academy of Dermatology and Venereology. 26 (Supl 3): 1–10. doi:10.1111/j.1468-3083.2012.04518.x. PMID 22512675. S2CID 36103291.
- ^ Fondo Mundial de Investigación del Cáncer AICR. Alimentación, Nutrición y Actividad Física y Prevención del Cáncer: Una Perspectiva Global. American Institute for Cancer Research, Washington, DC; 2007
- ^ Lim, Stephen S; Vos, Theo; Flaxman, Abraham D; Danaei, Goodarz; Shibuya, Kenji; Adair-Rohani, Heather; Almazroa, Mohammad A; Amann, Markus; Anderson, H Ross; Andrews, Kathryn G; Aryee, Martin; Atkinson, Charles; Bacchus, Loraine J; Bahalim "Una evaluación comparativa del riesgo de la carga de enfermedades y lesiones atribuibles a 67 factores de riesgo y grupos de factores de riesgo en 21 regiones, 1990-2010: Un análisis sistemático para el Estudio Global de Carga de Enfermedades 2010". El Lancet. 380 (9859): 2224–2260. doi:10.1016/S0140-6736(12)61766-8. PMC 4156511. PMID 23245609.
- ^ Wilson, Mark C (1995). "Guías de los usuarios a la literatura médica. VIII. Cómo utilizar guías de práctica clínica. B. ¿Cuáles son las recomendaciones y te ayudarán a cuidar a tus pacientes? The evidence-based medicine working group". JAMA. 274 (20): 1630–1632. doi:10.1001/jama.1995.03530200066040. PMID 7474251. S2CID 8593521.
- ^ Hadorn, David C; Baker, David; Hodges, James S; Hicks, Nicholas (1996). "Comer la calidad de la evidencia para las directrices de práctica clínica". Journal of Clinical Epidemiology. 49 (7): 749–754. doi:10.1016/0895-4356(96)00019-4. PMID 8691224.
- ^ Atkins, D; Best, D; Briss, P. A; Eccles, M; Falck-Ytter, Y; Flottorp, S; Guyatt, G. H; Harbour, R. T; Haugh, M. C; Henry, D; Hill, S; Jaeschke, R; Leng, G; Liberati, A; Magrini, N; Mason, J; Middleton, P; Mrukowicz, J; O'Connell, D; Oxman, A. D; Phillips, B; Schünemann, Working Group, T; Varonen, H; Vist, G. E; Williams Jrza (2004) "Grading quality of evidence and strength of recommendations". BMJ. 328 (7454): 1490. doi:10.1136/bmj.328.7454.1490. PMC 428525. PMID 15205295.
- ^ Jeremy Howick (2011-02-23). La filosofía de la medicina basada en la evidencia. John Wiley & Sons. ISBN 978-1-4443-4266-6.
- ^ Solomon M (octubre de 2011). "Sólo un paradigma: medicina basada en evidencias en contexto epistemológico". European Journal for Philosophy of Science. 1 3). Springer: 451-466. doi:10.1007/s13194-011-0034-6. S2CID 170193949.
- ^ Rawlins M (diciembre de 2008). "De Testimonio: sobre la evidencia de decisiones sobre el uso de intervenciones terapéuticas". Medicina Clínica. 8 (6). Royal College of Physicians: 579-588. doi:10.7861/clinmedicine.8-6-579. PMC 4954394. PMID 19149278.
- ^ Bluhm R (octubre de 2011). "De la jerarquía a la red: una visión más rica de la evidencia de la medicina basada en evidencias". Perspectivas en Biología y Medicina. 48 (4). Johns Hopkins University Press: 535-547. doi:10.1353/pbm.2005.0082. PMID 16227665. S2CID 1156284.
- ^ Gugiu, PC; Westine, CD; Coryn, CL; Hobson, KA (3 de abril de 2012). "Una aplicación de un nuevo sistema de clasificación de evidencias para investigar el modelo de cuidado crónico". Eval Health Prof. 36 (1): 3-43. CiteSeerX 10.1.1.1016.5990. doi:10.1177/0163278712436968. PMID 22473325. S2CID 206452088.
- ^ Stegenga, J (2011). "¿Es metaanálisis el estándar platino de evidencia?". Stud Hist Philos Biol Biomed Sci. 42 (4): 497–507. doi:10.1016/j.shpsc.2011.07.003. PMID 22035723.
- ^ Worrall, John (2002). "¿Qué evidencia en la medicina basada en la evidencia?". Filosofía de la Ciencia. 69: S316–S330. doi:10.1086/341855. S2CID 55078796.
- ^ Cartwright, Nancy (2007). "¿Son RCTs el Gold Standard?" (PDF). BioSocieties. 2: 11–20. doi:10.1017/s1745855207005029. S2CID 145592046.
- ^ Upshur RE (Autumn 2005). "Buscar reglas en un mundo de excepciones: reflexiones sobre la práctica basada en pruebas". Perspectivas en Biología y Medicina. 48 (4). Johns Hopkins University Press: 477–489. doi:10.1353/pbm.2005.0098. PMID 16227661. S2CID 36678226.
- ^ Borgerson K (Spring 2009). "Valorando evidencia: sesgo y jerarquía de evidencia de medicina basada en evidencia" (PDF). Perspectivas en Biología y Medicina. 52 2). Johns Hopkins University Press: 218–233. doi:10.1353/pbm.0.0086. PMID 19395821. S2CID 38324417.
- ^ La Caze A (enero de 2011). "El papel de la ciencia básica en la medicina basada en evidencias". Biología y filosofía. 26 1). Springer: 81–98. doi:10.1007/s10539-010-9231-5. S2CID 189902678.
- ^ Concato J (julio de 2004). "Estudios observacionales versus experimentales: ¿cuál es la evidencia de una jerarquía?". NeuroRx. 1 3). Springer: 341–347. doi:10.1602/neurorx.1.3.341. PMC 534936. PMID 15717036.
- ^ Blunt, Christopher J (septiembre 2015). Jerarquías de evidencia en medicina basada en evidencia. PhD Tesis (fd). London School of Economics and Political Science.
Obras citadas
- Burns, Patricia B.; Rohrich, Rod J.; Chung, Kevin C. (Julio 2011). "Los niveles de evidencia y su papel en la medicina basada en la evidencia". Cirugía plástica y reconstructiva. 128 (1): 305–310. doi:10.1097/PRS.0b013e318219c171. PMC 3124652. PMID 21701348.
Enlaces externos
- Niveles de evidencia con explicaciones – entrada en el Centro de Medicina Basada en Evidencias
- Página de recursos de medicamentos basados en pruebas – con un diagrama que muestra diferentes niveles de evidencia formando una pirámide
- Base de datos sistemática de 195 jerarquías de evidencia en medicina hasta 08/10/2020 por Christopher J Blunt para su tesis doctoral.
![]() Este artículo incorpora material de dominio público Dictionary of Cancer Terms. U.S. National Cancer Institute.
Este artículo incorpora material de dominio público Dictionary of Cancer Terms. U.S. National Cancer Institute.