Isocitrato deshidrogenasa
Isocitrate deshidrogenase ()IDH) (EC 1.1.1.42) y (EC 1.1.1.41) es una enzima que cataliza la decarboxilación oxidativa del isocitrate, produciendo alfa-ketoglutaato (α-ketoglutarate) y CO2. Este es un proceso de dos pasos, que implica la oxidación del isocitario (alcohol secundario) al oxalosuccinato (una ketona), seguido por la decarboxilación del grupo beta del carboxilo al ketone, formando alfa-ketoglutarate. En humanos, la IDH existe en tres isoformas: la IDH3 cataliza el tercer paso del ciclo de ácido cítrico, al tiempo que convierte NAD+ a NADH en la mitocondria. Los isoformes IDH1 y IDH2 catalizan la misma reacción fuera del contexto del ciclo de ácido cítrico y usan NADP+ como cofactor en lugar de NAD+. Localizan al citosol, así como al mitocondrión y el peróxido.
Estructura

El NAD-IDH está compuesto por 3 subunidades, está regulado alostéricamente y requiere un ion Mg2+ o Mn2+ integrado. El homólogo más cercano que tiene una estructura conocida es el E. coli IDH dependiente de NADP, que tiene solo 2 subunidades y un 13% de identidad y un 29% de similitud según las secuencias de aminoácidos, lo que la hace diferente a la IDH humana y no es adecuada para una comparación cercana. Todos los NADP-IDH conocidos son homodímeros.
La mayoría de las isocitrato deshidrogenasas son dímeros, concretamente homodímeros (dos subunidades monómeras idénticas que forman una unidad dimérica). Al comparar C. glutamicum y E. coli, monómero y dímero, respectivamente, se descubrió que ambas enzimas "catalizan eficientemente reacciones idénticas". Sin embargo, C. glutamicum se registró con diez veces más actividad que E. coli y siete veces más afinidad/específica para NADP. C. glutamicum favoreció a NADP+ sobre NAD+. En términos de estabilidad con respuesta a la temperatura, ambas enzimas tenían una Tm o temperatura de fusión similar, de aproximadamente 55 °C a 60 °C. Sin embargo, el monómero C. glutamicum mostró una estabilidad más consistente a temperaturas más altas, lo que se esperaba. El dímero E. coli mostró estabilidad a una temperatura más alta de lo normal debido a las interacciones entre las dos subunidades monoméricas.
La estructura de Mycobacterium tuberculosis (Mtb) ICDH-1 unida a NADPH y Mn(2+) se ha resuelto mediante cristalografía de rayos X. Es un homodímero en el que cada subunidad tiene un pliegue de Rossmann y un dominio superior común de láminas β entrelazadas. Mtb ICDH-1 es estructuralmente más similar a la ICDH humana mutante R132H que se encuentra en los astrocitomas de grado 4 de la OMS del SNC, anteriormente clasificados como glioblastomas. De manera similar al R132H ICDH humano, Mtb ICDH-1 también cataliza la formación de α-hidroxiglutarato.
Reglamento
El paso IDH del ciclo del ácido cítrico es a menudo (pero no siempre) una reacción irreversible debido a su gran cambio negativo en la energía libre. Por lo tanto, debe regularse cuidadosamente para evitar el agotamiento del isocitrato (y, por tanto, la acumulación de alfa-cetoglutarato). La reacción es estimulada por mecanismos simples de disponibilidad de sustrato (isocitrato, NAD+ o NADP+, Mg2+ / Mn2 +), inhibición del producto por NADH (o NADPH fuera del ciclo del ácido cítrico) y alfa-cetoglutarato, e inhibición por retroalimentación competitiva por ATP. Se ha informado en genomas bacterianos de un ncRNA conservado aguas arriba del gen icd que codifica la isocitrato deshidrogenasa (IDH) dependiente de NADP+; debido a sus características, este ncRNA se parece a los reguladores anteriores. motivos llamados riboswitches, el motivo icd-II ncRNA se ha propuesto como un fuerte candidato a riboswitch.
Mecanismos catalíticos
Isocitrate deshidrogenasa cataliza las reacciones químicas:
- Isocitrate + NAD+ ⇌ ⇌ {displaystyle rightleftharpoons } 2-oxoglutrato + CO2 + NADH + H+
- Isocitrate + NADP+ ⇌ ⇌ {displaystyle rightleftharpoons } 2-oxoglutrato + CO2 + NADPH + H+
La energía libre total para esta reacción es -8,4 kJ/mol.

Pasos
Dentro del ciclo del ácido cítrico, el isocitrato, producido a partir de la isomerización del citrato, sufre oxidación y descarboxilación. La enzima isocitrato deshidrogenasa (IDH) mantiene el isocitrato dentro de su sitio activo utilizando los aminoácidos circundantes, incluidos arginina, tirosina, asparagina, serina, treonina y ácido aspártico.
En la figura proporcionada, el primer cuadro muestra la reacción general de la isocitrato deshidrogenasa. Los reactivos necesarios para este mecanismo enzimático son isocitrato, NAD+/NADP+ y Mn2+ o Mg2+. Los productos de la reacción son alfa-cetoglutarato, dióxido de carbono y NADH + H+/NADPH + H+. Las moléculas de agua ayudan a desprotonar los átomos de oxígeno del isocitrato.
El segundo cuadro de la figura ilustra el paso 1 de la reacción, que es la oxidación del carbono alfa (C2 aquí, también llamado alfa-C). En este proceso, el grupo alcohol del carbono alfa se desprotona y el par de electrones solitarios resultante forma un grupo cetona en ese carbono. NAD+/NADP+ actúa como un cofactor aceptor de electrones y recoge el hidruro resultante del C2. La oxidación del carbono alfa introduce una disposición molecular en la que los electrones (en el siguiente paso) fluirán desde el grupo carboxilo cercano y empujarán los electrones del oxígeno con doble enlace hacia el propio átomo de oxígeno, que recoge un protón de una lisina cercana.
El tercer cuadro ilustra el paso 2, que es la descarboxilación del oxalosuccinato. En este paso, el oxígeno del grupo carboxilo es desprotonado por una tirosina cercana y esos electrones fluyen hacia C2. El dióxido de carbono, el grupo saliente, se desprende del carbono beta del isocitrato (C3) y los electrones fluyen hacia la cetona de oxígeno unida al carbono alfa, otorgando una carga negativa al átomo de oxígeno asociado y formando un doble enlace alfa-beta insaturado entre carbonos 2 y 3.
El cuarto y último cuadro ilustra el paso 3, que es la saturación del doble enlace alfa-beta insaturado que se formó en el paso anterior. El oxígeno cargado negativamente (unido al carbono alfa) dona sus electrones, reformando el doble enlace de la cetona y empujando a otro par solitario (el que forma el doble enlace entre los carbonos alfa y beta) "fuera" del carbono. la molécula. Este par solitario, a su vez, recoge un protón de la tirosina cercana. Esta reacción da como resultado la formación de alfa-cetoglutarato, NADH + H+/NADPH + H+ y CO2.
Mecanismo detallado
Dos residuos de aminoácidos de aspartato (abajo a la izquierda) interactúan con dos moléculas de agua adyacentes (w6 y w8) en el complejo IDH porcino isocitrato de Mn2+ para desprotonar el alcohol del átomo de carbono alfa.. La oxidación del alfa-C también tiene lugar en este cuadro donde el NAD+ acepta un hidruro dando como resultado oxalosuccinato. Junto con el cambio estereoquímico sp3 a sp2 alrededor del alfa-C, hay un grupo cetona que se forma a partir del grupo alcohol. La formación de este doble enlace cetónico permite que se produzca resonancia a medida que los electrones que descienden del grupo carboxilato saliente se mueven hacia la cetona.
La descarboxilación del oxalosuccinato (abajo en el centro) es un paso clave en la formación de alfa-cetoglutarato. En esta reacción, el par solitario del hidroxilo de tirosina adyacente extrae el protón del grupo carboxilo. Este grupo carboxilo también se conoce como subunidad beta en la molécula de isocitrato. La desprotonación del grupo carboxilo hace que el par solitario de electrones descienda produciendo dióxido de carbono y separándose del oxalosuccinato. Los electrones continúan moviéndose hacia el carbono alfa empujando los electrones del doble enlace (que forman la cetona) hacia arriba para extraer un protón de un residuo de lisina adyacente. Entre el carbono 2 y el carbono 3 se produce un doble enlace alfa-beta insaturado. Como puede ver en la imagen, el ion verde representa Mg2+ o Mn2+, que es un cofactor necesario para que se produzca esta reacción. El ion metálico forma un pequeño complejo a través de interacciones iónicas con los átomos de oxígeno en el cuarto y quinto carbono (también conocido como subunidad gamma del isocitrato).
Después de que el dióxido de carbono se separa del oxalosuccinato en el paso de descarboxilación (abajo a la derecha), el enol se tautomerizará hasta convertirse en ceto. La formación del doble enlace cetónico comienza con la desprotonación del oxígeno del carbono alfa (C#2) por la misma lisina que protonó el oxígeno en primer lugar. El par solitario de electrones desciende dando inicio a los pares solitarios que estaban formando el doble enlace. Este par solitario de electrones extrae un protón de la tirosina que desprotonó el grupo carboxilo en el paso de descarboxilación. La razón por la que podemos decir que los residuos Lys y Tyr serán los mismos del paso anterior es porque ayudan a mantener la molécula de isocitrato en el sitio activo de la enzima. Estos dos residuos podrán formar enlaces de hidrógeno de un lado a otro siempre que estén lo suficientemente cerca del sustrato.
 |  |  |
La enzima isocitrato deshidrogenasa, como se indicó anteriormente, produce alfa-cetoglutarato, dióxido de carbono y NADH + H+/NADPH + H+. Hay tres cambios que ocurrieron a lo largo de la reacción. La oxidación del carbono 2, la descarboxilación (pérdida de dióxido de carbono) del carbono 3 y la formación de un grupo cetona con un cambio estereoquímico de sp3 a sp2.
Sitio activo
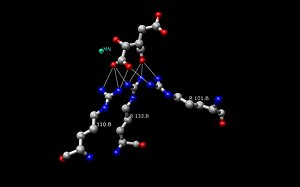
La estructura de la enzima isocitrato deshidrogenasa (IDH) en Escherichia coli fue la primera estructura ortóloga de IDH que se dilucida y comprende. Desde entonces, la mayoría de los investigadores han utilizado la estructura IDH de Escherichia coli para hacer comparaciones con otras enzimas isocitrato deshidrogenasa. Existe un conocimiento muy detallado sobre esta enzima bacteriana y se ha descubierto que la mayoría de las isocitrato deshidrogenasas son similares en estructura y, por tanto, también en función. Esta similitud de estructura y función da motivos para creer que las estructuras se conservan al igual que los aminoácidos. Por lo tanto, los sitios activos entre la mayoría de las enzimas isocitrato deshidrogenasa procarióticas también deben conservarse, lo que se observa en muchos estudios realizados sobre enzimas procarióticas. Por otro lado, las enzimas isocitrato deshidrogenasa eucariotas aún no se han descubierto por completo. Cada dímero de IDH tiene dos sitios activos. Cada sitio activo se une a una molécula de NAD+/NADP+ y a un ion metálico divalente (Mg2+, Mn2+). En general, cada sitio activo tiene una secuencia conservada de aminoácidos para cada sitio de unión específico. En Desulfotalea psychrophila (DpIDH) y porcino (PcIDH) hay tres sustratos unidos al sitio activo.
- Isocitrate se une dentro del sitio activo a una secuencia conservada de unos ocho aminoácidos a través de bonos de hidrógeno. Estos ácidos incluyen (puede variar en residuos pero con propiedades similares) tirosina, serina, asparagina, arginina, arginina, arginina, tirosina y lisina. Sus posiciones en la columna vertebral varían pero todas están dentro de un rango cercano (es decir, Arg131 DpIDH y Arg133 PcIDH, Tyr138 DpIDH y Tyr140 PcIDH).
- El ion de metal (Mg2+, Mn2+) se une a tres aminoácidos conservados a través de bonos de hidrógeno. Estos aminoácidos incluyen tres residuos aspartados.
- NAD+ y PNA+ se unen dentro del sitio activo dentro de cuatro regiones con propiedades similares entre las enzimas IDH. Estas regiones varían pero son alrededor [250-260], [280-290], [300-330], y [365-380]. Nuevamente las regiones varían pero se conserva la proximidad de las regiones.
Importancia clínica

Se han encontrado mutaciones específicas en el gen de la isocitrato deshidrogenasa IDH1 en varios tipos de tumores, en particular tumores cerebrales, incluidos astrocitoma y oligodendroglioma. Los pacientes cuyo tumor tenía una mutación IDH1 tuvieron una supervivencia más larga en comparación con los pacientes cuyo tumor tenía un tipo salvaje IDH1. Además, se encontraron mutaciones de IDH2 e IDH1 en hasta el 20% de las leucemias mieloides agudas (LMA) citogenéticamente normales. Se sabe que estas mutaciones producen D-2-hidroxiglutarato a partir de alfa-cetoglutarato. El D-2-hidroxiglutarato se acumula en concentraciones muy altas, lo que inhibe la función de las enzimas que dependen del alfa-cetoglutarato. Esto conduce a un estado hipermetilado del ADN y las histonas, lo que da como resultado una expresión genética diferente que puede activar oncogenes e inactivar genes supresores de tumores. En última instancia, esto puede conducir a los tipos de cáncer descritos anteriormente. También se han encontrado mutaciones en mosaico somático de este gen asociadas a la enfermedad de Ollier y al síndrome de Maffucci. Sin embargo, estudios recientes también han demostrado que el D-2-hidroxiglutarato puede volver a convertirse en alfa-cetoglutarato de forma enzimática o no enzimática. Se necesitan más estudios para comprender completamente las funciones de la mutación IDH1 (y del D-2-hidroxiglutarato) en el cáncer. Investigaciones recientes destacaron mutaciones cancerígenas en la isocitrato deshidrogenasa que pueden provocar la acumulación del metabolito D-2-hidroxiglutarato (D-2HG). Notarangelo et al. demostraron que concentraciones tan altas de D-2HG podrían actuar como un inhibidor directo de la lactato deshidrogenasa en células T de ratón. La inhibición de esta enzima metabólica alteró el metabolismo de la glucosa en las células T e inhibió su proliferación, producción de citoquinas y capacidad para matar células diana.
Isoenzimas
La siguiente es una lista de isocitrato deshidrogenasa humana:
Dependiente de NADP+
Cada isoenzima dependiente de NADP+funciona como un homodímero:
Dependiente de NAD+
La isoenzima isocitrato deshidrogenasa 3 es un heterotetrámero que se compone de dos subunidades alfa, una subunidad beta y una subunidad gamma: