Inmunoensayo
Un inmunoensayo (IA) es una prueba bioquímica que mide la presencia o concentración de una macromolécula o una pequeña molécula en una solución mediante el uso de un anticuerpo (generalmente ) o un antígeno (a veces). La molécula detectada por el inmunoensayo a menudo se denomina "analito" y en muchos casos es una proteína, aunque puede tratarse de otro tipo de moléculas, de diferentes tamaños y tipos, siempre y cuando se desarrollen los anticuerpos adecuados que tengan las propiedades requeridas para el ensayo. Los analitos en líquidos biológicos como el suero o la orina se miden frecuentemente mediante inmunoensayos con fines médicos y de investigación.
Los inmunoensayos vienen en muchos formatos y variaciones diferentes. Los inmunoensayos se pueden realizar en múltiples pasos con reactivos que se agregan y se lavan o separan en diferentes puntos del ensayo. Los ensayos de varios pasos a menudo se denominan inmunoensayos de separación o inmunoensayos heterogéneos. Algunos inmunoensayos se pueden realizar simplemente mezclando los reactivos y las muestras y realizando una medición física. Estos ensayos se denominan inmunoensayos homogéneos o, con menos frecuencia, inmunoensayos sin separación.
El uso de un calibrador se emplea a menudo en inmunoensayos. Los calibradores son soluciones que se sabe que contienen el analito en cuestión y la concentración de ese analito se conoce generalmente. La comparación de la respuesta de un ensayo a una muestra real con la respuesta del ensayo producida por los calibradores permite interpretar la intensidad de la señal en términos de la presencia o concentración del analito en la muestra.
Principio
Los inmunoensayos se basan en la capacidad de un anticuerpo para reconocer y unirse a una macromolécula específica en lo que podría ser una mezcla compleja de macromoléculas. En inmunología, la macromolécula particular unida por un anticuerpo se denomina antígeno y el área de un antígeno a la que se une el anticuerpo se denomina epítopo.
En algunos casos, un inmunoensayo puede utilizar un antígeno para detectar la presencia de anticuerpos, que reconocen ese antígeno, en una solución. En otras palabras, en algunos inmunoensayos, el analito puede ser un anticuerpo en lugar de un antígeno.
Además de la unión de un anticuerpo a su antígeno, la otra característica clave de todos los inmunoensayos es un medio para producir una señal mensurable en respuesta a la unión. La mayoría de los inmunoensayos, aunque no todos, implican la unión química de anticuerpos o antígenos con algún tipo de etiqueta detectable. En los inmunoensayos modernos existe una gran cantidad de etiquetas que permiten la detección por diferentes medios. Muchas etiquetas son detectables porque emiten radiación, producen un cambio de color en una solución, fluorescen bajo la luz o pueden inducirse a emitir luz.
Historia
A Rosalyn Sussman Yalow y Solomon Berson se les atribuye el desarrollo de los primeros inmunoensayos en la década de 1950. Yalow aceptó el Premio Nobel por su trabajo en inmunoensayos en 1977, convirtiéndose en la segunda mujer estadounidense en ganar el premio.
Los inmunoensayos se volvieron considerablemente más sencillos de realizar y más populares cuando a finales de los años 1960 se demostraron las técnicas de enzimas unidas químicamente a anticuerpos.
En 1983, el profesor Anthony Campbell en la Universidad de Cardiff reemplazó el yodo radiactivo utilizado en inmunoensayos por un éster de acridinio que produce su propia luz: la quimioluminiscencia. Este tipo de inmunoensayo se utiliza actualmente en alrededor de 100 millones de pruebas clínicas cada año en todo el mundo, lo que permite a los médicos medir una amplia gama de proteínas, patógenos y otras moléculas en muestras de sangre.
En 2012, la industria comercial de inmunoensayos ganaba 17.000.000.000 de dólares y se pensaba que tenía perspectivas de un lento crecimiento anual en el rango del 2 al 3 por ciento.
Etiquetas
Los inmunoensayos emplean una variedad de etiquetas diferentes para permitir la detección de anticuerpos y antígenos. Los marcadores suelen estar unidos químicamente o conjugados con el anticuerpo o antígeno deseado.
Enzimas
Posiblemente una de las etiquetas más populares para usar en inmunoensayos es la de enzimas. Los inmunoensayos que emplean enzimas se denominan inmunoensayos enzimáticos (EIA), de los cuales los ensayos inmunoabsorbentes ligados a enzimas (ELISA) y la técnica de inmunoensayo multiplicado por enzimas (EMIT) son los tipos más comunes.

Las enzimas utilizadas en los ELISA incluyen la peroxidasa de rábano picante (HRP), la fosfatasa alcalina (AP) o la glucosa oxidasa. Estas enzimas permiten la detección con frecuencia porque producen un cambio de color observable en presencia de ciertos reactivos. En algunos casos, estas enzimas están expuestas a reactivos que les hacen producir luz o quimioluminiscencia. Existen varios tipos de ELISA: directo, indirecto, sándwich, competitivo.
Isótopos radiactivos
Los isótopos radiactivos se pueden incorporar a reactivos de inmunoensayo para producir un radioinmunoensayo (RIA). La radiactividad emitida por los complejos anticuerpo-antígeno unidos se puede detectar fácilmente utilizando métodos convencionales.
Los RIA fueron algunos de los primeros inmunoensayos desarrollados, pero han perdido popularidad en gran medida debido a la dificultad y los peligros potenciales que presenta trabajar con radiactividad.
Reporteros de ADN
Un enfoque más nuevo para los inmunoensayos implica combinar la reacción en cadena de la polimerasa cuantitativa en tiempo real (RT qPCR) y técnicas de inmunoensayo tradicionales. La etiqueta utilizada en estos ensayos, denominada PCR inmunocuantitativa en tiempo real (iqPCR), es una sonda de ADN.
Reporteros fluorogénicos
Los reporteros fluorogénicos como la ficoeritrina se utilizan en varios inmunoensayos modernos. Los microarrays de proteínas son un tipo de inmunoensayo que a menudo emplea reporteros fluorogénicos.
Etiquetas electroquimioluminiscentes
Algunas etiquetas funcionan mediante electroquimioluminiscencia (ECL), en la que la etiqueta emite luz detectable en respuesta a una corriente eléctrica.
Inmunoensayos sin etiquetas
Si bien generalmente se emplea algún tipo de marcador en los inmunoensayos, existen ciertos tipos de ensayos que no se basan en marcadores, sino que emplean métodos de detección que no requieren la modificación o el etiquetado de los componentes del ensayo. La resonancia de plasmón superficial es un ejemplo de técnica que puede detectar la unión entre un anticuerpo no marcado y antígenos. Otro inmunoensayo sin etiquetas demostrado implica medir el cambio en la resistencia de un electrodo a medida que los antígenos se unen a él.
Clasificaciones y formatos

Los inmunoensayos se pueden ejecutar en varios formatos diferentes. Generalmente, un inmunoensayo se clasificará en una de varias categorías según cómo se realice.
Inmunoensayos competitivos y homogéneos
En un inmunoensayo competitivo y homogéneo, el analito no marcado en una muestra compite con el analito marcado para unirse a un anticuerpo. Luego se mide la cantidad de analito no unido marcado. En teoría, cuanto más analito hay en la muestra, más analito marcado se desplaza y luego se mide; por lo tanto, la cantidad de analito no unido marcado es proporcional a la cantidad de analito en la muestra.
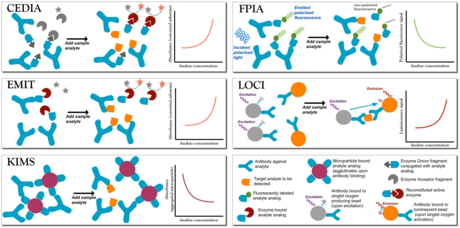
- El fluorescence polarization immunoassay (FPIA) mide la señal de polarización de fluorescencia después de la incubación, sin separar etiquetas fijas y libres. Las moléculas analógicas de analyte libres se añaden a la muestra, y su movimiento marroniano difiere cuando está ligado a un gran anticuerpo (A) versus libre en solución. El analyte compite por la unión a la Ab, y si el analyte etiquetado se une a la Ab, se produce una señal. La intensidad de la señal es inversamente proporcional a la concentración anal.
- En el enzima multiplied inmunoassay technique (EMIT), moléculas analógicas de análisis libres etiquetadas con una enzima (por ejemplo, la enzima de deshidrogenasa de glucosa-6-fosfato) compiten con el analito que se está probando. La enzima activa reduce la NAD (sin señal) a la NADH (que absorbe a 340 nm), por lo que la absorción se monitoriza a 340 nm. Cuando el analyte etiquetado se une a la Ab, la enzima se vuelve inactiva, y una señal es generada por la etiqueta gratuita. La intensidad de la señal es directamente proporcional a la concentración de analitos.
- El inmunoassay (LOCI) genera especies de oxigeno sintet en micro cristales unidos al analyte, y cuando el analyte se une a la respectiva molécula de Ab, unida a otro tipo de cuentas, el analyte reacciona con oxígeno sintetico, generando señales de quimioluminiscencia proporcionales a la concentración del complejo analyte-Ab.
- En el interacción cinética de la micropartícula en solución (KIMS) y inhibición turbidimétrica mejorada inmunoassay (PETINIA), anticuerpos libres se unen a los conjugados de micropartículas para formar agregados que absorben en el rango visible en ausencia del analyte. En presencia del analyte, el Ab se une al analyte libre, evitando la agregación de micropartículas y causando una reducción de la absorción. La señal es inversamente proporcional a la concentración de analito.
- El inmunoensaje de donantes de enzimas clonadas (CEDIA) implica la ingeniería genética de una enzima (por ejemplo, beta-galactosidase) en dos fragmentos inactivos: un pequeño donante de enzimas (ED) conjugado con el análogo del medicamento, y un mayor receptor de enzimas (EA). Cuando los dos fragmentos asocian, la enzima completa convierte un sustrato en un producto de color blanqueado. Si las moléculas analytes de drogas están presentes, compiten con el medicamento etiquetado con ED en solución para los sitios limitados de Ab. El analógico libre de ED se unirá a EA, generando una señal colorimétrica directamente proporcional a la cantidad de analyte.
Inmunoensayos competitivos y heterogéneos
Al igual que en un inmunoensayo competitivo y homogéneo, el analito no marcado en una muestra compite con el analito marcado para unirse a un anticuerpo. En los ensayos heterogéneos, el analito marcado no unido se separa o se lava y el analito marcado restante se mide.
Inmunoensayos no competitivos en un solo sitio
El analito desconocido en la muestra se une a los anticuerpos marcados. Los anticuerpos marcados y no unidos se eliminan por lavado y se miden los anticuerpos marcados y unidos. La intensidad de la señal es directamente proporcional a la cantidad de analito desconocido.
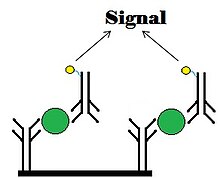
Inmunoensayos no competitivos de dos sitios
El analito en la muestra desconocida está ligado al sitio del anticuerpo, entonces el anticuerpo etiquetado está ligado al analyte. La cantidad de anticuerpo etiquetado en el sitio se mide entonces. Será directamente proporcional a la concentración del analito porque el anticuerpo etiquetado no se unirá si el analito no está presente en la muestra desconocida. Este tipo de inmunoensaje también se conoce como un ensayo de sándwich, ya que el analyte es "sandwiched" entre dos anticuerpos.
Ejemplos
Pruebas clínicas
Una amplia gama de pruebas médicas son inmunoensayos, llamados en este contexto inmunodiagnósticos. Muchas pruebas de embarazo caseras son inmunoensayos que detectan el marcador de embarazo gonadotropina coriónica humana. Más específicamente, son pruebas cualitativas que detectan si hay hCG presente, utilizando una configuración de flujo lateral. La prueba rápida de antígenos de COVID-19 también es una prueba cualitativa de flujo lateral.
Otros inmunoensayos clínicos son cuantitativos; miden cantidades. Los inmunoensayos pueden medir los niveles de CK-MB para evaluar enfermedades cardíacas, insulina para evaluar la hipoglucemia, antígeno prostático específico para detectar el cáncer de próstata y algunos también se utilizan para la detección y/o medición cuantitativa de algunos compuestos farmacéuticos (ver Técnica de inmunoensayo multiplicado por enzimas). para más detalles).
Las pruebas de detección de drogas también comienzan con un inmunoensayo cualitativo rápido.
Análisis antidopaje deportivo
Los inmunoensayos se utilizan en los laboratorios antidopaje deportivos para evaluar la calidad de los atletas. muestras de sangre para detectar la hormona de crecimiento humana recombinante prohibida (rhGH, rGH, hGH, GH).
Investigación
Inmunoensayo fotoacústico
El inmunoensayo fotoacústico mide señales acústicas de baja frecuencia generadas por etiquetas de nanopartículas metálicas. Iluminadas por una luz modulada en una longitud de onda de resonancia de plasmón, las nanopartículas generan una fuerte señal acústica, que puede medirse con un micrófono. El inmunoensayo fotoacústico se puede aplicar a pruebas de flujo lateral, que utilizan nanopartículas coloidales.