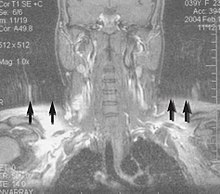
Imagen de resonancia magnética
La imagen por resonancia magnética (MRI) es una técnica de imagen médica utilizada en radiología para formar imágenes de la anatomía y los procesos fisiológicos del cuerpo. Los escáneres de resonancia magnética utilizan fuertes campos magnéticos, gradientes de campos magnéticos y ondas de radio para generar imágenes de los órganos del cuerpo. La resonancia magnética no involucra rayos X ni el uso de radiación ionizante, lo que la distingue de las tomografías computarizadas y las tomografías por emisión de positrones. La resonancia magnética es una aplicación médica de la resonancia magnética nuclear (RMN) que también se puede utilizar para obtener imágenes en otras aplicaciones de RMN, como la espectroscopia de RMN.
La resonancia magnética se usa ampliamente en hospitales y clínicas para el diagnóstico médico, la estadificación y el seguimiento de enfermedades. En comparación con la TC, la RM proporciona un mejor contraste en las imágenes de tejidos blandos, p. en el cerebro o el abdomen. Sin embargo, los pacientes pueden percibirlo como menos cómodo, debido a las mediciones generalmente más largas y más fuertes con el sujeto en un tubo largo y confinado, aunque 'abierto'. Los diseños de resonancia magnética en su mayoría alivian esto. Además, los implantes y otros metales no removibles en el cuerpo pueden representar un riesgo y pueden impedir que algunos pacientes se sometan a un examen de resonancia magnética de manera segura.
La resonancia magnética originalmente se llamaba NMRI (imágenes por resonancia magnética nuclear), pero "nuclear" se eliminó para evitar asociaciones negativas. Ciertos núcleos atómicos pueden absorber energía de radiofrecuencia cuando se colocan en un campo magnético externo; la polarización de espín en evolución resultante puede inducir una señal de RF en una bobina de radiofrecuencia y, por lo tanto, ser detectada. En la resonancia magnética clínica y de investigación, los átomos de hidrógeno se utilizan con mayor frecuencia para generar una polarización macroscópica que es detectada por antenas cercanas al sujeto que se examina. Los átomos de hidrógeno son naturalmente abundantes en los seres humanos y otros organismos biológicos, en particular en el agua y la grasa. Por esta razón, la mayoría de las resonancias magnéticas esencialmente mapean la ubicación del agua y la grasa en el cuerpo. Los pulsos de ondas de radio excitan la transición de energía de espín nuclear y los gradientes del campo magnético localizan la polarización en el espacio. Al variar los parámetros de la secuencia de pulsos, se pueden generar diferentes contrastes entre tejidos en función de las propiedades de relajación de los átomos de hidrógeno en ellos.
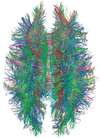
Desde su desarrollo en las décadas de 1970 y 1980, la resonancia magnética ha demostrado ser una técnica de imagen versátil. Si bien la resonancia magnética se usa de manera más prominente en la medicina de diagnóstico y la investigación biomédica, también se puede usar para formar imágenes de objetos no vivos, como momias. La resonancia magnética de difusión y la resonancia magnética funcional amplían la utilidad de la resonancia magnética para capturar tractos neuronales y flujo sanguíneo respectivamente en el sistema nervioso, además de imágenes espaciales detalladas. El aumento sostenido en la demanda de resonancia magnética dentro de los sistemas de salud ha generado preocupaciones sobre la rentabilidad y el sobrediagnóstico.
Mecanismo
Construcción y física
En la mayoría de las aplicaciones médicas, los núcleos de hidrógeno, que consisten únicamente en un protón, que se encuentran en los tejidos crean una señal que se procesa para formar una imagen del cuerpo en términos de la densidad de esos núcleos en una región específica. Dado que los protones se ven afectados por los campos de otros átomos a los que están unidos, es posible separar las respuestas del hidrógeno en compuestos específicos. Para realizar un estudio, la persona se coloca dentro de un escáner de resonancia magnética que forma un fuerte campo magnético alrededor del área de la que se va a obtener la imagen. Primero, la energía de un campo magnético oscilante se aplica temporalmente al paciente a la frecuencia de resonancia apropiada. El escaneo con bobinas de gradiente X e Y hace que una región seleccionada del paciente experimente el campo magnético exacto requerido para que se absorba la energía. Los átomos son excitados por un pulso de radiofrecuencia (RF) y la señal resultante es medida por una bobina receptora. La señal de RF se puede procesar para deducir la información de la posición observando los cambios en el nivel y la fase de RF causados por la variación del campo magnético local utilizando bobinas de gradiente. Como estas bobinas se cambian rápidamente durante la excitación y la respuesta para realizar una exploración de línea en movimiento, crean el ruido repetitivo característico de una exploración de resonancia magnética a medida que los devanados se mueven ligeramente debido a la magnetoestricción. El contraste entre diferentes tejidos está determinado por la velocidad a la que los átomos excitados vuelven al estado de equilibrio. Se pueden administrar agentes de contraste exógenos a la persona para que la imagen sea más clara.
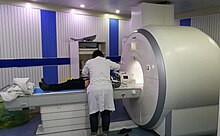
Los principales componentes de un escáner de resonancia magnética son el imán principal, que polariza la muestra, las bobinas de ajuste para corregir los cambios en la homogeneidad del campo magnético principal, el sistema de gradiente que se utiliza para localizar la región que se escaneará y el Sistema de RF, que excita la muestra y detecta la señal de RMN resultante. Todo el sistema está controlado por una o más computadoras.
La IRM requiere un campo magnético fuerte y uniforme de unas pocas partes por millón en todo el volumen de exploración. La intensidad del campo del imán se mide en teslas, y aunque la mayoría de los sistemas funcionan a 1,5 T, los sistemas comerciales están disponibles entre 0,2 y 7 T. Los sistemas de IRM de cuerpo entero para aplicaciones de investigación funcionan, p. 9,4 toneladas, 10,5 toneladas, 11,7 toneladas. Incluso los sistemas de resonancia magnética de cuerpo entero de mayor campo, p. 14 T y más allá están en propuesta conceptual o en diseño de ingeniería. La mayoría de los imanes clínicos son imanes superconductores, que requieren helio líquido para mantenerlos a bajas temperaturas. Se pueden lograr intensidades de campo más bajas con imanes permanentes, que a menudo se utilizan en entornos "abiertos" Escáneres de resonancia magnética para pacientes claustrofóbicos. Las intensidades de campo más bajas también se utilizan en un escáner de resonancia magnética portátil aprobado por la FDA en 2020. Recientemente, la resonancia magnética también se ha demostrado en campos ultrabajos, es decir, en el rango de microteslas a militeslas, donde la calidad de la señal es posible gracias a prepolarización (del orden de 10 a 100 mT) y midiendo los campos de precesión de Larmor a aproximadamente 100 microtesla con dispositivos superconductores de interferencia cuántica (SQUID) altamente sensibles.
T1 y T2
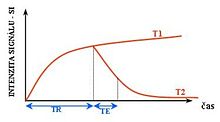
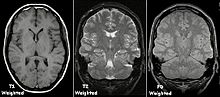
Cada tejido vuelve a su estado de equilibrio después de la excitación por los procesos de relajación independientes de T1 (spin-lattice; es decir, magnetización en la misma dirección que el campo magnético estático) y T2 (spin-spin; transversal al campo magnético estático). campo). Para crear una imagen ponderada en T1, se permite que la magnetización se recupere antes de medir la señal de RM cambiando el tiempo de repetición (TR). Esta ponderación de imágenes es útil para evaluar la corteza cerebral, identificar tejido graso, caracterizar lesiones hepáticas focales y, en general, obtener información morfológica, así como para imágenes post-contraste. Para crear una imagen ponderada en T2, se permite que la magnetización decaiga antes de medir la señal de RM cambiando el tiempo de eco (TE). Esta ponderación de imágenes es útil para detectar edema e inflamación, revelar lesiones de sustancia blanca y evaluar la anatomía zonal en la próstata y el útero.
La visualización estándar de las imágenes de resonancia magnética es representar las características de los fluidos en imágenes en blanco y negro, donde los diferentes tejidos resultan de la siguiente manera:
| Signal | Peso T1 | Peso T2 |
|---|---|---|
| Alto |
|
|
| Inter- mediate | La materia gris más oscura que la materia blanca | La materia blanca más oscura que la materia gris |
| Baja |
|
|
Diagnóstico
Uso por órgano o sistema
La resonancia magnética tiene una amplia gama de aplicaciones en el diagnóstico médico y se estima que hay más de 25 000 escáneres en uso en todo el mundo. La resonancia magnética afecta el diagnóstico y el tratamiento en muchas especialidades, aunque en ciertos casos se cuestiona el efecto sobre la mejora de los resultados de salud.
La resonancia magnética es la investigación de elección en la estadificación preoperatoria del cáncer de recto y próstata y tiene una función en el diagnóstico, la estadificación y el seguimiento de otros tumores, así como para determinar áreas de tejido para muestreo en biobancos.
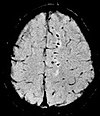
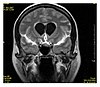
Neuroimagen
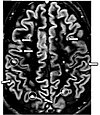
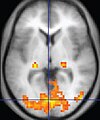
La resonancia magnética es la herramienta de investigación de elección para los cánceres neurológicos sobre la TC, ya que ofrece una mejor visualización de la fosa craneal posterior, que contiene el tronco encefálico y el cerebelo. El contraste proporcionado entre la materia gris y la blanca hace que la resonancia magnética sea la mejor opción para muchas afecciones del sistema nervioso central, incluidas las enfermedades desmielinizantes, la demencia, la enfermedad cerebrovascular, las enfermedades infecciosas, la enfermedad de Alzheimer y la epilepsia. Dado que muchas imágenes se toman con milisegundos de diferencia, muestra cómo responde el cerebro a diferentes estímulos, lo que permite a los investigadores estudiar las anomalías cerebrales tanto funcionales como estructurales en los trastornos psicológicos. La resonancia magnética también se usa en cirugía estereotáctica guiada y radiocirugía para el tratamiento de tumores intracraneales, malformaciones arteriovenosas y otras afecciones tratables quirúrgicamente mediante un dispositivo conocido como localizador N. Las nuevas herramientas que implementan la inteligencia artificial en el cuidado de la salud han demostrado una mayor calidad de imagen y análisis morfométrico en neuroimagen con la aplicación de un sistema de eliminación de ruido.
El récord de la resolución espacial más alta de un cerebro entero intacto (post mórtem) es de 100 micrones, del Hospital General de Massachusetts. Los datos se publicaron en NATURE el 30 de octubre de 2019.
Cardiovasculares
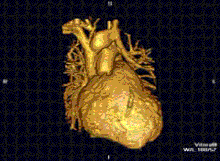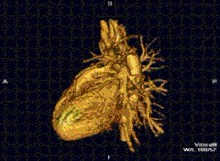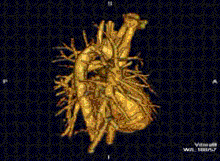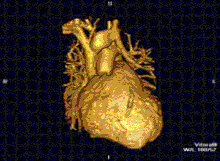
La resonancia magnética cardíaca es complementaria a otras técnicas de imagen, como la ecocardiografía, la tomografía computarizada cardíaca y la medicina nuclear. Se puede utilizar para evaluar la estructura y la función del corazón. Sus aplicaciones incluyen la evaluación de la isquemia y la viabilidad del miocardio, las miocardiopatías, la miocarditis, la sobrecarga de hierro, las enfermedades vasculares y las cardiopatías congénitas.
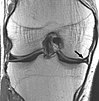
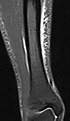
Musculoesquelético
Las aplicaciones en el sistema musculoesquelético incluyen imágenes de la columna, evaluación de enfermedades articulares y tumores de tejidos blandos. Además, las técnicas de resonancia magnética se pueden utilizar para el diagnóstico por imágenes de enfermedades musculares sistémicas, incluidas las enfermedades musculares genéticas.
El movimiento de deglución de la garganta y el esófago puede causar un artefacto de movimiento sobre la imagen de la columna vertebral. Por lo tanto, un pulso de saturación aplicado sobre esta región de la garganta y el esófago puede ayudar a evitar este artefacto. El artefacto de movimiento que surge debido al bombeo del corazón puede reducirse cronometrando el pulso de la resonancia magnética de acuerdo con los ciclos cardíacos. Los artefactos de flujo de los vasos sanguíneos se pueden reducir aplicando pulsos de saturación por encima y por debajo de la región de interés.
Hígado y gastrointestinal
La RM hepatobiliar se utiliza para detectar y caracterizar lesiones del hígado, el páncreas y las vías biliares. Los trastornos focales o difusos del hígado pueden evaluarse utilizando imágenes de fase opuesta ponderadas por difusión y secuencias de realce de contraste dinámico. Los agentes de contraste extracelulares se utilizan ampliamente en la resonancia magnética del hígado, y los agentes de contraste hepatobiliares más nuevos también brindan la oportunidad de realizar imágenes biliares funcionales. Las imágenes anatómicas de los conductos biliares se logran mediante el uso de una secuencia muy ponderada en T2 en colangiopancreatografía por resonancia magnética (CPRM). La imagen funcional del páncreas se realiza después de la administración de secretina. La enterografía por RM proporciona una evaluación no invasiva de la enfermedad inflamatoria intestinal y los tumores del intestino delgado. La colonografía por RM puede desempeñar un papel en la detección de pólipos grandes en pacientes con mayor riesgo de cáncer colorrectal.
Angiografía
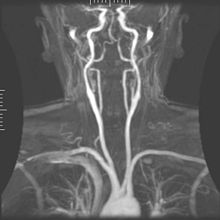
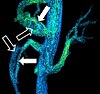
La angiografía por resonancia magnética (ARM) genera imágenes de las arterias para evaluarlas en busca de estenosis (estrechamiento anormal) o aneurismas (dilatación de la pared del vaso, con riesgo de ruptura). La MRA se usa a menudo para evaluar las arterias del cuello y el cerebro, la aorta torácica y abdominal, las arterias renales y las piernas (lo que se denomina 'run-off'). Se puede usar una variedad de técnicas para generar las imágenes, como la administración de un agente de contraste paramagnético (gadolinio) o el uso de una técnica conocida como "mejora relacionada con el flujo" (p. ej., secuencias de tiempo de vuelo en 2D y 3D), donde la mayor parte de la señal en una imagen se debe a la sangre que se movió recientemente en ese plano (ver también FLASH MRI).
Las técnicas que implican la acumulación de fase (conocidas como angiografía de contraste de fase) también se pueden utilizar para generar mapas de velocidad de flujo con facilidad y precisión. La venografía por resonancia magnética (MRV) es un procedimiento similar que se utiliza para obtener imágenes de las venas. En este método, el tejido ahora se excita en la parte inferior, mientras que la señal se recopila en el plano inmediatamente superior al plano de excitación, lo que genera imágenes de la sangre venosa que se movió recientemente desde el plano excitado.
Agentes de contraste
La IRM para obtener imágenes de estructuras anatómicas o del flujo sanguíneo no requiere agentes de contraste, ya que las diferentes propiedades de los tejidos o la sangre proporcionan contrastes naturales. Sin embargo, para tipos de imágenes más específicos, los agentes de contraste exógenos pueden administrarse por vía intravenosa, oral o intraarticular. La mayoría de los agentes de contraste son paramagnéticos (p. ej., gadolinio, manganeso, europio) y se usan para acortar T1 en el tejido en el que se acumulan, o superparamagnéticos (SPION), y se usan para acortar T2 y T2* en tejido sano reduciendo su intensidad de señal (agentes de contraste negativos). Los agentes de contraste intravenoso más utilizados se basan en quelatos de gadolinio, que es altamente paramagnético. En general, estos agentes han demostrado ser más seguros que los agentes de contraste yodados utilizados en la radiografía de rayos X o la TC. Las reacciones anafilactoides son raras y ocurren en aprox. 0,03-0,1%. De particular interés es la menor incidencia de nefrotoxicidad, en comparación con los agentes yodados, cuando se administran en las dosis habituales; esto ha hecho que la resonancia magnética con contraste sea una opción para los pacientes con insuficiencia renal, que de otro modo no podrían someterse a una TC con contraste.
Los reactivos de contraste a base de gadolinio suelen ser complejos octadentados de gadolinio (III). El complejo es muy estable (log K > 20) por lo que, en uso, la concentración de los iones Gd3+ no complejados debe estar por debajo del límite de toxicidad. El noveno lugar en la esfera de coordinación de los iones metálicos lo ocupa una molécula de agua que se intercambia rápidamente con moléculas de agua en el entorno inmediato de la molécula reactiva, lo que afecta el tiempo de relajación de la resonancia magnética. Para obtener más información, consulte Agente de contraste para resonancia magnética.
En diciembre de 2017, la Administración de Alimentos y Medicamentos (FDA) de los Estados Unidos anunció en un comunicado sobre la seguridad de los medicamentos que se incluirían nuevas advertencias en todos los agentes de contraste a base de gadolinio (GBCA). La FDA también solicitó una mayor educación del paciente y exigió a los proveedores de contraste de gadolinio que realicen estudios clínicos y en animales adicionales para evaluar la seguridad de estos agentes. Aunque los agentes de gadolinio han demostrado ser útiles para pacientes con insuficiencia renal, en pacientes con insuficiencia renal grave que requieren diálisis existe el riesgo de una enfermedad rara pero grave, fibrosis sistémica nefrogénica, que puede estar relacionada con el uso de ciertos agentes que contienen gadolinio. El más frecuentemente relacionado es la gadodiamida, pero también se han relacionado otros agentes. Aunque no se ha establecido definitivamente un vínculo causal, las pautas actuales en los Estados Unidos son que los pacientes de diálisis solo deben recibir agentes de gadolinio cuando sea esencial y que la diálisis debe realizarse lo antes posible después de la exploración para eliminar el agente del cuerpo rápidamente.
En Europa, donde hay más agentes que contienen gadolinio disponibles, se ha publicado una clasificación de agentes según los riesgos potenciales. En 2008, se aprobó para uso diagnóstico un nuevo agente de contraste llamado gadoxetato, de marca Eovist (EE. UU.) o Primovist (UE), que tiene el beneficio teórico de una vía de excreción dual.
Secuencias
Una secuencia de resonancia magnética es una configuración particular de pulsos y gradientes de radiofrecuencia, lo que da como resultado una apariencia de imagen particular. La ponderación T1 y T2 también se puede describir como secuencias de MRI.
Tabla de resumen
Esta tabla no incluye secuencias poco comunes y experimentales.
Otras configuraciones especializadas
Espectroscopía de resonancia magnética
La espectroscopia de resonancia magnética (MRS) se utiliza para medir los niveles de diferentes metabolitos en los tejidos del cuerpo, lo que se puede lograr a través de una variedad de técnicas basadas en imágenes o de un solo vóxel. La señal de RM produce un espectro de resonancias que corresponde a diferentes arreglos moleculares del isótopo que se 'excita'. Esta firma se utiliza para diagnosticar ciertos trastornos metabólicos, especialmente los que afectan al cerebro, y para proporcionar información sobre el metabolismo del tumor.
La imagen espectroscópica por resonancia magnética (MRSI) combina métodos espectroscópicos y de imagen para producir espectros espacialmente localizados desde dentro de la muestra o del paciente. La resolución espacial es mucho más baja (limitada por la SNR disponible), pero los espectros de cada vóxel contienen información sobre muchos metabolitos. Debido a que la señal disponible se usa para codificar información espacial y espectral, MRSI requiere una SNR alta que solo se puede lograr con intensidades de campo más altas (3 T y superiores). Los altos costos de adquisición y mantenimiento de la resonancia magnética con intensidades de campo extremadamente altas inhiben su popularidad. Sin embargo, se han propuesto algoritmos de software basados en sensores comprimidos recientes (p. ej.,, SAMV) para lograr una súper resolución sin requerir intensidades de campo tan altas.
IRM en tiempo real
La IRM en tiempo real hace referencia a la obtención continua de imágenes de objetos en movimiento (como el corazón) en tiempo real. Una de las muchas estrategias diferentes desarrolladas desde principios de la década de 2000 se basa en la resonancia magnética FLASH radial y la reconstrucción iterativa. Esto proporciona una resolución temporal de 20 a 30 ms para imágenes con una resolución en el plano de 1,5 a 2,0 mm. Las imágenes de precesión libre en estado estacionario equilibrado (bSSFP) tienen un mejor contraste de imagen entre la acumulación de sangre y el miocardio que la resonancia magnética FLASH, pero producirán un artefacto de bandas grave cuando la falta de homogeneidad B0 sea fuerte. Es probable que la resonancia magnética en tiempo real agregue información importante sobre enfermedades del corazón y las articulaciones y, en muchos casos, puede hacer que los exámenes de resonancia magnética sean más fáciles y cómodos para los pacientes, especialmente para los pacientes que no pueden contener la respiración o que tienen arritmia.
Resonancia magnética intervencionista
La falta de efectos nocivos para el paciente y el operador hacen que la resonancia magnética sea muy adecuada para la radiología intervencionista, donde las imágenes producidas por un escáner de resonancia magnética guían los procedimientos mínimamente invasivos. Dichos procedimientos no utilizan instrumentos ferromagnéticos.
Un subconjunto cada vez más especializado de resonancia magnética intervencionista es la resonancia magnética intraoperatoria, en la que se utiliza una resonancia magnética en la cirugía. Algunos sistemas de resonancia magnética especializados permiten obtener imágenes simultáneamente con el procedimiento quirúrgico. Más típicamente, el procedimiento quirúrgico se interrumpe temporalmente para que la resonancia magnética pueda evaluar el éxito del procedimiento o guiar el trabajo quirúrgico posterior.
Ultrasonido focalizado guiado por resonancia magnética
En la terapia guiada, los haces de ultrasonido enfocado de alta intensidad (HIFU) se enfocan en un tejido, que se controlan mediante imágenes térmicas de RM. Debido a la alta energía en el foco, la temperatura sube por encima de los 65 °C (150 °F), lo que destruye completamente el tejido. Esta tecnología puede lograr una ablación precisa del tejido enfermo. La resonancia magnética proporciona una vista tridimensional del tejido objetivo, lo que permite el enfoque preciso de la energía de ultrasonido. Las imágenes de RM proporcionan imágenes térmicas cuantitativas en tiempo real del área tratada. Esto permite al médico asegurarse de que la temperatura generada durante cada ciclo de energía ultrasónica sea suficiente para provocar la ablación térmica dentro del tejido deseado y, en caso contrario, adaptar los parámetros para garantizar un tratamiento eficaz.
Imágenes multinucleares
El hidrógeno tiene el núcleo que se visualiza con más frecuencia en la resonancia magnética porque está presente en gran cantidad en los tejidos biológicos y porque su alta relación giromagnética emite una señal fuerte. Sin embargo, cualquier núcleo con un espín nuclear neto podría potencialmente ser fotografiado con resonancia magnética. Dichos núcleos incluyen helio-3, litio-7, carbono-13, flúor-19, oxígeno-17, sodio-23, fósforo-31 y xenón-129. 23Na y 31P son naturalmente abundantes en el cuerpo, por lo que se pueden obtener imágenes directamente. Los isótopos gaseosos como 3He o 129Xe deben hiperpolarizarse y luego inhalarse, ya que su densidad nuclear es demasiado baja para producir una señal útil en condiciones normales. 17O y 19F se pueden administrar en cantidades suficientes en forma líquida (por ejemplo, 17O-agua) para que la hiperpolarización no sea necesaria. El uso de helio o xenón tiene la ventaja de reducir el ruido de fondo y, por lo tanto, aumentar el contraste de la imagen en sí, porque estos elementos normalmente no están presentes en los tejidos biológicos.
Además, el núcleo de cualquier átomo que tenga un espín nuclear neto y que esté unido a un átomo de hidrógeno podría potencialmente obtener imágenes a través de una resonancia magnética de transferencia de magnetización heteronuclear que generaría imágenes del núcleo de hidrógeno de alta relación giromagnética en lugar del núcleo de baja giromagnética. -relación del núcleo que está unido al átomo de hidrógeno. En principio, la resonancia magnética de transferencia de magnetización heteronuclear podría usarse para detectar la presencia o ausencia de enlaces químicos específicos.
La imagen multinuclear es principalmente una técnica de investigación en la actualidad. Sin embargo, las aplicaciones potenciales incluyen imágenes funcionales e imágenes de órganos que no se ven bien en resonancias magnéticas 1H (p. ej., pulmones y huesos) o como agentes de contraste alternativos. El 3He hiperpolarizado inhalado se puede utilizar para obtener imágenes de la distribución de los espacios de aire dentro de los pulmones. Las soluciones inyectables que contienen 13C o burbujas estabilizadas de 129Xe hiperpolarizado se han estudiado como agentes de contraste para imágenes de angiografía y perfusión. 31P puede potencialmente proporcionar información sobre la densidad y la estructura ósea, así como imágenes funcionales del cerebro. Las imágenes multinucleares tienen el potencial de trazar la distribución del litio en el cerebro humano, y este elemento encuentra uso como un fármaco importante para las personas con afecciones como el trastorno bipolar.
Imágenes moleculares por resonancia magnética
La resonancia magnética tiene las ventajas de tener una resolución espacial muy alta y es muy adecuada para la obtención de imágenes morfológicas y funcionales. Sin embargo, la resonancia magnética tiene varias desventajas. Primero, la resonancia magnética tiene una sensibilidad de alrededor de 10−3 mol/L a 10−5 mol/L, que, en comparación con otros tipos de imágenes, puede ser muy limitante. Este problema surge del hecho de que la diferencia de población entre los estados de espín nuclear es muy pequeña a temperatura ambiente. Por ejemplo, a 1,5 teslas, una intensidad de campo típica para la resonancia magnética clínica, la diferencia entre los estados de alta y baja energía es de aproximadamente 9 moléculas por 2 millones. Las mejoras para aumentar la sensibilidad de la RM incluyen el aumento de la fuerza del campo magnético y la hiperpolarización a través del bombeo óptico o la polarización nuclear dinámica. También hay una variedad de esquemas de amplificación de señales basados en el intercambio químico que aumentan la sensibilidad.
Para obtener imágenes moleculares de biomarcadores de enfermedades mediante resonancia magnética, se requieren agentes de contraste de resonancia magnética dirigidos con alta especificidad y alta relajación (sensibilidad). Hasta la fecha, se han dedicado muchos estudios al desarrollo de agentes de contraste dirigidos a MRI para lograr imágenes moleculares mediante MRI. Por lo general, se han aplicado péptidos, anticuerpos o ligandos pequeños y dominios de proteína pequeños, como aficuerpos HER-2, para lograr el direccionamiento. Para mejorar la sensibilidad de los agentes de contraste, estas fracciones de direccionamiento suelen estar vinculadas a agentes de contraste de MRI de alta carga útil o agentes de contraste de MRI con altas relajaciones. Se ha introducido una nueva clase de agentes de contraste de RM dirigidos a genes para mostrar la acción génica de proteínas de factor de transcripción de genes y ARNm únicos. Estos nuevos agentes de contraste pueden rastrear células con ARNm, microARN y virus únicos; respuesta tisular a la inflamación en cerebros vivos. El MR informa cambios en la expresión génica con correlación positiva con el análisis TaqMan, microscopía óptica y electrónica.
IRM paralela
Se necesita tiempo para recopilar datos de MRI mediante aplicaciones secuenciales de gradientes de campo magnético. Incluso para las secuencias de resonancia magnética más simplificadas, existen límites físicos y fisiológicos para la tasa de cambio de gradiente. La resonancia magnética paralela elude estos límites al recopilar una parte de los datos simultáneamente, en lugar de hacerlo de manera secuencial tradicional. Esto se logra utilizando conjuntos de bobinas detectoras de radiofrecuencia (RF), cada una con una 'vista' del cuerpo. Se aplica un conjunto reducido de pasos de gradiente y la información espacial restante se completa mediante la combinación de señales de varias bobinas, en función de sus patrones de sensibilidad espacial conocidos. La aceleración resultante está limitada por el número de bobinas y por la relación señal/ruido (que disminuye con el aumento de la aceleración), pero comúnmente se pueden lograr aceleraciones de dos a cuatro veces con configuraciones adecuadas de conjuntos de bobinas, y se han demostrado aceleraciones sustancialmente más altas. con matrices de bobinas especializadas. La resonancia magnética paralela se puede usar con la mayoría de las secuencias de resonancia magnética.
Después de que una serie de sugerencias iniciales para el uso de conjuntos de detectores para acelerar la obtención de imágenes pasaran desapercibidas en el campo de la resonancia magnética, las imágenes paralelas experimentaron un amplio desarrollo y aplicación tras la introducción de la técnica SiMultaneous Acquisition of Spatial Harmonics (SMASH) en 1996-1997.. Las técnicas SENSitivity Encoding (SENSE) y Generalized Autocalibrating Partially Parallel Acquisitions (GRAPPA) son los métodos de obtención de imágenes en paralelo de uso más común en la actualidad. El advenimiento de la RM paralela dio como resultado una amplia investigación y desarrollo en la reconstrucción de imágenes y el diseño de bobinas de RF, así como una rápida expansión del número de canales receptores disponibles en los sistemas de RM comerciales. La resonancia magnética paralela ahora se usa de forma rutinaria para exámenes de resonancia magnética en una amplia gama de áreas del cuerpo y aplicaciones clínicas o de investigación.
IRM cuantitativa
La mayoría de las resonancias magnéticas se centran en la interpretación cualitativa de los datos de RM mediante la adquisición de mapas espaciales de variaciones relativas en la intensidad de la señal que se "ponderan" por ciertos parámetros. En cambio, los métodos cuantitativos intentan determinar mapas espaciales de valores precisos de parámetros de relaxometría tisular o campo magnético, o medir el tamaño de ciertas características espaciales.
Ejemplos de métodos cuantitativos de MRI son:
- T1-mapping (notablemente utilizado en la resonancia magnética cardíaca)
- T2-mapping
- Cartografía de susceptibilidad cuantitativa (QSM)
- IRM de flujo de líquido cuantitativo (es decir, una IRM de flujo de líquido cefalorraquídeo)
- Elastografía de resonancia magnética (MRE)
La resonancia magnética cuantitativa tiene como objetivo aumentar la reproducibilidad de las imágenes e interpretaciones de resonancia magnética, pero históricamente ha requerido tiempos de exploración más largos.
La resonancia magnética cuantitativa (o qMRI) a veces se refiere más específicamente a la resonancia magnética cuantitativa multiparamétrica, el mapeo de múltiples parámetros de relaxometría tisular en una sola sesión de imágenes. Los esfuerzos para hacer que la resonancia magnética cuantitativa multiparamétrica sea más rápida ha producido secuencias que mapean múltiples parámetros simultáneamente, ya sea mediante la creación de métodos de codificación separados para cada parámetro en la secuencia, o ajustando la evolución de la señal de RM a un modelo multiparamétrico.
Resonancia magnética con gas hiperpolarizado
La resonancia magnética tradicional genera imágenes deficientes del tejido pulmonar porque hay menos moléculas de agua con protones que pueden ser excitadas por el campo magnético. Usando gas hiperpolarizado, una resonancia magnética puede identificar defectos de ventilación en los pulmones. Antes de la exploración, se le pide al paciente que inhale xenón hiperpolarizado mezclado con un gas amortiguador de helio o nitrógeno. Las imágenes pulmonares resultantes son de una calidad mucho mayor que con la resonancia magnética tradicional.
Seguridad
La resonancia magnética es, en general, una técnica segura, aunque pueden producirse lesiones como resultado de procedimientos de seguridad fallidos o errores humanos. Las contraindicaciones para la resonancia magnética incluyen la mayoría de los implantes cocleares y marcapasos cardíacos, metralla y cuerpos extraños metálicos en los ojos. La resonancia magnética en el embarazo parece ser segura, al menos durante el segundo y tercer trimestre si se realiza sin agentes de contraste. Dado que la resonancia magnética no utiliza ninguna radiación ionizante, su uso generalmente se prefiere a la TC cuando cualquiera de las dos modalidades podría proporcionar la misma información. Algunos pacientes experimentan claustrofobia y pueden requerir sedación o protocolos de resonancia magnética más breves. La amplitud y el cambio rápido de las bobinas de gradiente durante la adquisición de imágenes pueden causar estimulación de los nervios periféricos.
La resonancia magnética utiliza imanes potentes y, por lo tanto, puede hacer que los materiales magnéticos se muevan a gran velocidad, lo que representa un riesgo de proyectil y puede causar accidentes fatales. Sin embargo, dado que cada año se realizan millones de resonancias magnéticas en todo el mundo, las muertes son extremadamente raras.
Uso excesivo
Las sociedades médicas emiten pautas sobre cuándo los médicos deben usar la resonancia magnética en los pacientes y recomiendan que no se use en exceso. La resonancia magnética puede detectar problemas de salud o confirmar un diagnóstico, pero las sociedades médicas a menudo recomiendan que la resonancia magnética no sea el primer procedimiento para crear un plan para diagnosticar o manejar la queja de un paciente. Un caso común es utilizar la resonancia magnética para buscar la causa del dolor lumbar; el American College of Physicians, por ejemplo, desaconseja este procedimiento porque es poco probable que tenga un resultado positivo para el paciente.
Artefactos
Un artefacto de MRI es un artefacto visual, es decir, una anomalía durante la representación visual. Pueden ocurrir muchos artefactos diferentes durante la resonancia magnética nuclear (RMN), algunos afectan la calidad del diagnóstico, mientras que otros pueden confundirse con patología. Los artefactos se pueden clasificar como relacionados con el paciente, dependientes del procesamiento de señales y relacionados con el hardware (máquina).
Uso no médico
La resonancia magnética se utiliza industrialmente principalmente para el análisis de rutina de productos químicos. La técnica de resonancia magnética nuclear también se utiliza, por ejemplo, para medir la relación entre agua y grasa en los alimentos, monitorear el flujo de fluidos corrosivos en las tuberías o estudiar estructuras moleculares como los catalizadores.
Al ser no invasiva y no dañina, la resonancia magnética se puede utilizar para estudiar la anatomía de las plantas, sus procesos de transporte de agua y el equilibrio hídrico. También se aplica a la radiología veterinaria con fines de diagnóstico. Fuera de esto, su uso en zoología está limitado por su alto costo; pero se puede utilizar en muchas especies.
En paleontología se utiliza para examinar la estructura de los fósiles.
Las imágenes forenses proporcionan documentación gráfica de una autopsia, cosa que no ocurre con la autopsia manual. La tomografía computarizada proporciona imágenes rápidas de todo el cuerpo de las alteraciones esqueléticas y parenquimatosas, mientras que las imágenes de resonancia magnética brindan una mejor representación de la patología de los tejidos blandos. Pero la resonancia magnética es más costosa y lleva más tiempo utilizarla. Además, la calidad de las imágenes de RM se deteriora por debajo de los 10 °C.
Historia
En 1971, en la Universidad de Stony Brook, Paul Lauterbur aplicó gradientes de campo magnético en las tres dimensiones y una técnica de retroproyección para crear imágenes de RMN. Publicó las primeras imágenes de dos tubos de agua en 1973 en la revista Nature, seguidas por la imagen de un animal vivo, una almeja, y en 1974 por la imagen de la cavidad torácica de un ratón. Lauterbur llamó a su método de obtención de imágenes zeugmatografía, un término que fue reemplazado por imágenes (N)MR. A fines de la década de 1970, los físicos Peter Mansfield y Paul Lauterbur desarrollaron técnicas relacionadas con la resonancia magnética, como la técnica de imágenes ecoplanares (EPI).
Los avances en la tecnología de semiconductores fueron cruciales para el desarrollo de la resonancia magnética práctica, que requiere una gran cantidad de potencia computacional. Esto fue posible gracias al rápido aumento del número de transistores en un solo chip de circuito integrado. Mansfield y Lauterbur fueron galardonados con el Premio Nobel de Fisiología o Medicina en 2003 por sus "descubrimientos relacionados con la resonancia magnética".
Contenido relacionado
Psicofarmacología
Tono de instrumentos de metal
Analgésica(feminine)