Homocisteína
La homocisteína es un α-aminoácido no proteinogénico. Es un homólogo del aminoácido cisteína, diferenciándose por un puente metileno adicional (-CH2-). Se biosintetiza a partir de metionina mediante la eliminación de su grupo metilo Cε terminal. En el cuerpo, la homocisteína puede reciclarse en metionina o convertirse en cisteína con la ayuda de ciertas vitaminas B.
Los altos niveles de homocisteína en la sangre (hiperhomocisteinemia) se consideran un marcador de enfermedad cardiovascular, y probablemente actúan a través de la aterogénesis, lo que puede provocar una lesión isquémica. Por lo tanto, la hiperhomocisteinemia es un posible factor de riesgo para la enfermedad arterial coronaria. La enfermedad de las arterias coronarias ocurre cuando una placa aterosclerótica bloquea el flujo de sangre a las arterias coronarias, que suministran sangre oxigenada al corazón.
La hiperhomocisteinemia se ha relacionado con la aparición de coágulos de sangre, ataques cardíacos y accidentes cerebrovasculares, aunque no está claro si la hiperhomocisteinemia es un factor de riesgo independiente para estas afecciones. La hiperhomocisteinemia también se ha asociado con abortos espontáneos a término temprano y con defectos del tubo neural.
Estructura
La homocisteína existe en valores de pH neutros como un zwitterión.
Biosíntesis y funciones bioquímicas
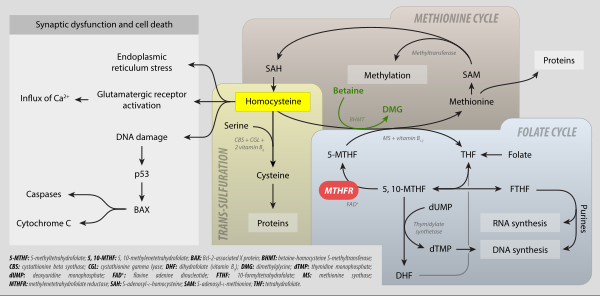
La homocisteína se biosintetiza de forma natural a través de un proceso de varios pasos. Primero, la metionina recibe un grupo adenosina del ATP, una reacción catalizada por la S-adenosil-metionina sintetasa, para dar S-adenosil metionina (SAM-e). SAM-e luego transfiere el grupo metilo a una molécula aceptora (p. ej., norepinefrina como aceptor durante la síntesis de epinefrina, ADN metiltransferasa como aceptor intermedio en el proceso de metilación del ADN). A continuación, la adenosina se hidroliza para producir L-homocisteína. La L-homocisteína tiene dos destinos principales: la conversión a través del tetrahidrofolato (THF) de nuevo en L-metionina o la conversión en L-cisteína.
Biosíntesis de cisteína
Los mamíferos biosintetizan el aminoácido cisteína a través de la homocisteína. La cistationina β-sintasa cataliza la condensación de homocisteína y serina para dar cistationina. Esta reacción utiliza piridoxina (vitamina B6) como cofactor. La cistationina γ-liasa luego convierte este doble aminoácido en cisteína, amoníaco y α-cetobutirato. Las bacterias y las plantas dependen de un camino diferente para producir cisteína, basándose en la O-acetilserina.
Metionina de rescate
La homocisteína se puede reciclar en metionina. Este proceso utiliza tetrahidrofolato de N5-metilo como donador de metilo y enzimas relacionadas con la cobalamina (vitamina B12). Se pueden encontrar más detalles sobre estas enzimas en el artículo sobre la metionina sintasa.
Otras reacciones de importancia bioquímica
La homocisteína puede ciclarse para dar homocisteína tiolactona, un heterociclo de cinco miembros. Debido a este "bucle automático" reacción, los péptidos que contienen homocisteína tienden a escindirse mediante reacciones que generan estrés oxidativo.
La homocisteína también actúa como un antagonista alostérico en los receptores de dopamina D2.
Se ha propuesto que tanto la homocisteína como su tiolactona pueden haber jugado un papel importante en la aparición de la vida en la Tierra primitiva.
Niveles de homocisteína
Los niveles de homocisteína suelen ser más altos en los hombres que en las mujeres y aumentan con la edad.
Los niveles comunes en las poblaciones occidentales son de 10 a 12 μmol/L, y se encuentran niveles de 20 μmol/L en poblaciones con ingestas bajas de vitamina B o en ancianos (p. ej., Rotterdam, Framingham).
Disminuye con la captura de metilfolato, donde se acompaña de una disminución del ácido metilmalónico, un aumento del folato y una disminución del ácido formiminoglutámico. Esto es lo contrario de las mutaciones MTHFR C677T, que dan como resultado un aumento de la homocisteína.
| Sexo | Edad | Límite inferior | Límite superior | Dependencia | Elevado | Objetivo terapéutico |
| Mujer | 12 a 19 años | 3.3 | 7.2 | μmol/L | ■ 10.4 μmol/L o Ø 140 μg/dl | μmol/L o μg/dL |
| 45 | 100 | μg/dL | ||||
| ■60 años | 4.9 | 11.6 | μmol/L | |||
| 66 | 160 | μg/dL | ||||
| Hombre | 12 a 19 años | 4.3 | 9.9 | μmol/L | Ø 11.4 μmol/L o Ø 150 μg/dL | |
| 60 | 130 | μg/dL | ||||
| ■60 años | 5.9 | 15.3 | μmol/L
+ TEN- | 80 | 210 | μg/dL |
Los rangos anteriores se proporcionan solo como ejemplos; los resultados de las pruebas siempre deben interpretarse utilizando el rango proporcionado por el laboratorio que produjo el resultado.
Homocisteína elevada
Los niveles anormalmente altos de homocisteína en el suero, por encima de 15 μmol/L, son una condición médica llamada hiperhomocisteinemia. Se ha afirmado que esto es un factor de riesgo significativo para el desarrollo de una amplia gama de enfermedades, que incluyen trombosis, enfermedades neuropsiquiátricas y fracturas. También se encuentra asociado con microalbuminuria, que es un fuerte indicador del riesgo de futuras enfermedades cardiovasculares y disfunción renal. Se ha descubierto que la deficiencia de vitamina B12, junto con niveles altos de folato sérico, también aumenta las concentraciones generales de homocisteína.
Por lo general, la hiperhomocisteinemia se trata con suplementos de vitamina B6, vitamina B9 y vitamina B12. Sin embargo, la suplementación con estas vitaminas no parece mejorar los resultados de la enfermedad cardiovascular.
Contenido relacionado
Quandong
EDE
Muerte clínica


