Historia de la reacción en cadena de la polimerasa
Contenido keyboard_arrow_down
- (Este artículo asume familiaridad con los términos y componentes utilizados en el proceso PCR.)
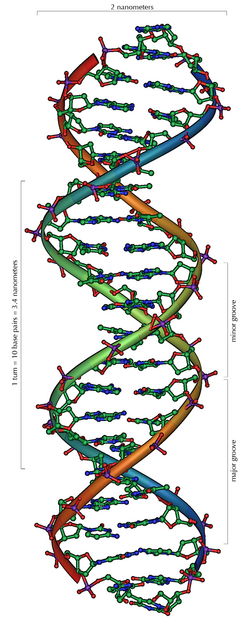
Estructura del ADN

Replicación de ADN

DNA Polymerase I (PDB)

Mecanismo molecular de PCR

Una tira de ocho tubos PCR
Preludio
- On 25 de abril de 1953 James D. Watson y Francis Crick publicaron "una estructura radicalmente diferente" para el ADN, fundando así el campo de la genética molecular. Su modelo estructural contó con dos hilos de ADN complementario de base, corriendo en direcciones opuestas como doble helix. Concluyeron su informe diciendo que "no ha escapado a nuestro aviso de que el emparejamiento específico que hemos postulado inmediatamente sugiere un posible mecanismo de copia del material genético". Para esta visión se les otorgó el Premio Nobel 1962.
- Comenzando en el mediados de 1950, Arthur Kornberg comenzó a estudiar el mecanismo de replicación de ADN. Por 1957 ha identificado la primera polimerasa de ADN. La enzima era limitada, creando ADN en una sola dirección y requiriendo una imprenta existente para iniciar la copia del hilo de plantilla. En general, el proceso de replicación de ADN es sorprendentemente complejo, requiriendo proteínas separadas para abrir el helix de ADN, mantenerlo abierto, crear cejas, sintetizar el ADN nuevo, eliminar las cartillas, y atar todas las piezas juntas. Kornberg recibió el Premio Nobel 1959.
- En el principios de 1960 H. Gobind Khorana hizo avances significativos en la elucidación del código genético. Posteriormente, inició un gran proyecto para sintetizar totalmente un gen humano funcional. Para lograrlo, Khorana fue pionero en muchas de las técnicas necesarias para hacer y utilizar oligonucleótidos de ADN sintéticos. Los oligonucleótidos específicos de secuencia se utilizaron como bloques de construcción para el gen, y como cartillas y plantillas para la polimerasa de ADN. In 1968 Khorana recibió el Premio Nobel por su trabajo en el Código Genético.
- In 1969 Thomas D. Brock reportó el aislamiento de una nueva especie de bacteria de una fuente caliente en el Parque Nacional Yellowstone. Thermus aquaticus (Taq) se convirtió en una fuente estándar de enzimas capaces de soportar temperaturas más altas que las de E. coli.
- In 1970 Klenow informó una versión modificada de ADN Polymerase I de E. coli. El tratamiento con una proteasa removió la actividad de la nucleasa de esta enzima. La actividad general del fragmento resultante de Klenow es, por tanto, sesgada hacia la síntesis del ADN, en lugar de su degradación.
- Por 1971 Investigadores en el proyecto de Khorana, preocupados por sus rendimientos de ADN, comenzaron a mirar "repair síntesis" – un sistema artificial de imprimaciones y plantillas que permite la polimerasa de ADN copiar segmentos del gen que están sintetizando. Aunque es similar al PCR en el uso de aplicaciones repetidas de polimerasa de ADN, el proceso que suelen describir emplea sólo un complejo de primer-templato único, y por lo tanto no conduciría a la amplificación exponencial vista en PCR.
- Circa 1971 Kjell Kleppe, investigador del laboratorio de Khorana, imaginó un proceso muy similar al PCR. Al final de un documento sobre la técnica anterior, describió cómo un sistema de dos primarias podría llevar a la replicación de un segmento específico de ADN:
- uno esperaría obtener dos estructuras, cada una conteniendo la longitud completa del hilo de plantilla adecuadamente complejo con el primer. La polimerasa de ADN se añadirá para completar el proceso de replicación de la reparación. Dos moléculas del dúplex original deben resultar. Todo el ciclo podría repetirse, cada vez se añade una dosis fresca de la enzima.
- No se muestran resultados allí, y la mención de experimentos inéditos en otro documento puede (o no puede) referirse al sistema de replicación de dos primarias. (Estos primeros precursores a PCR fueron cuidadosamente analizados en una demanda de patentes, y se discuten en los capítulos de Mullis en La reacción de la cadena de polimerasa (1994).
- También en 1971, Cetus Corporation fue fundada en Berkeley, California, por Ronald Cape, Peter Farley, y Donald Glaser. Inicialmente, la empresa diseñó microorganismos capaces de producir componentes utilizados en la fabricación de alimentos, productos químicos, vacunas o productos farmacéuticos. Después de mudarse a Emeryville, iniciaron proyectos relacionados con la nueva industria biotecnológica, principalmente la clonación y expresión de genes humanos, pero también el desarrollo de pruebas diagnósticas para mutaciones genéticas.
- In 1976 a DNA polimerase was isolated from T. aquaticus. Se encontró que retenía su actividad a temperaturas superiores a 75 °C.
- In 1977 Frederick Sanger reportó un método para determinar la secuencia de ADN. La técnica empleaba una cartilla de oligonucleótido, polimerasa de ADN y precursores de nucleótidos modificados que bloquean una mayor extensión del primer de manera dependiente de secuencias. Por esta innovación fue galardonado con el Premio Nobel 1980.
Tema
- In 1979 Cetus Corporation contrató a Kary Mullis para sintetizar oligonucleótidos para diversos proyectos de investigación y desarrollo en toda la empresa. Estos oligos se utilizaron como sondas para la detección de genes clonados, como cepas para secuenciación de ADN y síntesis de cDNA, y como bloques de construcción de genes. Originalmente sintetizando estos oligos a mano, Mullis posteriormente evaluó prototipos tempranos para sintetizadores automatizados.
- Por Mayo de 1983 Mullis sintetizó sondas oligonucleótido para un proyecto en Cetus para analizar una mutación de anemia falciforme. Escuchando problemas con su trabajo, Mullis propuso una técnica alternativa basada en el método de secuenciación de ADN de Sanger. Realizando la dificultad de hacer el método Sanger específico a una sola ubicación en el genoma, Mullis entonces modificó la idea de añadir una segunda cartilla en el hilo opuesto. Las aplicaciones repetidas de la polimerasa podrían llevar a una reacción en cadena de replicación para un segmento específico del genoma – PCR.
- Más tarde 1983 Mullis comenzó a probar su idea. Su primer experimento no implicaba el ciclismo térmico – esperaba que la polimerasa pudiera realizar la reproducción continua por su cuenta. Los experimentos posteriores de ese año incluyeron ciclos térmicos repetidos, y segmentaron pequeños segmentos de un gen clonado. Mullis consideró estos experimentos un éxito, pero no pudo convencer a otros investigadores.
- In Junio de 1984 Cetus celebró su reunión anual en Monterey, California. Sus científicos y consultores presentaron sus resultados y consideraron proyectos futuros. Mullis presentó un cartel sobre la producción de oligonucleótidos por su laboratorio, y presentó algunos de los resultados de sus experimentos con PCR. Sólo Joshua Lederberg, consultor de Cetus, mostró interés. Más tarde en la reunión, Mullis participó en un altercado físico con otro investigador de Cetus sobre una disputa no relacionada con PCR. El otro científico dejó la compañía, y Mullis fue eliminado como jefe del laboratorio de síntesis de oligo.
Desarrollo
- In Septiembre de 1984 Tom White, VP de Investigación en Cetus (y un amigo cercano), presionó a Mullis para tomar su idea al grupo desarrollando el ensayo de mutación genética. Juntos, pasaron los meses siguientes diseñando experimentos que podrían demostrar convincentemente que PCR está trabajando en ADN genómico. Desafortunadamente, el producto de amplificación esperado no era visible en la electroforesis de gel agarose, lo que llevó a confusión en cuanto a si la reacción era específica para la región específica.
- In Noviembre de 1984 los productos de amplificación fueron analizados por la hinchazón del sur, lo que demostró claramente el aumento de las cantidades del producto de ADN de 110 bp esperado. Teniendo la primera señal visible, los investigadores comenzaron a optimizar el proceso. Más tarde, los productos amplificados fueron clonados y secuenciados, mostrando que la mayoría del ADN amplificado era el objetivo deseado, y que el fragmento de Klenow se utilizaba sólo raramente incorporaba nucleótidos incorrectos durante la replicación.
Exposición
- Tras la práctica industrial normal, Mullis solicitó una patente que cubriera la idea básica de PCR y muchas aplicaciones potenciales, y fue pedido por la PTO para incluir más resultados. On 28 de marzo de 1985, el grupo de desarrollo de Mullis presentó una solicitud centrada en el análisis de la mutación de anemia falciforme a través de PCR y Oligomer restricción. Después de la modificación, ambas patentes fueron aprobadas 28 de julio de 1987.
- En el primavera de 1985 el grupo de desarrollo comenzó a aplicar la técnica PCR a otros objetivos. Las sondas y las sondas fueron diseñadas para un segmento variable del gen DQα del leucocito humano. Esta reacción fue mucho más específica que la del objetivo β-hemoglobina – el producto PCR esperado es directamente visible en la electroforesis de gel agarose. Los productos de amplificación de varias fuentes también fueron clonados y secuenciados, la primera determinación de nuevos alelos por PCR. Al mismo tiempo, la técnica original de ensayo de Restricción Oligomer fue reemplazada por el método más general de oligonucleótido específico Allele.
- También principios de 1985, el grupo comenzó a usar una polimerasa de ADN termostable (la enzima utilizada en la reacción original se destruye en cada paso de calentamiento). En ese momento sólo se habían descrito dos, de Taq y Bst. El informe sobre la polimerasa Taq fue más detallado, por lo que fue elegido para la prueba. La polimerasa Bst fue encontrada más tarde para PCR. Ese verano Mullis intentó aislar la enzima, y un grupo fuera de Cetus fue contratado para hacerlo, todo sin éxito. En el Fallo de 1985 Susanne Stoffel y David Gelfand en Cetus tienen éxito en hacer la polimerasa, y fue inmediatamente encontrado por Randy Saiki para apoyar el proceso PCR.
- Con patentes presentadas, el trabajo procedió a reportar PCR a la comunidad científica general. Un resumen para una reunión de la Sociedad Americana de Genética Humana en Salt Lake City fue presentado en Abril de 1985, y el primer anuncio de PCR fue hecho allí por Saiki en Octubre. Se planearon dos publicaciones: un documento "idea" de Mullis, y un documento de "aplicación" de todo el grupo de desarrollo. Mullis presentó su manuscrito a la revista Nature, que lo rechazó por no incluir resultados. El otro documento, principalmente describiendo el ensayo de análisis OR, fue presentado a Science on 20 de septiembre de 1985, y fue aceptado en noviembre. Después del rechazo del informe de Mullis en diciembre, los detalles sobre el proceso PCR se agregaron rápidamente al segundo documento, que aparece en 20 de diciembre de 1985.
- In Mayo de 1986 Mullis presentó PCR en el Simposio Cold Spring Harbor, y publicó una versión modificada de su manuscrito original 'idea' mucho más tarde. El primer informe no Cetus utilizando PCR fue presentado en 5 de septiembre de 1986, indicando lo rápido que otros laboratorios comenzaron a implementar la técnica. The Cetus development group published their detailed sequence analysis of PCR products on 8 de septiembre de 1986, y su uso de sondas ASO en 13 de noviembre de 1986.
- El uso de la polimerasa Taq en PCR fue anunciado por Henry Erlich en una reunión en Berlín sobre 20 de septiembre de 1986, presentado para su publicación en Octubre de 1987, y fue publicado a principios del próximo año '. La patente para PCR con polimerasa Taq fue presentada en 17 de junio de 1987, y se expidió 23 de octubre de 1990.
Variación
Coda
- On 22 de diciembre de 1989, la revista Science otorgó a Taq Polymerase (y PCR) su primera "Molécula del Año". El documento "Taq PCR" se convirtió durante varios años en la publicación más citada en biología.
- Después de la publicación del primer documento de PCR, el Gobierno de los Estados Unidos envió una carta severa a Randy Saiki, avisándole para publicar un informe sobre "reacciones de cadena" sin la revisión y aprobación previa requerida por el Departamento de Energía de los Estados Unidos. Cetus respondió, explicando las diferencias entre PCR y la bomba atómica.
- On 23 de julio de 1991, Cetus anunció que su venta a la vecina empresa biotecnológica Chiron. Como parte de la venta, los derechos a las patentes PCR se vendieron por US$300 millones a Hoffman-La Roche (quien en 1989 había adquirido derechos limitados a PCR). Muchos de los investigadores de Cetus PCR se trasladaron a la filial de Roche, Roche Molecular Systems.
- On 13 de octubre de 1993Kary Mullis, que había dejado Cetus en 1986, fue galardonado con el Premio Nobel de Química. En la mañana de su discurso de aceptación, fue arrestado por autoridades suecas por el "uso inapropiado de un puntero láser".
Referencias
- ^ a b c d Conferencia Nobel de Kary Mullis, 8 de diciembre de 1993
- ^ a b c d e Rabinow, Paul (1996). Hacer PCR: una historia de la biotecnología. Universidad de Chicago Press. ISBN 978-0-226-70146-2.
- ^ Watson JD, Crick FHC "A Structure for Deoxyribose Nucleic Acid", Nature vol. 171, págs. 737 a 738 (1953). [1]
- ^ (Arthur Kornberg's Discovery of DNA Polymerase I) J. Biol. Chem. vol. 280, p. 46. [2]
- ^ Lehman, IR, Bessman MJ, Simms ES, Kornberg A "Sintesis enzimática del ácido desoxiribonucleico. I. Preparación de Sustratos y Purificación Parcial de una Enzima de Escherichia coli" J. Biol. Chem. vol. 233(1) pp. 163–170 (1958).
- ^ Khorana HG et al. "Sintesis total del gen estructural para el precursor de una transferencia de supresor de tirosina RNA de Escherichia coli. 1. Introducción general" J. Biol. Chem. vol. 251(3) pp. 565–70 (1976).
- ^ Brock TD, Freeze H "Thermus aquaticus, a Nonsporulating Extreme Thermophile" J. Bacteriol. vol. 98(1) pp. 289–297 (1969).
- ^ Klenow H y Henningsen I "Selective Elimination of the Exonuclease Activity of the Deoxyribonucleic Acid Polymerase from Escherichia coli B by Limited Proteolysis" Proc Natl Acad Sci vol. 65 pp. 168–75 (1970).
- ^ a b Panet A, Khorana HG "Estudios en polinucleótidos" J. Biol. Chem. vol. 249(16), pp. 5213–21 (1974).
- ^ a b Kleppe K, Ohtsuka E, Kleppe R, Molineux I, Khorana HG "Estudios sobre polinucleótidos. XCVI. Reparación de réplicas de ADN sintético corto como catalizada por polimeras de ADN." J. Molec. Biol. vol. 56, págs. 341 a 61 (1971).
- ^ Mullis KB, Ferré F, Gibbs RA "La reacción de la cadena de polimerasa" Birkhäuser Press (1994) ISBN 0-8176-3750-8
- ^ a b Chien A, Edgar DB, Trela JM "Deoxyribonucleic acid polymerase from the extreme thermophile Thermus aquaticus" J. Bacteriol. vol. 174 pp. 1550–1557 (1976).
- ^ Sanger F, Nicklen S, Coulson AR "Secuencia de ADN con inhibidores de la cadena" Proc Natl Acad Sci vol. 74(12) pp. 5463–7 (1977).
- ^ a b c Mullis KB "The Unusual Origins of the Polymerase Chain Reaction" Scientific American, vol. 262, págs. 56 a 65 (abril de 1990).
- ^ a b c d e Scharf, Stephen; Horn, Glenn; Erlich, Henry (5 de septiembre de 1986). "Direct Cloning and Sequence Analysis of Enzymatically Amplified Genomic Sequences". Ciencia. 233 (4768): 1076 –8. doi:10.1126/science.3461561. PMID 3461561. Retrieved 8 de febrero 2024.
- ^ a b c Saiki RK et al. "Amplificación enzimática de β-globina Secuencias genómicas y Restricción Análisis del sitio para el diagnóstico de anemia de células secas" Science vol. 230 pp. 1350–54 (1985).
- ^ Mullis KB "Proceso para amplificar las secuencias de ácido nucleico." U.S. patent 4,683,202.
- ^ Mullis, KB et al. "Proceso para amplificar, detectar y/o cerrar secuencias de ácido nucleico." U.S. patent 4,683,195.
- ^ a b Saiki et al. "Análisis de ADN β-globina amplificada enzimáticamente y HLA DQα con sondas oligonucleótido específicas de alelo." Nature vol. 324 (6093) pp. 163–6 (1986).
- ^ Saiki, R et al. "A Novel Method for the Prenatal Diagnosis of Sickle Cell Anemia" Amer. Soc. Human Genetics, 9–13 de octubre de 1985.
- ^ Mullis KB et al. "Amplificación enzimática específica del ADN in vitro: la reacción de cadena de polimerasa". Coño de primavera frío. Biol. vol. 51 pp. 263–73 (1986).
- ^ Mullis KB y Faloona FA "Specific Synthesis of DNA in vitro via a Polymerase-Catalyzed Chain Reaction." Methods in Enzymology vol. 155(F) pp. 335–50 (1987).
- ^ Verlaan-de Vries M et al. "Un procedimiento de detección de manchas para ras oncogenes mutados utilizando oligodeoxinucleótidos sintéticos". Gene vol. 50(1–3) pp. 313–20 (1986).
- ^ a b c Saiki et al. "Amplificación enzimática dirigida por primitivo del ADN con una polimerasa de ADN termostable". Science vol. 239 pp. 487–91 (1988).
- ^ Mullis, KB et al. "Proceso para amplificar, detectar y/o clonar secuencias de ácido nucleico usando una enzima termostable". U.S. patent 4,965,188.
- ^ Kwok S et al. "Identificación de secuencias de VIH mediante la amplificación in vitro enzimática y detección de escote oligomer". J. Virol. vol. 61(5) pp. 1690–4 (1987).
- ^ Boehnke M et al. "La cartografía genética de estructura fina de los cromosomas humanos usando la reacción de cadena de polimerasa en un solo esperma". Am J Hum Genet vol. 45(1) pp. 21–32 (1989).
- ^ "Forensic Science Timeline (PDF)" (PDF). Archivado desde el original (PDF) el 2008-07-09. Retrieved 2008-04-12.
- ^ Jeffreys A et al. "Amplificación de minisatélites humanos". Nucleic Acids Research vol. 23 pp. 10953-71 (1988).
- ^ Higuchi R et al. "DNA escribiendo desde pelos individuales." Nature vol. 332(6164) pp. 543–6 (1988).
- ^ Mullis KB "Dancing Naked in the Mind Field" Pantheon Books (1998) ISBN 0-679-44255-3
Más resultados...