Hemodinámica
Hemodinámica o hemodinámica son las dinámicas del flujo sanguíneo. El sistema circulatorio está controlado por mecanismos homeostáticos de autorregulación, al igual que los circuitos hidráulicos están controlados por sistemas de control. La respuesta hemodinámica supervisa y se ajusta continuamente a las condiciones del cuerpo y su entorno. La hemodinámica explica las leyes físicas que gobiernan el flujo de sangre en los vasos sanguíneos.
El flujo sanguíneo asegura el transporte de nutrientes, hormonas, productos de desecho metabólicos, oxígeno y dióxido de carbono por todo el cuerpo para mantener el metabolismo a nivel celular, la regulación del pH, la presión osmótica y la temperatura de todo el cuerpo, y la protección del daño microbiano y mecánico.
La sangre es un fluido no newtoniano y se estudia de manera más eficiente mediante la reología en lugar de la hidrodinámica. Debido a que los vasos sanguíneos no son tubos rígidos, la hidrodinámica clásica y la mecánica de fluidos basada en el uso de viscosímetros clásicos no son capaces de explicar la hemodinámica.
El estudio del flujo sanguíneo se llama hemodinámica, y el estudio de las propiedades del flujo sanguíneo se llama hemorreología.
Sangre
La sangre es un líquido complejo. La sangre está compuesta de plasma y elementos formes. El plasma contiene 91,5% de agua, 7% de proteínas y 1,5% de otros solutos. Los elementos formados son plaquetas, glóbulos blancos y glóbulos rojos. La presencia de estos elementos formados y su interacción con las moléculas de plasma son las razones principales por las que la sangre difiere tanto de los fluidos newtonianos ideales.
Viscosidad del plasma
El plasma sanguíneo normal se comporta como un fluido newtoniano a velocidades de corte fisiológicas. Los valores típicos de la viscosidad del plasma humano normal a 37 °C son 1,4 mN·s/m2. La viscosidad del plasma normal varía con la temperatura de la misma manera que la de su disolvente agua; un aumento de temperatura de 5 °C en el rango fisiológico reduce la viscosidad del plasma en aproximadamente un 10 %.
Presión osmótica del plasma
La presión osmótica de la solución está determinada por el número de partículas presentes y por la temperatura. Por ejemplo, una solución 1 molar de una sustancia contiene 6.022×1023 moléculas por litro de esa sustancia y a 0 °C tiene una presión osmótica de 2,27 MPa (22,4 atm). La presión osmótica del plasma afecta la mecánica de la circulación de varias formas. Una alteración de la diferencia de presión osmótica a través de la membrana de un glóbulo provoca un desplazamiento del agua y un cambio del volumen celular. Los cambios de forma y flexibilidad afectan las propiedades mecánicas de la sangre entera. Un cambio en la presión osmótica del plasma altera el hematocrito, es decir, la concentración de volumen de glóbulos rojos en la sangre total al redistribuir el agua entre los espacios intravascular y extravascular. Esto a su vez afecta la mecánica de toda la sangre.
Glóbulos rojos
El glóbulo rojo es muy flexible y de forma bicóncava. Su membrana tiene un módulo de Young en la región de 106 Pa. La deformación en los glóbulos rojos es inducida por el esfuerzo cortante. Cuando se corta una suspensión, los glóbulos rojos se deforman y giran debido al gradiente de velocidad, y la velocidad de deformación y giro depende de la velocidad de corte y la concentración. Esto puede influir en la mecánica de la circulación y puede complicar la medición de la viscosidad de la sangre. Es cierto que en un flujo en estado estacionario de un fluido viscoso a través de un cuerpo esférico rígido sumergido en el fluido, donde asumimos que la inercia es despreciable en tal flujo, se cree que la fuerza gravitatoria hacia abajo de la partícula está balanceada por la fuerza de arrastre viscoso. A partir de este equilibrio de fuerzas, se puede demostrar que la velocidad de caída está dada por Stokes' ley
- Us=29()*** *** p− − *** *** f)μ μ ga2{displaystyle U_{s}={frac {2}{9}{frac {rho _{p}-rho _{f}}{mu }g,a^{2}} {}}} {c}} {cH0}} {cH0}} {cH0}} {cH0}} {ccH00}}}}} {cH0}}}}}}}}} {ccccccccH00}}}}}}}}}}} {ccccccccccccccccccccccH00}cH00}}}}}}ccccH00}cH00cccccH00}}}}cH00}}cH00}}}cH00}}}}}}}}}}}}}}}}
Donde a es el radio de la partícula, ρp, ρf son respectivamente la densidad de partículas y del fluido μ es la viscosidad del fluido, g es la aceleración gravitatoria. De la ecuación anterior podemos ver que la velocidad de sedimentación de la partícula depende del cuadrado del radio. Si la partícula se libera desde el reposo en el fluido, su velocidad de sedimentación Us aumenta hasta que alcanza el valor constante llamado velocidad terminal (U), como se muestra arriba.
Hemodilución
La hemodilución es la dilución de la concentración de glóbulos rojos y constituyentes del plasma mediante la sustitución parcial de la sangre por coloides o cristaloides. Es una estrategia para evitar la exposición de los pacientes a los peligros potenciales de las transfusiones de sangre homóloga.
La hemodilución puede ser normovolémica, lo que implica la dilución de los constituyentes normales de la sangre mediante el uso de expansores. Durante la hemodilución normovolémica aguda (ANH), la sangre perdida posteriormente durante la cirugía contiene proporcionalmente menos glóbulos rojos por mililitro, lo que minimiza la pérdida intraoperatoria de sangre completa. Por lo tanto, la sangre perdida por el paciente durante la cirugía no la pierde realmente el paciente, ya que este volumen se purifica y se redirige al paciente.
Por otro lado, la hemodilución hipervolémica (HVH) utiliza la expansión de volumen preoperatoria aguda sin extracción de sangre. Al elegir un fluido, sin embargo, se debe asegurar que cuando se mezcla, la sangre restante se comporta en la microcirculación como en el fluido sanguíneo original, conservando todas sus propiedades de viscosidad.
Al presentar qué volumen de ANH se debe aplicar, un estudio sugiere un modelo matemático de ANH que calcula el ahorro máximo posible de RCM usando ANH, dado el peso de los pacientes Hi y Hm.
Para mantener la normovolemia, la extracción de sangre autóloga debe ser sustituida simultáneamente por un hemodiluido adecuado. Idealmente, esto se logra mediante transfusión de intercambio de isovolemia de un sustituto de plasma con una presión osmótica coloidal (OP). Un coloide es un fluido que contiene partículas lo suficientemente grandes como para ejercer una presión oncótica a través de la membrana microvascular. Cuando se debate el uso de coloides o cristaloides, es imperativo pensar en todos los componentes de la ecuación de Starling:
- Q=K()[Pc− − Pi]S− − [Pc− − Pi]){displaystyle Q=K([P_{c}-P_{i}]S-[P_{c}-P_{i})}
Para identificar el hematocrito mínimo seguro deseable para un paciente determinado, la siguiente ecuación es útil:
- BLs=EBVIn HiHm{displaystyle BL_{s}=EBVln {frac {H_{i} {H_{m}}} {H_{i}} {H_} {H_}} {H_{m}}}} {H_}}} {} {}}} {}} {}}} {}} {}}} {}}} {}}}} {H_} {}}}} {}}}}} {}}}}}}}}} {} {}}}}}}}}}}}} {} {}} {}}}}}}}}}}}} {H_}}}}}} {} {}}}}} {}}}}}}}}}}}}}}}}}} {} {}}}}}} {H_} {} {}} {} {}}}}} {}}}}}}} {}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}} {
donde EBV es el volumen sanguíneo estimado; Se usaron 70 ml/kg en este modelo y h i (hematocrito inicial) es el hematocrito inicial del paciente.
De la ecuación anterior, está claro que el volumen de sangre eliminado durante el ANH hasta el H M es el mismo que el bl s .
La cantidad de sangre se eliminará generalmente se basa en el peso, no en el volumen. El número de unidades que deben eliminarse a hemodilute al hematocrito máximo seguro (ANH) se puede encontrar mediante
- ANH=BLs450{displaystyle ANH={frac {fnK} {fnK}}} {fnK}}}}}} {fnK}}}}}}}}} {fnK}}}}}}}}}} {fnK}}}}}}}}}}}}}}}}}}}} {f}}}}}}}}
Esto se basa en la suposición de que cada unidad extraída por hemodilución tiene un volumen de 450 ml (el volumen real de una unidad variará un poco, ya que la finalización de la recogida depende del peso y no del volumen). El modelo asume que el valor de hemodilución es igual al Hm previo a la cirugía, por lo tanto, la retransfusión de sangre obtenida por hemodilución debe comenzar cuando se inicia la LPS. El RCM disponible para la retransfusión después de la ANH (RCMm) se puede calcular a partir del Hi del paciente y el hematocrito final después de la hemodilución (H m)
- RCM=EVB× × ()Hi− − Hm){displaystyle RCM=EVBtimes (H_{i}-H_{m}}
La SBL máxima que es posible cuando se usa ANH sin caer por debajo de Hm (BLH) se encuentra suponiendo que toda la sangre extraída durante ANH se devuelve al paciente a una velocidad suficiente para mantener el hematocrito en el nivel mínimo seguro
- BLH=RCMHHm{displaystyle BL_{H}={frac {R} {H_}}} {H_}}}}}
Si se usa ANH siempre que SBL no exceda BLH, no habrá necesidad de transfusión de sangre. Podemos concluir de lo anterior que H por lo tanto no debe exceder s. Por lo tanto, la diferencia entre el BLH y el BLs es la pérdida de sangre quirúrgica incremental (BL i) posible cuando se usa ANH.
- BLi=BLH− − BLs{displaystyle {cH} {cH} {cH} {cH}} {cH}}} {cH}} {cH}}}} {cH}}}}} {cH}}}}}}}}}} {cH}
When expressed in terms of the RCMp>
- RCMi=BLi× × Hm{displaystyle {RCM_{i}={BL_{i}times {H_{m}}
Donde RCMi es la masa de glóbulos rojos que habría que administrar usando sangre homóloga para mantener la Hm si no se usa ANH y la pérdida de sangre es igual a BLH.
El modelo utilizado asume la ANH utilizada para un paciente de 70 kg con un volumen de sangre estimado de 70 ml/kg (4900 ml). Se evaluó un rango de Hi y Hm para comprender las condiciones en las que la hemodilución es necesaria para beneficiar al paciente.
Resultado
El resultado de los cálculos del modelo se presenta en una tabla proporcionada en el apéndice para un rango de Hi de 0,30 a 0,50 con ANH realizada a hematocritos mínimos de 0,30 a 0,15. Dado un Hi de 0,40, si se supone que Hm es 0,25, entonces a partir de la ecuación anterior el recuento de RCM sigue siendo alto y la ANH no es necesaria, si BLs no supera los 2303 ml, ya que el hematocrito no bajará de Hm, aunque cinco unidades de sangre debe eliminarse durante la hemodilución. En estas condiciones, para conseguir el máximo beneficio de la técnica si se utiliza ANH, no se requerirá sangre homóloga para mantener el Hm si la pérdida de sangre no supera los 2940 ml. En tal caso, la ANH puede ahorrar un máximo de 1,1 unidades equivalentes de concentrados de glóbulos rojos, y es necesaria una transfusión de sangre homóloga para mantener Hm, incluso si se utiliza la ANH. Este modelo se puede usar para identificar cuándo se puede usar ANH para un paciente determinado y el grado de ANH necesario para maximizar ese beneficio.
Por ejemplo, si Hi es 0,30 o menos, no es posible guardar una masa de glóbulos rojos equivalente a dos unidades de glóbulos rojos homólogos incluso si el paciente está hemodiluido a una Hm de 0,15. Esto se debe a que, a partir de la ecuación de RCM, el RCM del paciente se queda corto con respecto a la ecuación anterior. Si Hi es 0,40, se deben extraer al menos 7,5 unidades de sangre durante la ANH, lo que da como resultado un Hm de 0,20 para ahorrar dos unidades de equivalencia. Claramente, cuanto mayor es la Hi y mayor el número de unidades extraídas durante la hemodilución, más eficaz es la ANH para prevenir la transfusión de sangre homóloga. El modelo aquí está diseñado para permitir a los médicos determinar dónde la ANH puede ser beneficiosa para un paciente en función de su conocimiento de la Hi, el potencial de SBL y una estimación de la Hm. Aunque el modelo usó un paciente de 70 kg, el resultado se puede aplicar a cualquier paciente. Para aplicar estos resultados a cualquier peso corporal, cualquiera de los valores BLs, BLH y ANHH o PRBC dados en la tabla necesita ser multiplicado por el factor que llamaremos T
- T=peso del paciente en kg70{displaystyle T={frac {text{patient's weight in kg}{70}}
Básicamente, el modelo considerado anteriormente está diseñado para predecir el RCM máximo que puede salvar a la ANH.
En resumen, la eficacia de la ANH se ha descrito matemáticamente mediante mediciones de la pérdida de sangre quirúrgica y la medición del flujo de volumen de sangre. Esta forma de análisis permite una estimación precisa de la eficiencia potencial de las técnicas y muestra la aplicación de la medición en el campo médico.
Flujo sanguíneo
Gasto cardíaco
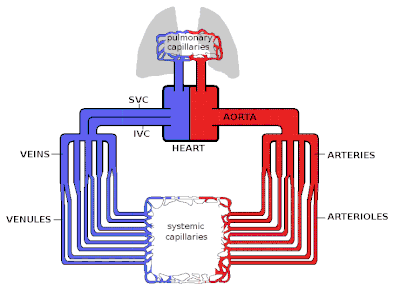
El corazón es el conductor del sistema circulatorio, bombeando sangre a través de la contracción y relajación rítmicas. La tasa de flujo de sangre que sale del corazón (a menudo expresada en L/min) se conoce como gasto cardíaco (CO).
La sangre que sale del corazón entra primero en la aorta, la arteria más grande del cuerpo. Luego procede a dividirse en arterias cada vez más pequeñas, luego en arteriolas y finalmente en capilares, donde se produce la transferencia de oxígeno. Los capilares se conectan a las vénulas y la sangre luego viaja de regreso a través de la red de venas hacia el lado derecho del corazón. La microcirculación (arteriolas, capilares y vénulas) constituye la mayor parte del área del sistema vascular y es el sitio de transferencia de O2, glucosa y sustratos enzimáticos a las células. El sistema venoso devuelve la sangre desoxigenada al corazón derecho donde se bombea a los pulmones para oxigenarse y CO2 y otros desechos gaseosos intercambiados y expulsados durante la respiración. Luego, la sangre regresa al lado izquierdo del corazón donde comienza el proceso nuevamente.
En un sistema circulatorio normal, el volumen de sangre que regresa al corazón cada minuto es aproximadamente igual al volumen que se bombea cada minuto (el gasto cardíaco). Debido a esto, la velocidad del flujo sanguíneo a través de cada nivel del sistema circulatorio está determinada principalmente por el área transversal total de ese nivel.
El gasto cardíaco se determina mediante dos métodos. Una es usar la ecuación de Fick:
CO=VO2/CaO2− − CvO2{displaystyle CO=VO2/C_{a}O_{2}-C_{v}O_{2}
El otro método de termodilución es detectar el cambio de temperatura de un líquido inyectado en el puerto proximal de un Swan-Ganz al puerto distal.
El gasto cardíaco se expresa matemáticamente mediante la siguiente ecuación:
- CO=SV× × HR{displaystyle CO=SVtimes ¡Risas!
dónde
- CO = salida cardiaca (L/sec)
- SV = volumen de trazo (ml)
- HR = frecuencia cardíaca (bpm)
El gasto cardíaco humano normal es de 5 a 6 l/min en reposo. No toda la sangre que ingresa al ventrículo izquierdo sale del corazón. Lo que queda al final de la diástole (EDV) menos el volumen sistólico constituyen el volumen sistólico final (ESV).
Características anatómicas
El sistema circulatorio de especies sujetas a presión arterial ortostática (como las serpientes arborícolas) ha evolucionado con características fisiológicas y morfológicas para superar la alteración circulatoria. Por ejemplo, en las serpientes arbóreas el corazón está más cerca de la cabeza, en comparación con las serpientes acuáticas. Esto facilita la perfusión de sangre al cerebro.
Turbulencia
El flujo sanguíneo también se ve afectado por la suavidad de los vasos, lo que da como resultado un flujo turbulento (caótico) o laminar (suave). La tersura se reduce por la acumulación de depósitos grasos en las paredes arteriales.
El número de Reynolds (denominado NR o Re) es una relación que ayuda a determinar el comportamiento de un fluido en un tubo, en este caso sangre en el vaso.
La ecuación para esta relación adimensional se escribe como:
- NR=*** *** vLμ μ {displaystyle NR={frac {rho vL}{mu }
- ***: densidad de la sangre
- v: velocidad media de la sangre
- L: dimensión característica del vaso, en este caso diámetro
- μ: viscosidad de sangre
El número de Reynolds es directamente proporcional a la velocidad y el diámetro del tubo. Tenga en cuenta que NR es directamente proporcional a la velocidad media, así como al diámetro. Un número de Reynolds inferior a 2300 es flujo de fluido laminar, que se caracteriza por un movimiento de flujo constante, mientras que un valor superior a 4000 se representa como flujo turbulento. Debido a su radio más pequeño y su velocidad más baja en comparación con otros recipientes, el número de Reynolds en los capilares es muy bajo, lo que da como resultado un flujo laminar en lugar de turbulento.
Velocidad
A menudo se expresa en cm/s. Este valor está inversamente relacionado con el área transversal total del vaso sanguíneo y también difiere según la sección transversal, porque en condiciones normales el flujo sanguíneo tiene características laminares. Por esta razón, la velocidad del flujo sanguíneo es más rápida en el medio del vaso y más lenta en la pared del vaso. En la mayoría de los casos, se utiliza la velocidad media. Hay muchas formas de medir la velocidad del flujo sanguíneo, como la microscopía videocapilar con análisis cuadro a cuadro o la anemometría láser Doppler. Las velocidades de la sangre en las arterias son más altas durante la sístole que durante la diástole. Un parámetro para cuantificar esta diferencia es el índice de pulsatilidad (PI), que es igual a la diferencia entre la velocidad sistólica máxima y la velocidad diastólica mínima dividida por la velocidad media durante el ciclo cardíaco. Este valor disminuye con la distancia al corazón.
- PI=vsSí.stole− − vdiastolevmean{displaystyle PI={frac {v_{systole}-v_{diastole} {v_{mean}}}
| Tipo de vasos sanguíneos | Superficie total de la sección transversal | Velocidad de sangre en cm/s |
|---|---|---|
| Aorta | 3-5 cm2 | 40 cm/s |
| Capillaries | 4500-6000 cm2 | 0,03 cm/s |
| Vena cavae inferior y superior | 14 cm2 | 15 cm/s |
Vasos sanguíneos
Resistencia vascular
La resistencia también está relacionada con el radio del vaso, la longitud del vaso y la viscosidad de la sangre.
En una primera aproximación basada en fluidos, como indica la ecuación de Hagen-Poiseuille. La ecuación es la siguiente:
- Δ Δ P=8μ μ lQπ π r4{displaystyle Delta P={frac {8mu lQ}{pi r^{4}}}
- ▪P: gota de presión/gradiente
- μ: viscosidad
- l: longitud de tubo. En el caso de los vasos con longitudes infinitamente largas, l es reemplazado con diámetro del vaso.
- Q: caudal de la sangre en el vaso
- r: radio de la nave
En un segundo enfoque, más realista de la resistencia vascular y proveniente de observaciones experimentales sobre los flujos sanguíneos, según Thurston, hay una capa de células de liberación de plasma en las paredes que rodean un flujo obstruido. Es una capa fluida en la que a una distancia δ, la viscosidad η es una función de δ escrita como η(δ), y estas capas circundantes no se encuentran en el centro del vaso en el flujo sanguíneo real. En cambio, existe el flujo obstruido que es hiperviscoso porque contiene una alta concentración de glóbulos rojos. Thurston ensambló esta capa con la resistencia al flujo para describir el flujo sanguíneo por medio de una viscosidad η(δ) y un espesor δ de la capa de la pared.
La ley de resistencia sanguínea aparece como R adaptada al perfil de flujo sanguíneo:
- R=cL.. ()δ δ )()π π δ δ r3){displaystyle R={frac {ceta (delta)}{(pi delta r^{3}}}}}
dónde
- R = resistencia al flujo sanguíneo
- c = coeficiente constante de flujo
- L = longitud del vaso
- (δ) = viscosidad de la sangre en la pared de liberación de células de plasma
- r = radio del vaso sanguíneo
- δ = distancia en la capa de células de liberación de plasma
La resistencia de la sangre varía según la viscosidad de la sangre y el tamaño de su flujo obstruido (o flujo de vaina, ya que son complementarios en la sección del vaso), así como del tamaño de los vasos. Suponiendo un flujo laminar constante en el vaso, el comportamiento de los vasos sanguíneos es similar al de una tubería. Por ejemplo, si p1 y p2 son presiones en los extremos del tubo, la caída/gradiente de presión es:
- p1− − p2l=Δ Δ P{fnMicroc} {p_{1}-p_{2} {l}}= Delta P}
Las arterias más grandes, incluidas todas lo suficientemente grandes como para verlas sin aumento, son conductos con baja resistencia vascular (suponiendo que no haya cambios ateroscleróticos avanzados) con altas tasas de flujo que generan solo pequeñas caídas de presión. Las arterias y arteriolas más pequeñas tienen mayor resistencia y confieren la principal caída de presión arterial a través de las arterias principales a los capilares del sistema circulatorio.

En las arteriolas la presión arterial es más baja que en las arterias principales. Esto se debe a las bifurcaciones, que provocan una caída de presión. Cuantas más bifurcaciones, mayor es el área de la sección transversal total, por lo tanto, la presión a través de la superficie cae. Esta es la razón por la cual las arteriolas tienen la caída de presión más alta. La caída de presión de las arteriolas es el producto del caudal y la resistencia: ∆P=Q x resistencia. La alta resistencia observada en las arteriolas, que tiene en cuenta en gran medida la ∆P, es el resultado de un radio más pequeño de aproximadamente 30 µm. Cuanto menor sea el radio de un tubo, mayor será la resistencia al flujo de fluido.
Inmediatamente después de las arteriolas se encuentran los capilares. Siguiendo la lógica observada en las arteriolas, esperamos que la presión arterial sea más baja en los capilares en comparación con las arteriolas. Dado que la presión es una función de la fuerza por unidad de área, (P = F/A), cuanto mayor sea el área de superficie, menor será la presión cuando una fuerza externa actúa sobre él. Aunque los radios de los capilares son muy pequeños, la red de capilares tiene el área superficial más grande de la red vascular. Se sabe que tienen el área de superficie más grande (485 mm ^ 2) en la red vascular humana. Cuanto mayor sea el área transversal total, menor será la velocidad media y la presión.
Las sustancias llamadas vasoconstrictores pueden reducir el tamaño de los vasos sanguíneos y, por lo tanto, aumentar la presión arterial. Los vasodilatadores (como la nitroglicerina) aumentan el tamaño de los vasos sanguíneos, lo que reduce la presión arterial.
Si aumenta la viscosidad de la sangre (se vuelve más espesa), el resultado es un aumento de la presión arterial. Ciertas condiciones médicas pueden cambiar la viscosidad de la sangre. Por ejemplo, la anemia (concentración baja de glóbulos rojos) reduce la viscosidad, mientras que el aumento de la concentración de glóbulos rojos aumenta la viscosidad. Se pensaba que la aspirina y los 'anticoagulantes' relacionados las drogas disminuyeron la viscosidad de la sangre, pero en cambio los estudios encontraron que actúan reduciendo la tendencia de la sangre a coagularse.
Para determinar la resistencia vascular sistémica (RVS) se utiliza la fórmula para calcular todas las resistencias.
R=()Δ Δ pressure)/flow.{displaystyle R=(Delta pressure)/flow.}
Esto se traduce para SVR en:
SVR=()MAP− − CVP)/CO{displaystyle SVR=(MAP-CVP)/CO}
Dónde
- SVR = resistencia vascular sistémica (mmHg/L/min)
- MAP = presión arterial media (mmHg)
- CVP = presión venosa central (mmHg)
- CO = salida cardiaca (L/min)
Para obtener esto en unidades de madera, la respuesta se multiplica por 80.
La resistencia vascular sistémica normal se encuentra entre 900 y 1440 dinas/seg/cm−5.
Tensión de pared

Independientemente del sitio, la presión arterial está relacionada con la tensión de la pared del vaso según la ecuación de Young-Laplace (suponiendo que el grosor de la pared del vaso es muy pequeño en comparación con el diámetro de la luz):
- σ σ Silencio Silencio =Prt{displaystyle sigma _{theta }={dfrac {Pr} { t}f}
dónde
- P es la presión arterial
- t es el espesor de la pared
- r es el radio interior del cilindro.
- σ σ Silencio Silencio {displaystyle sigma _{theta }! es el estrés del cilindro o "estrés rápido".
Para que la suposición de paredes delgadas sea válida, el recipiente debe tener un espesor de pared de no más de una décima parte (a menudo citado como una vigésima parte) de su radio.
La tensión del cilindro, a su vez, es la fuerza promedio ejercida circunferencialmente (perpendicular tanto al eje como al radio del objeto) en la pared del cilindro, y se puede describir como:
- σ σ Silencio Silencio =Ftl{displaystyle sigma _{theta - Sí.
donde:
- F es la fuerza ejercida circunferencialmente en una zona de la pared del cilindro que tiene las siguientes dos longitudes como lados:
- t es el espesor radial del cilindro
- l es la longitud axial del cilindro
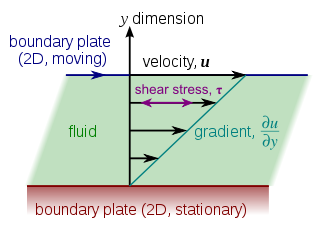
Estrés
Cuando se aplica fuerza a un material, comienza a deformarse o moverse. Como la fuerza necesaria para deformar un material (por ejemplo, para hacer fluir un fluido) aumenta con el tamaño de la superficie del material A, la magnitud de esta fuerza F es proporcional al área A de la porción de la superficie. Por lo tanto, la cantidad (F/A) que es la fuerza por unidad de área se llama tensión. El esfuerzo cortante en la pared que se asocia con el flujo de sangre a través de una arteria depende del tamaño y la geometría de la arteria y puede oscilar entre 0,5 y 4 Pa.
- σ σ =FA{displaystyle sigma ={frac {F}{A}}.
En condiciones normales, para evitar la aterogénesis, la trombosis, la proliferación del músculo liso y la apoptosis endotelial, la tensión de cizallamiento mantiene su magnitud y dirección dentro de un rango aceptable. En algunos casos que ocurren debido al golpe de sangre, el esfuerzo cortante alcanza valores mayores. Mientras que la dirección del estrés también puede cambiar por el flujo inverso, dependiendo de las condiciones hemodinámicas. Por lo tanto, esta situación puede conducir a la enfermedad de aterosclerosis.
Capacidad
Las venas se describen como los "vasos de capacitancia" del cuerpo porque más del 70% del volumen sanguíneo reside en el sistema venoso. Las venas son más distensibles que las arterias y se expanden para adaptarse a los cambios de volumen.
Presión arterial
La presión sanguínea en la circulación se debe principalmente a la acción de bombeo del corazón. La acción de bombeo del corazón genera un flujo sanguíneo pulsátil, que se conduce a las arterias, a través de la microcirculación y, finalmente, de vuelta al corazón a través del sistema venoso. Durante cada latido del corazón, la presión sanguínea arterial sistémica varía entre una presión máxima (sistólica) y una mínima (diastólica). En fisiología, a menudo se simplifican en un solo valor, la presión arterial media (PAM), que se calcula de la siguiente manera:
MAP=DP+1/3()PP){displaystyle MAP=DP+1/3(PP)}
donde:
- MAP = Presión Arterial media
- DP = Presión arterial diastólica
- PP = Presión de pulso que es presión sistólica menos presión diastólica.
Las diferencias en la presión arterial media son responsables del flujo sanguíneo de un lugar a otro en la circulación. La tasa de flujo sanguíneo medio depende tanto de la presión arterial como de la resistencia al flujo que presentan los vasos sanguíneos. La presión arterial media disminuye a medida que la sangre circulante se aleja del corazón a través de las arterias y los capilares debido a las pérdidas viscosas de energía. La presión arterial media cae en toda la circulación, aunque la mayor parte de la caída se produce a lo largo de las arterias y arteriolas pequeñas. La gravedad afecta la presión arterial a través de las fuerzas hidrostáticas (p. ej., al estar de pie), y las válvulas en las venas, la respiración y el bombeo por la contracción de los músculos esqueléticos también influyen en la presión arterial en las venas.
La relación entre presión, flujo y resistencia se expresa en la siguiente ecuación:
- Flow=Pressure/Resistance{displaystyle Flow=Pressure/Resistance}
Cuando se aplica al sistema circulatorio, obtenemos:
- CO=()MAP− − RAP)/TPR{displaystyle CO=(MAP-RAP)/TPR}
dónde
- CO = salida cardíaca (en L/min)
- MAP = presión arterial media (en mmHg), la presión media de la sangre mientras deja el corazón
- RAP = presión auricular derecha (en mmHg), la presión media de la sangre mientras regresa al corazón
- TPR = resistencia periférica total (en mmHg * min/L)
Una forma simplificada de esta ecuación supone que la presión de la aurícula derecha es aproximadamente 0:
- CO.. MAP/TPR{displaystyle COapprox MAP/TPR}
La presión arterial ideal en la arteria braquial, donde los manguitos de presión arterial estándar miden la presión, es <120/80 mmHg. Otras arterias principales tienen niveles similares de registros de presión arterial que indican disparidades muy bajas entre las arterias principales. En la arteria innominada, la lectura promedio es de 110/70 mmHg, la arteria subclavia derecha tiene un promedio de 120/80 y la aorta abdominal es de 110/70 mmHg. La presión relativamente uniforme en las arterias indica que estos vasos sanguíneos actúan como un depósito de presión para los fluidos que se transportan dentro de ellos.
La presión cae gradualmente a medida que la sangre fluye desde las arterias principales, a través de las arteriolas, los capilares hasta que la sangre regresa al corazón a través de las vénulas, las venas a través de la vena cava con la ayuda de los músculos. En cualquier caída de presión dada, la tasa de flujo está determinada por la resistencia al flujo de sangre. En las arterias, con la ausencia de enfermedades, hay muy poca o ninguna resistencia a la sangre. El diámetro del vaso es el principal determinante para controlar la resistencia. En comparación con otros vasos más pequeños del cuerpo, la arteria tiene un diámetro mucho mayor (4 mm), por lo que la resistencia es baja.
El gradiente brazo-pierna (presión arterial) es la diferencia entre la presión arterial medida en los brazos y la medida en las piernas. Normalmente es inferior a 10 mm Hg, pero puede aumentar, p. coartación de la aorta.
Importancia clínica
Monitoreo de presión

La monitorización hemodinámica es la observación de los parámetros hemodinámicos a lo largo del tiempo, como la presión arterial y la frecuencia cardíaca. La presión arterial se puede controlar de forma invasiva a través de un conjunto de transductor de presión arterial insertado (que proporciona un control continuo) o de forma no invasiva midiendo repetidamente la presión arterial con un manguito de presión arterial inflable.
La hipertensión se diagnostica por la presencia de presiones arteriales de 140/90 o más durante dos visitas clínicas.
Did you mean:Pulmonary Artery Wedge Pressure can show if there is congestive heart failure, mitral and aortic valve disorders, hyperkalemia, shunts, or cardiac tamponade.
Monitorización remota e indirecta del flujo sanguíneo mediante láser Doppler
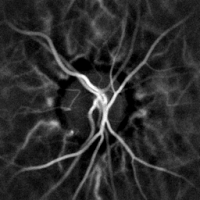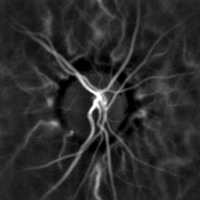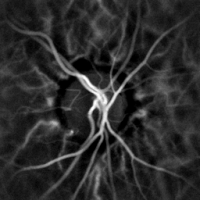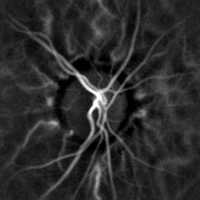
La monitorización hemodinámica no invasiva de los vasos del fondo del ojo se puede realizar mediante holografía con láser Doppler, con luz infrarroja cercana. El ojo ofrece una oportunidad única para la exploración no invasiva de las enfermedades cardiovasculares. Las imágenes de láser Doppler mediante holografía digital pueden medir el flujo sanguíneo en la retina y la coroides, cuyas respuestas Doppler exhiben un perfil en forma de pulso con el tiempo. el segmento posterior del ojo. Las diferencias en la presión arterial impulsan el flujo de sangre a lo largo de la circulación. La tasa de flujo sanguíneo medio depende tanto de la presión arterial como de la resistencia hemodinámica al flujo que presentan los vasos sanguíneos.
Glosario
- ANH
- Normovolémico agudo Hemodilución
- ANHu
- Número de unidades durante la ANH
- BLH
- Pérdida máxima de sangre posible cuando se utiliza ANH antes de la transfusión de sangre homologosa se necesita
- BLI
- Pérdida Incremental de Sangre Posible con ANH.(BLH - BLs)
- BLs
- Pérdida máxima de sangre sin ANH antes de la transfusión de sangre homologosa es necesaria
- EBV
- Volumen de sangre estimado (70 mL/kg)
- Hct
- Haematocrito siempre expresado aquí como una fractura
- Hi
- Haematocrito inicial
- Hm
- Haematocrito mínimo seguro
- PRBC
- Equivalente de células rojas empacadas Salvado por ANH
- RCM
- Masa de células rojas.
- RCMH
- Masa celular disponible para transfusión después de ANH
- RCMI
- Masa de células rojas salvada por ANH
- SBL
- Pérdida de sangre quirúrgica
Etimología y pronunciación
La palabra hemodinámica () combina formas de hemo- (que proviene del griego antiguo haima, que significa sangre) y dinámica, por lo tanto "la dinámica de la sangre". La vocal de la hemosílaba se escribe de diversas formas según la variación ae/e.
- Martillo de sangre
- Presión arterial
- Salida cardiaca
- Cardiovascular System Dynamics Society
- Cardiometría eléctrica
- Esofogeal doppler
- Hemodinámica de la aorta
- Cardiografía de impedancia
- Fotoplethysmogram
- Imágenes láser Doppler
- Efecto de Windkessel
- Espectroscopia funcional cercana al infrarrojo
Notas y referencias
- ^ a b Tortora, Gerard J.; Derrickson, Bryan (2012). "El sistema cardiovascular: la sangre". Principios de Anatomía " Fisiología (13a edición). John Wiley ' Sons. pp. 729–732. ISBN 978-0-470-56510-0.
- ^ Fieldman, Joel S.; Phong, Duong H.; Saint-Aubin, Yvan; Vinet, Luc (2007). "Rheología". Biología y Mecánica de Flujos de Sangre, Parte II: Aspectos Mecánicos y Médicos. Springer. pp. 119–123. ISBN 978-0-387-74848-1.
- ^ Rand, Peter (31 de mayo de 1963). "Sangre humana bajo condiciones normotérmicas e hipotérmicas" (PDF). Journal of Applied Physiology. 19: 117–122. doi:10.1152/jappl.1964.19.1.117. PMID 14104265. Retrieved 16 de septiembre 2014.
- ^ a b c Caro, C.G.; Pedley, T.J.; Schroter, R.C.; Seed, W.A. (1978). La Mecánica de la Circulación. Oxford University Press. pp. 3-60, 151–176. ISBN 978-0-19-263323-1.
- ^ Naqash, Imtiaz A.; Draboo, M. A.; Lone, Abdul Qayoom; Nengroo, Showkat H.; Kirmani, Altaf; Bhat, Abdul Rashid (2011). "Evaluación de la hemodilución normovolémica aguda y autotransfusión en pacientes neuroquirúrgicos sometidos a escisión de meningioma intracraneal". Journal of Anaesthesiology Clinical Pharmacology. 27 (1): 54–58. doi:10.4103/0970-9185.76645. ISSN 0970-9185. PMC3146160. PMID 21804707.
- ^ Saito, Chihiro; Kamei, Tetsuya; Kubota, Shoji; Yoshida, Kiyoshi; Hibiya, Makoto; Hashimoto, Shuji (diciembre de 2018). "Association of Primary Hemodilution and Retrograde Autologous Priming with Transfusion in Cardiac Surgery: Analysis of the Perfusion Case Database of the Japanese Society of Extra-Corporeal Technology in Medicine". The Journal of Extra-corporeal Technology. 50 (4): 231–236. ISSN 0022-1058. PMC6296452. PMID 30581230.
- ^ "Eficacia de hemodilución normovolémica aguda, accedida como una función de sangre perdida". la revista de la sociedad americana de inc anestesiólogo. Archivado desde el original el 29 de junio de 2012. Retrieved 5 de abril 2011.
- ^ a b Kaya, M.; Li, J.K.-J. (2001). "Hemodilución: Modelización y aspectos clínicos". Hemodilution:Modelling and clinincal Aspects. Vol. 1. IEEE. pp. 177–179. doi:10.1109/IEMBS.2001.1018881. ISBN 978-0-7803-7211-5. S2CID 73295413.
- ^ Feldman, Jeffrey M.; Roth, Jonathan V.; Bjoraker, David G. (enero de 1995). "Ahorro máximo de sangre por hemodilución aguda normovolémica". Anestesia & Analgesia. 80 (1): 108–113. doi:10.1097/00000539-199501000-00019. PMID 7802266. S2CID 24131754. Archivado desde el original el 23 de febrero de 2022. Retrieved 5 de abril 2011.
- ^ a b Costanzo, Linda S. (2003). Fisiología. Board Review Series (3rd ed.). Philadelphia: Lippincott Williams & Wilkins. pp. 73–113. ISBN 978-0781739191.
- ^ King, Jordan; Lowery, David R. (2022), "Physiology, Cardiac Output", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 29262215, recuperado 2022-05-16
- ^ Nasoori, Alireza; Taghipour, Ali; Shahbazzadeh, Delavar; Aminirissehei, Abdolhossein; Moghaddam, Sharif (2014). "Evaluación de lugar y longitud de la cola en Naja oxiana, Macrovipera lebetina y Montivipera latifii". Asian Pacific Journal of Tropical Medicine. 7: S137–S142. doi:10.1016/S1995-7645(14)60220-0. PMID 25312108.
- ^ Lillywhite, Harvey B.; Albert, James S.; Sheehy, Coleman M.; Seymour, Roger S. (2012). "La gravedad y la evolución de la morfología cardiopulmonar en las serpientes". Bioquímica Comparada y Fisiología. 161 (2): 230–242. doi:10.1016/j.cbpa.2011.10.029. PMC3242868. PMID 22079804.
- ^ a b c Munson BR, Young DF, Okiishi TH, Huebsch WW (2009). Fundamentos de Mecánica Fluida (Sexta edición). New Jersey: John Wiley &Sons, Inc. p. 725. ISBN 978-0-470-26284-9.
- ^ Fung, Yuan-cheng; Zweifach, B.W. (1971). "Microcirculación: Mecánica de Flujo de Sangre en Capillaries". Annual Review of Fluid Mechanics. 3: 189–210. Bibcode:1971AnRFM...3..189F. doi:10.1146/annurev.fl.03.010171.001201.
- ^ Tortora, Gerard J.; Derrickson, Bryan (2012). "El sistema cardiovascular: vasos sanguíneos y hemodinámicas". Principios de Anatomía " Fisiología (13a edición). John Wiley ' Sons. p. 816. ISBN 978-0470-56510-0.
- ^ Stücker, M.; Bailer, V.; Reuther, T.; Hoffman, K.; Kellam, K.; Altmeyer, P. (1996). "Velocidad de células de sangre capilar en cápsulas de piel humana ubicadas perpendicularmente a la superficie de la piel: Medida por un nuevo neumómetro láser Doppler". Microvascular Research. 52 (2): 188–192. doi:10.1006/mvre.1996.0054. PMID 8901447.
- ^ Tortora, Gerard J.; Derrickson, Bryan (2012). "El sistema cardiovascular: vasos sanguíneos y hemodinámicas". Principios de Anatomía " Fisiología (13a edición). John Wiley & Sons. Análisis de flujo laminar. p. 817. ISBN 978-0470-56510-0.
- ^ Marieb, Elaine N.; Hoehn, Katja (2013). "The Cardiovascular System:Blood Vessels". Anatomía humana " fisiología " (9a edición). Pearson Education. p. 712. ISBN 978-0-321-74326-8.
- ^ a b GB Thurston, Viscosidad y viscoelasticidad de sangre en tubos de pequeño diámetro, Microvasular Research 11, 133 146, 1976
- ^ Womersley JR (1955). "Método para el cálculo de velocidad, velocidad de flujo y arrastre viscoso en las arterias cuando se conoce el gradiente de presión". Journal of Physiology. 127 (3): 553-563. doi:10.1113/jphysiol.1955.sp005276. PMC1365740. PMID 14368548.
- ^ Sircar, Sabyasach (2008). Principios de Fisiología Médica. India: viewta Publishing. ISBN 978-1-58890-572-7.
- ^ a b c Fung, Yuan-cheng (1997). Biomecánica:Circulación. Nueva York: Springer. p. 571. ISBN 978-0-387-94384-8.
- ^ Rosenson RS, Wolff D, Green D, Boss AH, Kensey KR (febrero de 2004). "Aspirina. La aspirina no altera la viscosidad de sangre nativa". J. Thromb. Haemost. 2 (2): 340-341. doi:10.1111/j.1538-79333.2004.0615f.x. PMID 14996003.
- ^ a b Delong, Claire; Sharma, Sandeep (2022), "Physiology, Peripheral Vascular Resistance", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 30855892, recuperado 2022-05-16
- ^ Naderi, Nasim (2022-01-01), Maleki, Majid; Alizadehasl, Azin; Haghjoo, Majid (eds.), "Capítulo 11 - Estudio Hemodinámico", Cardiología práctica (segunda edición), Elsevier, pp. 201–216, ISBN 978-0-323-80915-3, recuperado 2022-05-22
- ^ Potters (13 de febrero de 2014). "Measuring Wall Shear Stress Using Velocity-Encoded MRI". Cardiovascular actual Informes de imágenes. 7 (4). doi:10.1007/s12410-014-9257-1. S2CID 55721300.
- ^ Tazraei, P.; Riasi, A.; Takabi, B. (2015). "La influencia de las propiedades no neotonianas de la sangre en el martillo sanguíneo a través de la arteria cerebral posterior". Biociencias matemáticas. 264: 119–127. doi:10.1016/j.mbs.2015.03.013. PMID 25865933.
- ^ Lough, Mary (2015-04-15). Hemodynamic Monitoring: Tecnologías giratorias y práctica clínica (1 ed.). St. Louis, Missouri: Elsevier Mosby. p. 25. ISBN 978-0-323-08512-0.
- ^ a b Caro, Colin G. (1978). La Mecánica de la Circulación. Oxford [Oxfordshire]: Oxford University Press. ISBN 978-0-19-263323-1.
- ^ "Número rango de presión arterial adultos". Salud y Vida. 2010-06-07. Archivado desde el original en 2016-03-18. Retrieved 2016-02-06.
- ^ DeMers, Daniel; Wachs, Daliah (2022), "Physiology, Mean Arterial Pressure", StatPearls, Treasure Island (FL): StatPearls Publishing, PMID 30855814, recuperado 2022-05-22
- ^ Klabunde, Richard (2005). Cardiovascular Conceptos de fisiología. Lippincott Williams & Wilkins. pp. 93–94. ISBN 978-0-7817-5030-1.
- ^ a b Markham LW, Knecht SK, Daniels SR, Mays WA, Khoury PR, Knilans TK (noviembre de 2004). "Development of exercise-induced arm-leg blood pressure gradient and anormal arterial compliance in patients with repaired coarctation of the aorta". Am. J. Cardiol. 94 (9): 1200–1202. doi:10.1016/j.amjcard.2004.07.097. PMID 15518624.
- ^ Centro Médico de la Universidad Vanderbilt. medsites.vumc.org. Retrieved 2022-05-16.
- ^ Puyo, L., M. Paques, M. Fink, J-A. Sahel y M. Atlan. "In vivo laser Doppler holografía de la retina humana." Óptica biomédica expresa 9, no. 9 (2018): 4113-4129.
- ^ Puyo, Léo, Michel Paques, Mathias Fink, José-Alain Sahel, y Michael Atlan. "Análisis de formas de flujo sanguíneo retininal y choroidal humano con holografía láser Doppler". Biomedical Optics Express 10, no 10 (2019): 4942-4963.
- ^ "haemodynamic". Lexico UK Diccionario Inglés. Oxford University Press. Archivado desde el original el 01/12/2005.
Contenido relacionado
Constipación
Deficiencia de calcio
Peritonitis

![Q=K([P_{c}-P_{i}]S-[P_{c}-P_{i}])](https://wikimedia.org/api/rest_v1/media/math/render/svg/e42f7529864cb1070a1a07048e10d7e06fb125f1)
























