Grafito
Grafito () es una forma cristalina del elemento carbono. Consiste en capas apiladas de grafeno. El grafito se produce de forma natural y es la forma más estable de carbono en condiciones estándar. El grafito sintético y natural se consume en gran escala (300 kton/año, en 1989) para usos en lápices, lubricantes y electrodos. Bajo altas presiones y temperaturas se convierte en diamante. Es un conductor débil del calor y la electricidad.
Tipos y variedades
Grafito natural
Los principales tipos de grafito natural, cada uno de los cuales se encuentra en diferentes tipos de depósitos minerales, son
- Los pequeños copos cristalinos de grafito (o grafito de flake) se producen como partículas aisladas, planas, tipo placa con bordes hexagonales si no se rompen. Cuando los bordes rotos pueden ser irregulares o angulares;
- Gráfico morfoso: la grafita de flake muy fina se llama a veces amorfo;
- El grafito de bulto (o grafito de vena) se produce en las venas o fracturas de fisura y aparece como intercrementos masivos de platina de agregados cristalinos fibrosos o aciculares, y es probablemente hidrotermal en origen.
- El grafito pirolítico de alta orden se refiere a grafito con una extensión angular entre las hojas de grafito de menos de 1°.
- El nombre "fibra gráfica" se utiliza a veces para referirse a fibras de carbono o polímero reforzado con fibra de carbono.
Ocurrencia
El grafito se encuentra en las rocas metamórficas como resultado de la reducción de los compuestos de carbono sedimentarios durante el metamorfismo. También ocurre en rocas ígneas y en meteoritos. Los minerales asociados con el grafito incluyen cuarzo, calcita, micas y turmalina. Las principales fuentes de exportación de grafito extraído son, por orden de tonelaje: China, México, Canadá, Brasil y Madagascar.
En los meteoritos, el grafito se presenta con minerales de troilita y silicato. Los pequeños cristales de grafito en el hierro meteorítico se llaman cliftonita. Algunos granos microscópicos tienen composiciones isotópicas distintivas, lo que indica que se formaron antes del Sistema Solar. Son uno de los 12 tipos conocidos de minerales anteriores al Sistema Solar y también se han detectado en nubes moleculares. Estos minerales se formaron en la eyección cuando las supernovas explotaron o las estrellas de tamaño bajo a intermedio expulsaron sus envolturas exteriores al final de sus vidas. El grafito puede ser el segundo o tercer mineral más antiguo del Universo.
Estructura
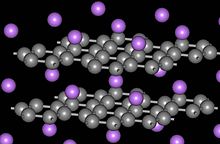
El grafito consiste en láminas de carbono plano trigonal. Las capas individuales se llaman grafeno. En cada capa, los átomos de carbono están dispuestos en una red de panal con una longitud de enlace de 0,142 nm y la distancia entre planos es de 0,335 nm. Los enlaces entre capas son enlaces de van der Waals relativamente débiles y, a menudo, están ocupados por gases, lo que permite que las capas similares al grafeno se separen fácilmente y se deslicen entre sí.
La conductividad eléctrica perpendicular a las capas es por lo tanto unas 1000 veces menor.
Las dos formas de grafito se llaman alfa (hexagonal) y beta (romboédrico). Sus propiedades son muy similares. Difieren en términos del apilamiento de las capas de grafeno: el apilamiento en grafito alfa es ABA, a diferencia del apilamiento ABC en grafito beta energéticamente menos estable y menos común. La forma alfa se puede convertir en forma beta a través de un tratamiento mecánico y la forma beta vuelve a la forma alfa cuando se calienta por encima de 1300 °C.
Termodinámica
Las condiciones de presión y temperatura de equilibrio para una transición entre el grafito y el diamante están bien establecidas teórica y experimentalmente. La presión cambia linealmente entre 1.7 GPa a 0 K y 12 GPa en 5000 K (el punto triple de diamante/grafito/líquido). Sin embargo, las fases tienen una amplia región alrededor de esta línea donde pueden coexistir. A temperatura y presión normales, 20 °C (293 K) y 1 atmósfera estándar (0,10 MPa), la fase estable del carbono es el grafito, pero el diamante es metaestable y su tasa de conversión a grafito es insignificante. Sin embargo, a temperaturas superiores a 4500 K, el diamante se convierte rápidamente en grafito. La conversión rápida de grafito a diamante requiere presiones muy por encima de la línea de equilibrio: a 2000 K, una presión de Se necesita 35 GPa.
Otras propiedades
Las propiedades acústicas y térmicas del grafito son altamente anisotrópicas, ya que los fonones se propagan rápidamente a lo largo de los planos estrechamente unidos, pero son más lentos para viajar de un plano a otro. La alta estabilidad térmica y la conductividad eléctrica y térmica del grafito facilitan su uso generalizado como electrodos y refractarios en aplicaciones de procesamiento de materiales a alta temperatura. Sin embargo, en atmósferas que contienen oxígeno, el grafito se oxida fácilmente para formar dióxido de carbono a temperaturas de 700 °C y superiores.
El grafito es un conductor eléctrico, por lo que es útil en aplicaciones tales como electrodos de lámparas de arco. Puede conducir electricidad debido a la gran deslocalización de electrones dentro de las capas de carbono (un fenómeno llamado aromaticidad). Estos electrones de valencia pueden moverse libremente, por lo que pueden conducir electricidad. Sin embargo, la electricidad se conduce principalmente dentro del plano de las capas. Las propiedades conductoras del grafito en polvo permiten su uso como sensor de presión en micrófonos de carbono.
El grafito y el polvo de grafito se valoran en aplicaciones industriales por sus propiedades autolubricantes y de lubricación en seco. Existe la creencia común de que las propiedades lubricantes del grafito se deben únicamente al acoplamiento interlamelar flojo entre las láminas de la estructura. Sin embargo, se ha demostrado que en un entorno de vacío (como en las tecnologías para uso en el espacio), el grafito se degrada como lubricante debido a las condiciones hipóxicas. Esta observación condujo a la hipótesis de que la lubricación se debe a la presencia de fluidos entre las capas, como el aire y el agua, que son naturalmente adsorbidos del medio ambiente. Esta hipótesis ha sido refutada por estudios que muestran que el aire y el agua no se absorben. Estudios recientes sugieren que un efecto llamado superlubricidad también puede explicar las propiedades lubricantes del grafito. El uso de grafito está limitado por su tendencia a facilitar la corrosión por picaduras en algunos aceros inoxidables y a promover la corrosión galvánica entre metales diferentes (debido a su conductividad eléctrica). También es corrosivo para el aluminio en presencia de humedad. Por esta razón, la Fuerza Aérea de EE. UU. prohibió su uso como lubricante en aviones de aluminio y desaconsejó su uso en armas automáticas que contengan aluminio. Incluso las marcas de lápiz de grafito en las piezas de aluminio pueden facilitar la corrosión. Otro lubricante de alta temperatura, el nitruro de boro hexagonal, tiene la misma estructura molecular que el grafito. A veces se le llama grafito blanco, debido a sus propiedades similares.
Cuando una gran cantidad de defectos cristalográficos unen estos planos, el grafito pierde sus propiedades lubricantes y se convierte en lo que se conoce como grafito pirolítico. También es altamente anisotrópico y diamagnético, por lo que flotará en el aire sobre un imán fuerte. Si se fabrica en un lecho fluidizado a 1000-1300 °C, entonces es turboestrático isotrópico y se usa en dispositivos de contacto con la sangre, como válvulas cardíacas mecánicas, se llama carbón pirolítico y no es diamagnético. El grafito pirolítico y el carbón pirolítico a menudo se confunden, pero son materiales muy diferentes.
Los grafitos naturales y cristalinos no suelen utilizarse en forma pura como materiales estructurales, debido a sus planos de corte, fragilidad y propiedades mecánicas inconsistentes.
Historia del uso del grafito natural
En el cuarto milenio a. C., durante el Neolítico en el sureste de Europa, la cultura Marița usó grafito en una pintura de cerámica para decorar la cerámica.
En algún momento antes de 1565 (algunas fuentes dicen que ya en 1500), se descubrió un enorme depósito de grafito al acercarse a Grey Knotts desde la aldea de Seathwaite en la parroquia de Borrowdale, Cumbria, Inglaterra, que los lugareños encontraron útil para marcar ovejas.. Durante el reinado de Isabel I (1558-1603), el grafito de Borrowdale se usó como material refractario para revestir moldes para balas de cañón, lo que resultó en bolas más redondas y suaves que podían dispararse más lejos, contribuyendo a la fuerza de la marina inglesa. Este depósito particular de grafito era extremadamente puro y suave, y podía cortarse fácilmente en barras. Por su importancia militar, esta singular mina y su producción estaban estrictamente controladas por la Corona.
Durante el siglo XIX, los usos del grafito se expandieron enormemente para incluir cera para estufas, lubricantes, pinturas, crisoles, revestimientos de fundición y lápices, un factor importante en la expansión de las herramientas educativas durante el primer gran auge de la educación para las masas. El Imperio Británico controlaba la mayor parte de la producción mundial (especialmente de Ceilán), pero la producción de los depósitos de Austria, Alemania y Estados Unidos se expandió a mediados de siglo. Por ejemplo, Dixon Crucible Company de Jersey City, Nueva Jersey, fundada por Joseph Dixon y su socio Orestes Cleveland en 1845, abrió minas en el distrito de Lake Ticonderoga de Nueva York, construyó allí una planta de procesamiento y una fábrica para fabricar lápices, crisoles y otros productos en New Jersey, descritos en Engineering & Mining Journal 21 de diciembre de 1878. El lápiz Dixon todavía está en producción.
Los comienzos del revolucionario proceso de flotación por espuma están asociados con la extracción de grafito. En el artículo de E&MJ sobre Dixon Crucible Company se incluye un boceto de los "tanques flotantes" utilizado en el antiguo proceso de extracción de grafito. Debido a que el grafito es tan liviano, la mezcla de grafito y desechos se envió a través de una serie final de tanques de agua donde "flotó" un grafito más limpio, lo que dejó que los desechos cayeran. En una patente de 1877, los dos hermanos Bessel (Adolph y August) de Dresden, Alemania, tomaron este "flotante" procesó un paso más y agregó una pequeña cantidad de aceite a los tanques y hirvió la mezcla (un paso de agitación o formación de espuma) para recolectar el grafito, los primeros pasos hacia el futuro proceso de flotación. Adolph Bessel recibió la Medalla Wohler por el proceso patentado que mejoró la recuperación de grafito al 90 % del depósito alemán. En 1977, la Sociedad Alemana de Ingenieros de Minas y Metalúrgicos organizó un simposio especial dedicado a su descubrimiento y, por lo tanto, al centenario de la flotación.
En los Estados Unidos, en 1885, Hezekiah Bradford de Filadelfia patentó un proceso similar, pero no está claro si su proceso se usó con éxito en los depósitos de grafito cercanos del condado de Chester, Pensilvania, un importante productor en la década de 1890. El proceso de Bessel tenía un uso limitado, principalmente debido a los abundantes depósitos de limpiadores que se encuentran en todo el mundo, que no necesitaban mucho más que una clasificación manual para recolectar el grafito puro. El estado del arte, ca. 1900, se describe en el informe del Departamento de Minas de Canadá sobre las minas de grafito y la minería cuando los depósitos canadienses comenzaron a convertirse en importantes productores de grafito.
Otros nombres
Históricamente, el grafito se llamaba plomo negro o plumbago. Plumbago se usaba comúnmente en su forma mineral masiva. Ambos nombres surgen de la confusión con los minerales de plomo de apariencia similar, particularmente la galena. La palabra latina para plomo, plumbum, dio nombre al término inglés para este mineral de brillo metálico gris e incluso a las Leadworts o plombagos, plantas con flores que se asemejan a este color.
El término plomo negro generalmente se refiere a un grafito en polvo o procesado, de color negro mate.
Abraham Gottlob Werner acuñó el nombre grafito ("piedra para escribir") en 1789. Intentó aclarar la confusión entre molibdena, plumbago y plomo negro después de que Carl Wilhelm Scheele en 1778 demostró que hay al menos tres minerales diferentes. El análisis de Scheele mostró que los compuestos químicos sulfuro de molibdeno (molibdenita), sulfuro de plomo (II) (galena) y grafito eran tres minerales negros blandos diferentes.
Usos del grafito natural
El grafito natural se usa principalmente para refractarios, baterías, fabricación de acero, grafito expandido, revestimientos de frenos, revestimientos de fundición y lubricantes.
Refractarios
El uso de grafito como material refractario (resistente al calor) comenzó antes de 1900 con crisoles de grafito que se usaban para contener metal fundido; esto es ahora una parte menor de los refractarios. A mediados de la década de 1980, el ladrillo de carbono-magnesita se hizo importante, y un poco más tarde la forma de alúmina-grafito. A partir de 2017, el orden de importancia es: formas de alúmina y grafito, ladrillos de carbono y magnesita, monolíticos (mezclas de gunitado y embestido) y luego crisoles.
Los crisoles comenzaron a usar grafito en escamas muy grandes y ladrillos de magnesita de carbono que requerían grafito en escamas no tan grandes; para estos y otros, ahora hay mucha más flexibilidad en el tamaño de las escamas requeridas, y el grafito amorfo ya no está restringido a los refractarios de gama baja. Las formas de alúmina y grafito se utilizan como elementos de colada continua, como boquillas y artesas, para transportar el acero fundido de la cuchara al molde, y los ladrillos de magnesita de carbono se alinean en convertidores de acero y hornos de arco eléctrico para soportar temperaturas extremas. Los bloques de grafito también se utilizan en partes de los revestimientos de los altos hornos donde la alta conductividad térmica del grafito es fundamental para garantizar un enfriamiento adecuado del fondo y la solera del horno. Los monolíticos de alta pureza se utilizan a menudo como un revestimiento de horno continuo en lugar de ladrillos de carbono y magnesita.
La industria de refractarios de EE. UU. y Europa tuvo una crisis entre 2000 y 2003, con un mercado indiferente para el acero y un consumo de refractarios por tonelada de acero en declive que subyace a las compras de empresas y muchos cierres de plantas. Muchos de los cierres de plantas se debieron a la adquisición de Harbison-Walker Refractories por parte de RHI AG y el equipo de algunas plantas fue subastado. Dado que gran parte de la capacidad perdida era para ladrillos de carbono y magnesita, el consumo de grafito dentro del área de refractarios se desplazó hacia las formas de alúmina y grafito y los monolíticos, y se alejó del ladrillo. La principal fuente de ladrillos de carbono y magnesita es ahora China. Casi todos los refractarios anteriores se utilizan para fabricar acero y representan el 75% del consumo de refractarios; el resto es utilizado por una variedad de industrias, como la del cemento.
Según el USGS, el consumo de grafito natural de EE. UU. en refractarios fue de 12 500 toneladas en 2010.
Baterías
El uso de grafito en baterías ha aumentado desde la década de 1970. El grafito natural y sintético se utiliza como material de ánodo para construir electrodos en las principales tecnologías de baterías.
La demanda de baterías, principalmente baterías de iones de litio e hidruro metálico de níquel, provocó un aumento en la demanda de grafito a fines de la década de 1980 y principios de la de 1990, un crecimiento impulsado por dispositivos electrónicos portátiles, como reproductores de CD portátiles y herramientas eléctricas. Las computadoras portátiles, los teléfonos móviles, las tabletas y los productos para teléfonos inteligentes han aumentado la demanda de baterías. Se prevé que las baterías de vehículos eléctricos aumenten la demanda de grafito. Por ejemplo, una batería de iones de litio en un Nissan Leaf totalmente eléctrico contiene casi 40 kg de grafito.
El grafito radiactivo de viejos reactores nucleares se está investigando como combustible. La batería de diamante nuclear tiene el potencial de suministro de energía de larga duración para la electrónica y el Internet de las cosas.
Acería
El grafito natural en la fabricación de acero se usa principalmente para aumentar el contenido de carbono en el acero fundido; también puede servir para lubricar las matrices utilizadas para extruir acero caliente. Los aditivos de carbono se enfrentan a precios competitivos frente a alternativas como el polvo de grafito sintético, el coque de petróleo y otras formas de carbono. Se agrega un elevador de carbono para aumentar el contenido de carbono del acero a un nivel específico. Una estimación basada en las estadísticas de consumo de grafito de USGS indica que las siderúrgicas de EE. UU. utilizaron 10.500 toneladas de esta manera en 2005.
Revestimientos de freno
El grafito natural amorfo y en escamas finas se usa en forros de freno o zapatas de freno para vehículos más pesados (no automotrices) y adquirió importancia con la necesidad de sustituir el asbesto. Este uso ha sido importante durante bastante tiempo, pero las composiciones orgánicas sin asbesto (NAO) están comenzando a reducir la participación de mercado del grafito. Una sacudida de la industria de revestimientos de frenos con algunos cierres de plantas no ha sido beneficiosa, ni lo ha sido un mercado automotriz indiferente. Según el USGS, el consumo de grafito natural de los EE. UU. en las pastillas de freno fue de 6.510 toneladas en 2005.
Revestimientos y lubricantes para fundición
Un lavado de moldes para fundición es una pintura a base de agua de grafito amorfo o en escamas finas. Pintar con él el interior de un molde y dejarlo secar deja una fina capa de grafito que facilitará la separación del objeto colado después de que el metal caliente se haya enfriado. Los lubricantes de grafito son artículos especiales para usar a temperaturas muy altas o muy bajas, como lubricantes para matrices de forja, agentes antiadherentes, lubricantes para engranajes de maquinaria minera y para lubricar cerraduras. Tener grafito de grano bajo, o incluso mejor, grafito sin grano (pureza ultra alta), es muy deseable. Puede usarse como polvo seco, en agua o aceite, o como grafito coloidal (una suspensión permanente en un líquido). Una estimación basada en las estadísticas de consumo de grafito del USGS indica que se utilizaron 2200 toneladas de esta manera en 2005. El metal también se puede impregnar en grafito para crear una aleación autolubricante para aplicaciones en condiciones extremas, como rodamientos para máquinas expuestas a altas o bajas temperaturas. temperaturas
Uso diario
Lápices
La capacidad de dejar marcas en el papel y otros objetos le dio al grafito su nombre, dado en 1789 por el mineralogista alemán Abraham Gottlob Werner. Proviene de γράφειν ("graphein"), que significa escribir o dibujar en griego antiguo.
Desde el siglo XVI, todos los lápices se fabricaban con minas de grafito natural inglés, pero la mina moderna suele ser una mezcla de grafito en polvo y arcilla; fue inventado por Nicolas-Jacques Conté en 1795. No tiene relación química con el metal plomo, cuyos minerales tenían una apariencia similar, de ahí la continuación del nombre. Plumbago es otro término más antiguo para el grafito natural que se usa para dibujar, generalmente como un trozo del mineral sin una cubierta de madera. El término dibujo de plumbago normalmente se restringe a obras de los siglos XVII y XVIII, en su mayoría retratos.
Hoy en día, los lápices siguen siendo un mercado pequeño pero importante para el grafito natural. Alrededor del 7% de los 1,1 millones de toneladas producidas en 2011 se utilizó para fabricar lápices. El grafito amorfo de baja calidad se utiliza y se obtiene principalmente de China.
En el arte, el grafito se usa normalmente para crear dibujos detallados y precisos, ya que permite lograr una amplia gama de valores (de claro a oscuro). También se puede utilizar para crear líneas y sombreados más suaves y sutiles. El grafito es popular entre los artistas porque es fácil de controlar, fácil de borrar y produce una apariencia limpia y profesional. También es relativamente económico y ampliamente disponible. Muchos artistas usan grafito junto con otros medios, como carboncillo o tinta, para crear una variedad de efectos y texturas en su trabajo.
Pasatiempos
Derby de madera de pino
El grafito es probablemente el lubricante más utilizado en los derbies de madera de pino.
Auriculares
El grafeno se utiliza para fabricar los controladores acústicos de 40 mm que transmiten el sonido al oído. Los controladores dinámicos, también conocidos como controladores de bobina móvil, emplean una bobina móvil cargada eléctricamente para mover un cono y producir ondas sonoras. Estos controladores están hechos de más del 95 % de grafeno y conservan la mayoría de las cualidades mecánicas del material, al mismo tiempo que son más fáciles de moldear y menos costosos de fabricar. Es un material ligero, rígido y de baja densidad, perfecto para membranas de altavoces. Cuanto más pesado sea el cono de un altavoz, más difícil será conducirlo. Dado que el grafeno tiene una relación resistencia-peso tan alta, los controladores de grafeno pueden reducir la cantidad de energía necesaria para mover la bobina hacia adelante y hacia atrás, lo que resulta en una mayor eficiencia y un mejor sonido. Como resultado, los auriculares con controladores de grafeno son más livianos y compactos.
Otros usos
El grafito natural ha encontrado usos en baterías de zinc-carbono, escobillas de motores eléctricos y diversas aplicaciones especializadas. El grafito de varias durezas o suavidades da como resultado diferentes calidades y tonos cuando se usa como medio artístico. Los ferrocarriles solían mezclar grafito en polvo con aceite usado o aceite de linaza para crear una capa protectora resistente al calor para las partes expuestas de la caldera de una locomotora de vapor, como la caja de humo o la parte inferior de la cámara de combustión. El soldador Scope utiliza una punta de grafito como elemento calefactor.
Grafito expandido
El grafito expandido se fabrica sumergiendo grafito natural en escamas en un baño de ácido crómico y luego ácido sulfúrico concentrado, que fuerza la separación de los planos de la red cristalina, expandiendo así el grafito. El grafito expandido se puede usar para hacer láminas de grafito o se puede usar directamente como un "techo caliente" compuesto para aislar el metal fundido en una cuchara o lingotes de acero al rojo vivo y disminuir la pérdida de calor, o como cortafuegos colocados alrededor de una puerta cortafuego o en collares de chapa que rodean la tubería de plástico (durante un incendio, el grafito se expande y se carboniza para resistir la penetración del fuego y propagación), o para hacer material de junta de alto rendimiento para uso a alta temperatura. Después de convertirse en lámina de grafito, la lámina se mecaniza y ensambla en las placas bipolares de las celdas de combustible. La lámina se convierte en disipadores de calor para computadoras portátiles que las mantiene frescas mientras ahorra peso, y se convierte en un laminado de lámina que se puede usar en empaques de válvulas o en juntas. Las empaquetaduras de estilo antiguo ahora son un miembro menor de este grupo: grafito en escamas finas en aceites o grasas para usos que requieren resistencia al calor. Una estimación de GAN del consumo actual de grafito natural de EE. UU. en este uso final es de 7500 toneladas.
Grafito intercalado
El grafito forma compuestos de intercalación con algunos metales y moléculas pequeñas. En estos compuestos, la molécula huésped o el átomo se "sandwich" entre las capas de grafito, resultando un tipo de compuesto con estequiometría variable. Un ejemplo destacado de un compuesto de intercalación es el grafito de potasio, indicado por la fórmula KC8. Algunos compuestos de intercalación de grafito son superconductores. La temperatura de transición más alta (en junio de 2009) Tc = 11,5 K se logra en CaC6, y aumenta aún más bajo la presión aplicada (15,1 K a 8 GPa). La capacidad del grafito para intercalar iones de litio sin daños significativos por la hinchazón es lo que lo convierte en el material de ánodo dominante en las baterías de iones de litio.
Usos del grafito sintético
Invención de un proceso para producir grafito sintético
En 1893, Charles Street de Le Carbone descubrió un proceso para fabricar grafito artificial. A mediados de la década de 1890, Edward Goodrich Acheson (1856–1931) inventó accidentalmente otra forma de producir grafito sintético después de sintetizar carborundum (carburo de silicio o SiC). Descubrió que el sobrecalentamiento del carborundo, a diferencia del carbono puro, producía grafito casi puro. Mientras estudiaba los efectos de las altas temperaturas en el carborundo, descubrió que el silicio se vaporiza a unos 4150 °C (7500 °F), dejando el carbono atrás en forma de carbono grafítico. Este grafito se volvió valioso como lubricante.
La técnica de Acheson para producir carburo de silicio y grafito se denomina proceso Acheson. En 1896, Acheson recibió una patente por su método de sintetizar grafito y en 1897 comenzó la producción comercial. Acheson Graphite Co. se formó en 1899.
El grafito sintético también se puede preparar a partir de poliimida y comercializarse.
Investigación científica
El grafito pirolítico altamente orientado (HOPG) es la forma sintética de grafito de la más alta calidad. Se utiliza en la investigación científica, en particular, como estándar de longitud para la calibración del escáner del microscopio de sonda de exploración.
Electrodos
Los electrodos de grafito transportan la electricidad que funde chatarra de hierro y acero y, a veces, hierro de reducción directa (DRI), en hornos de arco eléctrico, que son la gran mayoría de los hornos de acero. Están hechos de coque de petróleo después de mezclarlo con brea de alquitrán de hulla. Luego se extruyen y se les da forma, luego se hornean para carbonizar el aglutinante (brea) y finalmente se grafitan calentándolo a temperaturas cercanas a los 3000 °C, en las que los átomos de carbono se organizan en grafito. Pueden variar en tamaño hasta 3,5 m (11 ft) de largo y 75 cm (30 in) de diámetro. Una proporción cada vez mayor del acero mundial se fabrica utilizando hornos de arco eléctrico, y el propio horno de arco eléctrico se está volviendo más eficiente, produciendo más acero por tonelada de electrodo. Una estimación basada en datos del USGS indica que el consumo de electrodos de grafito fue de 197.000 toneladas en 2005.
La fundición electrolítica de aluminio también utiliza electrodos de carbón grafítico. En una escala mucho más pequeña, los electrodos de grafito sintético se utilizan en el mecanizado por descarga eléctrica (EDM), comúnmente para fabricar moldes de inyección para plásticos.
Polvo y chatarra
El polvo se fabrica calentando coque de petróleo en polvo por encima de la temperatura de grafitización, a veces con modificaciones menores. La chatarra de grafito proviene de piezas de material de electrodo inservible (en la etapa de fabricación o después de su uso) y virutas, generalmente después de triturado y dimensionado. La mayor parte del polvo de grafito sintético se destina al aumento de carbono en el acero (compitiendo con el grafito natural), y algunos se utilizan en baterías y pastillas de freno. Según el USGS, la producción de chatarra y polvo de grafito sintético estadounidense fue de 95.000 toneladas en 2001 (últimos datos).
Moderadora de neutrones
(feminine)Grados especiales de grafito sintético, como Gilsocarbon, también encuentran uso como matriz y moderador de neutrones dentro de los reactores nucleares. Su baja sección transversal de neutrones también lo recomienda para su uso en los reactores de fusión propuestos. Se debe tener cuidado de que el grafito apto para reactores esté libre de materiales absorbentes de neutrones como el boro, ampliamente utilizado como electrodo semilla en los sistemas comerciales de deposición de grafito; Reactores nucleares basados en grafito de la Segunda Guerra Mundial. Como no pudieron aislar la dificultad, se vieron obligados a utilizar moderadores de agua pesada mucho más caros. El grafito utilizado para reactores nucleares a menudo se denomina grafito nuclear. Herbert G. McPherson, un físico capacitado en Berkeley en National Carbon, una división de Union Carbide, fue clave en la confirmación de una conjetura de Leo Szilard de que las impurezas de boro, incluso en forma "pura" El grafito fue responsable de una sección transversal de absorción de neutrones en el grafito que comprometió las reacciones en cadena del U-235. McPherson estaba al tanto de la presencia de impurezas en el grafito porque, con el uso de Technicolor en cinematografía, los espectros de los arcos de electrodos de grafito utilizados en los proyectores de películas requerían impurezas para mejorar la emisión de luz en la región roja para mostrar tonos de piel más cálidos en la pantalla. Por lo tanto, si no hubiera sido por las películas en color, es probable que la primera reacción en cadena U natural sostenida hubiera requerido un reactor moderado por agua pesada.
Otros usos
La fibra de grafito (carbono) y los nanotubos de carbono también se utilizan en plásticos reforzados con fibra de carbono y en compuestos resistentes al calor como el carbono-carbono reforzado (RCC). Las estructuras comerciales hechas de compuestos de grafito de fibra de carbono incluyen cañas de pescar, ejes de palos de golf, marcos de bicicletas, paneles de carrocería de autos deportivos, el fuselaje del Boeing 787 Dreamliner y tacos de billar y se han empleado con éxito en hormigón armado. Las propiedades mecánicas de los compuestos plásticos reforzados con grafito de fibra de carbono y el hierro fundido gris están fuertemente influenciadas por el papel del grafito en estos materiales. En este contexto, el término "(100%) grafito" a menudo se usa vagamente para referirse a una mezcla pura de refuerzo de carbono y resina, mientras que el término "compuesto" se utiliza para materiales compuestos con ingredientes adicionales.
La pólvora moderna sin humo está recubierta de grafito para evitar la acumulación de carga estática.
El grafito se ha utilizado en al menos tres materiales absorbentes de radar. Se mezcló con caucho en Sumpf y Schornsteinfeger, que se usaron en los tubos respiradores de los submarinos para reducir su sección transversal de radar. También se usó en mosaicos en los primeros cazas furtivos F-117 Nighthawk.
Los compuestos de grafito se utilizan como absorbentes de partículas de alta energía, por ejemplo, en el volcado de haz del Gran Colisionador de Hadrones.
Las varillas de grafito, cuando se les da forma, se utilizan como herramienta en el trabajo del vidrio para manipular el vidrio fundido caliente.
Extracción, beneficio y molienda de grafito
El grafito se extrae mediante métodos subterráneos y a cielo abierto. El grafito generalmente necesita beneficio. Esto puede llevarse a cabo seleccionando a mano los trozos de ganga (roca) y cribando a mano el producto o triturando la roca y flotando el grafito. El beneficio por flotación se encuentra con la dificultad de que el grafito es muy blando y "marca" (recubre) las partículas de ganga. Esto hace que el "marcado" las partículas de ganga flotan con el grafito, produciendo un concentrado impuro. Hay dos formas de obtener un concentrado o producto comercial: trituración repetida y flotación (hasta siete veces) para purificar el concentrado, o por lixiviación ácida (disolución) de la ganga con ácido fluorhídrico (para una ganga de silicato) o ácido clorhídrico (para una ganga de silicato). una ganga de carbonato).
En la molienda, los productos y concentrados de grafito entrantes se pueden moler antes de clasificarlos (dimensionarlos o tamizarlos), con las fracciones de tamaño de hojuelas más gruesas (menos de 8 mallas, 8–20 mallas, 20–50 mallas) cuidadosamente preservadas y luego se determinan los contenidos de carbono. Se pueden preparar algunas mezclas estándar a partir de las diferentes fracciones, cada una con una determinada distribución del tamaño de las escamas y contenido de carbono. También se pueden hacer mezclas personalizadas para clientes individuales que desean una determinada distribución de tamaño de copos y contenido de carbono. Si el tamaño de los copos no es importante, el concentrado se puede moler más libremente. Los productos finales típicos incluyen un polvo fino para usar como suspensión en la extracción de petróleo y revestimientos para moldes de fundición, elevador de carbón en la industria del acero (el polvo de grafito sintético y el coque de petróleo en polvo también se pueden usar como elevador de carbón). Los impactos ambientales de las fábricas de grafito consisten en la contaminación del aire, incluida la exposición de los trabajadores a partículas finas, y también la contaminación del suelo por derrames de polvo que conducen a la contaminación del suelo con metales pesados.
Según el Servicio Geológico de los Estados Unidos (USGS), la producción mundial de grafito natural en 2016 fue de 1 200 000 toneladas, de las cuales los principales exportadores son: China (780 000 t), India (170 000 t), Brasil (80 000 t), Turquía (32.000 t) y Corea del Norte (6.000 t). El grafito aún no se extrae en los Estados Unidos. Sin embargo, Westwater Resources se encuentra actualmente en las etapas de desarrollo de la creación de una planta piloto para su mina de grafito Coosa cerca de Sylacauga, Alabama. La producción estadounidense de grafito sintético en 2010 fue de 134 000 t valoradas en 1070 millones de dólares.
Seguridad laboral
Las personas pueden estar expuestas al grafito en el lugar de trabajo al inhalarlo, así como a través del contacto con la piel o con los ojos.
Estados Unidos
La Administración de Salud y Seguridad Ocupacional (OSHA) ha establecido el límite legal (límite de exposición permisible) para la exposición al grafito en el lugar de trabajo como un promedio ponderado en el tiempo (TWA) de 15 millones de partículas por pie cúbico (1,5 mg/m3) durante una jornada laboral de 8 horas. El Instituto Nacional de Salud y Seguridad Ocupacional (NIOSH) ha establecido un límite de exposición recomendado (REL) de TWA de 2,5 mg/m3 de polvo respirable durante una jornada laboral de 8 horas. A niveles de 1250 mg/m3, el grafito es inmediatamente peligroso para la vida y la salud.
Reciclaje de grafito
La forma más común de reciclar el grafito se produce cuando se fabrican electrodos de grafito sintético y se cortan las piezas, o se descartan las virutas del torno para reutilizarlas, o cuando el electrodo (u otros materiales) se utilizan hasta el portaelectrodos. Un electrodo nuevo reemplaza al viejo, pero queda una parte considerable del electrodo viejo. Esto se tritura y se dimensiona, y el polvo de grafito resultante se usa principalmente para aumentar el contenido de carbono del acero fundido.
Los refractarios que contienen grafito a veces también se reciclan, pero a menudo no debido a su bajo contenido de grafito: los artículos de mayor volumen, como los ladrillos de carbono y magnesita que contienen solo entre un 15 y un 25 % de grafito, generalmente contienen muy poco grafito para vale la pena reciclar. Sin embargo, algunos ladrillos de magnesita de carbono reciclados se utilizan como base para materiales de reparación de hornos, y también los ladrillos de magnesita de carbono triturados se utilizan en acondicionadores de escoria.
Si bien los crisoles tienen un alto contenido de grafito, el volumen de crisoles utilizados y luego reciclados es muy pequeño.
Se puede fabricar un producto de grafito en escamas de alta calidad que se parece mucho al grafito en escamas natural a partir del kish siderúrgico. Kish es un desecho casi fundido de gran volumen desnatado de la alimentación de hierro fundido a un horno de oxígeno básico y consiste en una mezcla de grafito (precipitado del hierro sobresaturado), escoria rica en cal y algo de hierro. El hierro se recicla in situ, dejando una mezcla de grafito y escoria. El mejor proceso de recuperación utiliza la clasificación hidráulica (que utiliza un flujo de agua para separar los minerales por gravedad específica: el grafito es liviano y se asienta casi en último lugar) para obtener un concentrado bruto de 70 % de grafito. La lixiviación de este concentrado con ácido clorhídrico da un producto de 95 % de grafito con un tamaño de hojuela que varía desde malla 10 (2 mm) hacia abajo.