Glioblastoma
Glioblastoma, anteriormente conocido como glioblastoma multiforme (GBM), es el tipo de cáncer más agresivo y común que se origina en el cerebro., y tiene muy mal pronóstico de supervivencia. Los signos y síntomas iniciales del glioblastoma son inespecíficos. Pueden incluir dolores de cabeza, cambios de personalidad, náuseas y síntomas similares a los de un derrame cerebral. Los síntomas a menudo empeoran rápidamente y pueden progresar hasta la pérdida del conocimiento.
No se conoce la causa de la mayoría de los casos de glioblastoma. Los factores de riesgo poco comunes incluyen trastornos genéticos, como la neurofibromatosis y el síndrome de Li-Fraumeni y la radioterapia previa. Los gllioblastomas representan el 15% de todos los tumores cerebrales. Se cree que surgen de los astrocitos. El diagnóstico generalmente se realiza mediante una combinación de una tomografía computarizada, una tomografía por resonancia magnética y una biopsia de tejido.
No existe un método conocido para prevenir el cáncer. El tratamiento generalmente implica cirugía, después de lo cual se usa quimioterapia y radioterapia. El medicamento temozolomida se usa frecuentemente como parte de la quimioterapia. Los esteroides de dosis alta pueden utilizarse para ayudar a reducir la inflamación y disminuir los síntomas. La extirpación quirúrgica (decompresión) del tumor está vinculada a una mayor supervivencia, pero sólo por algunos meses.
A pesar del tratamiento máximo, el cáncer casi siempre reaparece. La duración típica de la supervivencia después del diagnóstico es de 10 a 13 meses, y menos del 5 al 10% de las personas sobreviven más de cinco años. Sin tratamiento, la supervivencia suele ser de tres meses. Es el cáncer más común que comienza dentro del cerebro y el segundo tumor cerebral más común, después del meningioma, que es benigno en la mayoría de los casos. Aproximadamente 3 de cada 100.000 personas desarrollan la enfermedad cada año. La edad promedio en el momento del diagnóstico es 64 años y la enfermedad ocurre con más frecuencia en hombres que en mujeres.
Signos y síntomas
Los síntomas comunes incluyen convulsiones, dolores de cabeza, náuseas y vómitos, pérdida de memoria, cambios de personalidad, estado de ánimo o concentración y problemas neurológicos localizados. El tipo de síntomas producidos depende más de la localización del tumor que de sus propiedades patológicas. El tumor puede comenzar a producir síntomas rápidamente, pero ocasionalmente es un estado asintomático hasta alcanzar un tamaño enorme.
Factores de riesgo
La causa de la mayoría de los casos no está clara. El factor de riesgo más conocido es la exposición a radiaciones ionizantes, y la radiación de la tomografía computarizada es una causa importante. Alrededor del 5% se desarrolla a partir de ciertos síndromes hereditarios.
Genética
Los factores de riesgo poco comunes incluyen trastornos genéticos como la neurofibromatosis, el síndrome de Li-Fraumeni, la esclerosis tuberosa o el síndrome de Turcot. La radioterapia previa también es un riesgo. Por razones desconocidas, ocurre más comúnmente en hombres.
Medio ambiente
Otras asociaciones incluyen la exposición al tabaquismo, pesticidas y el trabajo en la refinación de petróleo o la fabricación de caucho.
El glioblastoma se ha asociado con los virus SV40, HHV-6 y citomegalovirus.
Otro
Se han realizado investigaciones para ver si el consumo de carne curada es un factor de riesgo. No se había confirmado ningún riesgo hasta 2003. De manera similar, se ha estudiado como factores de riesgo la exposición al formaldehído y a campos electromagnéticos residenciales, como los de teléfonos móviles y cableado eléctrico dentro de los hogares. Hasta 2015, no se había demostrado que causaran GBM.
Patogenia
Se desconoce el origen celular del glioblastoma. Debido a las similitudes en la inmunotinción de las células gliales y el glioblastoma, durante mucho tiempo se ha supuesto que los gliomas como el glioblastoma se originan a partir de células madre de tipo glial que se encuentran en la zona subventricular. Estudios más recientes sugieren que los astrocitos, las células progenitoras de oligodendrocitos y las células madre neurales podrían servir como célula de origen.
Los GBM generalmente se forman en la sustancia blanca cerebral, crecen rápidamente y pueden llegar a ser muy grandes antes de producir síntomas. El tumor puede extenderse hacia las meninges o la pared ventricular, lo que provoca un alto contenido de proteínas en el líquido cefalorraquídeo (LCR) (> 100 mg/dl), así como una pleocitosis ocasional de 10 a 100 células, en su mayoría linfocitos. Las células malignas transportadas en el LCR pueden diseminarse (rara vez) a la médula espinal o causar gliomatosis meníngea. Sin embargo, la metástasis de GBM más allá del sistema nervioso central es extremadamente inusual. Alrededor del 50% de los GBM ocupan más de un lóbulo de un hemisferio o son bilaterales. Los tumores de este tipo suelen surgir del cerebro y pueden presentar la clásica infiltración a través del cuerpo calloso, produciendo un glioma en mariposa (bilateral).
Clasificación del glioblastoma
La clasificación de los tumores cerebrales se ha basado tradicionalmente en la histopatología a nivel macroscópico, medida en cortes de hematoxilina-eosina. La Organización Mundial de la Salud publicó la primera clasificación estándar en 1979 y sigue haciéndolo desde entonces. La Clasificación de Tumores del Sistema Nervioso Central de la OMS de 2007 fue la última clasificación basada principalmente en características microscópicas. La nueva Clasificación de Tumores del Sistema Nervioso Central de la OMS de 2016 supuso un cambio de paradigma: algunos de los tumores se definieron también por su composición genética y por su morfología celular.
En 2021 se publicó la quinta edición de la Clasificación de Tumores del Sistema Nervioso Central de la OMS. Esta actualización eliminó la clasificación de glioblastoma secundario y reclasificó esos tumores como astrocitoma, mutante de IDH, grado 4. Ahora solo los tumores que son de tipo natural IDH se clasifican como glioblastoma.
| Sinónimos | Glioblastoma, GBM |
| Célula de origen | Astrocyte |
| Edad mediana al diagnóstico | ~62 años |
| Male:Female ratio | 1.42:1 |
| Longitud mediana de la historia clínica al diagnóstico | 4 meses |
| Supervivencia mediana | |
| Cirugía + radioterapia | 9,9 meses |
| Cirugía + radioterapia + quimioterapia | 15 meses |
| Ubicación | Por lo general supratentorial, rara vez cerebello o columna vertebral |
| Necrosis y proliferación microvascular | Extensivo |
| mutaciones moleculares y genéticas asociadas | mutación TERT promotor, ganancia combinada del cromosoma 7 y pérdida del cromosoma 10; Amplificación EGFR |
alteraciones moleculares
Actualmente hay tres subtipos moleculares de glioblastoma que se identificaron en base a la expresión génica:
- Clásico: Alrededor del 97% de los tumores en este subtipo llevan copias extra del receptor del factor de crecimiento epidérmico (EGFR) gen, y la mayoría tienen una expresión más alta de lo normal EGFR, mientras que el gen TP53 (p53), que a menudo se muta en glioblastoma, rara vez se muta en este subtipo. La pérdida de heterocigosidad en el cromosoma 10 también se ve con frecuencia en el subtipo clásico junto con el cromosoma 7 amplificación.
- El subtipo proneural a menudo tiene altas tasas de alteraciones en TP53 (p53), y PDGFRA el gen codificando un tipo de receptor de factor de crecimiento derivado de plaquetas.
- El subtipo mesenquimal se caracteriza por altas tasas de mutaciones u otras alteraciones en NF1, el gen encoding neurofibromin 1 y menos alteraciones en el EGFR gen y menos expresión de EGFR que otros tipos.
Los análisis iniciales de la expresión génica habían revelado un cuarto subtipo neuronal. Sin embargo, análisis adicionales revelaron que este subtipo no es específico de tumores y es una contaminación potencial causada por las células normales.
Se han descrito muchas otras alteraciones genéticas en el glioblastoma, y la mayoría de ellas se agrupan en dos vías, el RB y el PI3K/AKT. El 68–78% y el 88% de los glioblastomas tienen alteraciones en estas vías, respectivamente.
Otra alteración importante es la metilación de MGMT, A " suicidio " Enzima de reparación de ADN. La metilación perjudica la transcripción de ADN y la expresión del gen MGMT. Dado que la enzima MGMT puede reparar solo una alquilación de ADN debido a su mecanismo de reparación de suicidios, la capacidad de reserva es baja y la metilación del promotor del gen MGMT afecta en gran medida la capacidad de reparación de ADN. La metilación de MGMT se asocia con una respuesta mejorada al tratamiento con quimioterapéutica que daña el ADN, como la temozolomida.
Células madre del cáncer
En los glioblastomas se han encontrado células de glioblastoma con propiedades similares a las células progenitoras (células madre cancerosas de glioblastoma). Su presencia, unida a la naturaleza difusa del glioblastoma, dificulta su extirpación quirúrgica por completo, por lo que se cree que es la posible causa de la resistencia a los tratamientos convencionales y de la alta tasa de recurrencia. Las células madre del cáncer de glioblastoma comparten cierta semejanza con las células progenitoras neurales, y ambas expresan el receptor de superficie CD133. CD44 también se puede utilizar como marcador de células madre cancerosas en un subconjunto de células tumorales de glioblastoma. Las células madre del cáncer de glioblastoma parecen exhibir una mayor resistencia a la radioterapia y la quimioterapia mediada, al menos en parte, por la regulación positiva de la respuesta al daño del ADN.
Metabolismo
El gen IDH1 codifica la enzima isocitrato deshidrogenasa 1 y no está mutado en el glioblastoma. Como tal, estos tumores se comportan de manera más agresiva en comparación con los astrocitomas con mutación IDH1.
Canales de iones
Además, GBM exhibe numerosas alteraciones en los genes que codifican canales iónicos, incluida la regulación positiva de los canales de potasio gBK y los canales de cloruro ClC-3. Se supone que al regular positivamente estos canales iónicos, las células tumorales de glioblastoma facilitan un mayor movimiento de iones sobre la membrana celular, aumentando así el movimiento de H2O a través de la ósmosis, lo que ayuda a las células de glioblastoma a cambiar el volumen celular muy rápidamente. Esto es útil en su comportamiento invasivo extremadamente agresivo porque las adaptaciones rápidas en el volumen celular pueden facilitar el movimiento a través de la sinuosa matriz extracelular del cerebro.
MicroARN
A partir de 2012, la interferencia del ARN, generalmente microARN, estaba bajo investigación en cultivos de tejidos, muestras patológicas y modelos animales preclínicos de glioblastoma. Además, las observaciones experimentales sugieren que el microARN-451 es un regulador clave de la señalización de LKB1/AMPK en células de glioma cultivadas y que la agrupación de miARN controla las vías epigenéticas en la enfermedad.
Vasculatura tumoral
GBM se caracteriza por vasos anormales que presentan morfología y funcionalidad alteradas. La alta permeabilidad y la mala perfusión de la vasculatura dan como resultado un flujo sanguíneo desorganizado dentro del tumor y pueden provocar un aumento de la hipoxia, lo que a su vez facilita la progresión del cáncer al promover procesos como la inmunosupresión.
Diagnóstico

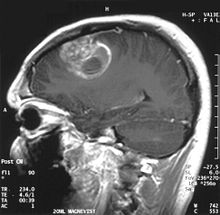
Cuando se observan con resonancia magnética, los glioblastomas a menudo aparecen como lesiones que realzan los anillos. Sin embargo, la apariencia no es específica, ya que otras lesiones como abscesos, metástasis, esclerosis múltiple tumefactiva y otras entidades pueden tener una apariencia similar. El diagnóstico definitivo de una sospecha de GBM mediante TC o RM requiere una biopsia estereotáxica o una craneotomía con resección del tumor y confirmación patológica. Debido a que el grado del tumor se basa en la porción más maligna del tumor, la biopsia o la resección subtotal del tumor pueden dar como resultado una subclasificación de la lesión. Las imágenes del flujo sanguíneo del tumor mediante resonancia magnética de perfusión y la medición de la concentración de metabolitos tumorales con espectroscopia de resonancia magnética pueden agregar valor diagnóstico a la resonancia magnética estándar en casos seleccionados al mostrar un aumento relativo del volumen sanguíneo cerebral y un aumento del pico de colina, respectivamente, pero la patología sigue siendo el estándar de oro para el diagnóstico y la evaluación molecular. caracterización.
Es importante distinguir el glioblastoma del astrocitoma de alto grado. Estos tumores ocurren espontáneamente (de novo) y no han progresado desde un glioma de grado inferior, como en los astrocitomas de grado alto. Los glioblastomas tienen un peor pronóstico y una biología tumoral diferente, y pueden tener una respuesta diferente al tratamiento., lo que hace que esta sea una evaluación crítica para determinar el pronóstico y la terapia del paciente. Los astrocitomas portan una mutación en IDH1 o IDH2, mientras que esta mutación no está presente en el glioblastoma. Así, las mutaciones IDH1 e IDH2 son una herramienta útil para distinguir glioblastomas de astrocitomas, ya que histopatológicamente son similares y la distinción sin biomarcadores moleculares no es fiable. Los glioblastomas de tipo salvaje con IDH suelen tener una expresión de OLIG2 más baja en comparación con los astrocitomas de grado inferior con mutaciones de IDH.
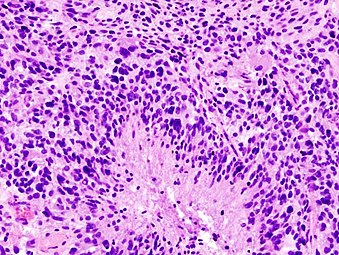
- Histopatología del glioblastoma, mostrando características astrocitoma de alto grado del pleommorfismo nuclear marcado, múltiples mitoses (uno a la flecha blanca) y células multinucleadas (uno a la flecha negra), con células que tienen un arreglo sin patrón en un fondo fibrilar rosado en la mancha H bordeE.
- Hetopatología de aumento inferior, mostrando necrosis rodeada de pseudopalisades de células tumorales, conferiendo un diagnóstico de glioblastoma en lugar de astrocitoma anaplásico
Prevención
No hay métodos conocidos para prevenir el glioblastoma. Es el caso de la mayoría de los gliomas, a diferencia de otras formas de cáncer, que ocurren sin una advertencia previa y no hay formas conocidas de prevenirlos.
tratamiento
Tratar el glioblastoma es difícil debido a varios factores complicados:
- Las células tumorales son resistentes a las terapias convencionales.
- El cerebro es susceptible a daño por terapia convencional.
- El cerebro tiene una capacidad limitada para repararse.
- Muchos fármacos no pueden cruzar la barrera de sangre-cerebro para actuar en el tumor.
El tratamiento de los tumores cerebrales primarios consiste en cuidados paliativos (sintomáticos) y terapias destinadas a mejorar la supervivencia.
Terapia sintomática
El tratamiento de apoyo se centra en aliviar los síntomas y mejorar la función neurológica del paciente. Los principales agentes de apoyo son los anticonvulsivos y los corticosteroides.
- Históricamente, alrededor del 90% de los pacientes con glioblastoma fueron sometidos a tratamiento anticonvulsivo, aunque sólo un 40% estimado de los pacientes requirieron este tratamiento. Los neurocirujanos han recomendado que los anticonvulsivos no se administren profilácticamente, y deben esperar hasta que se produzca un ataque antes de prescribir este medicamento. Aquellos que reciben fenitoína concurrente con la radiación pueden tener reacciones cutáneas graves como el erythema multiforme y el síndrome de Stevens-Johnson.
- Los corticosteroides, generalmente dexamethasona, pueden reducir el edema peritumoral (a través de la reorganización de la barrera sanguínea-cerebro), disminuir el efecto de masa y disminuir la presión intracraneal, con una disminución del dolor de cabeza o somnolencia.
Cirugía

La cirugía es la primera etapa del tratamiento del glioblastoma. Un tumor GBM promedio contiene 1011 células, que en promedio se reduce a 109 células después de la cirugía (una reducción del 99%). Los beneficios de la cirugía incluyen la resección para un diagnóstico patológico, el alivio de los síntomas relacionados con el efecto de masa y la posible eliminación de la enfermedad antes de que se produzca una resistencia secundaria a la radioterapia y la quimioterapia.
Cuanto mayor sea el alcance de la extirpación del tumor, mejor. En análisis retrospectivos, la extirpación del 98 % o más del tumor se ha asociado con un tiempo de salud significativamente más largo que si se extirpa menos del 98 % del tumor. Las posibilidades de una extirpación inicial casi completa del tumor pueden aumentar si la cirugía se guía por un tinte fluorescente conocido como ácido 5-aminolevulínico. Las células GBM se infiltran ampliamente a través del cerebro en el momento del diagnóstico y, a pesar de una "resección total" De todos los tumores obvios, la mayoría de las personas con GBM desarrollan posteriormente tumores recurrentes, ya sea cerca del sitio original o en ubicaciones más distantes dentro del cerebro. Otras modalidades, generalmente radiación y quimioterapia, se utilizan después de la cirugía en un esfuerzo por suprimir y retardar la enfermedad recurrente al dañar el ADN de las células GBM de rápida proliferación.
Radioterapia

Después de la cirugía, la radioterapia se convierte en la base del tratamiento para las personas con glioblastoma. Por lo general, se realiza junto con la administración de temozolomida. Un ensayo clínico fundamental llevado a cabo a principios de la década de 1970 mostró que entre 303 pacientes con GBM asignados al azar a radiación o la mejor terapia médica, los que recibieron radiación tuvieron una supervivencia media de más del doble que los que no la recibieron. La investigación clínica posterior ha intentado aprovechar la base de la cirugía seguida de radiación. La radioterapia de todo el cerebro no mejora en comparación con la radioterapia conformada tridimensional, más precisa y dirigida. Se ha descubierto que una dosis total de radiación de 60 a 65 Gy es óptima para el tratamiento.
Es bien sabido que los tumores GBM contienen zonas de tejido que exhiben hipoxia, que son altamente resistentes a la radioterapia. Se han seguido varios enfoques para los radiosensibilizadores de quimioterapia, con un éxito limitado a partir de 2016. A partir de 2010, los enfoques de investigación más nuevos incluyeron investigaciones preclínicas y clínicas sobre el uso de un compuesto que mejora la difusión de oxígeno, como el crocetinato transsódico, como radiosensibilizadores, y a partir de 2015. se estaba realizando un ensayo clínico. La terapia de captura de neutrones con boro se ha probado como tratamiento alternativo para el glioblastoma, pero no es de uso común.
Quimioterapia
La mayoría de los estudios no muestran ningún beneficio al agregar quimioterapia. Sin embargo, un gran ensayo clínico de 575 participantes asignados al azar a radiación estándar versus radiación más quimioterapia con temozolomida mostró que el grupo que recibió temozolomida sobrevivió una mediana de 14,6 meses en comparación con 12,1 meses para el grupo que recibió radiación sola. Este régimen de tratamiento es ahora estándar para la mayoría de los casos de glioblastoma en los que la persona no está inscrita en un ensayo clínico. La temozolomida parece actuar sensibilizando las células tumorales a la radiación y parece más eficaz para los tumores con metilación del promotor MGMT. Las dosis altas de temozolomida en los gliomas de alto grado producen una toxicidad baja, pero los resultados son comparables a las dosis estándar. La terapia antiangiogénica con medicamentos como bevacizumab controla los síntomas, pero no parece afectar la supervivencia general en personas con glioblastoma. El beneficio general de las terapias antiangiogénicas a partir de 2019 no está claro. En personas de edad avanzada con glioblastoma recién diagnosticado que están razonablemente en forma, la quimiorradioterapia concurrente y adyuvante proporciona la mejor supervivencia general, pero se asocia con un mayor riesgo de eventos adversos hematológicos que la radioterapia sola.
Inmunoterapia
Los ensayos clínicos de fase 3 de tratamientos de inmunoterapia para el glioblastoma han fracasado en gran medida.
Otros trámites
La terapia de campo eléctrico alterno es una terapia aprobada por la FDA para el glioblastoma recurrente y recién diagnosticado. En 2015, los resultados iniciales de un ensayo clínico aleatorizado de fase III de terapia de campo eléctrico alterno más temozolomida en glioblastoma recién diagnosticado informaron una mejora de tres meses en la supervivencia libre de progresión y una mejora de cinco meses en la supervivencia general en comparación con la terapia con temozolomida sola., lo que representa el primer gran ensayo en una década que muestra una mejora en la supervivencia en este contexto. A pesar de estos resultados, la eficacia de este enfoque sigue siendo controvertida entre los expertos médicos. Sin embargo, una mayor comprensión de la base mecanicista a través de la cual la terapia con campos eléctricos alternos ejerce efectos anticancerígenos y los resultados de los ensayos clínicos de fase III en curso en cánceres extracraneales pueden ayudar a facilitar una mayor aceptación clínica para tratar el glioblastoma en el futuro.
Pronóstico
La duración de supervivencia más común después del diagnóstico es de 10 a 13 meses (aunque investigaciones recientes apuntan a una tasa de supervivencia media de 15 meses), y menos del 1 al 3 % de las personas sobreviven más de cinco años. En Estados Unidos, entre 2012 y 2016, la supervivencia a cinco años fue del 6,8%. Sin tratamiento, la supervivencia suele ser de tres meses. Las curas completas son extremadamente raras, pero se han informado.
El aumento de la edad (>60 años) conlleva un peor riesgo de pronóstico. La muerte suele deberse a una infiltración tumoral generalizada con edema cerebral y aumento de la presión intracraneal.
Una buena puntuación inicial de rendimiento de Karnofsky (KPS) y la metilación de MGMT se asocian con una supervivencia más larga. Se puede realizar una prueba de ADN en los glioblastomas para determinar si el promotor del gen MGMT está metilado o no. Los pacientes con un promotor MGMT metilado tienen una supervivencia más prolongada que aquellos con un promotor MGMT no metilado, debido en parte a una mayor sensibilidad a la temozolomida.
Los beneficios a largo plazo también se han asociado con aquellos pacientes que reciben cirugía, radioterapia y quimioterapia con temozolomida. Sin embargo, aún se desconoce mucho sobre por qué algunos pacientes sobreviven más tiempo con glioblastoma. La edad menor de 50 años está relacionada con una supervivencia más larga en el GBM, al igual que una resección superior al 98 % y el uso de quimioterapia con temozolomida y mejores KPS. Un estudio reciente confirma que una edad más temprana se asocia con un pronóstico mucho mejor, y una pequeña fracción de pacientes menores de 40 años logran una curación basada en la población. Se cree que la curación se produce cuando el riesgo de muerte de una persona vuelve al de la población normal y, en el caso del GBM, se cree que esto ocurre después de 10 años.
UCLA Neuro-oncology publica datos de supervivencia en tiempo real para pacientes con este diagnóstico.
Según un estudio de 2003, el pronóstico del GBM se puede dividir en tres subgrupos dependiendo del KPS, la edad del paciente y el tratamiento.
| Análisis de partición Recursiva (RPA) class | Definición | Tiempo de supervivencia medieval histórico | Sobrevivencia histórica de 1 año | Sobrevivencia histórica de 3 años | Sobrevivencia histórica de 5 años |
|---|---|---|---|---|---|
| III | Edad 50, KPS ≥ 90 | 17,1 meses | 70% | 20% | 14% |
| IV | Edad: 50, KPS | 11.2 meses | 46% | 7% | 4% |
| Edad ≥ 50, KPS ≥ 70, extirpación quirúrgica con buena función neurológica | |||||
| V + VI | Edad ≥ 50, KPS ≥ 70, sin extirpación quirúrgica | 7.5 meses | 28% | 1% | 0% |
| Edad ≥ 50, KPS |
Epidemiología
Aproximadamente tres de cada 100.000 personas desarrollan la enfermedad al año, aunque la frecuencia regional puede ser mucho mayor. La frecuencia en Inglaterra se duplicó entre 1995 y 2015.
Es el segundo tumor más común del sistema nervioso central después del meningioma. Ocurre más comúnmente en hombres que en mujeres. Aunque la edad promedio en el momento del diagnóstico es 64 años, en 2014 la amplia categoría de cánceres cerebrales ocupaba el segundo lugar después de la leucemia en personas menores de 20 años en los Estados Unidos.
Historia
El término glioblastoma multiforme fue introducido en 1926 por Percival Bailey y Harvey Cushing, basándose en la idea de que el tumor se origina a partir de precursores primitivos de las células gliales (glioblastos) y la apariencia altamente variable debido a la presencia de necrosis, hemorragia y quistes (multiformes).
Investigación
Terapia génica
La terapia génica se ha explorado como método para tratar el glioblastoma y, aunque los modelos animales y los ensayos clínicos de fase temprana han tenido éxito, a partir de 2017, todos los medicamentos de terapia génica que se habían probado en ensayos clínicos de fase III para el glioblastoma había fracasado. Los científicos han desarrollado LPLNP-PPT nanoestructurado de núcleo-cubierta (nanopartículas de luminiscencia persistentes largas. PPT se refiere a polieterimida, PEG y transactivador de la transcripción, y TRAIL es el ligando inducido por apoptosis relacionado con el factor de necrosis tumoral humano) para la administración eficaz de genes y seguimiento, con resultados positivos. Se trata de un ligando TRAIL que ha sido codificado para inducir la apoptosis de células cancerosas, más específicamente de glioblastomas. Aunque este estudio todavía estaba en ensayos clínicos en 2017, ha demostrado funcionalidades diagnósticas y terapéuticas, y abrirá un gran interés para las aplicaciones clínicas en la terapia basada en células madre.
Viroterapia oncolítica
La viroterapia oncolítica es un tratamiento novedoso emergente que está bajo investigación tanto en etapas preclínicas como clínicas. Actualmente se están probando varios virus, incluidos el virus del herpes simple, el adenovirus, el poliovirus y el reovirus, en las fases I y II de ensayos clínicos para el tratamiento del glioblastoma y se ha demostrado que mejoran la supervivencia general.
Entrega de medicamentos por vía intranasal
Se está explorando la administración directa de fármacos de la nariz al cerebro como medio para lograr concentraciones de fármaco más altas y, con suerte, más efectivas en el cerebro. Un estudio clínico de fase I/II con pacientes con glioblastoma en Brasil investigó el compuesto natural alcohol perilílico para su administración intranasal en forma de aerosol. Los resultados fueron alentadores y, a partir de 2016, se inició un ensayo similar en Estados Unidos.
Cannabinoides
La eficacia de los cannabinoides (derivados del cannabis) es conocida en oncología (a través de cápsulas de tetrahidrocannabinol (THC) o del análogo sintético nabilona), por un lado para combatir las náuseas y los vómitos inducidos por la quimioterapia, por otro para estimular el apetito y disminuir la sensación de angustia o el dolor real. Se ha demostrado su capacidad para inhibir el crecimiento y la angiogénesis en gliomas malignos en modelos de ratón. Los resultados de un estudio piloto sobre el uso de THC en pacientes terminales con glioblastoma recurrente parecieron dignos de estudio adicional. Una posible vía para futuras investigaciones se basa en el descubrimiento de que los cannabinoides son capaces de atacar las células madre neoplásicas del glioblastoma en modelos de ratón, con el resultado, por un lado, de inducir su diferenciación en células más maduras y posiblemente más "tratables".; células, y por otro lado para inhibir la tumorigénesis.