Formación reticular
La formación reticular es un conjunto de núcleos interconectados que se encuentran a lo largo de todo el tronco del encéfalo. No está bien definido anatómicamente, porque incluye neuronas ubicadas en diferentes partes del cerebro. Las neuronas de la formación reticular forman un complejo conjunto de redes en el núcleo del tronco encefálico que se extienden desde la parte superior del mesencéfalo hasta la parte inferior del bulbo raquídeo. La formación reticular incluye vías ascendentes hacia la corteza en el sistema activador reticular ascendente (ARAS) y vías descendentes hacia la médula espinal a través de los tractos reticuloespinales. .
Las neuronas de la formación reticular, particularmente las del sistema activador reticular ascendente, desempeñan un papel crucial en el mantenimiento de la excitación conductual y la conciencia. Las funciones generales de la formación reticular son moduladoras y premotoras, involucrando control motor somático, control cardiovascular, modulación del dolor, sueño y conciencia, y habituación. Las funciones moduladoras se encuentran principalmente en el sector rostral de la formación reticular y las funciones premotoras se localizan en las neuronas de las regiones más caudales.
La formación reticular se divide en tres columnas: núcleos del rafe (mediana), núcleos reticulares gigantocelulares (zona medial) y núcleos reticulares parvocelulares (zona lateral). Los núcleos del rafe son el lugar de síntesis del neurotransmisor serotonina, que desempeña un papel importante en la regulación del estado de ánimo. Los núcleos gigantocelulares participan en la coordinación motora. Los núcleos parvocelulares regulan la exhalación.
La formación reticular es esencial para gobernar algunas de las funciones básicas de los organismos superiores y es una de las porciones filogenéticamente más antiguas del cerebro.
Estructura

La formación reticular humana está compuesta por casi 100 núcleos cerebrales y contiene muchas proyecciones hacia el prosencéfalo, el tronco del encéfalo y el cerebelo, entre otras regiones. Incluye los núcleos reticulares, fibras de proyección reticulotalámica, proyecciones talamocorticales difusas, proyecciones colinérgicas ascendentes, proyecciones no colinérgicas descendentes y proyecciones reticuloespinales descendentes. La formación reticular también contiene dos subsistemas neurales principales, el sistema activador reticular ascendente y los tractos reticuloespinales descendentes, que median distintos procesos cognitivos y fisiológicos. Se ha escindido funcionalmente tanto sagital como coronalmente.
Tradicionalmente los núcleos reticulares se dividen en tres columnas:
- En la columna mediana – los núcleos raphe
- En la columna medial – núcleos gigantescelulares (por el tamaño más grande de las células)
- En la columna lateral – núcleos parvocelulares (por el tamaño más pequeño de las células)
La diferenciación funcional original era una división de caudal y rostral. Esto se basó en la observación de que la lesión de la formación reticular rostral induce hipersomnia en el cerebro del gato. Por el contrario, la lesión de la porción más caudal de la formación reticular produce insomnio en los gatos. Este estudio ha llevado a la idea de que la porción caudal inhibe la porción rostral de la formación reticular.
La división sagital revela más distinciones morfológicas. Los núcleos del rafe forman una cresta en el medio de la formación reticular y, directamente en su periferia, hay una división llamada formación reticular medial. El RF medial es grande y tiene largas fibras ascendentes y descendentes, y está rodeado por la formación reticular lateral. El RF lateral está cerca de los núcleos motores de los nervios craneales y media principalmente en su función.
Formación reticular medial y lateral
La formación reticular medial y la formación reticular lateral son dos columnas de núcleos con límites mal definidos que envían proyecciones a través de la médula y hacia el mesencéfalo. Los núcleos se pueden diferenciar por función, tipo de célula y proyecciones de nervios eferentes o aferentes. Moviéndose caudalmente desde el mesencéfalo rostral, en el sitio de la protuberancia rostral y el mesencéfalo, el RF medial se vuelve menos prominente y el RF lateral se vuelve más prominente.
A los lados de la formación reticular medial existe su primo lateral, que es particularmente pronunciado en la médula rostral y la protuberancia caudal. De esta zona surgen los nervios craneales, incluido el muy importante nervio vago. El RF lateral es conocido por sus ganglios y áreas de interneuronas alrededor de los nervios craneales, que sirven para mediar sus reflejos y funciones características.
Función
La formación reticular consta de más de 100 pequeñas redes neuronales, con funciones variadas que incluyen las siguientes:
- Control de motores somáticos – Algunas neuronas motoras envían sus ejes a los núcleos de formación reticular, dando lugar a las vías reticulospinales de la médula espinal. Estos aparatos funcionan para mantener el tono, el equilibrio y la postura, especialmente durante los movimientos corporales. La formación reticular también transmite señales de ojos y oídos al cerebelo para que el cerebelo pueda integrar estímulos visuales, auditivos y vestibulares en coordinación motora. Otros núcleos de motor incluyen centros de mirada, que permiten a los ojos rastrear y fijar objetos, y generadores de patrón central, que producen señales rítmicas de respiración y deglución.
- Control cardiovascular – La formación reticular incluye los centros cardíacos y vasomotores de la medulla oblongata.
- Modulación del dolor – La formación reticular es un medio por el cual las señales de dolor del cuerpo inferior llegan a la corteza cerebral. También es el origen de los caminos analgésicos descendentes. Las fibras nerviosas de estas vías actúan en la médula espinal para bloquear la transmisión de algunas señales de dolor al cerebro.
- El sueño y la conciencia – La formación reticular tiene proyecciones al talamo y la corteza cerebral que le permiten ejercer algún control sobre el cual las señales sensoriales llegan al cerebro y llegan a nuestra atención consciente. Juega un papel central en los estados de conciencia como la alerta y el sueño. La lesión a la formación reticular puede resultar en coma irreversible.
- Habituación – Este es un proceso en el que el cerebro aprende a ignorar estímulos repetitivos y sin sentido mientras permanece sensible a otros. Un buen ejemplo de esto es una persona que puede dormir a través del tráfico fuerte en una gran ciudad, pero se despierta rápidamente debido al sonido de una alarma o bebé llorando. Los núcleos de formación reticular que modulan la actividad de la corteza cerebral forman parte del sistema de activación reticular ascendente.
Subsistemas principales
Sistema activador reticular ascendente
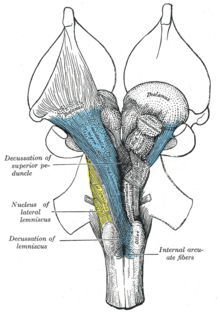
El sistema activador reticular ascendente (ARAS), también conocido como sistema modulador de control extratalámico o simplemente sistema activador reticular (RAS), es un conjunto de núcleos conectados en el cerebro de los vertebrados que se encarga de regular la vigilia y las transiciones sueño-vigilia. El ARAS es parte de la formación reticular y está compuesto principalmente por varios núcleos en el tálamo y varios núcleos cerebrales dopaminérgicos, noradrenérgicos, serotoninérgicos, histaminérgicos, colinérgicos y glutamatérgicos.
Estructura del ARAS
El ARAS está compuesto por varios circuitos neuronales que conectan la parte dorsal del mesencéfalo posterior y la protuberancia anterior con la corteza cerebral a través de distintas vías que se proyectan a través del tálamo y el hipotálamo. El ARAS es un conjunto de núcleos diferentes: más de 20 a cada lado en la parte superior del tronco encefálico, la protuberancia, la médula y el hipotálamo posterior. Los neurotransmisores que liberan estas neuronas incluyen dopamina, norepinefrina, serotonina, histamina, acetilcolina y glutamato. Ejercen influencia cortical a través de proyecciones axonales directas y proyecciones indirectas a través de relevos talámicos.
La vía talámica consta principalmente de neuronas colinérgicas en el tegmento pontino, mientras que la vía hipotalámica está compuesta principalmente de neuronas que liberan neurotransmisores monoamino, a saber, dopamina, norepinefrina, serotonina e histamina. Las neuronas liberadoras de glutamato en el ARAS se identificaron mucho más recientemente en relación con los núcleos monoaminérgicos y colinérgicos; el componente glutamatérgico del ARAS incluye un núcleo en el hipotálamo y varios núcleos del tronco del encéfalo. Las neuronas orexina del hipotálamo lateral inervan todos los componentes del sistema activador reticular ascendente y coordinan la actividad dentro de todo el sistema.
| Tipo de nucleus | núcleos correspondientes que median excitación | Fuentes |
|---|---|---|
| núcleos dopaminérgicos |
| |
| Noradrenergic nuclei |
| |
| núcleos serotonérgicos |
| |
| núcleos histéricos |
| |
| núcleos cholinergicos |
| |
| Glutamatergic nuclei |
| |
| núcleos Thalamic |
|
El ARAS consta de áreas evolutivamente antiguas del cerebro, que son cruciales para la supervivencia del animal y están protegidas durante períodos adversos, como durante los períodos inhibidores del reflejo de Totsell, también conocido como "hipnosis animal" . El sistema activador reticular ascendente que envía proyecciones neuromoduladoras a la corteza, se conecta principalmente a la corteza prefrontal. Parece haber una baja conectividad con las áreas motoras de la corteza.
Funciones del ARAS
Conciencia
El sistema activador reticular ascendente es un importante factor habilitante para el estado de conciencia. Se considera que el sistema ascendente contribuye a la vigilia, caracterizada por la excitación cortical y conductual.
Regulación de las transiciones sueño-vigilia
La función principal del ARAS es modificar y potenciar la función talámica y cortical de modo que se produzca la desincronización del electroencefalograma (EEG). Existen claras diferencias en la actividad eléctrica del cerebro durante los períodos de vigilia y sueño: las ondas cerebrales de ráfaga rápida de bajo voltaje (desincronización EEG) se asocian con la vigilia y el sueño REM (que son electrofisiológicamente similares); Las ondas lentas de alto voltaje se encuentran durante el sueño no REM. En términos generales, cuando las neuronas de relevo talámicas están en modo ráfaga, el EEG está sincronizado y cuando están en modo tónico, está desincronizado. La estimulación del ARAS produce desincronización del EEG al suprimir ondas corticales lentas (0,3 a 1 Hz), ondas delta (1 a 4 Hz) y oscilaciones de ondas del huso (11 a 14 Hz) y al promover oscilaciones de la banda gamma (20 a 40 Hz). .
El cambio fisiológico de un estado de sueño profundo a vigilia es reversible y está mediado por el ARAS. El núcleo preóptico ventrolateral (VLPO) del hipotálamo inhibe los circuitos neuronales responsables del estado de vigilia y la activación del VLPO contribuye al inicio del sueño. Durante el sueño, las neuronas del ARAS tendrán una velocidad de activación mucho menor; por el contrario, tendrán un mayor nivel de actividad durante el estado de vigilia. Para que el cerebro pueda dormir, debe haber una reducción de la actividad aferente ascendente que llega a la corteza mediante la supresión del ARAS.
Atención
El ARAS también ayuda a mediar en las transiciones desde la vigilia relajada hasta períodos de alta atención. Hay un aumento del flujo sanguíneo regional (presumiblemente indicando una mayor medida de actividad neuronal) en la formación reticular del mesencéfalo (MRF) y en los núcleos intralaminares talámicos durante las tareas que requieren mayor estado de alerta y atención.
Importancia clínica del ARAS
Las lesiones masivas en los núcleos ARAS del tronco encefálico pueden causar alteraciones graves en el nivel de conciencia (p. ej., coma). El daño bilateral a la formación reticular del mesencéfalo puede provocar coma o muerte.
La estimulación eléctrica directa del ARAS produce respuestas de dolor en gatos y provoca informes verbales de dolor en humanos. La activación reticular ascendente en gatos puede producir midriasis, que puede resultar de un dolor prolongado. Estos resultados sugieren alguna relación entre los circuitos ARAS y las vías fisiológicas del dolor.
Patologías
Algunas patologías del ARAS pueden atribuirse a la edad, ya que parece haber una disminución general en la reactividad del ARAS con el paso de los años. Se ha sugerido que los cambios en el acoplamiento eléctrico explican algunos cambios en la actividad de ARAS: si el acoplamiento se regulara negativamente, habría una disminución correspondiente en la sincronización de frecuencias más altas (banda gamma). Por el contrario, el acoplamiento eléctrico regulado al alza aumentaría la sincronización de los ritmos rápidos, lo que podría conducir a un aumento de la excitación y del impulso del sueño REM. Específicamente, la alteración del ARAS se ha implicado en los siguientes trastornos:
- Narcolepsia: Los iones a lo largo de los núcleos pedunculopontine (PPT/PPN) / tegmental laterodorsal (LDT) están asociados con la narcolepsia. Hay una baja regulación significativa de la salida PPN y una pérdida de péptidos orexinos, promoviendo la excesiva somnolencia diurna que es característica de este trastorno.
- Parálisis supranuclear progresiva (PSP): El funcionamiento de la señalización de óxido nitroso ha sido implicado en el desarrollo de PSP.
- Enfermedad de Parkinson: Las perturbaciones del sueño REM son comunes en Parkinson. Es principalmente una enfermedad dopaminérgica, pero los núcleos cholinergicos también están agotados. La degeneración en el ARAS comienza temprano en el proceso de enfermedad.
Influencias del desarrollo
Existen varios factores potenciales que pueden influir negativamente en el desarrollo del sistema activador reticular ascendente:
- Nacimiento prematuro: Independientemente del peso del nacimiento o semanas de gestación, el nacimiento prematuro induce efectos perjudiciales persistentes en las anomalías preatenciosas (anormalidades auditivas y del sueño), la atención (tiempo de reacción y el cálculo sensorial) y los mecanismos corticales a lo largo del desarrollo.
- Fumar durante el embarazo: Se sabe que la exposición prenatal al humo del cigarrillo produce déficits de excitación, atención y cognición duraderos en los seres humanos. Esta exposición puede inducir a la regulación de los receptores nicotinicos α4β2 en las células del núcleo pedunculopontino (PPN), dando lugar a una mayor actividad tónica, potencial de reposo de la membrana y corriente de cación activada de hiperpolarización. Estas principales perturbaciones de las propiedades de membrana intrínsecas de las neuronas PPN provocan un aumento de los niveles de gatión excitante y sensorial, déficits (demostrados por una disminución de la habituación a estímulos auditivos repetidos). Es hipotetizado que estos cambios fisiológicos pueden intensificar la disregulación de la atención más adelante en la vida.
Descendiendo las vías reticulospinales
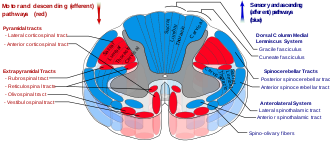
Los tractos reticuloespinales, también conocidos como tractos reticuloespinales descendentes o anteriores, son tractos motores extrapiramidales que descienden de la formación reticular en dos tractos para actuar sobre las neuronas motoras que irrigan el tronco y los flexores proximales de las extremidades. y extensores. Los haces reticuloespinales participan principalmente en la locomoción y el control postural, aunque también tienen otras funciones. Los tractos reticuloespinales descendentes son una de las cuatro vías corticales principales hacia la médula espinal para la actividad musculoesquelética. Los tractos reticuloespinales trabajan con las otras tres vías para brindar un control coordinado del movimiento, incluidas manipulaciones delicadas. Las cuatro vías se pueden agrupar en dos vías sistémicas principales: un sistema medial y un sistema lateral. El sistema medial incluye la vía reticuloespinal y la vía vestibuloespinal, y este sistema proporciona control de la postura. Las vías corticoespinal y rubroespinal pertenecen al sistema lateral que proporciona un control preciso del movimiento.
Vástagos mediales y laterales
Este tracto descendente se divide en dos partes, los tractos reticuloespinales medial (o pontino) y lateral (o medular) (MRST y LRST).
- El tracto reticulospinal medial es responsable de excitantes músculos antigravedad, extensores. Las fibras de este tracto surgen del núcleo reticular pontino caudal y del núcleo reticular pontino oral y proyecto a laminado VII y laminado VIII de la médula espinal.
- El tracto reticulospinal lateral es responsable de inhibir los músculos axiales excitatorios del movimiento. También es responsable de la respiración automática. Las fibras de este tracto surgen de la formación reticular medular, principalmente del núcleo gigantocelular, y bajan la longitud de la médula espinal en la parte anterior de la columna lateral. El tracto termina en lamina VII principalmente con algunas fibras terminando en lamina IX de la médula espinal.
El tracto sensorial ascendente que transmite información en la dirección opuesta se conoce como tracto espinorreticular.
Funciones de los tractos reticuloespinales
- Integra información de los sistemas de motor para coordinar los movimientos automáticos de locomoción y postura
- Facilita e inhibe el movimiento voluntario; influye en el tono muscular
- Media funciones autonómicas
- Modula los impulsos del dolor
- Influencias de flujo sanguíneo al núcleo geniculado lateral del tálamo.
Significado clínico de las vías reticulospinales
Los tractos reticuloespinales proporcionan una vía por la cual el hipotálamo puede controlar el flujo simpático toracolumbar y el flujo sacro parasimpático.
Dos sistemas descendentes principales que transportan señales desde el tronco del encéfalo y el cerebelo a la médula espinal pueden desencadenar una respuesta postural automática para el equilibrio y la orientación: los tractos vestibuloespinales de los núcleos vestibulares y los tractos reticuloespinales de la protuberancia y la médula. Las lesiones de estos tractos provocan ataxia profunda e inestabilidad postural.
El daño físico o vascular al tronco del encéfalo que desconecta el núcleo rojo (cerebro medio) y los núcleos vestibulares (protuberancia) puede causar rigidez de descerebración, que tiene el signo neurológico de aumento del tono muscular y reflejos de estiramiento hiperactivos. En respuesta a un estímulo sorprendente o doloroso, ambos brazos y piernas se extienden y giran internamente. La causa es la actividad tónica de los tractos vestibuloespinal y reticuloespinal laterales que estimulan las motoneuronas extensoras sin las inhibiciones del tracto rubroespinal.
El daño del tronco encefálico por encima del nivel del núcleo rojo puede causar rigidez de decorticación. En respuesta a un estímulo sorprendente o doloroso, los brazos se flexionan y las piernas se extienden. La causa es el núcleo rojo, a través del tracto rubroespinal, que contrarresta la excitación de la neurona motora extensora desde los tractos vestibuloespinal y reticuloespinal laterales. Debido a que el tracto rubroespinal solo se extiende hasta la médula espinal cervical, actúa principalmente en los brazos excitando los músculos flexores e inhibiendo los extensores, en lugar de las piernas.
El daño a la médula debajo de los núcleos vestibulares puede causar parálisis fláccida, hipotonía, pérdida del impulso respiratorio y cuadriplejía. No hay reflejos que se parezcan a las primeras etapas del shock espinal debido a la pérdida completa de actividad en las neuronas motoras, ya que ya no hay actividad tónica que surja de los haces vestibuloespinal y reticuloespinal laterales.
Historia
El término "formación reticular" fue acuñado a finales del siglo XIX por Otto Deiters, coincidiendo con Ramon y Cajal neurona doctrina. Allan Hobson declara en su libro La formación reticular revisitada que el nombre es un vestigio etimológico de la era caída de la teoría del campo agregado en las ciencias neuronales. El término "reticulum" significa "estructura similar", que es lo que la formación reticular se asemeja a primera vista. Se ha descrito como demasiado complejo para estudiar o una parte no diferenciada del cerebro sin ninguna organización. Eric Kandel describe la formación reticular como organizada de manera similar a la materia gris intermedia de la médula espinal. Esta forma caótica, floja e intrincada de organización es lo que ha rechazado a muchos investigadores de mirar más lejos en esta área particular del cerebro. Las células carecen de límites gangliónicos claros, pero tienen una organización funcional clara y tipos de células diferentes. El término "formación reticular" rara vez se usa más excepto para hablar en generalidades. Los científicos modernos generalmente se refieren a los núcleos individuales que componen la formación reticular.
Moruzzi y Magoun investigaron por primera vez los componentes neuronales que regulan los mecanismos de sueño-vigilia del cerebro en 1949. Los fisiólogos habían propuesto que alguna estructura profunda dentro del cerebro controlaba la vigilia y el estado de alerta mentales. Se pensaba que la vigilia dependía únicamente de la recepción directa de estímulos aferentes (sensoriales) en la corteza cerebral.
Dado que la estimulación eléctrica directa del cerebro podría simular relés electrocorticales, Magoun utilizó este principio para demostrar, en dos áreas separadas del tronco encefálico de un gato, cómo producir la vigilia a partir del sueño. Primero estimuló las vías ascendentes somáticas y auditivas; en segundo lugar, una serie de "relés ascendentes desde la formación reticular de la parte inferior del tronco del encéfalo a través del tegmento del mesencéfalo, el subtálamo y el hipotálamo hasta la cápsula interna". Esto último fue de particular interés, ya que esta serie de relés no correspondía a ninguna vía anatómica conocida para la transducción de señales de vigilia y se acuñó el sistema de activación reticular ascendente (ARAS).
A continuación, se evaluó la importancia de este sistema de retransmisión recientemente identificado colocando lesiones en las porciones medial y lateral de la parte frontal del mesencéfalo. Los gatos con interrupciones mesencefálicas del ARAS entraron en un sueño profundo y mostraron las ondas cerebrales correspondientes. De manera alternativa, los gatos con interrupciones similares en las vías auditivas y somáticas ascendentes exhibieron un sueño y una vigilia normales, y pudieron despertarse con estímulos físicos. Debido a que las interrupciones bloquearían el camino de estos estímulos externos hacia la corteza, esto indicó que la transmisión ascendente debe viajar a través del recién descubierto ARAS.
Finalmente, Magoun registró potenciales dentro de la porción medial del tronco del encéfalo y descubrió que los estímulos auditivos activaban directamente porciones del sistema de activación reticular. Además, la estimulación con una sola descarga del nervio ciático también activó la formación reticular medial, el hipotálamo y el tálamo. La excitación del ARAS no dependió de una mayor propagación de la señal a través de los circuitos cerebelosos, ya que se obtuvieron los mismos resultados después de la descerebelación y la decorticación. Los investigadores propusieron que una columna de células que rodean la formación reticular del mesencéfalo recibía información de todos los tractos ascendentes del tronco encefálico y transmitía estas aferencias a la corteza y, por lo tanto, regulaba la vigilia.