Fiebre tifoidea
La fiebre tifoidea, también conocida como tifoidea, es una enfermedad causada por la bacteria Salmonella serotipo Typhi. Los síntomas varían de leves a graves y, por lo general, comienzan de seis a 30 días después de la exposición. A menudo hay un inicio gradual de fiebre alta durante varios días. Esto suele ir acompañado de debilidad, dolor abdominal, estreñimiento, dolores de cabeza y vómitos leves. Algunas personas desarrollan una erupción cutánea con manchas de color rosa. En casos severos, las personas pueden experimentar confusión. Sin tratamiento, los síntomas pueden durar semanas o meses. La diarrea puede ser grave, pero es poco común. Otras personas pueden portar la bacteria sin verse afectadas, pero aun así pueden propagar la enfermedad. La fiebre tifoidea es un tipo de fiebre entérica, junto con la fiebre paratifoidea. Se cree que S. enterica Typhi infecta y se replica solo dentro de los humanos.
La fiebre tifoidea es causada por la bacteria Salmonella enterica subsp. enterica serovar Typhi que crece en los intestinos, placas de Peyers, ganglios linfáticos mesentéricos, bazo, hígado, vesícula biliar, médula ósea y sangre. La fiebre tifoidea se transmite al comer o beber alimentos o agua contaminados con las heces de una persona infectada. Los factores de riesgo incluyen acceso limitado a agua potable limpia y saneamiento deficiente. Aquellos que aún no han estado expuestos al patógeno e ingieren agua potable o alimentos contaminados tienen mayor riesgo de desarrollar síntomas. Solo los humanos pueden infectarse; no hay reservorios animales conocidos.
El diagnóstico se realiza mediante cultivo e identificación de S. enterica Typhi a partir de muestras de pacientes o detectando una respuesta inmunitaria al patógeno a partir de muestras de sangre. Recientemente, los nuevos avances en la recopilación y el análisis de datos a gran escala han permitido a los investigadores desarrollar mejores diagnósticos, como la detección de cantidades cambiantes de pequeñas moléculas en la sangre que pueden indicar específicamente fiebre tifoidea. Las herramientas de diagnóstico en las regiones donde la fiebre tifoidea es más frecuente son bastante limitadas en su precisión y especificidad, y el tiempo requerido para un diagnóstico adecuado, la creciente propagación de la resistencia a los antibióticos y el costo de las pruebas también son dificultades para los sistemas de atención médica con recursos insuficientes.
Una vacuna contra la fiebre tifoidea puede prevenir entre el 40 % y el 90 % de los casos durante los primeros dos años. La vacuna puede tener algún efecto hasta por siete años. Para aquellos con alto riesgo o personas que viajan a áreas donde la enfermedad es común, se recomienda la vacunación. Otros esfuerzos para prevenir la enfermedad incluyen proporcionar agua potable limpia, buen saneamiento y lavado de manos. Hasta que se confirme que la infección ha desaparecido, la persona infectada no debe preparar alimentos para los demás. La fiebre tifoidea se trata con antibióticos como azitromicina, fluoroquinolonas o cefalosporinas de tercera generación. Se ha ido desarrollando resistencia a estos antibióticos, lo que ha dificultado el tratamiento.
En 2015, se informaron 12,5 millones de nuevos casos de fiebre tifoidea. La enfermedad es más común en la India. Los niños son los más comúnmente afectados. La fiebre tifoidea disminuyó en el mundo desarrollado en la década de 1940 como resultado de la mejora del saneamiento y el uso de antibióticos. Cada año se informan alrededor de 400 casos en los EE. UU. y se estima que 6000 personas tienen fiebre tifoidea. En 2015, provocó unas 149 000 muertes en todo el mundo, frente a las 181 000 de 1990. Sin tratamiento, el riesgo de muerte puede llegar al 20 %. Con tratamiento, está entre el 1% y el 4%.
El tifus es una enfermedad diferente. Debido a sus síntomas similares, no se reconocieron como enfermedades distintas hasta el siglo XIX. "Tifoidea" significa "parecido al tifus".
Signos y síntomas
Clásicamente, la progresión de la fiebre tifoidea no tratada tiene tres etapas distintas, cada una de las cuales dura aproximadamente una semana. En el transcurso de estas etapas, el paciente se vuelve exhausto y demacrado.
- En la primera semana, la temperatura corporal aumenta lentamente, y las fluctuaciones de la fiebre se observan con bradicardia relativa (Signo débil), malestar, dolor de cabeza y tos. Una nariz sangrienta (epistaxis) se ve en un cuarto de casos, y el dolor abdominal también es posible. Una disminución del número de glóbulos blancos circulantes (leucopenia) se produce con eosinopenia y linfocitis relativa; los cultivos sanguíneos son positivos para S. enterica Subsp. enterica serovar Typhi. La prueba Widal suele ser negativa.
- En la segunda semana, la persona suele estar demasiado cansada para levantarse, con fiebre alta en meseta alrededor de 40 °C (104 °F) y bradicardia (disociación esfigmotérmica o signo Faget), clásicamente con una onda de pulso dicrota. El delirio puede ocurrir, donde el paciente es a menudo calmado, pero a veces se agita. Este delirio ha dado tifoidea el apodo "fiebre nerviosa". Las manchas de rosa aparecen en el pecho inferior y el abdomen alrededor de un tercio de los pacientes. Rhonchi (sonidos respiratorios) se escuchan en la base de los pulmones. El abdomen es desatendido y doloroso en el cuadrante inferior derecho, donde se puede escuchar un sonido retumbante. La diarrea puede ocurrir en esta etapa, pero el estreñimiento también es común. El bazo y el hígado se agrandan (hepatosplenomegalia) y tierna, y las transaminasas hepáticas son elevadas. La prueba Widal es muy positiva, con anticuerpos antiO y antiH. Las culturas sanguíneas a veces siguen siendo positivas.
- En la tercera semana de fiebre tifoidea se pueden producir varias complicaciones:
- La fiebre sigue siendo muy alta y oscila muy poco más de 24 horas. La deshidratación se produce junto con la malnutrición, y el paciente es delirante. Un tercio de las personas afectadas desarrollan una erupción macular en el maletero.
- La hemorragia intestinal debido al sangrado en los parches de Peyer congestionados ocurre; esto puede ser muy grave, pero generalmente no es fatal.
- La perforación intestinal en el íleo distal es una complicación muy grave y a menudo fatal. Puede ocurrir sin síntomas alarmantes hasta que se establezca la peritonitis septicemia o difusa.
- Enfermedades respiratorias como neumonía y bronquitis aguda
- Encefalitis
- Síntomas neuropsiquiátricos (descritos como "delirio de tráfico" o "vigilancia de coma"), con la recogida en manteles o objetos imaginarios.
- Abscesos metastásicos, colecistitis, endocarditis y osteitis.
- El recuento de plaquetas bajos (trombocitopenia) a veces se ve.
Causas
Bacterias
La bacteria Gram-negativa que causa la fiebre tifoidea es Salmonella enterica subsp. enterica serovariedad Typhi. Según el esquema de subtipificación MLST, los dos tipos de secuencia principales de S. Typhi son ST1 y ST2, que están muy extendidos en todo el mundo. El análisis filogeográfico global mostró la dominancia de un haplotipo 58 (H58), que probablemente se originó en India a fines de la década de 1980 y ahora se está extendiendo por todo el mundo con resistencia a múltiples fármacos. En 2016 se informó un esquema de genotipado más detallado y ahora se usa ampliamente. Este esquema reclasificó la nomenclatura de H58 al genotipo 4.3.1.
Transmisión
A diferencia de otras cepas de Salmonella, no se conocen animales portadores de la fiebre tifoidea. Los humanos son los únicos portadores conocidos de la bacteria. S. entérica subsp. enterica serovar Typhi se transmite por vía fecal-oral de personas infectadas y de portadores asintomáticos de la bacteria. Un portador humano asintomático es alguien que aún excreta bacterias tifoideas en sus heces un año después de la etapa aguda de la infección.
Diagnóstico
El diagnóstico se realiza mediante cualquier cultivo de sangre, médula ósea o heces y con la prueba de Widal (demostración de anticuerpos contra los antígenos O-somático y H-flagelar de Salmonella). En países epidémicos y menos ricos, después de excluir malaria, disentería o neumonía, generalmente se realiza un tiempo de prueba terapéutica con cloranfenicol en espera de los resultados de la prueba de Widal y hemocultivos y coprocultivos.
Prueba de Widal
La prueba de Widal se utiliza para identificar anticuerpos específicos en el suero de personas con fiebre tifoidea mediante interacciones antígeno-anticuerpo.
En esta prueba, el suero se mezcla con una suspensión bacteriana muerta de salmonella con antígenos específicos. Si el suero del paciente contiene anticuerpos contra esos antígenos, se adhieren a ellos y forman grumos. Si no se produce aglomeración, la prueba es negativa. La prueba de Widal requiere mucho tiempo y es propensa a falsos positivos significativos. También puede ser falso negativo en personas recientemente infectadas. Pero a diferencia de la prueba de Typhidot, la prueba de Widal cuantifica la muestra con títulos.
Pruebas de diagnóstico rápido
Las pruebas de diagnóstico rápido como Tubex, Typhidot y Test-It han mostrado una precisión diagnóstica moderada.
Tifidota
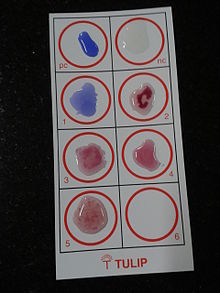
Typhidot se basa en la presencia de anticuerpos IgM e IgG específicos contra un antígeno OMP específico de 50 kd. Este ensayo se lleva a cabo sobre una membrana de nitrato de celulosa donde se produce un S. typhi la proteína de la membrana externa se adjunta como líneas de prueba fijas. Identifica por separado los anticuerpos IgM e IgG. IgM muestra infección reciente; IgG significa infección remota.
La almohadilla de muestra de este kit contiene IgG antihumana de oro coloidal o IgM antihumana de oro. Si la muestra contiene anticuerpos IgG e IgM contra esos antígenos, estos reaccionarán y se volverán rojos. La prueba de la fiebre tifoidea se vuelve positiva dentro de los 2 a 3 días posteriores a la infección.
Dos bandas de colores indican una prueba positiva. Una sola banda de control indica una prueba negativa. Una sola primera línea fija o ninguna banda indica una prueba no válida. La mayor limitación de Typhidot es que no es cuantitativa, solo positiva o negativa.
Prueba Tubex
La prueba Tubex contiene dos tipos de partículas: partículas magnéticas marrones recubiertas con antígeno y partículas indicadoras azules recubiertas con anticuerpo O9. Durante la prueba, si los anticuerpos están presentes en el suero, se unirán a las partículas magnéticas marrones y se asentarán en la base, mientras que las partículas indicadoras azules permanecerán en la solución, produciendo un color azul, lo que significa que la prueba es positiva.
Si el suero no contiene un anticuerpo, las partículas azules se adhieren a las partículas marrones y se asientan en el fondo, produciendo una solución incolora, lo que significa que la prueba es negativa.
Prevención
El saneamiento y la higiene son importantes para prevenir la fiebre tifoidea. Solo se puede propagar en entornos donde las heces humanas pueden entrar en contacto con alimentos o agua potable. La preparación cuidadosa de los alimentos y el lavado de manos son cruciales para prevenir la fiebre tifoidea. La industrialización contribuyó en gran medida a la eliminación de la fiebre tifoidea, ya que eliminó los peligros para la salud pública asociados con tener estiércol de caballo en la vía pública, lo que generó una gran cantidad de moscas, que son vectores de muchos patógenos, incluida la Salmonella spp. Según las estadísticas de los Centros para el Control y la Prevención de Enfermedades de EE. UU., la cloración del agua potable ha llevado a una disminución drástica en la transmisión de la fiebre tifoidea.
Vacunación
Dos vacunas contra la fiebre tifoidea están autorizadas para su uso en la prevención de la fiebre tifoidea: la vacuna Ty21a oral viva (vendida como Vivotif por Crucell Switzerland AG) y la vacuna inyectable de polisacáridos contra la fiebre tifoidea (vendida como Typhim Vi por Sanofi Pasteur y Typherix por GlaxoSmithKline). Ambos son eficaces y recomendados para viajeros a áreas donde la fiebre tifoidea es endémica. Se recomiendan refuerzos cada cinco años para la vacuna oral y cada dos años para la forma inyectable. Todavía se usa una vacuna de células enteras muertas más antigua en países donde las preparaciones más nuevas no están disponibles, pero ya no se recomienda el uso de esta vacuna porque tiene más efectos secundarios (principalmente dolor e inflamación en el sitio de la inyección).
Para ayudar a disminuir las tasas de fiebre tifoidea en los países en desarrollo, la Organización Mundial de la Salud (OMS) respaldó el uso de un programa de vacunación a partir de 1999. La vacunación ha demostrado ser eficaz para controlar los brotes en áreas de alta incidencia y también es muy costosa. eficaz: los precios normalmente son inferiores a 1 dólar EE.UU. por dosis. Debido a que el precio es bajo, las comunidades afectadas por la pobreza están más dispuestas a aprovechar las vacunas. Aunque los programas de vacunación contra la fiebre tifoidea han demostrado su eficacia, por sí solos no pueden eliminar la fiebre tifoidea. Combinar las vacunas con los esfuerzos de salud pública es la única forma comprobada de controlar esta enfermedad.
Desde la década de 1990, la OMS ha recomendado dos vacunas contra la fiebre tifoidea. La vacuna ViPS se administra por inyección y la Ty21a por cápsulas. Solo se recomienda vacunar a las personas mayores de dos años con la vacuna ViPS, y requiere una revacunación después de 2-3 años, con una eficacia del 55% al 72%. La vacuna Ty21a se recomienda para personas mayores de cinco años, con una duración de 5 a 7 años con una eficacia del 51 % al 67 %. Las dos vacunas han demostrado ser seguras y eficaces para el control de enfermedades epidémicas en múltiples regiones.
También está disponible una versión de la vacuna combinada con una vacuna contra la hepatitis A.
Los resultados de un ensayo de fase 3 de la vacuna conjugada contra la fiebre tifoidea (TCV) en diciembre de 2019 informaron un 81 % menos de casos entre los niños.
Tratamiento
Terapia de rehidratación oral
El redescubrimiento de la terapia de rehidratación oral en la década de 1960 proporcionó una forma sencilla de prevenir muchas de las muertes por enfermedades diarreicas en general.
Antibióticos
Cuando la resistencia es poco común, el tratamiento de elección es una fluoroquinolona como la ciprofloxacina. De lo contrario, una cefalosporina de tercera generación como ceftriaxona o cefotaxima es la primera opción. La cefixima es una alternativa oral adecuada.
Si se trata adecuadamente, la fiebre tifoidea no es fatal en la mayoría de los casos. Los antibióticos como la ampicilina, el cloranfenicol, la trimetoprima-sulfametoxazol, la amoxicilina y la ciprofloxacina se han usado comúnmente para tratarla. El tratamiento con antibióticos reduce la tasa de letalidad a alrededor del 1%.
Sin tratamiento, algunos pacientes desarrollan fiebre sostenida, bradicardia, hepatoesplenomegalia, síntomas abdominales y, ocasionalmente, neumonía. En los pacientes de piel blanca aparecen en la piel del tronco hasta un 20% de los casos manchas rosadas que desaparecen a la presión. En la tercera semana, los casos no tratados pueden desarrollar complicaciones gastrointestinales y cerebrales, que pueden resultar fatales en 10 a 20% de los casos. Las tasas de letalidad más altas se reportan en niños menores de 4 años. Alrededor del 2% al 5% de los que contraen fiebre tifoidea se vuelven portadores crónicos, ya que las bacterias persisten en el tracto biliar después de que los síntomas han desaparecido.
Cirugía
La cirugía suele estar indicada si se produce una perforación intestinal. Un estudio encontró una tasa de mortalidad a los 30 días del 9 % (8/88) e infecciones del sitio quirúrgico del 67 % (59/88), y la carga de la enfermedad la soportan predominantemente los países de bajos recursos.
Para el tratamiento quirúrgico, la mayoría de los cirujanos prefieren el cierre simple de la perforación con drenaje del peritoneo. La resección del intestino delgado está indicada para pacientes con múltiples perforaciones. Si el tratamiento antibiótico no logra erradicar el estado de portador hepatobiliar, se debe resecar la vesícula biliar. La colecistectomía a veces tiene éxito, especialmente en pacientes con cálculos biliares, pero no siempre tiene éxito en la erradicación del estado de portador debido a la persistencia de la infección hepática.
Resistencia
Como ahora es común la resistencia a la ampicilina, el cloranfenicol, la trimetoprima-sulfametoxazol y la estreptomicina, estos agentes ya no se usan como tratamiento de primera línea para la fiebre tifoidea. La fiebre tifoidea resistente a estos agentes se conoce como fiebre tifoidea resistente a múltiples fármacos.
La resistencia a la ciprofloxacina es un problema creciente, especialmente en el subcontinente indio y el sudeste asiático. Muchos centros están pasando de la ciprofloxacina a la ceftriaxona como primera línea para el tratamiento de la posible fiebre tifoidea originada en América del Sur, India, Pakistán, Bangladesh, Tailandia o Vietnam. Además, se ha sugerido que la azitromicina es mejor para tratar la fiebre tifoidea resistente que las fluoroquinolonas y la ceftriaxona. La azitromicina se puede tomar por vía oral y es menos costosa que la ceftriaxona, que se administra por inyección.
Existe un problema separado con las pruebas de laboratorio para la susceptibilidad reducida a la ciprofloxacina; Las recomendaciones actuales son que los aislamientos deben analizarse simultáneamente frente a ciprofloxacina (CIP) y frente a ácido nalidíxico (NAL), que los aislamientos sensibles tanto a CIP como a NAL deben informarse como "sensibles a ciprofloxacino", y que los aislamientos sensibles a La CIP, pero no la NAL, debe informarse como "sensibilidad reducida a la ciprofloxacina". Pero un análisis de 271 aislamientos encontró que alrededor del 18 % de los aislamientos con una susceptibilidad reducida a las fluoroquinolonas, la clase a la que pertenece CIP (MIC 0.125–1.0 mg/L), no serían detectados por este método.
Epidemiología
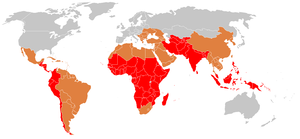
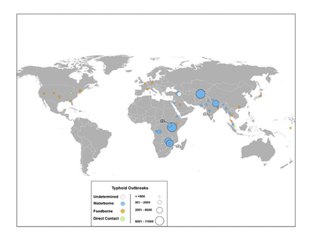
En 2000, la fiebre tifoidea causó aproximadamente 21,7 millones de enfermedades y 217.000 muertes. Ocurre con mayor frecuencia en niños y adultos jóvenes entre 5 y 19 años. En 2013, provocó unas 161 000 muertes, frente a las 181 000 de 1990. Los bebés, niños y adolescentes del centro-sur y sudeste de Asia tienen las tasas más altas de fiebre tifoidea. Los brotes también se informan a menudo en el África subsahariana y el sudeste asiático. En el año 2000, más del 90% de la morbilidad y mortalidad por fiebre tifoidea ocurrió en Asia. En los EE. UU., ocurren alrededor de 400 casos cada año, el 75 % de los cuales se adquieren durante viajes internacionales.
Antes de la era de los antibióticos, la tasa de letalidad de la fiebre tifoidea era del 10 % al 20 %. Hoy en día, con un tratamiento oportuno, es menos del 1 %, pero entre el 3 % y el 5 % de las personas infectadas desarrollan una infección crónica en la vesícula biliar. Desde S. entérica subsp. enterica serovar Typhi está restringida a humanos, estos portadores crónicos se convierten en el reservorio crucial, que puede persistir durante décadas para una mayor propagación de la enfermedad, lo que complica aún más su identificación y tratamiento. Últimamente, el estudio de S. entérica subsp. enterica serovar Typhi asociado con un gran brote y un portador a nivel del genoma proporciona una nueva visión de la patogenia del patógeno.
En los países industrializados, las mejoras en el saneamiento del agua y la manipulación de alimentos han reducido el número de casos de fiebre tifoidea. Los países en desarrollo, como los de partes de Asia y África, tienen las tasas más altas. Estas áreas carecen de acceso a agua limpia, sistemas de saneamiento adecuados e instalaciones de atención médica adecuadas. En estas áreas, dicho acceso a las necesidades básicas de salud pública no se espera en un futuro cercano.
En 2004–2005, un brote en la República Democrática del Congo resultó en más de 42 000 casos y 214 muertes. Desde noviembre de 2016, Pakistán ha tenido un brote de fiebre tifoidea extremadamente resistente a los medicamentos (XDR).
En Europa, un informe basado en datos de 2017 recuperados del Sistema Europeo de Vigilancia (TESSy) sobre la distribución de casos confirmados de fiebre tifoidea y paratifoidea encontró que 22 países de la UE/EEE informaron un total de 1098 casos, el 90,9 % de los cuales estaban relacionados con los viajes, adquiridos principalmente durante los viajes al sur de Asia.
Historia
Primeras descripciones
La peste de Atenas, durante la Guerra del Peloponeso, probablemente fue un brote de fiebre tifoidea. Durante la guerra, los atenienses se retiraron a una ciudad amurallada para escapar del ataque de los espartanos. Esta afluencia masiva de humanos en un espacio concentrado abrumó el suministro de agua y la infraestructura de desechos, lo que probablemente condujo a condiciones insalubres a medida que se hizo más difícil obtener agua dulce y los desechos se volvieron más difíciles de recolectar y eliminar más allá de las murallas de la ciudad. En 2006, el examen de los restos de un lugar de entierro masivo de Atenas de la época de la peste (~430 a. C.) reveló que se detectaron fragmentos de ADN similares al ADN actual de S. Typhi, mientras que Yersinia pestis (peste), Rickettsia prowazekii (tifus), Mycobacterium tuberculosis, virus de la viruela vacuna y Bartonella henselae no se detectaron en ninguno de los restos analizados.
Es posible que el emperador romano Augusto César tuviera un absceso hepático o fiebre tifoidea y sobreviviera usando baños de hielo y compresas frías como medio de tratamiento para la fiebre. Hay una estatua del médico griego Antonius Musa, que trató su fiebre.
Definición y evidencia de transmisión
A los médicos franceses Pierre-Fidele Bretonneau y Pierre-Charles-Alexandre Louis se les atribuye la descripción de la fiebre tifoidea como una enfermedad específica, única del tifus. Ambos médicos realizaron autopsias a personas que murieron en París debido a la fiebre e indicaron que muchas tenían lesiones en las placas de Peyer que se correlacionaban con distintos síntomas antes de la muerte. Los médicos británicos se mostraron escépticos sobre la diferenciación entre la fiebre tifoidea y el tifus porque ambos eran endémicos en Gran Bretaña en ese momento. Sin embargo, en Francia sólo estaba presente la fiebre tifoidea circulando en la población. Pierre-Charlles-Alexandre Louis también realizó estudios de casos y análisis estadísticos para demostrar que la fiebre tifoidea era contagiosa y que las personas que ya tenían la enfermedad parecían estar protegidas. Posteriormente, varios médicos estadounidenses confirmaron estos hallazgos, y luego Sir William Jenner convenció a los escépticos restantes de que la fiebre tifoidea es una enfermedad específica reconocible por lesiones en las placas de Peyer al examinar sesenta y seis autopsias de pacientes con fiebre y concluir que los síntomas de dolores de cabeza, la diarrea, las manchas de erupción y el dolor abdominal solo estaban presentes en pacientes que luego tenían lesiones intestinales después de la muerte; lo que solidificó la asociación de la enfermedad con el tracto intestinal y dio la primera pista sobre la ruta de transmisión.
En 1847, William Budd se enteró de una epidemia de fiebre tifoidea en Clifton e identificó que los 13 de los 34 residentes que habían contraído la enfermedad sacaban el agua potable del mismo pozo. En particular, esta observación fue dos años antes de que John Snow descubriera la ruta del agua contaminada como la causa de un brote de cólera. Budd luego se convirtió en oficial de salud de Bristol y aseguró un suministro de agua limpia, y documentó más evidencia de fiebre tifoidea como una enfermedad transmitida por el agua a lo largo de su carrera.
Causa
El científico polaco Tadeusz Browicz describió un bacilo pequeño en los órganos y las heces de las víctimas de la fiebre tifoidea en 1874. Browicz pudo aislar y cultivar los bacilos, pero no fue tan lejos como para insinuar o probar que causaban la enfermedad.
En abril de 1880, tres meses antes de la publicación de Eberth, Edwin Klebs describió bacilos cortos y filamentosos en las placas de Peyer en víctimas de fiebre tifoidea. El papel de la bacteria en la enfermedad se especuló pero no se confirmó.
En 1880, Karl Joseph Eberth describió un bacilo que sospechaba que era la causa de la fiebre tifoidea. A Eberth se le da crédito por descubrir la bacteria definitivamente al aislar con éxito la misma bacteria de 18 de 40 víctimas de la fiebre tifoidea y no pudo descubrir la bacteria presente en ningún "control" víctimas de otras enfermedades. En 1884, el patólogo Georg Theodor August Gaffky (1850–1918) confirmó los hallazgos de Eberth. Gaffky aisló la misma bacteria que Eberth del bazo de una víctima de fiebre tifoidea y pudo cultivar la bacteria en medios sólidos. El organismo recibió nombres como bacilo de Eberth, Eberthella Typhi y bacilo de Gaffky-Eberth. Hoy en día, el bacilo que causa la fiebre tifoidea recibe el nombre científico de Salmonella enterica serovar Typhi.
Cloración del agua
La mayoría de los países desarrollados tuvieron tasas decrecientes de fiebre tifoidea durante la primera mitad del siglo XX debido a las vacunas y los avances en el saneamiento y la higiene públicos. En 1893 se intentó clorar el suministro de agua en Hamburgo, Alemania, y en 1897 Maidstone, Inglaterra, fue la primera ciudad en clorar todo su suministro de agua. En 1905, tras un brote de fiebre tifoidea, la ciudad de Lincoln, Inglaterra, instituyó la cloración permanente del agua. La primera desinfección permanente del agua potable en los EE. UU. se realizó en 1908 en el suministro de agua de la ciudad de Jersey, Nueva Jersey. El crédito por la decisión de construir el sistema de cloración se le ha dado a John L. Leal. La instalación de cloración fue diseñada por George W. Fuller.
Los brotes en los grupos militares itinerantes llevaron a la creación de la bolsa de Lyster en 1915; una bolsa con grifo que se puede colgar de un árbol o poste, se llena de agua y viene con una pastilla de cloración para echar en el agua. La bolsa de Lyster fue fundamental para la supervivencia de los soldados estadounidenses en la Guerra de Vietnam.
Transmisión directa y portadores
Hubo varios casos de repartidores de leche que propagaron la fiebre tifoidea en las comunidades a las que servían. Aunque la fiebre tifoidea no se transmite a través de la leche en sí, hubo varios ejemplos de distribuidores de leche en muchos lugares que diluyeron su leche con agua contaminada o limpiaron las botellas de vidrio en las que se colocó la leche con agua contaminada. Boston tuvo dos casos de este tipo a principios del siglo XX. En 1899 hubo 24 casos de fiebre tifoidea atribuidos a un solo lechero, cuya esposa había muerto de fiebre tifoidea una semana antes del brote. En 1908, J. J. Fallon, que también era lechero, murió de fiebre tifoidea. Luego de su muerte y la confirmación del diagnóstico de fiebre tifoidea, la ciudad llevó a cabo una investigación de los síntomas y casos de fiebre tifoidea a lo largo de su ruta y encontró evidencia de un brote significativo. Un mes después de que se informara por primera vez sobre el brote, el Boston Globe publicó una breve declaración declarando que el brote había terminado, afirmando que en Jamaica Plain hay un ligero aumento, con un total de 272 casos. En toda la ciudad hay un total de 348 casos." Se informó al menos una muerte durante este brote: la Sra. Sophia S. Engstrom, de 46 años. La fiebre tifoidea continuó devastando el vecindario de Jamaica Plain en particular durante 1908, y se informó la muerte de varias personas más debido a la fiebre tifoidea, aunque estos casos fueron no está explícitamente relacionado con el brote. El vecindario de Jamaica Plain en ese momento era el hogar de muchos inmigrantes pobres y de clase trabajadora, en su mayoría de Irlanda.
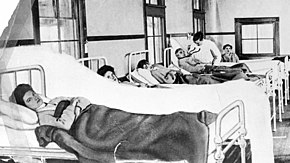
La portadora más notoria de la fiebre tifoidea, pero de ninguna manera la más destructiva, fue Mary Mallon, conocida como Typhoid Mary. Aunque en ese momento se conocían otros casos de propagación de la fiebre tifoidea de persona a persona, el concepto de un portador asintomático, que podía transmitir la enfermedad, solo se había planteado como hipótesis y aún no se había identificado ni probado. Mary Mallon se convirtió en el primer ejemplo conocido de una portadora asintomática de una enfermedad infecciosa, lo que convirtió a la fiebre tifoidea en la primera enfermedad conocida transmisible a través de huéspedes asintomáticos. Los casos y muertes causados por Mallon fueron principalmente familias de clase alta en la ciudad de Nueva York. En el momento del mandato de Mallon como cocinero personal para familias de clase alta, la ciudad de Nueva York reportaba entre 3000 y 4500 casos de fiebre tifoidea al año. En el verano de 1906, dos hijas de una familia adinerada y las criadas que trabajaban en su casa enfermaron de fiebre tifoidea. Después de investigar las fuentes de agua de su hogar y descartar la contaminación del agua, la familia contrató al ingeniero civil George Soper para realizar una investigación de la posible fuente de fiebre tifoidea en el hogar. Soper se describió a sí mismo como un "luchador de epidemias". Su investigación descartó muchas fuentes de alimentos y lo llevó a preguntarse si el cocinero que la familia contrató justo antes del brote en su hogar, Mallon, era la fuente. Como ella ya se había ido y había comenzado a trabajar en otro lugar, procedió a localizarla para obtener una muestra de heces. Cuando finalmente pudo conocer a Mallon en persona, la describió diciendo: "Mary tenía una buena figura y podría haber sido llamada atlética si no hubiera sido un poco demasiado pesada". En los relatos de la búsqueda de Mallon por parte de Soper, su único remordimiento parece ser que no se le dio suficiente crédito por su incesante búsqueda y publicación de su información de identificación personal, afirmando que los medios de comunicación "me roban". de cualquier crédito pertenece al descubrimiento del primer portador de fiebre tifoidea que se encuentra en América." En última instancia, se sospechó que 51 casos y 3 muertes fueron causados por Mallon.
En 1924, la ciudad de Portland, Oregón, experimentó un brote de fiebre tifoidea, que consta de 26 casos y 5 muertes, todas muertes por hemorragia intestinal. Se llegó a la conclusión de que todos los casos se debían a un solo trabajador de una granja lechera, que excretaba grandes cantidades del patógeno de la fiebre tifoidea en la orina. Identificación errónea de la enfermedad, debido a resultados inexactos de la prueba de Widal, identificación tardía del portador y tratamiento adecuado. Finalmente, se tomaron cuatro muestras de diferentes secreciones de todos los trabajadores de la lechería para identificar con éxito al portador. Tras el descubrimiento, el trabajador de la lechería fue puesto en cuarentena a la fuerza durante siete semanas, y se tomaron muestras regulares, la mayoría de las veces las muestras de heces no arrojaron fiebre tifoidea y, a menudo, la orina produjo el patógeno. Se informó que el portador tenía 72 años y parecía estar en excelente estado de salud sin síntomas. El tratamiento farmacológico disminuyó la cantidad de bacterias secretadas, sin embargo, la infección nunca se eliminó por completo de la orina y el portador fue dado de alta "con órdenes de nunca más involucrarse en el manejo de alimentos para consumo humano". En el momento del lanzamiento, los autores señalaron que "durante más de cincuenta años se ha ganado la vida principalmente ordeñando vacas y sabe poco de otras formas de trabajo, debe esperarse que sea necesaria la vigilancia más cercana para asegurarse que no vuelva a dedicarse a esta ocupación."
En general, a principios del siglo XX, la profesión médica comenzó a identificar portadores de la enfermedad y evidencia de transmisión independiente de la contaminación del agua. En una publicación de la Asociación Médica Estadounidense de 1933, los médicos' el tratamiento de los portadores asintomáticos se resume mejor en la primera línea 'Los portadores de bacilos tifoideos son una amenaza'. Dentro de la misma publicación, se da la primera estimación oficial de portadores de fiebre tifoidea: 2 a 5% de todos los pacientes de fiebre tifoidea, y se distingue entre portadores temporales y portadores crónicos. Los autores estiman además que hay de cuatro a cinco mujeres portadoras crónicas por cada hombre portador, aunque no ofrecieron datos para explicar esta afirmación de una diferencia de género en la tasa de portadores de fiebre tifoidea. En cuanto al tratamiento, los autores sugieren: "Cuando se reconozcan, los transportistas deben ser instruidos sobre la eliminación de excrementos, así como sobre la importancia del aseo personal. Se les debe prohibir manipular alimentos o bebidas destinados a otros, y sus movimientos y paraderos deben ser informados a los funcionarios de salud pública.
Hoy en día, existen portadores de fiebre tifoidea en todo el mundo, pero es probable que la incidencia más alta de infección asintomática ocurra en los países del sur y sureste de Asia y del Subsahara. El departamento de salud pública del condado de Los Ángeles rastrea a los portadores de fiebre tifoidea e informa anualmente la cantidad de portadores identificados dentro del condado; entre 2006 y 2016 se identificaron 0-4 nuevos casos de portadores de fiebre tifoidea por año. Los casos de fiebre tifoidea deben notificarse en el plazo de un día laborable a partir de la identificación. A partir de 2018, los portadores de fiebre tifoidea crónica deben firmar un "Acuerdo de transporte" y están obligados a realizar pruebas de eliminación de la fiebre tifoidea dos veces al año, idealmente cada 6 meses. Los transportistas pueden ser liberados de sus acuerdos al cumplir con "liberar" requisitos, basado en la realización de un plan de tratamiento personalizado diseñado con profesionales médicos. Requisitos de liberación de portadores de heces o vesícula biliar: 6 muestras negativas consecutivas de heces y orina enviadas a intervalos de 1 mes o más, comenzando al menos 7 días después de completar la terapia. Requisitos de liberación de portadores urinarios o renales: 6 muestras de orina negativas consecutivas enviadas a intervalos de 1 mes o más comenzando al menos 7 días después de la finalización de la terapia. A partir de 2016, la proporción de portadores hombre: mujer en el condado de Los Ángeles fue de 3: 1.
Debido a la naturaleza de los casos asintomáticos, quedan muchas preguntas sobre cómo las personas pueden tolerar la infección durante períodos prolongados, cómo identificar dichos casos y las opciones eficaces de tratamiento. Actualmente, los investigadores están trabajando para comprender la infección asintomática con especies de Salmonella mediante el estudio de infecciones en animales de laboratorio, lo que en última instancia conducirá a mejores opciones de prevención y tratamiento para los portadores de fiebre tifoidea. En 2002, el Dr. John Gunn describió la capacidad de Salmonella sp. para formar biopelículas en cálculos biliares en ratones, proporcionando un modelo para estudiar el transporte en la vesícula biliar. La Dra. Denise Monack y el Dr. Stanley Falkow describieron un modelo de ratón de infección intestinal y sistémica asintomática en 2004, y el Dr. Monack continuó demostrando que una subpoblación de superpropagadores es responsable de la mayoría de la transmisión a nuevos huéspedes, siguiendo la 80/20 regla de transmisión de enfermedades, y que la microbiota intestinal probablemente juega un papel en la transmisión. El modelo de ratón del Dr. Monack permite el transporte a largo plazo de salmonella en los ganglios linfáticos mesentéricos, el bazo y el hígado.
Desarrollo de vacunas
El bacteriólogo británico Almroth Edward Wright desarrolló por primera vez una vacuna eficaz contra la fiebre tifoidea en la Escuela de Medicina del Ejército en Netley, Hampshire. Fue introducido en 1896 y utilizado con éxito por los británicos durante la Segunda Guerra de los Bóers en Sudáfrica. En ese momento, la fiebre tifoidea a menudo mataba a más soldados en la guerra que los que se perdían debido al combate enemigo. Wright desarrolló aún más su vacuna en un departamento de investigación recién abierto en la Facultad de Medicina del Hospital St Mary's en Londres desde 1902, donde estableció un método para medir sustancias protectoras (opsonina) en la sangre humana. La versión de Wright de la vacuna contra la fiebre tifoidea se produjo cultivando la bacteria a temperatura corporal en caldo, luego calentando la bacteria a 60 °C para 'inactivarla con calor'. el patógeno, matándolo, mientras mantiene intactos los antígenos de superficie. Luego, la bacteria muerta por calor se inyectó en un paciente. Para mostrar evidencia de la eficacia de la vacuna, Wright luego recolectó muestras de suero de pacientes varias semanas después de la vacunación y probó la capacidad de su suero para aglutinar bacterias tifoideas vivas. Un "positivo" El resultado estuvo representado por la acumulación de bacterias, lo que indica que el cuerpo estaba produciendo antisuero (ahora llamado anticuerpos) contra el patógeno.
Citando el ejemplo de la Segunda Guerra de los Bóers, durante la cual muchos soldados murieron a causa de enfermedades fácilmente prevenibles, Wright convenció al ejército británico de que se debían producir 10 millones de dosis de vacunas para las tropas enviadas al frente occidental, ahorrando así hasta la mitad un millón de vidas durante la Primera Guerra Mundial. El ejército británico fue el único combatiente al estallar la guerra que tenía sus tropas completamente inmunizadas contra la bacteria. Por primera vez, sus bajas debidas al combate superaron a las de las enfermedades.
En 1909, Frederick F. Russell, un médico del ejército de EE. UU., adoptó la vacuna contra la fiebre tifoidea de Wright para su uso en el ejército y, dos años después, su programa de vacunación se convirtió en el primero en el que se inmunizó a todo un ejército. Eliminó la fiebre tifoidea como una causa importante de morbilidad y mortalidad en el ejército de los EE. UU. La vacunación contra la fiebre tifoidea para los miembros del ejército estadounidense se hizo obligatoria en 1911. Antes de la vacuna, la tasa de fiebre tifoidea en el ejército era de 14 000 o más por cada 100 000 soldados. Para la Primera Guerra Mundial, la tasa de fiebre tifoidea en los soldados estadounidenses era de 37 por 100.000.
Durante la Segunda Guerra Mundial, el ejército de los Estados Unidos autorizó el uso de una vacuna trivalente que contenía patógenos de la fiebre tifoidea, Paratyphi A y Paratyphi B inactivados por calor.
En 1934, el descubrimiento del antígeno capsular Vi por parte de Arthur Felix y la señorita S. R. Margaret Pitt permitió el desarrollo de la vacuna más segura del antígeno Vi, que se usa ampliamente en la actualidad. Arthur Felix y Margaret Pitt también aislaron la cepa Ty2, que se convirtió en la cepa original de Ty21a, la cepa que se usa hoy en día como vacuna viva atenuada para la fiebre tifoidea.
Antibióticos y resistencia
El Dr. David Gotlieb aisló el cloranfenicol de Streptomyces durante la década de 1940. En 1948, los médicos del ejército estadounidense probaron su eficacia en el tratamiento de pacientes con fiebre tifoidea en Kuala Lumpur, Malasia. Las personas que recibieron un curso completo de tratamiento eliminaron la infección, mientras que los pacientes que recibieron una dosis más baja tuvieron una recaída. Los portadores asintomáticos continuaron eliminando bacilos a pesar del tratamiento con cloranfenicol; solo los pacientes enfermos mejoraron con cloranfenicol. La resistencia al cloranfenicol se volvió frecuente en el sudeste asiático en la década de 1950 y, en la actualidad, el cloranfenicol solo se usa como último recurso debido a la alta prevalencia de resistencia.
Terminología
La enfermedad ha recibido varios nombres, a menudo asociados con síntomas, como fiebre gástrica, fiebre entérica, tifus abdominal, fiebre remitente infantil, fiebre lenta, fiebre nerviosa, fiebre pitógena, fiebre de drenaje y fiebre baja.
Personas notables
- Sobrevivió el Emperador Augusto de Roma (suspeciado basado en registros históricos pero no confirmado).
- Albert, Prince Consort, esposo de la Reina Victoria del Reino Unido, murió en 24 días después del primer registro de "sentir terriblemente enfermo". Murió el 14 de diciembre de 1861 después de sufrir pérdida de apetito, insomnio, fiebre, escalofríos, sudoración profusa, vómitos, manchas eruptivas, delirios, incapacidad para reconocer a los miembros de la familia, empeorando la erupción en el abdomen, un cambio en el color de la lengua, y finalmente un estado de fatiga extrema. El médico asistente William Jenner, experto en fiebre tifoidea en ese momento, lo diagnosticó.
- Edward VII del Reino Unido, hijo de la reina Victoria, mientras todavía Príncipe de Gales, tenía un caso casi fatal de fiebre tifoidea.
- El zar Nicolás II de Rusia, sobrevivió, la enfermedad fue alrededor de 1900-1901.
- William Henry Harrison, el noveno presidente de los Estados Unidos de América, murió 32 días en su mandato, en 1841. Este es el plazo más corto que presta un Presidente de los Estados Unidos.
- Wilbur Wright, co-inventor del avión con su hermano Orville murió de tifoidea 32 años antes de Orville.
- Stephen A. Douglas, oponente político de Abraham Lincoln en 1858 y 1860, murió de tifoidea el 3 de junio de 1861.
- Ignacio Zaragoza, general y político mexicano, murió a los 33 años de fiebre tifoidea el 8 de septiembre de 1862.
- William Wallace Lincoln, hijo del presidente estadounidense Abraham y Mary Todd Lincoln, murió de tifoidea en 1862.
- Martha Bulloch Roosevelt, madre del presidente Theodore Roosevelt y abuela paterna de Eleanor Roosevelt, murió de fiebre tifoidea en 1884.
- Mary Mallon, "Typhoid Mary" - ver la sección de historia, "carriers" para más detalles
- Leland Stanford Jr., hijo de magnate estadounidense y político A. Leland Stanford y eponym de Leland Stanford Junior University, murió de fiebre tifoidea en 1884 a los 15 años.
- Tres de los cinco niños de Louis Pasteur murieron de fiebre tifoidea.
- Gerard Manley Hopkins, poeta inglés, murió de fiebre tifoidea en 1889.
- Lizzie van Zyl, reclusa sudafricana del campo de concentración de Bloemfontein durante la Segunda Guerra de Boer, murió de fiebre tifoidea en 1901.
- El Dr. HJH 'Tup' Scott, capitán del equipo de cricket australiano de 1886 que recorrió Inglaterra, murió de tifoidea en 1910.
- Arnold Bennett, novelista inglés, murió en 1932 de tifoidea, dos meses después de beber un vaso de agua en un hotel de París para probar que era seguro.
- Hakaru Hashimoto, Científico médico japonés, murió de fiebre tifoidea en 1934.
Brotes
- Plague of Athens (suspected)
- El brote "Burning Fever" entre indígenas americanos. Entre 1607 y 1624, el 85% de la población del río James murió de una epidemia de tifoidea. La Organización Mundial de la Salud estima que el número de muertos fue de más de 6.000 durante este tiempo.
- Maidstone, brote de Kent en 1897-1898: 1.847 pacientes fueron registrados para tener fiebre tifoidea. Este brote es notable porque fue la primera vez que se desplegó una vacuna tifoidea durante un brote civil. La vacuna de Almoth Edward Wright se ofreció a 200 proveedores de atención médica, y de los 84 individuos que recibieron la vacuna no desarrollaron tifoidea mientras que 4 que no habían sido vacunados se enfermaron.
- Ejército estadounidense en la guerra español-estadounidense: los registros gubernamentales estiman que más de 21.000 tropas tenían tifoidea, lo que dio lugar a 2.200 muertes.
- En 1902, los invitados a los banquetes de alcalde en Southampton y Winchester, Inglaterra, se enfermaron y cuatro murieron, incluyendo el decano de Winchester, después de consumir ostras. La infección se debió a ostras provenientes de Emsworth, donde las camas de ostra habían sido contaminadas con aguas residuales crudas.
- Jamaica Plain, Boston en 1908 - vinculada a la entrega de leche. Ver sección de historia, "carriers" para más detalles.
- Brote en neoyorquinos de clase superior que emplearon a Mary Mallon - 51 casos y 3 muertes de 1907 a 1915.
- Aberdeen, Escocia, en verano de 1964 - rastreado de nuevo a carne contaminada procedente de Argentina vendida en mercados. Más de 500 pacientes fueron en cuarentena en el hospital durante un mínimo de cuatro semanas, y el brote fue contenido sin ninguna muerte.
- Dushanbe, Tayikistán, en 1996–1997: 10.677 casos denunciados, 108 muertes
- Kinshasa, Democratic República del Congo, en 2004: 43.000 casos y más de 200 muertes. Un estudio prospectivo de especímenes recogidos en la misma región entre 2007 y 2011 reveló que un tercio de las muestras obtenidas de muestras de pacientes eran resistentes a múltiples antibióticos.
- Kampala, Uganda en 2015: 10.230 casos denunciados
Contenido relacionado
Bradicardia
Resistencia antimicrobiana
Encefalomielitis diseminada aguda