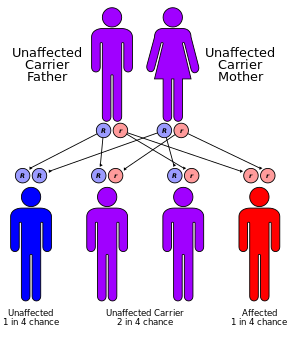
Fibrosis quística
fibrosis quística (FQ) es un trastorno genético raro que afecta principalmente a los pulmones, pero también al páncreas, el hígado, los riñones y el intestino. Los problemas a largo plazo incluyen dificultad para respirar y tos con mucosidad como resultado de infecciones pulmonares frecuentes. Otros signos y síntomas pueden incluir infecciones de los senos nasales, crecimiento deficiente, heces grasosas, palpitaciones en los dedos de manos y pies e infertilidad en la mayoría de los hombres. Diferentes personas pueden tener diferentes grados de síntomas.
La fibrosis quística se hereda de forma autosómica recesiva. Está causada por la presencia de mutaciones en ambas copias del gen de la proteína reguladora de la conductancia transmembrana de la fibrosis quística (CFTR). Los que tienen una sola copia de trabajo son portadores y, por lo demás, en su mayoría sanos. CFTR está involucrado en la producción de sudor, fluidos digestivos y moco. Cuando el CFTR no es funcional, las secreciones que normalmente son finas se vuelven espesas. La afección se diagnostica mediante una prueba de sudor y pruebas genéticas. La detección de bebés al nacer se lleva a cabo en algunas áreas del mundo.
No existe una cura conocida para la fibrosis quística. Las infecciones pulmonares se tratan con antibióticos que se pueden administrar por vía intravenosa, por inhalación o por vía oral. A veces, el antibiótico azitromicina se usa a largo plazo. La solución salina hipertónica inhalada y el salbutamol también pueden ser útiles. El trasplante de pulmón puede ser una opción si la función pulmonar sigue empeorando. El reemplazo de enzimas pancreáticas y la suplementación con vitaminas liposolubles son importantes, especialmente en los jóvenes. Las técnicas de limpieza de las vías respiratorias, como la fisioterapia torácica, tienen algún beneficio a corto plazo, pero los efectos a largo plazo no están claros. La expectativa de vida promedio es de 42 a 50 años en el mundo desarrollado. Los problemas pulmonares son responsables de la muerte del 80% de las personas con fibrosis quística.
La FQ es más común entre las personas de ascendencia del norte de Europa, para quienes afecta aproximadamente a 1 de cada 3000 recién nacidos, y entre los cuales alrededor de 1 de cada 25 personas es portador. Es menos común en africanos y asiáticos, aunque ocurre en todas las razas. Fue reconocida por primera vez como una enfermedad específica por Dorothy Andersen en 1938, con descripciones que se ajustan a la condición ocurriendo al menos desde 1595. El nombre "fibrosis quística" se refiere a la característica fibrosis y quistes que se forman dentro del páncreas.
Signos y síntomas
La fibrosis quística generalmente se manifiesta temprano en la vida. Los recién nacidos y los bebés con fibrosis quística tienden a tener heces grasosas, abundantes y frecuentes (como resultado de la malabsorción) y tienen un peso inferior al normal para su edad. Entre el 15 y el 20 % de los recién nacidos tienen el intestino delgado bloqueado por meconio, lo que a menudo requiere cirugía para corregirlo. Los recién nacidos ocasionalmente tienen ictericia neonatal debido a la obstrucción de los conductos biliares. Los niños con fibrosis quística pierden demasiada sal en el sudor, y los padres a menudo notan que la sal se cristaliza en la piel o un sabor salado cuando besan a su hijo.
La principal causa de morbilidad y muerte en las personas con fibrosis quística es la enfermedad pulmonar progresiva, que finalmente provoca insuficiencia respiratoria. Esto generalmente comienza como una infección respiratoria prolongada que continúa hasta que se trata con antibióticos. La infección crónica del tracto respiratorio es casi universal en personas con fibrosis quística, con Pseudomonas aeruginosa, hongos y micobacterias cada vez más comunes con el tiempo. La inflamación de las vías respiratorias superiores produce secreción nasal frecuente y obstrucción nasal. Los pólipos nasales son comunes, particularmente en niños y adolescentes. A medida que avanza la enfermedad, las personas tienden a tener dificultad para respirar y una tos crónica que produce esputo. Los problemas respiratorios dificultan cada vez más el ejercicio, y la enfermedad prolongada hace que los afectados tengan un peso inferior al normal para su edad. En la adolescencia tardía o la edad adulta, las personas comienzan a desarrollar signos graves de enfermedad pulmonar: sibilancias, hipocratismo digital, cianosis, tos con sangre, cardiopatía pulmonar y pulmón colapsado (atelectasia o neumotórax).
En casos raros, la fibrosis quística puede manifestarse como un trastorno de la coagulación. La vitamina K normalmente se absorbe de la leche materna, la fórmula y, más tarde, de los alimentos sólidos. Esta absorción está alterada en algunos pacientes con FQ. Los niños pequeños son especialmente sensibles a los trastornos de malabsorción de la vitamina K porque solo una cantidad muy pequeña de vitamina K atraviesa la placenta, lo que deja al niño con reservas muy bajas y una capacidad limitada para absorber la vitamina K de fuentes dietéticas después del nacimiento. Debido a que los factores de coagulación II, VII, IX y X dependen de la vitamina K, los niveles bajos de vitamina K pueden provocar problemas de coagulación. En consecuencia, cuando un niño presenta hematomas inexplicables, puede justificarse una evaluación de la coagulación para determinar si existe una enfermedad subyacente.
Pulmones y senos paranasales
La enfermedad pulmonar es el resultado de la obstrucción de las vías respiratorias debido a la acumulación de moco, la disminución de la eliminación mucociliar y la inflamación resultante. En etapas posteriores, los cambios en la arquitectura del pulmón, como la patología en las principales vías respiratorias (bronquiectasias), exacerban aún más las dificultades para respirar. Otros signos incluyen presión arterial alta en los pulmones (hipertensión pulmonar), insuficiencia cardíaca, dificultades para llevar suficiente oxígeno al cuerpo (hipoxia) e insuficiencia respiratoria que requiere apoyo con máscaras de respiración, como máquinas de presión positiva en las vías respiratorias de dos niveles o ventiladores. Staphylococcus aureus, Haemophilus influenzae y Pseudomonas aeruginosa son los tres organismos más comunes que causan infecciones pulmonares en pacientes con FQ. Además, puede ocurrir una infección oportunista por el complejo Burkholderia cepacia, especialmente por transmisión de paciente a paciente.
Además de las infecciones bacterianas típicas, las personas con FQ desarrollan más comúnmente otros tipos de enfermedades pulmonares. Entre estos se encuentra la aspergilosis broncopulmonar alérgica, en la que la respuesta del organismo al hongo común Aspergillus fumigatus provoca el empeoramiento de los problemas respiratorios. Otra es la infección por el complejo Mycobacterium avium, un grupo de bacterias relacionadas con la tuberculosis, que pueden causar daño pulmonar y no responden a los antibióticos comunes.
La mucosidad en los senos paranasales es igualmente espesa y también puede causar el bloqueo de los conductos de los senos paranasales, lo que lleva a una infección. Esto puede causar dolor facial, fiebre, secreción nasal y dolores de cabeza. Las personas con FQ pueden desarrollar un crecimiento excesivo del tejido nasal (pólipos nasales) debido a la inflamación de las infecciones crónicas de los senos paranasales. Los pólipos nasosinusales recurrentes pueden ocurrir en el 10% al 25% de los pacientes con FQ. Estos pólipos pueden bloquear las fosas nasales y aumentar las dificultades para respirar.
Las complicaciones cardiorrespiratorias son las causas más comunes de muerte (alrededor del 80 %) en pacientes en la mayoría de los centros de FQ en los Estados Unidos.
Aparato digestivo
Además, la protrusión de las membranas rectales internas (prolapso rectal) es más común, ocurre en hasta un 10 % de los niños con FQ y es causada por un aumento del volumen fecal, desnutrición y aumento de la presión intraabdominal debido a tosiendo
La mucosidad espesa que se ve en los pulmones tiene su contraparte en las secreciones espesas del páncreas, un órgano responsable de proporcionar los jugos digestivos que ayudan a descomponer los alimentos. Estas secreciones bloquean el movimiento exocrino de las enzimas digestivas hacia el duodeno y provocan daños irreversibles en el páncreas, a menudo con inflamación dolorosa (pancreatitis). Los conductos pancreáticos se obstruyen por completo en los casos más avanzados, por lo general en niños mayores o adolescentes. Esto provoca atrofia de las glándulas exocrinas y fibrosis progresiva.
Las personas con FQ también tienen dificultades para absorber las vitaminas liposolubles A, D, E y K.
Además de los problemas del páncreas, las personas con FQ experimentan más acidez estomacal, obstrucción intestinal por intususcepción y estreñimiento. Las personas mayores con FQ pueden desarrollar el síndrome de obstrucción intestinal distal, que ocurre cuando las heces se vuelven espesas con mucosidad (espesadas) y pueden causar distensión abdominal, dolor y obstrucción intestinal incompleta o completa.
La insuficiencia pancreática exocrina ocurre en la mayoría (85–90 %) de los pacientes con FQ. Se asocia principalmente con "grave" Mutaciones CFTR, donde ambos alelos son completamente no funcionales (por ejemplo, ΔF508/ΔF508). Ocurre en el 10-15% de los pacientes con una enfermedad "grave" y uno "leve" Mutación de CFTR en la que todavía se produce poca actividad de CFTR, o en la que dos mutaciones "leve" Existen mutaciones de CFTR. En estos casos más leves, todavía hay suficiente función exocrina pancreática, por lo que no se requiere la suplementación con enzimas. Por lo general, no se presentan otras complicaciones gastrointestinales en fenotipos con suficiente páncreas y, en general, estos individuos suelen tener un crecimiento y desarrollo excelentes. A pesar de esto, la pancreatitis crónica idiopática puede ocurrir en un subgrupo de personas con FQ con pancreas suficiente y se asocia con dolor abdominal recurrente y complicaciones potencialmente mortales.
Las secreciones espesas también pueden causar problemas hepáticos en pacientes con FQ. La bilis secretada por el hígado para ayudar en la digestión puede bloquear los conductos biliares y provocar daño hepático. La mala digestión o absorción de lípidos puede provocar esteatorrea. Con el tiempo, esto puede provocar cicatrices y nodularidad (cirrosis). El hígado no logra eliminar las toxinas de la sangre y no produce proteínas importantes, como las responsables de la coagulación de la sangre. La enfermedad hepática es la tercera causa más común de muerte asociada con la FQ.
Alrededor del 5 al 7 % de las personas experimentan daño hepático lo suficientemente grave como para causar síntomas: por lo general, cálculos biliares que causan cólico biliar.
Endocrino
El páncreas contiene los islotes de Langerhans, que son responsables de producir insulina, una hormona que ayuda a regular la glucosa en sangre. El daño al páncreas puede provocar la pérdida de las células de los islotes, lo que lleva a un tipo de diabetes exclusivo de las personas con la enfermedad. Esta diabetes relacionada con la fibrosis quística comparte características de la diabetes tipo 1 y tipo 2, y es una de las principales complicaciones no pulmonares de la FQ.
La vitamina D participa en la regulación del calcio y el fosfato. La absorción deficiente de vitamina D de la dieta debido a la malabsorción puede conducir a la osteoporosis, una enfermedad ósea en la que los huesos debilitados son más susceptibles a las fracturas.
Infertilidad
La infertilidad afecta tanto a hombres como a mujeres. Al menos el 97% de los hombres con fibrosis quística son infértiles, pero no estériles, y pueden tener hijos con técnicas de reproducción asistida. La principal causa de infertilidad en hombres con fibrosis quística es la ausencia congénita del conducto deferente (que normalmente conecta los testículos con los conductos eyaculadores del pene), pero también puede deberse a otros mecanismos, como la falta de espermatozoides, espermatozoides de forma anormal y pocos espermatozoides con poca motilidad. Muchos hombres que tienen una ausencia congénita de los conductos deferentes durante la evaluación de la infertilidad tienen una forma leve de fibrosis quística no diagnosticada previamente. Alrededor del 20 % de las mujeres con FQ tienen dificultades de fertilidad debido a la desnutrición o al moco cervical espesado. En casos severos, la desnutrición interrumpe la ovulación y provoca la falta de menstruación.
Causas
La FQ es causada por una mutación en el gen regulador de la conductancia transmembrana de la fibrosis quística (CFTR). La mutación más común, ΔF508, es una deleción (Δ significa deleción) de tres nucleótidos que resulta en una pérdida del aminoácido fenilalanina (F) en la posición 508 de la proteína. Esta mutación representa dos tercios (66 a 70 %) de los casos de FQ en todo el mundo y 90 % de los casos en Estados Unidos; sin embargo, más de 1500 otras mutaciones pueden producir FQ. Aunque la mayoría de las personas tienen dos copias funcionales (alelos) del gen CFTR, solo se necesita una para prevenir la fibrosis quística. La FQ se desarrolla cuando ningún alelo puede producir una proteína CFTR funcional. Por lo tanto, la FQ se considera una enfermedad autosómica recesiva.
El gen CFTR, que se encuentra en el locus q31.2 del cromosoma 7, tiene una longitud de 230 000 pares de bases y crea una proteína de 1480 aminoácidos. Más específicamente, la ubicación está entre el par de bases 117.120.016 y 117.308.718 en el brazo largo del cromosoma 7, región 3, banda 1, subbanda 2, representada como 7q31.2. Estructuralmente, el CFTR es un tipo de gen conocido como gen ABC. El producto de este gen (la proteína CFTR) es un canal de iones de cloruro importante en la creación de sudor, jugos digestivos y mucosidad. Esta proteína posee dos dominios de hidrolización de ATP, lo que permite que la proteína use energía en forma de ATP. También contiene dos dominios que comprenden seis hélices alfa cada uno, que permiten que la proteína atraviese la membrana celular. Un sitio de unión regulador en la proteína permite la activación por fosforilación, principalmente por la proteína quinasa dependiente de cAMP. El carboxilo terminal de la proteína está anclado al citoesqueleto por una interacción del dominio PDZ. La mayoría de CFTR en los conductos pulmonares es producido por células raras transportadoras de iones que regulan las propiedades de la mucosidad.
Además, cada vez hay más pruebas de que los modificadores genéticos además de CFTR modulan la frecuencia y la gravedad de la enfermedad. Un ejemplo es la lectina de unión a manano, que participa en la inmunidad innata al facilitar la fagocitosis de los microorganismos. Los polimorfismos en uno o ambos alelos de lectina de unión a manano que dan como resultado niveles circulantes más bajos de la proteína se asocian con un riesgo tres veces mayor de enfermedad pulmonar en etapa terminal, así como con una mayor carga de infecciones bacterianas crónicas.
Transportistas
Hasta uno de cada 25 individuos de ascendencia del norte de Europa se considera portador genético. La enfermedad aparece solo cuando dos de estas portadoras tienen hijos, ya que cada embarazo entre ellas tiene un 25% de posibilidades de producir un hijo con la enfermedad. Aunque solo uno de cada 3000 recién nacidos de la ascendencia afectada tiene FQ, se conocen más de 900 mutaciones del gen que causa la FQ. Las pruebas actuales buscan las mutaciones más comunes.
Las mutaciones detectadas por la prueba varían según el grupo étnico de una persona o según la presencia de FQ en la familia. Más de 10 millones de estadounidenses, incluido uno de cada 25 estadounidenses blancos, son portadores de una mutación del gen de la FQ. La FQ está presente en otras razas, aunque no con tanta frecuencia como en los blancos. Aproximadamente uno de cada 46 hispanoamericanos, uno de cada 65 afroamericanos y uno de cada 90 asiático-americanos portan una mutación del gen de la FQ.
Fisiopatología

Pueden ocurrir varias mutaciones en el gen CFTR, y diferentes mutaciones causan diferentes defectos en la proteína CFTR, lo que a veces provoca una enfermedad más leve o más grave. Estos defectos proteicos también son objetivos de fármacos que, en ocasiones, pueden restaurar su función. La mutación del gen ΔF508-CFTR, que ocurre en >90% de los pacientes en los EE. UU., crea una proteína que no se pliega normalmente y no se transporta adecuadamente a la membrana celular, lo que provoca su degradación.
Otras mutaciones dan como resultado proteínas que son demasiado cortas (truncadas) porque la producción finaliza prematuramente. Otras mutaciones producen proteínas que normalmente no utilizan energía (en forma de ATP), no permiten que el cloruro, el yoduro y el tiocianato atraviesen la membrana de forma adecuada y se degradan a un ritmo más rápido de lo normal. Las mutaciones también pueden conducir a que se produzcan menos copias de la proteína CFTR.
La proteína creada por este gen está anclada a la membrana externa de las células de las glándulas sudoríparas, los pulmones, el páncreas y todas las demás glándulas exocrinas restantes del cuerpo. La proteína atraviesa esta membrana y actúa como un canal que conecta la parte interna de la célula (citoplasma) con el líquido circundante. Este canal es el principal responsable de controlar el movimiento de los aniones haluro desde el interior hacia el exterior de la célula; sin embargo, en los conductos sudoríparos, facilita el movimiento de cloruro desde el conducto sudoríparo hacia el citoplasma. Cuando la proteína CFTR no reabsorbe los iones en los conductos sudoríparos, el cloruro y el tiocianato liberados por las glándulas sudoríparas quedan atrapados dentro de los conductos y se bombean a la piel.
Además, el hipotiocianito, OSCN, no puede ser producido por el sistema de defensa inmunitario. Debido a que el cloruro tiene carga negativa, esto modifica el potencial eléctrico dentro y fuera de la celda que normalmente hace que los cationes entren en la celda. El sodio es el catión más común en el espacio extracelular. El exceso de cloruro dentro de los conductos sudoríparos impide la reabsorción de sodio por los canales de sodio epiteliales y la combinación de sodio y cloruro crea la sal, que se pierde en grandes cantidades en el sudor de las personas con FQ. Esta sal perdida forma la base para la prueba del sudor.
La mayor parte del daño en la FQ se debe a la obstrucción de los conductos estrechos de los órganos afectados con secreciones espesas. Estos bloqueos conducen a remodelación e infección en el pulmón, daño por enzimas digestivas acumuladas en el páncreas, bloqueo de los intestinos por heces espesas, etc. Se han postulado varias teorías sobre cómo los defectos en la función proteica y celular causan los efectos clínicos. La teoría más actual sugiere que el transporte iónico defectuoso conduce a la deshidratación en el epitelio de las vías respiratorias, espesando la mucosidad. En las células epiteliales de las vías respiratorias, los cilios existen entre la superficie apical de la célula y la mucosidad en una capa conocida como líquido de la superficie de las vías respiratorias (ASL). El flujo de iones desde la célula hacia esta capa está determinado por canales iónicos como CFTR. CFTR no solo permite que los iones de cloruro se extraigan de la célula y entren en el ASL, sino que también regula otro canal llamado ENac, que permite que los iones de sodio abandonen el ASL y entren en el epitelio respiratorio. CFTR normalmente inhibe este canal, pero si el CFTR es defectuoso, entonces el sodio fluye libremente desde el ASL hacia la célula.
A medida que el agua sigue al sodio, la profundidad de ASL se reducirá y los cilios quedarán en la capa mucosa. Como los cilios no pueden moverse con eficacia en un entorno espeso y viscoso, el aclaramiento mucociliar es deficiente y se produce una acumulación de mucosidad que obstruye las vías respiratorias pequeñas. La acumulación de moco más viscoso y rico en nutrientes en los pulmones permite que las bacterias se escondan del sistema inmunitario del cuerpo, lo que provoca infecciones respiratorias repetidas. La presencia de las mismas proteínas CFTR en el conducto pancreático y las glándulas sudoríparas en la piel también provocan síntomas en estos sistemas.
Infecciones crónicas
Los pulmones de las personas con fibrosis quística son colonizados e infectados por bacterias desde una edad temprana. Estas bacterias, que a menudo se propagan entre las personas con FQ, prosperan en la mucosidad alterada, que se acumula en las vías respiratorias pequeñas de los pulmones. Este moco conduce a la formación de microambientes bacterianos conocidos como biopelículas que son difíciles de penetrar para las células inmunitarias y los antibióticos. Las secreciones viscosas y las infecciones respiratorias persistentes dañan repetidamente el pulmón al remodelar gradualmente las vías respiratorias, lo que hace que la infección sea aún más difícil de erradicar. La historia natural de las infecciones pulmonares con FQ y la remodelación de las vías respiratorias es poco conocida, en gran parte debido a la inmensa heterogeneidad espacial y temporal tanto dentro como entre los microbiomas de los pacientes con FQ.
Con el tiempo, tanto los tipos de bacterias como sus características individuales cambian en las personas con FQ. En la etapa inicial, bacterias comunes como S. aureus y H. influenzae colonizan e infectan los pulmones. Finalmente, domina Pseudomonas aeruginosa (ya veces Burkholderia cepacia). A los 18 años, el 80 % de los pacientes con FQ clásica albergan P. aeruginosa, y el 3,5% albergan B. cepacia. Una vez dentro de los pulmones, estas bacterias se adaptan al medio ambiente y desarrollan resistencia a los antibióticos de uso común. Pseudomonas puede desarrollar características especiales que permiten la formación de grandes colonias, conocidas como colonias "mucoides" Pseudomonas, que rara vez se ven en personas que no tienen FQ. La evidencia científica sugiere que la vía de la interleucina 17 juega un papel clave en la resistencia y la modulación de la respuesta inflamatoria durante la P. aeruginosa en la FQ. En particular, la inmunidad mediada por la interleucina 17 tiene una actividad de doble filo durante la infección crónica de las vías respiratorias; por un lado, contribuye al control de P. aeruginosa, mientras que por otro propaga la neutrofilia pulmonar exacerbada y el remodelado tisular.
La infección se puede propagar al pasar entre diferentes personas con FQ. En el pasado, las personas con FQ solían participar en los 'campamentos de FQ' de verano. y otras reuniones recreativas. Los hospitales agruparon a los pacientes con FQ en áreas comunes y el equipo de rutina (como los nebulizadores) no se esterilizó entre pacientes individuales. Esto condujo a la transmisión de cepas de bacterias más peligrosas entre grupos de pacientes. Como resultado, las personas con FQ ahora se aíslan rutinariamente unas de otras en el entorno de atención médica, y se alienta a los proveedores de atención médica a usar batas y guantes cuando examinen a los pacientes con FQ para limitar la propagación de cepas bacterianas virulentas.
Los pacientes con FQ también pueden tener sus vías respiratorias crónicamente colonizadas por hongos filamentosos (como Aspergillus fumigatus, Scedosporium apiospermum, Aspergillus terreus) y/ o levaduras (como Candida albicans); otros hongos filamentosos que se aíslan con menos frecuencia incluyen Aspergillus flavus y Aspergillus nidulans (se producen de forma transitoria en las secreciones respiratorias de la FQ) y Exophiala dermatitidis y Scedosporium prolificans (colonizadores crónicos de las vías respiratorias); algunos hongos filamentosos como Penicillium emersonii y Acrophialophora fusispora se encuentran en pacientes casi exclusivamente en el contexto de la FQ. El aclaramiento mucociliar defectuoso que caracteriza a la FQ se asocia con trastornos inmunológicos locales. Además, la terapia prolongada con antibióticos y el uso de tratamientos con corticoides también pueden facilitar el crecimiento de hongos. Aunque la relevancia clínica de la colonización fúngica de las vías respiratorias sigue siendo un tema de debate, los hongos filamentosos pueden contribuir a la respuesta inflamatoria local y, por tanto, al deterioro progresivo de la función pulmonar, como suele ocurrir con la aspergilosis broncopulmonar alérgica, la enfermedad fúngica más frecuente en el contexto de la FQ, que involucra una respuesta inmune impulsada por Th2 a las especies de Aspergillus.
Diagnóstico
En muchas localidades, todos los recién nacidos se someten a pruebas de detección de fibrosis quística durante los primeros días de vida, generalmente mediante un análisis de sangre para detectar niveles altos de tripsinógeno inmunorreactivo. Los recién nacidos con pruebas positivas o aquellos de los que se sospecha que tienen fibrosis quística según los síntomas o antecedentes familiares, luego se someten a una prueba de sudor. Se utiliza una corriente eléctrica para impulsar la pilocarpina en la piel, estimulando la sudoración. El sudor se recoge y se analiza para los niveles de sal. Tener niveles inusualmente altos de cloruro en el sudor sugiere que CFTR es disfuncional; luego se diagnostica a la persona con fibrosis quística. Las pruebas genéticas también están disponibles para identificar las mutaciones de CFTR típicamente asociadas con la fibrosis quística. Muchos laboratorios pueden analizar las 30 a 96 mutaciones CFTR más comunes, que pueden identificar a más del 90 % de las personas con fibrosis quística.
Las personas con FQ tienen menos tiocianato e hipotiocianito en la saliva y la mucosidad (Banfi et al.). En el caso de las formas más leves de FQ, las mediciones de la diferencia de potencial transepitelial pueden ser útiles. La FQ también se puede diagnosticar mediante la identificación de mutaciones en el gen CFTR.
En muchos casos, un padre hace el diagnóstico porque el bebé sabe salado. Los niveles de tripsinógeno inmunorreactivo pueden aumentar en individuos que tienen una sola copia mutada del gen CFTR (portadores) o, en raras ocasiones, en individuos con dos copias normales del CFTR gene. Debido a estos falsos positivos, el cribado de FQ en recién nacidos puede ser controvertido.
Para 2010, todos los estados de EE. UU. habían instituido programas de detección de recién nacidos y, a partir de 2016, 21 países europeos tenían programas en al menos algunas regiones.
Prenatal
Las mujeres que están embarazadas o las parejas que planean un embarazo pueden hacerse la prueba de mutaciones del gen CFTR para determinar el riesgo de que su hijo nazca con FQ. La prueba generalmente se realiza primero en uno o ambos padres y, si el riesgo de FQ es alto, se realiza la prueba en el feto. El Colegio Estadounidense de Obstetras y Ginecólogos recomienda que todas las personas que estén pensando en quedar embarazadas se hagan pruebas para ver si son portadoras.
Debido a que el desarrollo de la FQ en el feto requiere que cada padre transmita una copia mutada del gen CFTR y debido a que las pruebas de FQ son costosas, las pruebas a menudo se realizan inicialmente en uno de los padres. Si las pruebas muestran que el padre es portador de la mutación del gen CFTR, se analiza al otro padre para calcular el riesgo de que sus hijos tengan FQ. La FQ puede resultar de más de mil mutaciones diferentes. A partir de 2016, normalmente solo se analizan las mutaciones más comunes, como ΔF508. La mayoría de las pruebas disponibles en el mercado buscan 32 mutaciones diferentes o menos. Si una familia tiene una mutación poco común conocida, se puede realizar una detección específica para esa mutación. Debido a que no todas las mutaciones conocidas se encuentran en las pruebas actuales, una prueba negativa no garantiza que un niño no tenga FQ.
Durante el embarazo, las pruebas se pueden realizar en la placenta (muestra de vellosidades coriónicas) o en el líquido que rodea al feto (amniocentesis). Sin embargo, la muestra de vellosidades coriónicas tiene un riesgo de muerte fetal de uno en 100 y amniocentesis de uno en 200; un estudio reciente ha indicado que esto puede ser mucho menor, aproximadamente uno en 1600.
Económicamente, para las parejas portadoras de fibrosis quística, al comparar el diagnóstico genético preimplantacional (DGP) con la concepción natural (NC) seguida de pruebas prenatales y aborto de los embarazos afectados, el DGP proporciona beneficios económicos netos hasta una edad materna alrededor de los 40 años, después de lo cual la CN, las pruebas prenatales y el aborto tienen mayor beneficio económico.
Administración
Si bien no se conocen curas para la FQ, se utilizan varios métodos de tratamiento. El manejo de la FQ ha mejorado significativamente en los últimos 70 años. Si bien es poco probable que los bebés que nacieron con él hace 70 años vivieran más allá de su primer año, es probable que los bebés de hoy vivan hasta bien entrada la edad adulta. Los avances recientes en el tratamiento de la fibrosis quística han significado que las personas con fibrosis quística pueden vivir una vida más plena y menos agobiadas por su condición. Los pilares del manejo son el tratamiento proactivo de la infección de las vías respiratorias y el fomento de una buena nutrición y un estilo de vida activo. La rehabilitación pulmonar como tratamiento de la FQ continúa a lo largo de la vida de una persona y tiene como objetivo maximizar la función de los órganos y, por lo tanto, la calidad de vida. Los terapeutas ocupacionales utilizan técnicas de conservación de energía (TEC) en el proceso de rehabilitación de pacientes con Fibrosis Quística. Ejemplos de técnicas de conservación de energía son los principios ergonómicos, la respiración con los labios fruncidos y la respiración diafragmática. Los pacientes con FQ tienden a tener fatiga y disnea debido a infecciones pulmonares crónicas, por lo que reducir la cantidad de energía gastada durante las actividades puede ayudar a los pacientes a sentirse mejor y ganar más independencia. En el mejor de los casos, los tratamientos actuales retrasan la disminución de la función de los órganos. Debido a la amplia variación en los síntomas de la enfermedad, el tratamiento generalmente se lleva a cabo en centros multidisciplinarios especializados y se adapta al individuo. Los objetivos de la terapia son los pulmones, el tracto gastrointestinal (incluidos los suplementos de enzimas pancreáticas), los órganos reproductivos (incluida la tecnología de reproducción asistida) y el apoyo psicológico.
El aspecto más constante de la terapia en la FQ es limitar y tratar el daño pulmonar causado por la mucosidad espesa y la infección, con el objetivo de mantener la calidad de vida. Los antibióticos intravenosos, inhalados y orales se usan para tratar infecciones crónicas y agudas. Se utilizan dispositivos mecánicos y medicamentos de inhalación para alterar y eliminar la mucosidad espesa. Estas terapias, si bien son efectivas, pueden llevar mucho tiempo. Se recomienda la terapia de oxígeno en el hogar en aquellos con niveles de oxígeno significativamente bajos. Muchas personas con FQ usan probióticos, que se cree que pueden corregir la disbiosis intestinal y la inflamación, pero la evidencia de los ensayos clínicos con respecto a la efectividad de los probióticos para reducir las exacerbaciones pulmonares en personas con FQ es incierta.
Antibióticos
Muchas personas con FQ toman uno o más antibióticos en todo momento, incluso cuando están sanas, para suprimir la infección de manera profiláctica. Los antibióticos son absolutamente necesarios siempre que se sospeche neumonía o se observe una disminución notable en la función pulmonar, y generalmente se eligen en función de los resultados de un análisis de esputo y la respuesta anterior de la persona. Esta terapia prolongada a menudo requiere hospitalización e inserción de una vía intravenosa más permanente, como un catéter central de inserción periférica o Port-a-Cath. La terapia inhalada con antibióticos como tobramicina, colistina y aztreonam a menudo se administra durante meses para mejorar la función pulmonar al impedir el crecimiento de bacterias colonizadas. La terapia con antibióticos inhalados ayuda a la función pulmonar al combatir las infecciones, pero también tiene inconvenientes importantes, como el desarrollo de resistencia a los antibióticos, tinnitus y cambios en la voz. La levofloxacina inhalada se puede usar para tratar Pseudomonas aeruginosa en personas con fibrosis quística que están infectadas. El manejo temprano de la infección por Pseudomonas aeruginosa es más fácil y mejor, el uso de antibióticos nebulizados con o sin antibióticos orales puede sostener su erradicación hasta dos años. Al elegir antibióticos para tratar pacientes con FQ e infecciones pulmonares causadas por Pseudomonas aeruginosa en personas con fibrosis quística, aún no está claro si la elección de los antibióticos debe basarse en los resultados de las pruebas de antibióticos por separado (uno a la vez). tiempo) o en combinación entre sí.
Se administran antibióticos por vía oral, como ciprofloxacina o azitromicina, para ayudar a prevenir infecciones o controlar infecciones en curso. Los antibióticos aminoglucósidos (p. ej., tobramicina) utilizados pueden causar pérdida de audición, daños en el sistema de equilibrio del oído interno o insuficiencia renal con el uso a largo plazo. Para prevenir estos efectos secundarios, la cantidad de antibióticos en la sangre se mide de forma rutinaria y se ajusta en consecuencia.
Todos estos factores relacionados con el uso de antibióticos, la cronicidad de la enfermedad y la aparición de bacterias resistentes exigen una mayor exploración de diferentes estrategias, como la terapia adyuvante con antibióticos. Actualmente, ninguna prueba clínica confiable muestra la efectividad de los antibióticos para las exacerbaciones pulmonares en personas con fibrosis quística y el complejo Burkholderia cepacia o para el uso de antibióticos para tratar micobacterias no tuberculosas en personas con FQ.
Otros medicamentos
Los medicamentos en aerosol que ayudan a aflojar las secreciones incluyen dornasa alfa y solución salina hipertónica. Dornase es una desoxirribonucleasa humana recombinante, que descompone el ADN en el esputo, lo que reduce su viscosidad. Dornasa alfa mejora la función pulmonar y probablemente disminuye el riesgo de exacerbaciones, pero no hay evidencia suficiente para saber si es más o menos eficaz que otros medicamentos similares. La dornasa alfa puede mejorar la función pulmonar; sin embargo, no hay pruebas sólidas de que sea mejor que otras terapias hiperosmolares.
Denufosol, un fármaco en investigación, abre un canal de cloruro alternativo y ayuda a licuar la mucosidad. No está claro si los corticosteroides inhalados son útiles, pero es seguro suspender la terapia con corticosteroides inhalados. Hay evidencia débil de que el tratamiento con corticosteroides puede causar daño al interferir con el crecimiento. La vacunación antineumocócica no se ha estudiado hasta 2014. Hasta 2014, no hay pruebas claras de ensayos controlados aleatorios de que la vacuna contra la influenza sea beneficiosa para las personas con fibrosis quística.
Ivacaftor es un medicamento que se toma por vía oral para el tratamiento de la FQ debido a una serie de mutaciones específicas que responden a la potenciación de la proteína CFTR inducida por ivacaftor. Mejora la función pulmonar en aproximadamente un 10%; sin embargo, a partir de 2014 es caro. El primer año que estuvo en el mercado, el precio de lista superaba los $300,000 por año en los Estados Unidos. En julio de 2015, la Administración de Drogas y Alimentos de los EE. UU. aprobó lumacaftor/ivacaftor. En 2018, la FDA aprobó la combinación ivacaftor/tezacaftor; el fabricante anunció un precio de lista de $ 292,000 por año. Tezacaftor ayuda a mover la proteína CFTR a la posición correcta en la superficie celular y está diseñado para tratar a personas con la mutación F508del.
En 2019, se aprobó el fármaco combinado elexacaftor/ivacaftor/tezacaftor, comercializado como Trikafta en los Estados Unidos, para pacientes con FQ mayores de 12 años. En 2021, se amplió para incluir a pacientes mayores de 12 años. la edad de 6 años. En Europa, este medicamento fue aprobado en 2020 y comercializado como Kaftrio. Se usa en aquellos que tienen una mutación f508del, que ocurre en aproximadamente el 90% de los pacientes con fibrosis quística. Según la Cystic Fibrosis Foundation, "este medicamento representa el mayor avance terapéutico individual en la historia de la FQ y ofrece un tratamiento para la causa subyacente de la enfermedad que eventualmente podría llevar la terapia moduladora al 90 por ciento de las personas con FQ.& #34; En un ensayo clínico, los participantes a los que se les administró el fármaco combinado experimentaron una disminución posterior del 63 % en las exacerbaciones pulmonares y una disminución de 41,8 mmol/l en la concentración de cloruro en el sudor. Al mitigar un repertorio de síntomas asociados con la fibrosis quística, el fármaco combinado también mejoró significativamente las métricas de calidad de vida entre los pacientes con la enfermedad. También se sabe que el fármaco combinado interactúa con los inductores de CYP3A, como la carbamazepina utilizada en el tratamiento del trastorno bipolar, lo que provoca que elexafaftor/ivacaftor/tezacaftor circule por el cuerpo en concentraciones reducidas. Como tal, no se recomienda el uso concomitante. El precio de lista en los Estados Unidos será de $311,000 por año; sin embargo, el seguro puede cubrir gran parte del costo del medicamento.
Se ha utilizado ácido ursodesoxicólico, una sal biliar, sin embargo, no hay datos suficientes para demostrar si es eficaz.
Suplemento de nutrientes
No está claro si los suplementos de vitamina A o betacaroteno tienen algún efecto sobre los problemas oculares y cutáneos causados por la deficiencia de vitamina A.
No hay pruebas sólidas de que las personas con fibrosis quística puedan prevenir la osteoporosis aumentando su consumo de vitamina D.
Para las personas con deficiencia de vitamina E y fibrosis quística, existen pruebas de que la administración de suplementos de vitamina E puede mejorar los niveles de vitamina E, aunque todavía no se sabe qué efecto tiene la administración de suplementos sobre los trastornos por deficiencia específicos de vitamina E o sobre la función pulmonar.
Falta evidencia sólida sobre los efectos de la suplementación con vitamina K en personas con fibrosis quística a partir de 2020.
Varios estudios han examinado los efectos de la suplementación con ácidos grasos omega-3 para personas con fibrosis quística, pero la evidencia es incierta sobre si tiene algún beneficio o efecto adverso.
Procedimientos
Se utilizan varias técnicas mecánicas para expulsar el esputo y estimular su expectoración. Una buena técnica para la limpieza de las vías respiratorias a corto plazo es la fisioterapia torácica, en la que un terapeuta respiratorio percute el tórax de una persona con la mano varias veces al día para aflojar las secreciones. Este "efecto de percusión" puede administrarse también a través de dispositivos específicos que utilizan la oscilación de la pared torácica o un ventilador de percusión intrapulmonar. Otros métodos, como la ventilación de coraza bifásica y el modo de limpieza asociado disponible en dichos dispositivos, integran una fase de asistencia para la tos, así como una fase de vibración para desalojar las secreciones. Estos son portátiles y adaptados para uso doméstico.
Otra técnica es la fisioterapia con presión espiratoria positiva que consiste en proporcionar una contrapresión a las vías respiratorias durante la espiración. Este efecto lo proporcionan dispositivos que consisten en una máscara o una boquilla en la que se aplica una resistencia solo en la fase de espiración. Los principios operativos de esta técnica parecen ser el aumento de la presión del gas detrás de la mucosidad a través de la ventilación colateral junto con un aumento temporal en la capacidad residual funcional que previene el colapso temprano de las vías respiratorias pequeñas durante la exhalación.
A medida que empeora la enfermedad pulmonar, es posible que se necesite asistencia respiratoria mecánica. Es posible que las personas con FQ deban usar máscaras especiales por la noche para ayudar a empujar el aire hacia los pulmones. Estas máquinas, conocidas como ventiladores de presión positiva en las vías respiratorias de dos niveles (BiPAP), ayudan a prevenir los niveles bajos de oxígeno en la sangre durante el sueño. Se pueden usar ventiladores no invasivos durante la fisioterapia para mejorar la eliminación del esputo. No se sabe si este tipo de terapia tiene un impacto sobre las exacerbaciones pulmonares o la progresión de la enfermedad. No se sabe qué papel tiene la terapia de ventilación no invasiva para mejorar la capacidad de ejercicio en pacientes con fibrosis quística. Sin embargo, los autores señalaron que "la ventilación no invasiva puede ser un complemento útil de otras técnicas de limpieza de las vías respiratorias, en particular en personas con fibrosis quística que tienen dificultad para expectorar el esputo". Durante una enfermedad grave, se puede colocar un tubo en la garganta (un procedimiento conocido como traqueotomía) para permitir la respiración asistida por un ventilador.
Para los niños, los estudios preliminares muestran que la terapia de masaje puede ayudar a las personas y a sus familias' calidad de vida.
Algunas infecciones pulmonares requieren la extirpación quirúrgica de la parte infectada del pulmón. Si esto es necesario muchas veces, la función pulmonar se reduce severamente. Las opciones de tratamiento más efectivas para las personas con FQ que tienen neumotórax espontáneos o recurrentes no están claras.
Trasplante
El trasplante de pulmón puede ser necesario para las personas con FQ a medida que disminuye la función pulmonar y la tolerancia al ejercicio. Aunque el trasplante de un solo pulmón es posible en otras enfermedades, las personas con FQ deben reemplazar ambos pulmones porque el pulmón restante podría contener bacterias que podrían infectar el pulmón trasplantado. Se puede realizar un trasplante de páncreas o de hígado al mismo tiempo para aliviar la enfermedad del hígado y/o la diabetes. El trasplante de pulmón se considera cuando la función pulmonar disminuye hasta el punto en que se requiere la asistencia de dispositivos mecánicos o la supervivencia de alguien se ve amenazada. Según el Manual Merck, “el trasplante de pulmón bilateral para la enfermedad pulmonar grave se está volviendo más rutinario y exitoso con la experiencia y técnicas mejoradas. Entre los adultos con FQ, la mediana de supervivencia posterior al trasplante es de aproximadamente 9 años."
Otros aspectos
Los recién nacidos con obstrucción intestinal generalmente requieren cirugía, mientras que los adultos con síndrome de obstrucción intestinal distal generalmente no. El tratamiento de la insuficiencia pancreática mediante el reemplazo de las enzimas digestivas faltantes permite que el duodeno absorba adecuadamente los nutrientes y las vitaminas que de otro modo se perderían en las heces. Sin embargo, la mejor dosis y forma de reemplazo de enzimas pancreáticas no está clara, al igual que los riesgos y la efectividad a largo plazo de este tratamiento.
Hasta ahora, no se ha realizado ninguna investigación a gran escala sobre la incidencia de aterosclerosis y enfermedad coronaria en adultos con fibrosis quística. Esto probablemente se deba a que la gran mayoría de las personas con fibrosis quística no viven lo suficiente como para desarrollar aterosclerosis clínicamente significativa o enfermedad coronaria.
La diabetes es la complicación no pulmonar más común de la FQ. Combina características de la diabetes tipo 1 y tipo 2, y se reconoce como una entidad distinta, la diabetes relacionada con la fibrosis quística. Si bien a veces se usan medicamentos antidiabéticos orales, el tratamiento recomendado es el uso de inyecciones de insulina o una bomba de insulina y, a diferencia de la diabetes tipo 1 y 2, no se recomiendan restricciones dietéticas. Si bien Stenotrophomonas maltophilia es relativamente común en personas con fibrosis quística, la evidencia sobre la efectividad de los antibióticos para S. maltophilia es incierta.
Los bisfosfonatos orales o intravenosos se pueden usar para mejorar la densidad mineral ósea en personas con fibrosis quística. Cuando se toman bifosfatos por vía intravenosa, los efectos adversos como el dolor y los síntomas similares a los de la gripe pueden ser un problema. Se desconocen los efectos adversos de los bifosfatos tomados por vía oral en el tracto gastrointestinal.
El crecimiento deficiente se puede evitar mediante la inserción de una sonda de alimentación para aumentar la energía de los alimentos a través de alimentos complementarios o mediante la administración de hormona de crecimiento inyectada.
Las infecciones de los senos paranasales se tratan con ciclos prolongados de antibióticos. El desarrollo de pólipos nasales u otros cambios crónicos dentro de las fosas nasales puede limitar severamente el flujo de aire a través de la nariz y, con el tiempo, reducir el sentido del olfato de la persona. La cirugía de los senos se usa a menudo para aliviar la obstrucción nasal y limitar futuras infecciones. Los esteroides nasales como el propionato de fluticasona se usan para disminuir la inflamación nasal.
La infertilidad femenina se puede superar con la tecnología de reproducción asistida, en particular con las técnicas de transferencia de embriones. La infertilidad masculina causada por la ausencia de los conductos deferentes puede superarse con la extracción de espermatozoides testiculares, recolectando espermatozoides directamente de los testículos. Si la muestra recolectada contiene muy pocos espermatozoides como para tener una fertilización espontánea, se puede realizar una inyección intracitoplasmática de espermatozoides. La reproducción por terceros también es una posibilidad para las mujeres con FQ. No está claro si tomar antioxidantes afecta los resultados.
El ejercicio físico suele ser parte de la atención ambulatoria de las personas con fibrosis quística. El ejercicio aeróbico parece ser beneficioso para la capacidad de ejercicio aeróbico, la función pulmonar y la calidad de vida relacionada con la salud; sin embargo, la calidad de la evidencia fue deficiente.
Debido al uso de antibióticos aminoglucósidos, la ototoxicidad es común. Los síntomas pueden incluir "tinnitus, pérdida de audición, hiperacusia, plenitud auditiva, mareos y vértigo".
Aparato digestivo
Los problemas con el sistema gastrointestinal, incluidos el estreñimiento y la obstrucción del tracto gastrointestinal, incluido el síndrome de obstrucción intestinal distal, son complicaciones frecuentes para las personas con fibrosis quística. El tratamiento de los problemas gastrointestinales es necesario para prevenir una obstrucción completa, reducir otros síntomas de FQ y mejorar la calidad de vida. Si bien a menudo se sugieren ablandadores de heces, laxantes y procinéticos (tratamientos enfocados en el GI), no existe un consenso claro entre los expertos sobre qué enfoque es el mejor y el que conlleva menos riesgos. A veces también se sugieren mucolíticos o tratamientos sistémicos dirigidos a CFTR disfuncional para mejorar los síntomas.
Pronóstico
El pronóstico de la fibrosis quística ha mejorado debido a un diagnóstico más temprano a través de exámenes de detección y un mejor tratamiento y acceso a la atención médica. En 1959, la mediana de edad de supervivencia de los niños con FQ en los Estados Unidos era de seis meses. En 2010, la supervivencia se estima en 37 años para las mujeres y 40 para los hombres. En Canadá, la mediana de supervivencia aumentó de 24 años en 1982 a 47,7 en 2007. En los Estados Unidos, las personas nacidas con FQ en 2016 tienen una expectativa de vida prevista de 47,7 cuando reciben atención en clínicas especializadas.
En los EE. UU., de las personas con FQ que tenían más de 18 años en 2009, el 92 % se había graduado de la escuela secundaria, el 67 % tenía al menos alguna educación universitaria, el 15 % estaba discapacitado, el 9 % estaba desempleado, 56 % eran solteros y el 39% estaban casados o vivían en pareja.
Calidad de vida
Las enfermedades crónicas pueden ser difíciles de manejar. La FQ es una enfermedad crónica que afecta a las "vías digestivas y respiratorias y provoca desnutrición generalizada e infecciones respiratorias crónicas". Las secreciones espesas obstruyen las vías respiratorias de los pulmones, lo que a menudo causa inflamación e infecciones pulmonares graves. Si se ve comprometida, afecta la calidad de vida de una persona con FQ y su capacidad para completar tareas como las tareas cotidianas.
Según Schmitz y Goldbeck (2006), la FQ aumenta significativamente el estrés emocional tanto en el individuo como en la familia, "y la necesaria rutina diaria de tratamiento que requiere mucho tiempo puede tener efectos negativos adicionales en la calidad de vida". Sin embargo, Havermans y colegas (2006) establecieron que los pacientes ambulatorios jóvenes con FQ que participaron en el Cuestionario de Fibrosis Quística-Revisado "calificaron algunos dominios de calidad de vida más altos que sus padres". En consecuencia, los pacientes ambulatorios con FQ tienen una perspectiva más positiva de sí mismos. Como señala el Manual Merck, "con el apoyo adecuado, la mayoría de los pacientes pueden hacer un ajuste apropiado para su edad en el hogar y la escuela. A pesar de la miríada de problemas, los éxitos educativos, laborales y matrimoniales de los pacientes son impresionantes."
Además, hay muchas maneras de mejorar la calidad de vida de los pacientes con FQ. Se promueve el ejercicio para aumentar la función pulmonar. La integración de un régimen de ejercicio en la rutina diaria del paciente con FQ puede mejorar significativamente la calidad de vida. No se conoce una cura definitiva para la FQ, pero se utilizan diversos medicamentos, como mucolíticos, broncodilatadores, esteroides y antibióticos, que tienen como finalidad aflojar la mucosidad, expandir las vías respiratorias, disminuir la inflamación y combatir las infecciones pulmonares, respectivamente.
Epidemiología
| Mutación | Frecuencia en todo el mundo |
|---|---|
| ΔF508 | 66-70% |
| G542X | 2,4% |
| G551D | 1,6% |
| N1303K | 1,3% |
| W1282X | 1,2% |
| Todos los demás | 27.5% |
La fibrosis quística es la enfermedad autosómica recesiva que limita la vida más común entre las personas de ascendencia europea. En los Estados Unidos, unas 30 000 personas tienen FQ; la mayoría son diagnosticados a los seis meses de edad. En Canadá, unas 4000 personas tienen FQ. Alrededor de 1 de cada 25 personas de ascendencia europea, y una de cada 30 de estadounidenses blancos, es portador de una mutación de FQ. Aunque la FQ es menos común en estos grupos, aproximadamente uno de cada 46 hispanos, uno de cada 65 africanos y uno de cada 90 asiáticos tienen al menos un gen CFTR anormal. Irlanda tiene la prevalencia de FQ más alta del mundo, una en 1353.
Aunque técnicamente es una enfermedad rara, la FQ está clasificada como una de las enfermedades genéticas que acortan la vida más extendidas. Es más común entre las naciones del mundo occidental. Una excepción es Finlandia, donde solo una de cada 80 personas porta una mutación de FQ. La Organización Mundial de la Salud afirma: "En la Unión Europea, uno de cada 2000–3000 recién nacidos se encuentra afectado por FQ". En los Estados Unidos, uno de cada 3500 niños nace con FQ. En 1997, aproximadamente uno de cada 3300 niños blancos en los Estados Unidos nació con FQ. Por el contrario, solo uno de cada 15 000 niños afroamericanos lo tiene, y en los asiáticos americanos, la tasa fue aún más baja, uno de cada 32 000.
La fibrosis quística se diagnostica por igual en hombres y mujeres. Por razones que aún no están claras, los datos han demostrado que los hombres tienden a tener una esperanza de vida más larga que las mujeres, aunque estudios recientes sugieren que esta brecha de género ya no existe, tal vez debido a las mejoras en las instalaciones de atención médica. Un estudio reciente de Irlanda identificó un vínculo entre la hormona femenina estrógeno y peores resultados en la FQ.
La distribución de los alelos de FQ varía entre las poblaciones. La frecuencia de portadores de ΔF508 se ha estimado en uno de cada 200 en el norte de Suecia, uno de cada 143 en lituanos y uno de cada 38 en Dinamarca. No se encontraron portadores de ΔF508 entre 171 finlandeses y 151 saami. ΔF508 ocurre en Finlandia, pero es un alelo minoritario allí. Se sabe que la FQ ocurre en solo 20 familias (pedigríes) en Finlandia.
Evolución
Se estima que la mutación ΔF508 tiene una antigüedad de hasta 52 000 años. Se han propuesto numerosas hipótesis sobre por qué una mutación tan letal ha persistido y se ha extendido en la población humana. Se ha descubierto que otras enfermedades autosómicas recesivas comunes, como la anemia de células falciformes, protegen a los portadores de otras enfermedades, una compensación evolutiva conocida como ventaja heterocigota. Se ha propuesto la resistencia a lo siguiente como posibles fuentes de ventaja heterocigota:
- Cholera: Con el descubrimiento de que la toxina del cólera requiere proteínas normales del huésped CFTR para funcionar correctamente, se hipotetizó que portadores de mutante CFTR genes se beneficiaron de la resistencia al cólera y otras causas de la diarrea. Otros estudios no han confirmado esta hipótesis.
- Tifoidea: Las proteínas normales de CFTR también son esenciales para la entrada de Salmonella Typhi en células, sugiriendo que portadores de mutantes CFTR Los genes pueden ser resistentes a la fiebre tifoidea. No in vivo el estudio ha confirmado esto. En ambos casos, el bajo nivel de fibrosis quística fuera de Europa, en lugares donde tanto el cólera como la fiebre tifoidea son endémicas, no es inmediatamente explicable.
- Diarrea: La prevalencia de FQ en Europa podría estar relacionada con el desarrollo de la domesticación ganadera. En esta hipótesis, portadores de un solo mutante CFTR tenía cierta protección contra la diarrea causada por la intolerancia a la lactosa, antes de que aparecieran las mutaciones que crearon tolerancia a la lactosa.
- Tuberculosis: Otra posible explicación es que los portadores del gen podrían tener alguna resistencia a la tuberculosis. Esta hipótesis se basa en la tesis de que CFTR los portadores de mutación genética no tienen suficiente acción en una de sus enzimas – arilsulfatasa - que es necesaria para Mycobacterium tuberculosis virulencia. As M. tuberculosis utilizaría las fuentes de su anfitrión para afectar al individuo, y debido a la falta de enzima que no podía presentar su virulencia, siendo un portador de CFTR la mutación podría proporcionar resistencia contra la tuberculosis.
Historia
Se supone que la FQ apareció alrededor del año 3000 a. C. debido a la migración de pueblos, mutaciones genéticas y nuevas condiciones en la alimentación. Aunque el espectro clínico completo de la FQ no se reconoció hasta la década de 1930, ciertos aspectos de la FQ se identificaron mucho antes. De hecho, la literatura de Alemania y Suiza en el siglo XVIII advirtió "Wehe dem Kind, das beim Kuß auf die Stirn salzig schmeckt, es ist verhext und muss bald sterben" ("Ay del niño que sabe salado con un beso en la frente, porque está maldito y pronto debe morir"), reconociendo el asociación entre la pérdida de sal en la FQ y la enfermedad.
En el siglo XIX, Carl von Rokitansky describió un caso de muerte fetal con peritonitis meconial, una complicación del íleo meconial asociado con la FQ. El íleo meconial fue descrito por primera vez en 1905 por Karl Landsteiner. En 1936, Guido Fanconi describió una conexión entre la enfermedad celíaca, la fibrosis quística del páncreas y las bronquiectasias.
En 1938, Dorothy Hansine Andersen publicó un artículo, "Fibrosis quística del páncreas y su relación con la enfermedad celíaca: un estudio clínico y patológico", en el American Journal of Diseases of Children. Fue la primera en describir la fibrosis quística característica del páncreas y en correlacionarla con la enfermedad pulmonar e intestinal prominente en la FQ. También planteó por primera vez la hipótesis de que la FQ era una enfermedad recesiva y utilizó por primera vez el reemplazo de enzimas pancreáticas para tratar a los niños afectados. En 1952, Paul di Sant'Agnese descubrió anomalías en los electrolitos del sudor; se desarrolló y mejoró una prueba de sudor durante la próxima década.
Hans Eiberg encontró el primer vínculo entre la FQ y otro marcador (paraoxonasa) en 1985, lo que indica que solo existe un locus para la FQ. En 1988, Francis Collins, Lap-Chee Tsui y John R. Riordan descubrieron la primera mutación para la FQ, ΔF508, en el séptimo cromosoma. Investigaciones posteriores han encontrado más de 1000 mutaciones diferentes que causan FQ.
Debido a que las mutaciones en el gen CFTR suelen ser pequeñas, las técnicas genéticas clásicas no han podido identificar con precisión el gen mutado. Usando marcadores de proteínas, los estudios de vinculación de genes pudieron mapear la mutación en el cromosoma 7. Luego se usaron técnicas de caminata cromosómica y salto cromosómico para identificar y secuenciar el gen. En 1989, Lap-Chee Tsui dirigió un equipo de investigadores en el Hospital for Sick Children de Toronto que descubrió el gen responsable de la FQ. CF representa un ejemplo clásico de cómo un trastorno genético humano fue elucidado estrictamente por el proceso de la genética avanzada.
Investigación
Las personas con FQ pueden incluirse en un registro de enfermedades que permite a los investigadores y médicos realizar un seguimiento de los resultados de salud e identificar candidatos para ensayos clínicos.
Terapia génica
La terapia génica se ha explorado como una posible cura para la FQ. Los resultados de los ensayos clínicos han mostrado un éxito limitado a partir de 2016, y no se sugiere el uso de la terapia génica como terapia de rutina. Un pequeño estudio publicado en 2015 encontró un pequeño beneficio.
Gran parte de la investigación sobre la terapia génica de la FQ se centra en tratar de colocar una copia normal del gen CFTR en las células afectadas. La transferencia del gen CFTR normal a las células epiteliales afectadas daría como resultado la producción de proteína CFTR funcional en todas las células diana, sin reacciones adversas ni una respuesta inflamatoria. Para prevenir las manifestaciones pulmonares de la FQ, solo se necesita del 5 al 10% de la cantidad normal de expresión del gen CFTR. Se han probado múltiples enfoques para la transferencia de genes, como liposomas y vectores virales en modelos animales y ensayos clínicos. Sin embargo, ambos métodos resultaron ser opciones de tratamiento relativamente ineficientes, principalmente porque muy pocas células captan el vector y expresan el gen, por lo que el tratamiento tiene poco efecto. Además, se han observado problemas en la recombinación de cDNA, de modo que el gen introducido por el tratamiento se vuelve inutilizable. Ha habido una reparación funcional en cultivo de CFTR por CRISPR/Cas9 en organoides de células madre intestinales de pacientes con fibrosis quística.
Terapia de fagos
Se está estudiando la terapia con fagos para bacterias resistentes a múltiples fármacos en personas con FQ.
Moduladores de genes
Se están desarrollando varias moléculas pequeñas que pretenden compensar diversas mutaciones del gen CFTR. Las terapias moduladoras de CFTR se han utilizado en lugar de otros tipos de terapias genéticas. Estas terapias se centran en la expresión de una mutación genética en lugar del propio gen mutado. Los moduladores se dividen en dos clases: potenciadores y correctores. Los potenciadores actúan sobre los canales de iones CFTR que están incrustados en la membrana celular, y estos tipos de fármacos ayudan a abrir el canal para permitir el flujo transmembrana. Los correctores están destinados a ayudar en el transporte de proteínas nacientes, una proteína formada por los ribosomas antes de que se transforme en una forma específica, a la superficie celular para implementarse en la membrana celular.
La mayoría se dirige a la etapa de transcripción de la expresión genética. Un enfoque ha sido tratar de desarrollar medicamentos que hagan que el ribosoma supere el codón de parada y produzca una proteína CFTR de longitud completa. Alrededor del 10 % de la FQ resulta de un codón de terminación prematuro en el ADN, lo que lleva a la terminación temprana de la síntesis de proteínas y proteínas truncadas. Estos medicamentos se dirigen a mutaciones sin sentido como G542X, que consiste en que el aminoácido glicina en la posición 542 se reemplaza por un codón de parada. Los antibióticos aminoglucósidos interfieren con la síntesis de proteínas y la corrección de errores. En algunos casos, pueden hacer que la célula supere un codón de parada prematuro mediante la inserción de un aminoácido aleatorio, lo que permite la expresión de una proteína de longitud completa. La investigación futura de estos moduladores se centra en los objetivos celulares que pueden verse afectados por un cambio en la expresión de un gen. En caso contrario, se utilizará la terapia genética como tratamiento cuando las terapias moduladoras no funcionen dado que el 10% de las personas con fibrosis quística no se ven afectadas por estos fármacos.
Elexacaftor/ivacaftor/tezacaftor se aprobó en los Estados Unidos en 2019 para la fibrosis quística. Esta combinación de medicamentos desarrollados previamente puede tratar hasta el 90 % de las personas con fibrosis quística. Estos medicamentos restauran cierta eficacia de la proteína CFTR para que pueda funcionar como un canal de iones en la superficie de la célula.
Terapia ecológica
Se ha demostrado previamente que las interacciones entre especies contribuyen de manera importante a la patología de las infecciones pulmonares con fibrosis quística. Los ejemplos incluyen la producción de enzimas que degradan los antibióticos, como las β-lactamasas, y la producción de subproductos metabólicos, como los ácidos grasos de cadena corta (AGCC), por especies anaerobias, que pueden aumentar la patogenicidad de los patógenos tradicionales, como Pseudomonas aeruginosa . Debido a esto, se ha sugerido que la alteración directa de la composición de la comunidad microbiana y la función metabólica de la FQ proporcionaría una alternativa a las terapias tradicionales con antibióticos.
Sociedad y cultura
- La vida y la muerte de Bob Flanagan, supermasoquista, un documental de 1997
- 65 Redroses, un documental de 2009
- Respirar para vivir, una memoria de Laura Rothenberg
- Cada respiración que tomo, sobrevivir y conducir con fibrosis quística, libro de Claire Wineland
- Cinco pies aparte, una película de drama romántico 2019 protagonizada por Cole Sprouse y Haley Lu Richardson
- Orla Tinsley: Guerrero, un documental de 2018 sobre la campaña CF Orla Tinsley
- El arte de la actuación de Martin O'Brien
- Continente Chasers, un viajero y paciente CF documentando viajes y blogs CF, continentechasers.com
Contenido relacionado
Congestión
Arteritis de células gigantes
Dosis