Fermentación ácida mixta

En bioquímica, la fermentación ácida mixta es el proceso metabólico por el cual un azúcar de seis carbonos (p. ej., glucosa, C6H12O6) se convierte en una mezcla compleja y variable de ácidos. Es una reacción de fermentación anaeróbica (que no requiere oxígeno) que es común en las bacterias. Es característica de los miembros de Enterobacteriaceae, una gran familia de bacterias gramnegativas que incluye a E. coli.
La mezcla de productos finales producida por la fermentación ácida mixta incluye lactato, acetato, succinato, formato, etanol y los gases H2 y CO2. La formación de estos productos finales depende de la presencia de ciertas enzimas clave en la bacteria. La proporción en la que se forman varía entre diferentes especies bacterianas. La vía de fermentación ácida mixta difiere de otras vías de fermentación, que producen menos productos finales en cantidades fijas. Los productos finales de la fermentación ácida mixta pueden tener muchas aplicaciones útiles en biotecnología e industria. Por ejemplo, el etanol se usa ampliamente como biocombustible. Por lo tanto, se han diseñado metabólicamente múltiples cepas bacterianas en el laboratorio para aumentar los rendimientos individuales de ciertos productos finales. Esta investigación se ha llevado a cabo principalmente en E. coli y está en curso. Se producen variaciones de la fermentación ácida mixta en varias especies bacterianas, incluidos patógenos bacterianos como Haemophilus influenzae, donde se producen principalmente acetato y succinato y el lactato puede servir como sustrato de crecimiento.
fermentación de ácido mixto en E. coli
E. coli utiliza vías de fermentación como una opción final para el metabolismo energético, ya que produce muy poca energía en comparación con la respiración. La fermentación ácida mixta en E. coli ocurre en dos etapas. Estas etapas están descritas en la base de datos biológica de E. coli, EcoCyc.
La primera de estas dos etapas es una reacción de glucólisis. En condiciones anaeróbicas, se produce una reacción de glucólisis en la que la glucosa se convierte en piruvato:
glucosa → 2 piruvato
Hay una producción neta de 2 moléculas de ATP y 2 de NADH por cada molécula de glucosa convertida. El ATP se genera por fosforilación a nivel de sustrato. El NADH se forma a partir de la reducción del NAD.
En la segunda etapa, el piruvato producido por la glucólisis se convierte en uno o más productos finales mediante las siguientes reacciones. En cada caso, ambas moléculas de NADH generadas por la glucólisis se reoxidan a NAD+. Cada vía alternativa requiere una enzima clave diferente en E. coli. Después de que se forman cantidades variables de diferentes productos finales mediante estas vías, se secretan de la célula.
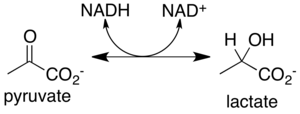
Formación lactante
El piruvato producido por la glucólisis se convierte en lactato. Esta reacción está catalizada por la enzima lactato deshidrogenasa (LDHA).
piruvato + NADH + H+ → lactato + NAD+
Formación de acetatos
El piruvato se convierte en acetil-coenzima A (acetil-CoA) por acción de la enzima piruvato deshidrogenasa. Esta acetil-CoA se convierte luego en acetato en E. coli, mientras se produce ATP por fosforilación a nivel de sustrato. La formación de acetato requiere dos enzimas: fosfato acetiltransferasa y acetato quinasa.

acetil-CoA + fosfato → acetil-fosfato + CoA
acetilfosfato + ADP → acetato + ATP
Formación de etanol
El etanol se forma en E. coli mediante la reducción de la acetil coenzima A con NADH. Esta reacción de dos pasos requiere la enzima alcohol deshidrogenasa (ADHE).
acetil-CoA + NADH + H+ → acetaldehído + NAD+ + CoA
acetaldehído + NADH + H+ → etanol + NAD+
Formate formation
El formato se produce por la escisión del piruvato. Esta reacción está catalizada por la enzima piruvato-formiato liasa (PFL), que desempeña un papel importante en la regulación de la fermentación anaeróbica en E. coli.
piruvato + CoA → acetil-CoA + formiato
Formación sucinta

El fosfoenolpiruvato (PEP), un intermediario de la vía de la glucólisis, es carboxilado por la enzima PEP carboxilasa para formar oxaloacetato. A esto le sigue la conversión del oxaloacetato en malato por la enzima malato deshidrogenasa. A continuación, la fumarato hidratasa cataliza la deshidratación del malato para producir fumarato.
fosfoenolpiruvato + HCO3 → oxaloacetato + fosfato
oxaloacetato + NADH + H+ → malato + NAD+
malato → fumarato + H2O
La reacción final en la formación del succinato es la reducción del fumarato. Está catalizada por la enzima fumarato reductasa.
fumarato + NADH + H+ → succinato + NAD+
Esta reducción es una reacción de respiración anaeróbica en E. coli, ya que utiliza electrones asociados con la NADH deshidrogenasa y la cadena de transporte de electrones. El ATP se genera mediante un gradiente electroquímico y la ATP sintasa. Este es el único caso en la vía de fermentación ácida mixta en el que el ATP no se produce mediante fosforilación a nivel de sustrato.
La vitamina K2, también conocida como menaquinona, es muy importante para el transporte de electrones al fumarato en E. coli.
Formación de hidrógeno y dióxido de carbono
El formato se puede convertir en gas hidrógeno y dióxido de carbono en E. coli. Esta reacción requiere la enzima formato-hidrógeno liasa. Se puede utilizar para evitar que las condiciones dentro de la célula se vuelvan demasiado ácidas.
Formiato → H2 y CO2
Prueba de metil rojo

La prueba del rojo de metilo (MR) puede detectar si se produce la vía de fermentación ácida mixta en los microbios cuando se les administra glucosa. Se utiliza un indicador de pH que tiñe de rojo la solución de prueba si el pH cae por debajo de 4,4. Si se ha producido la vía de fermentación, la mezcla de ácidos que ha producido hará que la solución sea muy ácida y provocará un cambio de color rojo.
La prueba del rojo de metilo pertenece a un grupo conocido como pruebas IMViC.
Ingeniería metabólica
Se han modificado metabólicamente múltiples cepas bacterianas para aumentar los rendimientos individuales de los productos finales formados por la fermentación ácida mixta. Por ejemplo, se han desarrollado cepas para aumentar la producción de etanol, lactato, succinato y acetato debido a la utilidad de estos productos en la biotecnología. El principal factor limitante para esta modificación es la necesidad de mantener un equilibrio redox en la mezcla de ácidos producida por la vía de fermentación.
Para la producción de etanol


Para la producción de acetato
La cepa W3110 de E. coli fue modificada genéticamente para generar 2 moles de acetato por cada mol de glucosa que pasa por fermentación. Esto se conoce como vía del homoacetato.
Para producción lactada
El lactato se puede utilizar para producir un bioplástico llamado ácido poliláctico (PLA). Las propiedades del PLA dependen de la proporción de los dos isómeros ópticos del lactato (D-lactato y L-lactato). El D-lactato se produce mediante fermentación ácida mixta en E. coli. Los primeros experimentos diseñaron la cepa RR1 de E. coli para que produjera uno de los dos isómeros ópticos del lactato.
Experimentos posteriores modificaron la cepa KO11 de E. coli, desarrollada originalmente para mejorar la producción de etanol. Los científicos lograron aumentar el rendimiento de D-lactato de la fermentación realizando varias eliminaciones.
Para producción sucinta
El aumento del rendimiento de succinato a partir de la fermentación ácida mixta se realizó primero sobreexpresando la enzima PEP carboxilasa. Esto produjo un rendimiento de succinato que fue aproximadamente tres veces mayor que lo normal. Se han realizado varios experimentos con un enfoque similar.
Se han utilizado métodos alternativos para alterar el equilibrio redox y de ATP a fin de optimizar el rendimiento de succinato.
Pautas de fermentación relacionadas
Existen otras vías de fermentación que se dan en los microbios. Todas estas vías comienzan con la conversión de piruvato, pero sus productos finales y las enzimas clave que requieren son diferentes. Estas vías incluyen:
- fermentación de etanol
- fermentación de ácido láctico
- fermentación de ácido propiónico
- Fermentación de butanol
- fermentación butanediol
Enlaces externos
- fermentación de ácido mixto
- EcoCyc Resumen de Fermentación
Referencias
- ^ a b c d e f g h Keseler, Ingrid M.; et al. (2011). "EcoCyc: una base de datos completa de la biología Escherichia coli". Nucleic Acids Research. 39 (Problema de datos): D583-D590. doi:10.1093/nar/gkq1143. PMC 3013716. PMID 21097882.
- ^ a b c d Förster, Andreas H. " Johannes Gescher (2014). "Ingeniería metabólica de Escherichia coli para la producción de productos finales de fermentación mixta-ácido". Fronteras en Bioingeniería y Biotecnología. 2: 506-508. doi:10.3389/fbioe.2014.00016. PMC 4126452. PMID 25152889.
- ^ M.Magidan " J. Martinko (2006). "Brock's Biology of Microorganisms, NJ, Pearson Prentice Hall". 11: 352.
{{cite journal}}: Cite journal requires|journal=(Ayuda) - ^ a b Sharma, P.D. (2007). "Microbiología": 104.
{{cite journal}}: Cite journal requires|journal=(Ayuda) - ^ Farrell, Alexander E.; et al. (2006). "El etanol puede contribuir a objetivos energéticos y ambientales". Ciencia. 311 (5760): 506-508. Bibcode:2006...311..506F. doi:10.1126/science.1121416. PMID 16439656. S2CID 16061891.
- ^ Hosmer, Jennifer; Nasreen, Marufa; Dhouib, Rabeb; Essilfie, Ama-Tawiah; Schirra, Horst Joachim; Henningham, Anna; Fantino, Emmanuelle; Sly, Peter; McEwan, Alastair G.; Kappler, Ulrike (2022-01-27). "El acceso a sustratos de crecimiento altamente especializados y la producción de metabolitos epiteliales inmunomoduladores determinan la supervivencia de la gripe hemofílica en las células epiteliales de la vía aérea humana". PLOS Patógenos. 18 (1): e1010209. doi:10.1371/journal.ppat.1010209. ISSN 1553-7374. PMC 8794153. PMID 35085362.
- ^ Sawers, R. Gary; Blokesch, Melanie; Böck, agosto (2004). "Anaerobic formate and hydro metabolism". EcoSal Plus. 1 (1). doi:10.1128/ecosalplus.3.5.4. PMID 26443350.
- ^ Knappe, Joachim " Gary Sawers (1990). "Una ruta radical-química acetyl-CoA: el sistema anaerobicamente inducido de piruvato formate-lyase de Escherichia coli". FEMS Microbiología Reseñas. 6 (4): 383-398. doi:10.1111/j.1574-6968.1990.tb04108.x. PMID 2248795.
- ^ Kai, Yasushi, Hiroyoshi Matsumura y Katsura Izui (2003). "Phosphoenolpyruvate carboxylase: estructura tridimensional y mecanismos moleculares". Archivos de Bioquímica y Biofísica. 414 (2): 170–179. doi:10.1016/S0003-9861(03)00170-X. PMID 12781768.
{{cite journal}}: CS1 maint: múltiples nombres: lista de autores (link) - ^ Thakker, Chandresh; et al. (2012). "Producción de esquirichia coli". Biotechnology Journal. 7 (2): 213–224. doi:10.1002/biot.201100061. PMC 3517001. PMID 21932253.
- ^ Invitado, JOHN R (1977). " Biosíntesis de menaquinona: mutantes de Escherichia coli K-12 que requieren 2-succinylbenzoate". Journal of Bacteriology. 130 (3): 1038-1046. doi:10.1128/jb.130.3.1038-1046.1977. PMC 235325. PMID 324971.
- ^ H. T. Clarke; W. R. Kirner (1922). "Metil Rojo". Org. Synth. 2: 47. doi:10.15227/orgsyn.002.0047.
- ^ van Hoek; Milan JA & Roeland MH Merks (2012). "El balance redox es clave para explicar el cambio parcial completo al metabolismo de bajo rendimiento". BMC Systems Biology. 6 1): 22. doi:10.1186/1752-0509-6-22. PMC 3384451. PMID 22443685.
- ^ Ingram, L. O.; et al. (1987). "Ingeniería genética de producción de etanol en Escherichia coli". Microbiología aplicada y ambiental. 53 (10): 2420–2425. Bibcode:1987ApEnM..53.2420I. doi:10.1128/aem.53.10.2420-2425.1987. PMC 204123. PMID 3322191.
- ^ Ohta, Kazuyoshi; et al. (1991). "Mejoramiento genético de Escherichia coli para la producción de etanol: integración cromosómica de los genes Zymomonas mobilis encoding pyruvate decarboxylase y alcohol deshidrogenase II". Microbiología aplicada y ambiental. 57 (4): 893–900. Código:1991ApEnM.57..893O. doi:10.1128/aem.57.4.893-900.1991. PMC 182819. PMID 2059047.
- ^ Turner, Peter C.; et al. (2012). "La cartografía óptica y secuenciación del genoma Escherichia coli KO11 revelan extensas reorganizaciones cromosómicas y múltiples copias tándem de los genes Zymomonas mobilis pdc y adhB". Journal of Industrial Microbiology " Biotechnology. 39 (4): 629-639. doi:10.1007/s10295-011-1052-2. PMID 22075923. S2CID 15100287.
- ^ Causey, T. B.; et al. (2003). "Engineering the metabolism of Escherichia coli W3110 for the conversion of sugar to redox-neutral and oxidized products: homoacetate production". Actas de la Academia Nacional de Ciencias. 100 (3): 825-832. Código de la Biblia: 2003 PNAS..100..825C. doi:10.1073/pnas.0337684100. PMC 298686. PMID 12556564.
- ^ Clark, David P (1989). "Las vías de fermentación de Escherichia coli". FEMS Microbiología Reseñas. 5 (3): 223–234. doi:10.1111/j.1574-6968..tb03398.x. PMID 2698228.
- ^ Chang, Dong-Eun; et al. (1999). "Producción Homofermentativa de d-orl-lactate en Escherichia coli RR1 metabólicamente diseñada". Microbiología aplicada y ambiental. 65 (4): 1384–1389. Bibcode:1999ApEnM..65.1384C. doi:10.1128/AEM.65.4.1384-1389.1999. PMC 91196. PMID 10103226.
- ^ Zhou, S.; et al. (2005). "Fermentación de 10%(w/v) de azúcar a D (−)-lactate por ingeniería Escherichia coli B". Biotechnology Letters. 27 (23–24): 1891–1896. doi:10.1007/s10529-005-3899-7. PMID 16328986. S2CID 43204090.
- ^ Millard, Cynthia Sanville; et al. (1996). "Producción mejorada de ácido sucinco por sobreexpresión de fosfoenolpyruvate carboxylase en Escherichia coli". Microbiología aplicada y ambiental. 62 (5): 1808-1810. Código:1996ApEnM..62.1808M. doi:10.1128/aem.62.5.1808-1810.1996. PMC 167956. PMID 8633880.
- ^ Singh, Amarjeet; et al. (2011). "Manipulación de redox y equilibrio ATP para mejorar la producción de sucinado en E. coli". Ingeniería metabólica. 13 (1): 76–81. doi:10.1016/j.ymben.2010.10.006. PMID 21040799.