Fenoles
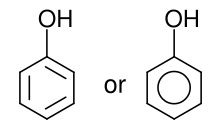
En química orgánica, los fenoles, a veces llamados fenólicos, son una clase de compuestos químicos que consisten en uno o más grupos hidroxilo (-OH) unidos directamente a un hidrocarburo aromático. grupo. El más simple es el fenol, C
6H
5OH. Los compuestos fenólicos se clasifican como fenoles simples o polifenoles según el número de unidades de fenol en la molécula.
Los fenoles se sintetizan industrialmente y son producidos por plantas y microorganismos.
Propiedades
Acidez
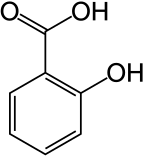
Los fenoles son más ácidos que los alcoholes típicos. La acidez del grupo hidroxilo de los fenoles suele ser intermedia entre la de los alcoholes alifáticos y los ácidos carboxílicos (su pKa suele estar entre 10 y 12). La desprotonación de un fenol forma un correspondiente ion fenolato o ion fenóxido negativo, y las sales correspondientes se denominan fenolatos o fenóxidos (arilóxidos según el Libro de Oro de la IUPAC).
Condensación con aldehídos y cetonas
Los fenoles son susceptibles a las sustituciones aromáticas electrófilas. La condensación con formaldehído da materiales resinosos, la famosa baquelita.
Otra sustitución aromática electrófila a escala industrial es la producción de bisfenol A, que se produce por condensación con acetona.
C-Alquilación con alquenos
El fenol se alquila fácilmente en las posiciones orto utilizando alquenos en presencia de un ácido de Lewis como el fenóxido de aluminio:
- CH2= CR2 + C6H5OH → R2CHCH2-2-C6H4Oh.
Más de 100.000 toneladas de terc-butilfenoles se producen anualmente (año: 2000) de esta forma, utilizando isobutileno (CH2=CMe2) como agente alquilante. agente. Especialmente importante es el 2,6-diterc-butilfenol, un antioxidante versátil.
Otras reacciones
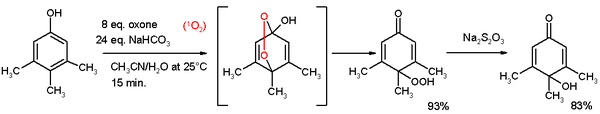
Los fenoles sufren esterificación. Los ésteres de fenol son ésteres activos, siendo propensos a la hidrólisis. Los fenoles son especies reactivas hacia la oxidación. Desdoblamiento oxidativo, por ejemplo, desdoblamiento de 1,2-dihidroxibenceno al monometiléster de ácido 2,4 hexadienodioico con oxígeno, cloruro de cobre en piridina Desaromatización oxidativa a quinonas también conocida como reacción de Teuber. y oxona. En la reacción que se muestra a continuación, el 3,4,5-trimetilfenol reacciona con el oxígeno singulete generado a partir de oxona/carbonato de sodio en una mezcla de acetonitrilo/agua a un para-peroxiquinol. Este hidroperóxido se reduce a quinol con tiosulfato de sodio.
Los fenoles se oxidan a hidroquinonas en la oxidación del persulfato de Elbs.
Reacción de naftoles e hidrazinas y bisulfito de sodio en la síntesis de carbazol de Bucherer.
Síntesis
Muchos fenoles de interés comercial se preparan por elaboración de fenol o cresoles. Por lo general, se producen mediante la alquilación de benceno/tolueno con propileno para formar cumeno y luego O
2 se agrega con H
2SO
4 para formar fenol (proceso Hock). Además de las reacciones anteriores, muchas otras reacciones más especializadas producen fenoles:
- reorganización de esteres en la reorganización de Fries
- reorganización de N-fenilhidroxilaminas en la reorganización de Bamberger
- trato de éteres fenólicos
- reducción de los quinones
- sustitución de una amina aromática por un grupo hidroxil con agua y bisulfido sodio en la reacción de Bucherer
- descomposición térmica de sales de aryl diazonium, las sales se convierten a fenol
- por la oxidación de silanes aryl: una variación aromática de la oxidación Fleming-Tamao
- síntesis catalítica de bromides de aryl e iodidos utilizando óxido nitroso
Clasificación
Existen varios esquemas de clasificación. Un esquema de uso común se basa en el número de carbonos y fue ideado por Jeffrey Harborne y Simmonds en 1964 y publicado en 1980:
| Phenol | el compuesto padre, utilizado como desinfectante y para síntesis química |
| Bisphenol A | y otras galletas producidas de cetonas y fenoles / cresol |
| BHT | (hidroxitolueno butilado) - un antioxidante liposoluble y aditivo alimenticio |
| 4-Nonylphenol | un producto de degradación de detergentes y nonoxynol-9 |
| Orthophenyl phenol | un fungicida usado para depilar frutas cítricas |
| Ácido picante | (trinitrophenol) - un material explosivo |
| Phenolphthalein | p Indicador H |
| Xylenol | utilizados en antisépticos " desinfectantes " |
Fármacos y productos naturales bioactivos
| tirolina | uno de los 20 aminoácidos estándar |
| L-DOPA | medicamento de dopamina usado para tratar la enfermedad de Parkinson |
| propofol | agente anestésico intravenoso de acción corta |
| vitamina K hydroquinone | agente de sangre que convierte |
| levothyroxina (L-thyroxina) | Medicamento de venta superior para tratar la deficiencia de hormona tiroidea. |
| amoxicillina | Antibiótico de venta superior |
| estradiol | la mayor hormona sexual femenina |
Contenido relacionado
Aldosa
Dimetilhidrazina asimétrica
Splenda