Factor de crecimiento vascular endotelial
Factor de crecimiento endotelial vascular ()VEGF,), originalmente conocido como Factor de permeabilidad vascular ()VPF), es una proteína de señal producida por muchas células que estimula la formación de vasos sanguíneos. Para ser específico, el VEGF es una sub-familia de factores de crecimiento, la familia de factores de crecimiento derivado de plaquetas de factores de crecimiento de los citos. Son proteínas de señalización importantes involucradas en la vasculogénesis (la de novo formación del sistema circulatorio embrionario) y angiogénesis (el crecimiento de los vasos sanguíneos de la vasculatura preexistente).
Es parte del sistema que restablece el suministro de oxígeno a los tejidos cuando la circulación sanguínea es inadecuada, como en condiciones hipóxicas. La concentración sérica de VEGF es alta en el asma bronquial y la diabetes mellitus. La función normal del VEGF es crear nuevos vasos sanguíneos durante el desarrollo embrionario, nuevos vasos sanguíneos después de una lesión, músculos después del ejercicio y nuevos vasos (circulación colateral) para evitar los vasos bloqueados. Puede contribuir a la enfermedad. Los cánceres sólidos no pueden crecer más allá de un tamaño limitado sin un suministro de sangre adecuado; Los cánceres que pueden expresar VEGF pueden crecer y metastatizar. La sobreexpresión de VEGF puede causar enfermedades vasculares en la retina del ojo y otras partes del cuerpo. Fármacos como aflibercept, bevacizumab, ranibizumab y pegaptanib pueden inhibir el VEGF y controlar o retardar esas enfermedades.
Historia
En 1970, Judah Folkman et al. describieron un factor secretado por los tumores que causaba la angiogénesis y lo denominaron factor de angiogénesis tumoral. En 1983, Senger et al. identificaron un factor de permeabilidad vascular secretado por tumores en cobayas y hámsteres. En 1989, Ferrara y Henzel describieron un factor idéntico en células foliculares de la hipófisis bovina que purificaron, clonaron y denominaron VEGF. Tischer et al. descubrió un empalme alternativo de VEGF similar en 1991. Entre 1996 y 1997, Christinger y De Vos obtuvieron la estructura cristalina de VEGF, primero con una resolución de 2,5 Å y luego con 1,9 Å.
Ferrara et al. demostró en 1992 que la tirosina quinasa-1 similar a Fms (flt-1) era un receptor de VEGF. Se demostró que el receptor de dominio de inserción de quinasa (KDR) era un Receptor de VEGF por Terman et al. en 1992 también. En 1998, se demostró que la neuropilina 1 y la neuropilina 2 actúan como receptores de VEGF.
Clasificación

En los mamíferos, la familia VEGF comprende cinco miembros: VEGF-A, factor de crecimiento placentario (PGF), VEGF-B, VEGF-C y VEGF-D. Estos últimos miembros fueron descubiertos después de VEGF-A; Antes de su descubrimiento, VEGF-A se conocía como VEGF. También se han descubierto varias proteínas relacionadas con el VEGF codificadas por virus (VEGF-E) y en el veneno de algunas serpientes (VEGF-F).
| Tipo | Función |
|---|---|
| VEGF-A |
|
| VEGF-B | Angiogénesis embrionaria (tejido miocardial, para ser específico) |
| VEGF-C | Lymphangiogenesis |
| VEGF-D | Necesidad para el desarrollo de la vasculatura linfática alrededor de bronquiolos pulmonares |
| PlGF | Importante para Vasculogénesis, También se necesita para la angiogénesis durante la isquemia, inflamación, curación de heridas y cáncer. |
La actividad de VEGF-A, como su nombre implica, ha sido estudiada principalmente en las células del endotelio vascular, aunque tiene efectos en varios otros tipos de células (por ejemplo, la estimulación de monocitos/migraciones de tumores, neuronas, células cancerosas, células epiteliales renales). In vitro, VEGF-A ha demostrado estimular la mitogenesis celular endotelial y la migración celular. VEGF-A es también un vasodilatador y aumenta la permeabilidad microvascular y originalmente se denomina factor de permeabilidad vascular.
Isoformas

Existen múltiples isoformas de VEGF-A que resultan del corte y empalme alternativo del ARNm de un único gen VEGFA de 8 exones. Estos se clasifican en dos grupos a los que se hace referencia según el sitio de empalme del exón terminal (exón 8): el sitio de empalme proximal (denominado VEGFxxx) o el sitio de empalme distal (VEGFxxx). sub>b). Además, el corte y empalme alternativo de los exones 6 y 7 altera su afinidad de unión a heparina y su número de aminoácidos (en humanos: VEGF121, VEGF121b, VEGF145 , VEGF165, VEGF165b, VEGF189, VEGF206; los ortólogos de roedores de estas proteínas contienen un aminoácido menos). Estos dominios tienen importantes consecuencias funcionales para las variantes de empalme de VEGF, ya que el sitio de empalme terminal (exón 8) determina si las proteínas son proangiogénicas (sitio de empalme proximal, expresado durante la angiogénesis) o antiangiogénicas (sitio de empalme distal, expresado en condiciones normales). tejidos). Además, la inclusión o exclusión de los exones 6 y 7 median las interacciones con los proteoglicanos de heparán sulfato (HSPG) y los correceptores de neuropilina en la superficie celular, mejorando su capacidad para unirse y activar los receptores de VEGF (VEGFR). Recientemente, se ha demostrado que VEGF-C es un importante inductor de la neurogénesis en la zona subventricular murina, sin ejercer efectos angiogénicos.
Mecanismo
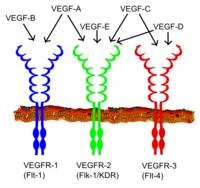
Todos los miembros de la familia VEGF estimulan las respuestas celulares uniéndose a los receptores de tirosina quinasa (los VEGFR) en la superficie celular, lo que hace que se dimericen y se activen mediante la transfosforilación, aunque en diferentes sitios, tiempos y grados. Los receptores de VEGF tienen una porción extracelular que consta de siete dominios similares a inmunoglobulinas, una única región transmembrana y una porción intracelular que contiene un dominio de tirosina-quinasa dividido. VEGF-A se une a VEGFR-1 (Flt-1) y VEGFR-2 (KDR/Flk-1). VEGFR-2 parece mediar en casi todas las respuestas celulares conocidas al VEGF. La función de VEGFR-1 está menos definida, aunque se cree que modula la señalización de VEGFR-2. Otra función de VEGFR-1 puede ser actuar como un receptor simulado/señuelo, secuestrando el VEGF de la unión de VEGFR-2 (esto parece ser particularmente importante durante la vasculogénesis en el embrión). VEGF-C y VEGF-D, pero no VEGF-A, son ligandos para un tercer receptor (VEGFR-3/Flt4), que media en la linfangiogénesis. El receptor (VEGFR3) es el sitio de unión de los ligandos principales (VEGFC y VEGFD), que media la acción perpetua y la función de los ligandos en células diana. El factor de crecimiento endotelial vascular C puede estimular la linfangiogénesis (a través de VEGFR3) y la angiogénesis a través de VEGFR2. El factor de crecimiento endotelial vascular R3 se ha detectado en células endoteliales linfáticas en CL de muchas especies, bovinos, búfalos y primates.
Además de unirse a los VEGFR, el VEGF se une a complejos receptores que consisten tanto en neuropilinas como en VEGFR. Este complejo receptor ha aumentado la actividad de señalización de VEGF en las células endoteliales (vasos sanguíneos). Las neuropilinas (NRP) son receptores pleiotrópicos y, por tanto, otras moléculas pueden interferir con la señalización de los complejos receptores NRP/VEGFR. Por ejemplo, las semaforinas de Clase 3 compiten con VEGF165 por la unión a NRP y, por lo tanto, podrían regular la angiogénesis mediada por VEGF.
Expresión
La producción de VEGF-A se puede inducir en una célula que no recibe suficiente oxígeno. Cuando una célula tiene deficiencia de oxígeno, produce HIF, factor inducible por hipoxia, un factor de transcripción. HIF estimula la liberación de VEGF-A, entre otras funciones (incluida la modulación de la eritropoyesis). El VEGF-A circulante luego se une a los receptores de VEGF en las células endoteliales, lo que desencadena una vía de tirosina quinasa que conduce a la angiogénesis. La expresión de angiopoyetina-2 en ausencia de VEGF conduce a la muerte de las células endoteliales y a la regresión vascular. Por el contrario, un estudio alemán realizado in vivo encontró que las concentraciones de VEGF en realidad disminuyeron después de una reducción del 25 % en la ingesta de oxígeno durante 30 minutos. HIF1 alfa y HIF1 beta se producen constantemente, pero HIF1 alfa es altamente lábil O2, por lo que, en condiciones aeróbicas, se degrada. Cuando la célula se vuelve hipóxica, HIF1 alfa persiste y el complejo HIF1 alfa/beta estimula la liberación de VEGF. el uso combinado de microvesículas y 5-FU dio como resultado una mayor quimiosensibilidad de las células del carcinoma de células escamosas más que el uso de 5-FU o microvesículas solos. Además, la regulación negativa de la expresión del gen VEGF se asoció con una disminución de la expresión del gen CD1.
Importancia clínica
En enfermedad
VEGF-A y los receptores correspondientes se regulan rápidamente después de una lesión traumática del sistema nervioso central (SNC). VEGF-A se expresa altamente en las etapas aguda y subaguda de la lesión del SNC, pero la expresión de la proteína disminuye con el tiempo. Este período de expresión de VEGF-A se corresponde con la capacidad de revascularización endógena después de la lesión. Esto sugeriría que VEGF-A/VEGF165 podría usarse como objetivo para promover la angiogénesis después de lesiones traumáticas del SNC. Sin embargo, existen informes científicos contradictorios sobre los efectos de los tratamientos con VEGF-A en modelos de lesión del SNC.
Aunque no se ha asociado como biomarcador para el diagnóstico de ictus isquémico agudo, si niveles elevados de VEGF en suero en las primeras 48 horas se han asociado con mal pronóstico en infartos cerebrales mayores de 6 meses y 2 años.
VEGF-A se ha relacionado con un mal pronóstico en el cáncer de mama. Numerosos estudios muestran una disminución de la supervivencia general y de la supervivencia libre de enfermedad en aquellos tumores que sobreexpresan VEGF. La sobreexpresión de VEGF-A puede ser un paso temprano en el proceso de metástasis, un paso que está involucrado en la función "angiogénica" cambiar. Aunque VEGF-A se ha correlacionado con una supervivencia deficiente, su mecanismo de acción exacto en la progresión de los tumores aún no está claro.
VEGF-A también se libera en la artritis reumatoide en respuesta al TNF-α, lo que aumenta la permeabilidad y la inflamación endotelial y también estimula la angiogénesis (formación de capilares).
VEGF-A también es importante en la retinopatía diabética (RD). Los problemas microcirculatorios en la retina de las personas con diabetes pueden causar isquemia retiniana, lo que resulta en la liberación de VEGF-A y un cambio en el equilibrio de las isoformas proangiogénicas de VEGFxxx respecto del VEGF expresado normalmente. Isoformas xxxb. VEGFxxx puede provocar la creación de nuevos vasos sanguíneos en la retina y en otras partes del ojo, presagiando cambios que pueden amenazar la vista.
VEGF-A desempeña un papel en la patología de la degeneración macular asociada a la edad (DMAE) de forma húmeda, que es la principal causa de ceguera entre las personas mayores del mundo industrializado. La patología vascular de la DMAE comparte ciertas similitudes con la retinopatía diabética, aunque la causa de la enfermedad y la fuente típica de neovascularización difieren entre las dos enfermedades.
Los niveles séricos de VEGF-D están significativamente elevados en pacientes con angiosarcoma.
Una vez liberado, VEGF-A puede provocar varias respuestas. Puede hacer que una célula sobreviva, se mueva o se diferencie aún más. Por tanto, VEGF es un objetivo potencial para el tratamiento del cáncer. El primer fármaco anti-VEGF, un anticuerpo monoclonal llamado bevacizumab, se aprobó en 2004. Aproximadamente entre 10 y 15% de los pacientes se benefician del tratamiento con bevacizumab; sin embargo, aún no se conocen los biomarcadores de la eficacia de bevacizumab.
Los estudios actuales muestran que los VEGF no son los únicos promotores de la angiogénesis. En particular, FGF2 y HGF son potentes factores angiogénicos.
Se ha descubierto que los pacientes que padecen enfisema pulmonar tienen niveles reducidos de VEGF en las arterias pulmonares.
También se ha demostrado que VEGF-D está sobreexpresado en la linfangioleiomiomatosis y actualmente se utiliza como biomarcador de diagnóstico en el tratamiento de esta rara enfermedad.
En el riñón, el aumento de la expresión de VEGF-A en los glomérulos causa directamente la hipertrofia glomerular que se asocia con la proteinuria.
Las alteraciones del VEGF pueden predecir la preeclampsia de aparición temprana.
Las terapias génicas para la angina refractaria establecen la expresión de VEGF en las células epicárdicas para promover la angiogénesis.