Estreptococo
Streptococcus es un género de cocos (plural cocos) o bacteria esférica que pertenece a la familia Streptococcaceae, dentro del orden Lactobacillales (bacterias del ácido láctico), en el filo Bacillota. La división celular en los estreptococos ocurre a lo largo de un solo eje, por lo que, a medida que crecen, tienden a formar pares o cadenas que pueden parecer dobladas o retorcidas. Esto difiere de los estafilococos, que se dividen a lo largo de múltiples ejes, generando así grupos de células irregulares, similares a uvas. La mayoría de los estreptococos son oxidasa negativos y catalasa negativos, y muchos son anaerobios facultativos (capaces de crecer tanto aeróbicamente como anaeróbicamente).
El término fue acuñado en 1877 por el cirujano vienés Albert Theodor Billroth (1829–1894), al combinar el prefijo "strepto-" (del griego antiguo: στρεπτός, romanizado: streptós, lit. 'fácilmente torcido, flexible'), junto con el sufijo "-coccus" (del latín moderno: coccus, del griego antiguo: κόκκος, romanizado: kókkos, lit. 'grano, semilla, baya'). En 1984, muchas bacterias anteriormente agrupadas en el género Streptococcus se separaron en los géneros Enterococcus y Lactococcus. Actualmente, se reconocen más de 50 especies en este género. Se ha descubierto que este género es parte del microbioma salival.
Patogénesis y clasificación
Además de la faringitis estreptocócica (faringitis estreptocócica), ciertas especies de Streptococcus son responsables de muchos casos de conjuntivitis, meningitis, neumonía bacteriana, endocarditis, erisipela y fascitis necrosante (la ' infecciones bacterianas carnívoras). Sin embargo, muchas especies de estreptococos no son patógenas y forman parte de la microbiota humana comensal de la boca, la piel, el intestino y el tracto respiratorio superior. Los estreptococos también son un ingrediente necesario en la producción de queso emmental ("suizo").
Las especies de Streptococcus se clasifican según sus propiedades hemolíticas. Las especies alfa-hemolíticas causan la oxidación del hierro en las moléculas de hemoglobina dentro de los glóbulos rojos, dándole un color verdoso en el agar sangre. Las especies beta-hemolíticas causan la ruptura completa de los glóbulos rojos. En agar sangre, esto aparece como amplias áreas libres de células sanguíneas que rodean las colonias bacterianas. Las especies gamma-hemolíticas no causan hemólisis.
Los estreptococos beta-hemolíticos se clasifican además por el agrupamiento de Lancefield, una clasificación de serotipo (es decir, que describe carbohidratos específicos presentes en la pared celular bacteriana). Los 21 serotipos descritos se denominan grupos de Lancefield A a W (excluyendo I y J). Este sistema de clasificación fue desarrollado por Rebecca Lancefield, científica de la Universidad Rockefeller.
En el ámbito médico, los grupos más importantes son los estreptococos alfa-hemolíticos S. pneumoniae y Streptococcus viridans grupo, y los estreptococos beta-hemolíticos de los grupos A y B de Lancefield (también conocidos como “estreptococo del grupo A” y “estreptococo del grupo B ”).
Tabla: Estreptococos médicamente relevantes (no todos son alfa-hemolíticos)
| Especies | Host | Enfermedad |
| S. pyogenes | humanos | faringitis, celulitis, erisipelas |
| S. agalactiae | humanos, ganado | meningitis neonatal y sepsis |
| S. dysgalactiae | humanos, animales | endocarditis, bacteremia, neumonía, meningitis, infecciones respiratorias |
| S. gallyticus | humanos, animales | Infecciones del tracto biliar o urinario, endocarditis |
| S. anginosus | humanos, animales | abscesos subcutáneos/organ, meningitis, infecciones respiratorias |
| S. sanguinis | humanos | endocarditis, caries dentales |
| S. suis | cerdo | meningitis |
| S. mitis | humanos | endocarditis |
| S. mutans | humanos | caries dentales |
| S. pneumoniae | humanos | neumonía |
Alfa-hemolítico
Cuando hay alfa-hemólisis (α-hemólisis), el agar debajo de la colonia aparecerá oscuro y verdoso debido a la conversión de la hemoglobina en biliverdina verde. Streptococcus pneumoniae y un grupo de estreptococos orales (Streptococcus viridans o estreptococos viridans) presentan hemólisis alfa. La hemólisis alfa también se denomina hemólisis incompleta o hemólisis parcial porque las membranas celulares de los glóbulos rojos se dejan intactas. Esto también se denomina a veces hemólisis verde debido al cambio de color en el agar.
Neumococos
- S. pneumoniae (a veces llamada neumococo), es una causa principal de neumonía bacteriana y etiología ocasional de los medios de otitis, sinusitis, meningitis y peritonitis. Se cree que la inflamación es la principal causa de cómo la neumococci causa la enfermedad, por lo que la tendencia de los diagnósticos asociados con ellos a involucrar la inflamación. No poseen antígenos Lancefield.
El grupo viridans: alfa-hemolítico
- Los viridans streptococci son un gran grupo de bacterias comunales que son alfa-hemolíticas, produciendo una coloración verde en placas de agar de sangre (de ahí el nombre "viridans", de latín vdesignardis, verde), o no hemolítica. No poseen antígenos Lancefield.
Beta-hemolítico
La beta-hemólisis (β-hemólisis), a veces llamada hemólisis completa, es una lisis completa de los glóbulos rojos en el medio alrededor y debajo de las colonias: el área aparece más clara (amarilla) y transparente. La estreptolisina, una exotoxina, es la enzima producida por la bacteria que provoca la lisis completa de los glóbulos rojos. Hay dos tipos de estreptolisina: estreptolisina O (SLO) y estreptolisina S (SLS). La estreptolisina O es una citotoxina sensible al oxígeno, secretada por la mayoría de los estreptococos del grupo A (GAS) e interactúa con el colesterol en la membrana de las células eucariotas (principalmente glóbulos rojos y blancos, macrófagos y plaquetas). y por lo general resulta en beta-hemólisis debajo de la superficie del agar sangre. La estreptolisina S es una citotoxina estable al oxígeno que también producen la mayoría de las cepas de GAS y que produce una limpieza en la superficie del agar sangre. El SLS afecta a las células inmunitarias, incluidos los leucocitos polimorfonucleares y los linfocitos, y se cree que evita que el sistema inmunitario del huésped elimine la infección. Streptococcus pyogenes, o GAS, presenta hemólisis beta.
Algunas especies débilmente beta-hemolíticas causan hemólisis intensa cuando se cultivan junto con una cepa de Staphylococcus. Esto se llama la prueba CAMP. Streptococcus agalactiae muestra esta propiedad. Clostridium perfringens puede identificarse presuntivamente con esta prueba. Listeria monocytogenes también es positivo en agar sangre de carnero.
Grupo A
Grupo A S. pyogenes es el agente causal de una amplia gama de infecciones por estreptococos del grupo A (GAS). Estas infecciones pueden ser no invasivas o invasivas. Las infecciones no invasivas tienden a ser más comunes y menos graves. Las más comunes de estas infecciones incluyen faringitis estreptocócica (faringitis estreptocócica) e impétigo. La escarlatina es otro ejemplo de infección no invasiva del Grupo A.
Las infecciones invasivas causadas por el estreptococo beta-hemolítico del grupo A tienden a ser más graves y menos comunes. Esto ocurre cuando la bacteria es capaz de infectar áreas donde normalmente no se encuentra, como la sangre y los órganos. Las enfermedades que pueden ser causadas incluyen síndrome de choque tóxico estreptocócico, fascitis necrosante, neumonía y bacteriemia. A nivel mundial, se ha estimado que el GAS causa más de 500 000 muertes cada año, lo que lo convierte en uno de los principales patógenos del mundo.
Los GAS pueden causar complicaciones adicionales, a saber, fiebre reumática aguda y glomerulonefritis aguda. La fiebre reumática, una enfermedad que afecta las articulaciones, los riñones y las válvulas cardíacas, es una consecuencia de una infección por estreptococo A no tratada que no es causada por la bacteria en sí, sino por los anticuerpos creados por el sistema inmunitario para combatir la infección que reaccionan de forma cruzada con otras proteínas en el cuerpo. Esta "reacción cruzada" hace que el cuerpo esencialmente se ataque a sí mismo y provoque el daño anterior. Se supone que un mecanismo autoinmune similar iniciado por la infección por estreptococos beta-hemolíticos del grupo A (GABHS, por sus siglas en inglés) causa trastornos neuropsiquiátricos autoinmunes pediátricos asociados con infecciones estreptocócicas (PANDAS), en los que los anticuerpos autoinmunes afectan los ganglios basales, provocando una aparición rápida de trastornos psiquiátricos, motores, del sueño, y otros síntomas en pacientes pediátricos.
La infección por GAS generalmente se diagnostica con una prueba rápida de estreptococo o por cultivo.
Grupo B
S. agalactiae, o estreptococo del grupo B, GBS, causa neumonía y meningitis en recién nacidos y ancianos, con bacteriemia sistémica ocasional. Es importante destacar que Streptococcus agalactiae es la causa más común de meningitis en bebés de un mes a tres meses de edad. También pueden colonizar los intestinos y el tracto reproductivo femenino, aumentando el riesgo de ruptura prematura de membranas durante el embarazo y la transmisión del organismo al bebé. El Colegio Estadounidense de Obstetras y Ginecólogos, la Academia Estadounidense de Pediatría y los Centros para el Control de Enfermedades recomiendan que todas las mujeres embarazadas entre las semanas 35 y 37 de gestación se hagan la prueba de GBS. Las mujeres con resultados positivos deben recibir antibióticos profilácticos durante el trabajo de parto, lo que generalmente evitará la transmisión al bebé.
El Reino Unido ha optado por adoptar un protocolo basado en factores de riesgo, en lugar del protocolo basado en la cultura seguido en los EE. UU. Las pautas actuales establecen que si uno o más de los siguientes factores de riesgo están presentes, entonces la mujer debe ser tratada con antibióticos intraparto:
- GBS bacteriuria durante este embarazo
- Historia de la enfermedad de GBS en un bebé anterior
- Fiebre intraparto (≥38 °C)
- Trabajo prematuro (Se realizaron 37 semanas)
- Rotura prolongada de membranas (> 18 horas)
Este protocolo da como resultado la administración de antibióticos intraparto al 15-20 % de las mujeres embarazadas y la prevención del 65-70 % de los casos de sepsis por EGB de aparición temprana.
Grupo C
Este grupo incluye S. equi, que provoca estrangulamientos en los caballos, y S. zooepidemicus—S. equi es un descendiente clonal o biovar del ancestral S. zooepidemicus—que causa infecciones en varias especies de mamíferos, incluyendo ganado y caballos. S. dysgalactiae subesp. dysgalactiae también es miembro del grupo C, estreptococos beta-hemolíticos que pueden causar faringitis y otras infecciones piógenas similares a los estreptococos del grupo A.
Grupo D (enterococos)
Muchos estreptococos del antiguo grupo D han sido reclasificados y colocados en el género Enterococcus (incluidos E. faecalis, E. faecium, E. durans, y E. avium). Por ejemplo, Streptococcus faecalis ahora es Enterococcus faecalis. E. faecalis es a veces alfa-hemolítico y E. faecium es a veces beta hemolítico.
Las cepas restantes del grupo D no enterocócicas incluyen Streptococcus gallolyticus, Streptococcus bovis, Streptococcus equinus y Streptococcus suis.
Los estreptococos no hemolíticos rara vez causan enfermedades. Sin embargo, los estreptococos beta-hemolíticos del grupo D débilmente hemolíticos y la Listeria monocytogenes (que en realidad es un bacilo grampositivo) no deben confundirse con los estreptococos no hemolíticos.
Estreptococos del grupo F
Los estreptococos del grupo F fueron descritos por primera vez en 1934 por Long y Bliss entre los "estreptococos hemolíticos diminutos". También se les conoce como Streptococcus anginosus (según el sistema de clasificación de Lancefield) o como miembros del grupo S. milleri (según el sistema europeo).
Estreptococos del grupo G
Estos estreptococos son por lo general, pero no exclusivamente, beta-hemolíticos. Streptococcus dysgalactiae subesp. canis es la subespecie predominante encontrada. Es un SGG particularmente común en humanos, aunque normalmente se encuentra en animales. S. phocae es una subespecie de GGS que se ha encontrado en especies de mamíferos marinos y peces marinos. En mamíferos marinos se ha asociado principalmente a meningoencefalitis, sepsis y endocarditis, pero también se asocia a muchas otras patologías. Su reservorio ambiental y medio de transmisión en mamíferos marinos no está bien caracterizado.
Estreptococos del grupo H
Los estreptococos del grupo H causan infecciones en caninos de tamaño mediano. Los estreptococos del grupo H rara vez causan enfermedades en humanos a menos que un humano tenga contacto directo con la boca de un canino. Una de las formas más comunes en que esto se puede propagar es el contacto boca a boca de humano a canino. Sin embargo, el canino puede lamer la mano del humano y la infección también se puede propagar.
Taxonomía molecular y filogenética
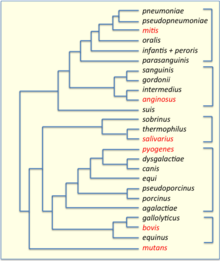
Los estreptococos se han dividido en seis grupos según sus secuencias de ADNr 16S: S. anginosus, S. gallolyticus, S. mitis, S. mutans, S. pyogenes y S. salivario. Los grupos 16S han sido confirmados por secuenciación del genoma completo (ver figura). Los patógenos importantes S. pneumoniae y S. pyogenes pertenecen al S. mitis y S. pyogenes, respectivamente, mientras que el agente causante de la caries dental, Streptococcus mutans, es basal al grupo Streptococcus.
Los avances tecnológicos recientes han resultado en un aumento de las secuencias genómicas disponibles para las especies de Streptococcus, lo que permite realizar análisis filogenéticos y genómicos comparativos más robustos y confiables. En 2018, Patel y Gupta volvieron a examinar las relaciones evolutivas dentro de Streptococcus a través del análisis de árboles filogenéticos integrales construidos en base a cuatro conjuntos de datos diferentes de proteínas y la identificación de 134 firmas moleculares altamente específicas (en el forma de indels característicos conservados) que son compartidos exclusivamente por todo el género o sus distintos subclades.
Los resultados revelaron la presencia de dos clados principales en el nivel más alto dentro de Streptococcus, denominados clados "Mitis-Suis" y "Pyogenes-Equinus-Mutans". El clado principal "Mitis-Suis" comprende el subclado Suis y el clado Mitis, que abarca los subclados Angiosus, Pneumoniae, Gordonii y Parasanguinis. El segundo clado principal, el "Pyogenes-Equinus-Mutans", incluye los subclados Pyogenes, Mutans, Salivarius, Equinus, Sobrinus, Halotolerans, Porci, Entericus y Orisratti. En total, se han identificado 14 subclades distintos dentro del género Streptococcus, cada uno respaldado por patrones de ramificación confiables en árboles filogenéticos y por la presencia de múltiples indeles característicos conservados en diferentes proteínas que son características distintivas de los miembros de estos 14 clados. En la figura de esta página se muestra un diagrama resumido que muestra las relaciones generales entre los Streptococcus basados en estos estudios.
Genómica
Se han secuenciado los genomas de cientos de especies. La mayoría de los genomas de Streptococcus tienen un tamaño de 1,8 a 2,3 Mb y codifican de 1700 a 2300 proteínas. En la tabla se enumeran algunos genomas importantes. Las cuatro especies que se muestran en la tabla (S. pyogenes, S. agalactiae, S. pneumoniae y S. mutans) tienen una identidad de secuencia de proteína por pares promedio de alrededor del 70 %..
| función | S. pyogenes | S. agalactiae | S. pneumoniae | S. mutans |
|---|---|---|---|---|
| pares base | 1,852,442 | 2,211,488 | 2.160.837 | 2.030.921 |
| ORFs | 1792 | 2118 | 2236 | 1963 |
| profages | Sí. | no | no | no |
Bacteriófago
Se han descrito bacteriófagos para muchas especies de Streptococcus. Se han descrito 18 profagos en S. pneumoniae que varían en tamaño de 38 a 41 kb, codificando de 42 a 66 genes cada uno. Algunos de los primeros fagos de Streptococcus descubiertos fueron Dp-1 y ω1 (alias ω-1). En 1981 se descubrió la familia Cp (fago 1 Complutense, oficialmente Streptococcus virus Cp1, Picovirinae) con Cp-1 como su primer miembro. Dp-1 y Cp-1 infectan ambos S. pneumoniae y S. mitis. Sin embargo, los rangos de huéspedes de la mayoría de los fagos Streptococcus no se han investigado sistemáticamente.
Transformación genética natural
La transformación genética natural implica la transferencia de ADN de una bacteria a otra a través del medio circundante. La transformación es un proceso complejo que depende de la expresión de numerosos genes. Para ser capaz de transformación, una bacteria debe entrar en un estado fisiológico especial denominado competencia. S. pneumoniae, S. mitis y S. oralis pueden volverse competentes y, como resultado, adquirir activamente ADN homólogo para su transformación mediante un mecanismo fratricida depredador. Este mecanismo fratricida explota principalmente a hermanos no competentes presentes en el mismo nicho. Entre aislados altamente competentes de S. pneumoniae, Li et al. mostró que la aptitud y la virulencia de la colonización nasal (infecciosidad pulmonar) dependen de un sistema de competencia intacto. La competencia puede permitir que el patógeno estreptocócico use ADN homólogo externo para la reparación recombinacional de daños en el ADN causados por el ataque oxidativo del huésped.
Contenido relacionado
Luciérnaga
Interferón
Lorisidae