Estereoquímica
La estereoquímica, una subdisciplina de la química, implica el estudio de la disposición espacial relativa de los átomos que forman la estructura de las moléculas y su manipulación. El estudio de la estereoquímica se centra en los estereoisómeros, que por definición tienen la misma fórmula molecular y secuencia de átomos enlazados (constitución), pero difieren en las orientaciones tridimensionales de sus átomos en el espacio. Por esta razón, también se conoce como química 3D: el prefijo "estéreo-" significa "tridimensionalidad".
Una rama importante de la estereoquímica es el estudio de las moléculas quirales. La estereoquímica abarca todo el espectro de la química orgánica, inorgánica, biológica, física y especialmente supramolecular. La estereoquímica incluye métodos para determinar y describir estas relaciones; el efecto sobre las propiedades físicas o biológicas que estas relaciones imparten a las moléculas en cuestión, y la manera en que estas relaciones influyen en la reactividad de las moléculas en cuestión (estereoquímica dinámica).
Historia
Louis Pasteur bien podría ser descrito como el primer estereoquímico, habiendo observado en 1842 que las sales de ácido tartárico recolectadas de los recipientes de producción de vino podían rotar el plano de la luz polarizada, pero que las sales de otras fuentes no lo hacían. Esta propiedad, la única propiedad física en la que se diferencian los dos tipos de sales de tartrato, se debe a la isomería óptica. En 1874, Jacobus Henricus van 't Hoff y Joseph Le Bel explicaron la actividad óptica en términos de la disposición tetraédrica de los átomos unidos al carbono. Kekulé usó modelos tetraédricos a principios de 1862, pero nunca los publicó; Emanuele Paternò probablemente los conocía, pero fue el primero en dibujar y discutir estructuras tridimensionales, como la del 1,2-dibromoetano en el Giornale di Scienze Naturali ed Economiche en 1869.Lord Kelvin introdujo el término "quiral" en 1904. Arthur Robertson Cushny, farmacólogo escocés, en 1908, ofreció por primera vez un ejemplo definitivo de una diferencia de bioactividad entre los enantiómeros de una molécula quiral, a saber. La (-)-adrenalina es dos veces más potente que la forma (±)- como vasoconstrictor y en 1926 sentó las bases de la farmacología quiral/estereofarmacología (relaciones biológicas de sustancias ópticamente isoméricas). Posteriormente, en 1966, se ideó la nomenclatura Cahn-Ingold-Prelog o la regla de secuencia para asignar una configuración absoluta al centro estereogénico/quiral (notación R y S) y se amplió para aplicarse a través de enlaces olefínicos (notación E y Z).
Significado
Las reglas de prioridad de Cahn-Ingold-Prelog son parte de un sistema para describir la estereoquímica de una molécula. Clasifican los átomos alrededor de un estereocentro de una manera estándar, lo que permite describir sin ambigüedades la posición relativa de estos átomos en la molécula. Una proyección de Fischer es una forma simplificada de representar la estereoquímica alrededor de un estereocentro.
Ejemplo de talidomida
Un ejemplo citado a menudo de la importancia de la estereoquímica se relaciona con el desastre de la talidomida. La talidomida es un fármaco, preparado por primera vez en 1957 en Alemania, prescrito para tratar las náuseas matutinas en mujeres embarazadas. Se descubrió que el fármaco es teratogénico, lo que causa un daño genético grave en el crecimiento y desarrollo embrionario temprano, lo que lleva a la deformación de las extremidades en los bebés. Algunos de los diversos mecanismos propuestos de teratogenicidad implican una función biológica diferente para los enantiómeros (R)- y (S)-talidomida. Sin embargo, en el cuerpo humano, la talidomida sufre una racemización: incluso si solo uno de los dos enantiómeros se administra como fármaco, el otro enantiómero se produce como resultado del metabolismo.En consecuencia, es incorrecto afirmar que un estereoisómero es seguro mientras que el otro es teratogénico. La talidomida se utiliza actualmente para el tratamiento de otras enfermedades, en particular el cáncer y la lepra. Se han habilitado estrictas regulaciones y controles para evitar su uso por mujeres embarazadas y prevenir deformaciones en el desarrollo. Este desastre fue la fuerza que impulsó la exigencia de pruebas estrictas de los medicamentos antes de ponerlos a disposición del público.
Definiciones
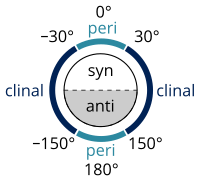
Existen muchas definiciones que describen un confórmero específico (Libro de oro de la IUPAC), desarrolladas por William Klyne y Vladimir Prelog, que constituyen su sistema de nomenclatura Klyne-Prelog:
- un ángulo de torsión de ±60° se llama gauche
- un ángulo de torsión entre 0° y ±90° se denomina sin (s)
- un ángulo de torsión entre ±90° y 180° se llama anti (a)
- un ángulo de torsión entre 30° y 150° o entre –30° y –150° se denomina clinal
- un ángulo de torsión entre 0° y 30° o 150° y 180° se llama periplanar (p)
- un ángulo de torsión entre 0° y 30° se denomina conformación sinperiplanar o sin o cis (sp)
- un ángulo de torsión entre 30° a 90° y –30° a –90° se llama sinclinal o torcido o sesgado (sc)
- un ángulo de torsión entre 90° a 150° y –90° a –150° se llama anticlinal (ac)
- un ángulo de torsión entre ±150° a 180° se denomina antiperiplanar o anti o trans (ap).
La deformación torsional resulta de la resistencia a la torsión alrededor de un enlace.
Tipos
- atropisomerismo
- Isomería cis - trans
- isomería conformacional
- diastereómeros
- enantiómeros
Contenido relacionado
Hidrato de clatrato
Reacción de adición
Hidrógeno