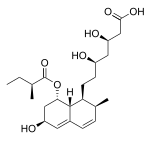
Estatina
Los transportadores de colesterol de lipoproteínas de baja densidad (LDL) desempeñan un papel clave en el desarrollo de la aterosclerosis y la enfermedad coronaria a través de los mecanismos descritos por la hipótesis de los lípidos. Las estatinas son efectivas para reducir el colesterol LDL y, por lo tanto, se usan ampliamente para la prevención primaria en personas con alto riesgo de enfermedad cardiovascular, así como en la prevención secundaria para quienes han desarrollado una enfermedad cardiovascular.
Los efectos secundarios de las estatinas incluyen dolor muscular, mayor riesgo de diabetes mellitus y niveles sanguíneos anormales de enzimas hepáticas. Además, tienen efectos adversos raros pero severos, particularmente daño muscular. Inhiben la enzima HMG-CoA reductasa que juega un papel central en la producción de colesterol. Los niveles altos de colesterol se han asociado con enfermedades cardiovasculares.
Existen varias formas de estatinas, algunas de las cuales incluyen atorvastatina, fluvastatina, lovastatina, pitavastatina, pravastatina, rosuvastatina y simvastatina. También se encuentran disponibles preparaciones combinadas de una estatina y otro agente, como ezetimiba/simvastatina. La clase está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud y la simvastatina es el medicamento incluido en la lista. En 2005, las ventas se estimaron en 18.700 millones de dólares estadounidenses en los Estados Unidos. La estatina más vendida es la atorvastatina, también conocida como Lipitor, que en 2003 se convirtió en el fármaco más vendido de la historia. El fabricante Pfizer registró ventas por 12.400 millones de dólares en 2008.
Usos médicos
Las estatinas generalmente se usan para reducir los niveles de colesterol en la sangre y reducir el riesgo de enfermedades relacionadas con la aterosclerosis, con un grado variable de efecto según los factores de riesgo subyacentes y los antecedentes de enfermedad cardiovascular. Las guías de práctica clínica generalmente recomiendan que las personas comiencen con la modificación del estilo de vida a través de una dieta para reducir el colesterol y el ejercicio físico. Para aquellos que no pueden cumplir con sus objetivos de reducción de lípidos a través de tales métodos, las estatinas pueden ser útiles. El medicamento parece funcionar igualmente bien independientemente del sexo, aunque se describieron algunas diferencias relacionadas con el sexo en la respuesta al tratamiento.
Si existe un historial subyacente de enfermedad cardiovascular, tiene un impacto significativo en los efectos de las estatinas. Esto se puede utilizar para dividir el uso de medicamentos en categorías amplias de prevención primaria y secundaria.
Prevención primaria
Para la prevención primaria de enfermedades cardiovasculares, las pautas del Grupo de trabajo de servicios preventivos de los Estados Unidos (USPSTF) de 2016 recomiendan las estatinas para quienes tienen al menos un factor de riesgo de enfermedad coronaria, tienen entre 40 y 75 años y tienen al menos menos un 10 % de riesgo de enfermedad cardíaca a 10 años, según lo calculado por el algoritmo de cohorte agrupada ACC/AHA de 2013. Los factores de riesgo para la enfermedad coronaria incluyen niveles anormales de lípidos en la sangre, diabetes mellitus, presión arterial alta y tabaquismo. Recomendaron el uso selectivo de dosis bajas a moderadas de estatinas en los mismos adultos que tienen un riesgo calculado de eventos de enfermedad cardiovascular a 10 años de 7,5 a 10 % o más. En personas mayores de 70 años, las estatinas disminuyen el riesgo de enfermedad cardiovascular, pero solo en aquellas con antecedentes de bloqueo intenso de colesterol en las arterias.
La mayoría de la evidencia sugiere que las estatinas también son efectivas para prevenir enfermedades cardíacas en personas con colesterol alto pero sin antecedentes de enfermedades cardíacas. Una revisión Cochrane de 2013 encontró una disminución en el riesgo de muerte y otros malos resultados sin ninguna evidencia de daño. Por cada 138 personas tratadas durante 5 años, muere una menos; por cada 49 atendidos, uno menos tiene un episodio de cardiopatía. Una revisión de 2011 llegó a conclusiones similares y una revisión de 2012 encontró beneficios tanto en mujeres como en hombres. Una revisión de 2010 concluyó que el tratamiento sin antecedentes de enfermedad cardiovascular reduce los eventos cardiovasculares en los hombres, pero no en las mujeres, y no proporciona beneficios de mortalidad en ninguno de los sexos. Otros dos metanálisis publicados ese año, uno de los cuales utilizó datos obtenidos exclusivamente de mujeres, no encontraron beneficios en la mortalidad en la prevención primaria.
El Instituto Nacional para la Salud y la Excelencia Clínica (NICE, por sus siglas en inglés) recomienda el tratamiento con estatinas para adultos con un riesgo estimado de desarrollar enfermedad cardiovascular a 10 años superior al 10 %. Las pautas del Colegio Estadounidense de Cardiología y la Asociación Estadounidense del Corazón recomiendan el tratamiento con estatinas para la prevención primaria de enfermedades cardiovasculares en adultos con colesterol LDL ≥ 190 mg/dL o aquellos con diabetes, de 40 a 75 años con LDL-C 70–190 mg/dl; o en aquellos con un riesgo de 10 años de sufrir un ataque al corazón o un accidente cerebrovascular del 7,5 % o más. En este último grupo, la asignación de estatinas no fue automática, pero se recomendó que ocurriera solo después de una discusión sobre el riesgo médico-paciente con toma de decisiones compartida donde se abordan otros factores de riesgo y el estilo de vida, se sopesa el potencial de beneficio de una estatina contra el potencial de se obtienen los efectos adversos o las interacciones farmacológicas y la preferencia informada del paciente. Además, si una decisión de riesgo era incierta, se sugirieron factores como antecedentes familiares, puntaje de calcio coronario, índice tobillo-brazo y una prueba de inflamación (hs-CRP ≥ 2,0 mg/L) para informar la decisión de riesgo. Los factores adicionales que podrían usarse fueron un LDL-C ≥ 160 o un riesgo de por vida muy alto. Sin embargo, críticos como Steven E. Nissen dicen que las pautas de la AHA/ACC no se validaron correctamente, sobrestiman el riesgo en al menos un 50 % y recomiendan estatinas para las personas que no se beneficiarán, según las poblaciones cuyo riesgo observado es menor que el previsto. por las directrices. La Sociedad Europea de Cardiología y la Sociedad Europea de Aterosclerosis recomiendan el uso de estatinas para la prevención primaria, según la puntuación cardiovascular estimada inicial y los umbrales de LDL.
Prevención secundaria
Las estatinas son eficaces para disminuir la mortalidad en personas con enfermedades cardiovasculares preexistentes. La enfermedad preexistente puede tener muchas manifestaciones. Las enfermedades definitorias incluyen un ataque cardíaco previo, accidente cerebrovascular, angina estable o inestable, aneurisma aórtico u otra enfermedad isquémica arterial, en presencia de aterosclerosis. También se recomienda su uso en personas con alto riesgo de desarrollar enfermedad coronaria. En promedio, las estatinas pueden reducir el colesterol LDL en 1,8 mmol/L (70 mg/dL), lo que se traduce en una disminución estimada del 60 % en la cantidad de eventos cardíacos (ataque cardíaco, muerte cardíaca súbita) y una reducción del 17 % en el riesgo de accidente cerebrovascular después de un tratamiento a largo plazo. Se observa un mayor beneficio con el tratamiento con estatinas de alta intensidad. Tienen menos efecto que los fibratos o la niacina en la reducción de los triglicéridos y el aumento del colesterol HDL ("colesterol bueno").
Ningún estudio ha examinado el efecto de las estatinas sobre la cognición en pacientes con accidente cerebrovascular previo. Sin embargo, dos grandes estudios (HPS y PROSPER) que incluyeron personas con enfermedades vasculares informaron que la simvastatina y la pravastatina no afectaron la cognición.
Se han estudiado las estatinas para mejorar los resultados operativos en cirugía cardiaca y vascular. La mortalidad y los eventos cardiovasculares adversos se redujeron en los grupos de estatinas.
Se han estudiado adultos mayores que reciben tratamiento con estatinas en el momento del alta del hospital después de una estancia hospitalaria. Las personas con isquemia cardíaca que no tomaban previamente estatinas en el momento de la admisión tienen un menor riesgo de eventos adversos cardíacos importantes y de readmisión hospitalaria dos años después de la hospitalización.
Eficacia comparativa
Si bien no existe una comparación directa, todas las estatinas parecen eficaces independientemente de la potencia o el grado de reducción del colesterol. La simvastatina y la pravastatina parecen tener una incidencia reducida de efectos secundarios.
Una comparación de simvastatina, pravastatina y atorvastatina, basada en su eficacia frente a placebos, no encontró diferencias en la reducción de la enfermedad cardiovascular o los niveles de lípidos en la sangre. Una actualización de la revisión sistemática Cochrane de 2015 informó que la rosuvastatina es tres veces más potente que la atorvastatina.
Mujeres
Según la revisión sistemática Cochrane de 2015, la atorvastatina mostró un mayor efecto reductor del colesterol en mujeres que en hombres en comparación con la rosuvastatina.
Niños
En los niños, las estatinas son efectivas para reducir los niveles de colesterol en aquellos con hipercolesterolemia familiar. Sin embargo, su seguridad a largo plazo no está clara. Algunos recomiendan que si los cambios en el estilo de vida no son suficientes, las estatinas deben comenzar a los 8 años.
Hipercolesterolemia familiar
Las estatinas pueden ser menos eficaces para reducir el colesterol LDL en personas con hipercolesterolemia familiar, especialmente aquellas con deficiencias homocigóticas. Estas personas suelen tener defectos en los genes del receptor de LDL o de la apolipoproteína B, los cuales son responsables de la eliminación de LDL de la sangre. Las estatinas siguen siendo un tratamiento de primera línea en la hipercolesterolemia familiar, aunque pueden ser necesarias otras medidas para reducir el colesterol. En personas con deficiencias homocigotas, las estatinas aún pueden resultar útiles, aunque en dosis altas y en combinación con otros medicamentos para reducir el colesterol.
Nefropatía inducida por contraste
Un metanálisis de 2014 encontró que las estatinas podrían reducir el riesgo de nefropatía inducida por contraste en un 53 % en personas que se someten a angiografía coronaria/intervenciones percutáneas. Se encontró que el efecto era más fuerte entre aquellos con disfunción renal preexistente o diabetes mellitus.
Efectos adversos
| Elegir un estatín para personas con consideraciones especiales | |||
|---|---|---|---|
| Estado | Estatinas recomendadas comúnmente | Explicación | |
| Receptores de trasplante de riñón tomando ciclosporin | Pravastatina o fluvastatina | Las interacciones con los fármacos son posibles, pero los estudios no han demostrado que estas estatinas aumenten la exposición a ciclosporin. | |
| Personas seropositivas que toman inhibidores de la proteasa | Atorvastatina, pravastatina o fluvastatina | Las interacciones negativas son más probables con otras opciones | |
| Personas que toman gemfibrozil, un medicamento lipídico que no estático | Atorvastatin | Combinar gemfibrozil y una estatina aumenta el riesgo de rabdomiosis y posteriormente insuficiencia renal | |
| Personas que toman el anticoagulante warfarina | Cualquier estatin | El uso de estatina puede requerir que se cambie la dosis de warfarina, ya que algunos estatinas aumentan el efecto de warfarina. | |
Los efectos secundarios adversos más importantes son los problemas musculares, un mayor riesgo de diabetes mellitus y un aumento de las enzimas hepáticas en la sangre debido al daño hepático. Más de 5 años de tratamiento con estatinas dan como resultado 75 casos de diabetes, 7,5 casos de derrame cerebral hemorrágico y 5 casos de daño muscular por cada 10 000 personas tratadas. Esto podría deberse a que las estatinas inhiben la enzima (HMG-CoA reductasa), que es necesaria para producir colesterol, pero también para otros procesos, como la producción de CoQ10, que es importante para la función muscular y la regulación del azúcar.
Otros posibles efectos adversos incluyen neuropatía, disfunción pancreática y hepática y disfunción sexual. La tasa a la que ocurren tales eventos ha sido ampliamente debatida, en parte porque la relación riesgo/beneficio de las estatinas en poblaciones de bajo riesgo depende en gran medida de la tasa de eventos adversos. Un metanálisis de Cochrane de ensayos clínicos con estatinas en prevención primaria no encontró evidencia de un exceso de eventos adversos entre los tratados con estatinas en comparación con el placebo. Otro metanálisis encontró un aumento del 39 % en los eventos adversos en las personas tratadas con estatinas en relación con las que recibieron placebo, pero ningún aumento en los eventos adversos graves. El autor de un estudio argumentó que los eventos adversos son más comunes en la práctica clínica que en los ensayos clínicos aleatorios. Una revisión sistemática concluyó que, si bien los metanálisis de los ensayos clínicos subestiman la tasa de dolor muscular asociado con el uso de estatinas, las tasas de rabdomiólisis siguen siendo "bajas y tranquilizadoras" y similares a los observados en los ensayos clínicos (alrededor de 1 a 2 por 10 000 años-persona). Otra revisión sistemática del Centro Internacional para la Salud Circulatoria del Instituto Nacional del Corazón y los Pulmones en Londres concluyó que solo una pequeña fracción de los efectos secundarios informados por las personas que toman estatinas son en realidad atribuibles a la estatina.
Efectos cognitivos
Múltiples revisiones sistemáticas y metanálisis han concluido que la evidencia disponible no respalda una asociación entre el uso de estatinas y el deterioro cognitivo. Se ha demostrado que las estatinas disminuyen el riesgo de demencia, enfermedad de Alzheimer y mejoran el deterioro cognitivo en algunos casos en 2010. Además, tanto el estudio de investigación centrada en el paciente sobre los resultados que prefieren los pacientes con accidentes cerebrovasculares y su eficacia (PROSPER) como el Health Protection Study (HPS) demostró que la simvastatina y la pravastatina no afectaron la cognición de los pacientes con factores de riesgo o antecedentes de enfermedades vasculares.
Hay informes de deterioro cognitivo reversible con estatinas. El prospecto de la Administración de Drogas y Alimentos de los EE. UU. (FDA) sobre las estatinas incluye una advertencia sobre la posibilidad de efectos secundarios cognitivos no graves y reversibles con el medicamento (pérdida de memoria, confusión).
Músculos
En estudios de observación, entre el 10 % y el 15 % de las personas que toman estatinas experimentan problemas musculares; en la mayoría de los casos estos consisten en dolor muscular. Estas tasas, que son mucho más altas que las observadas en los ensayos clínicos aleatorios, han sido tema de amplio debate y discusión.
Los síntomas musculares y de otro tipo a menudo hacen que los pacientes dejen de tomar una estatina. Esto se conoce como intolerancia a las estatinas. Un ensayo controlado aleatorizado (RCT, por sus siglas en inglés) reciente les dio a los pacientes intolerantes a las estatinas una estatina o un placebo dentro de cápsulas que tenían el mismo aspecto, lo que hizo que el estudio fuera doble ciego: los participantes no sabían qué estaban tomando en ningún período, estatina o placebo. Esto se repitió 3 veces, por lo que hubo 6 períodos en orden aleatorio. Se preguntó a los pacientes acerca de sus síntomas, que fueron similares con la estatina y con el placebo, lo que demuestra que la intolerancia a las estatinas depende de que las personas sepan que están tomando una estatina. Un ECA doble ciego más pequeño obtuvo resultados similares. Después de que se les mostraran las puntuaciones de sus síntomas, la mayoría de los participantes en estos 2 estudios tenían la intención de reiniciar el tratamiento con estatinas. Los resultados de estos estudios ayudan a explicar por qué las tasas de síntomas de las estatinas en los estudios observacionales son mucho más altas que en los ECA doble ciego. La diferencia resulta del efecto nocebo, que es lo opuesto al efecto placebo: los síntomas son causados por expectativas de daño.
La información de los medios sobre las estatinas suele ser negativa, y los folletos para pacientes informan a los pacientes que pueden ocurrir problemas musculares raros pero potencialmente graves durante el tratamiento con estatinas. Estos crean expectativas de daño. Los síntomas de Nocebo son reales y molestos y son una barrera importante para el tratamiento. Debido a esto, muchas personas dejan de tomar estatinas, que han demostrado en numerosos ECA a gran escala que reducen los ataques cardíacos, los accidentes cerebrovasculares y las muertes, siempre que las personas continúen tomándolas.
Los problemas musculares graves, como la rabdomiolisis (destrucción de las células musculares) y la miopatía autoinmune asociada a las estatinas, ocurren en menos del 0,1 % de las personas tratadas. La rabdomiólisis puede, a su vez, provocar una lesión renal potencialmente mortal. El riesgo de rabdomiólisis inducida por estatinas aumenta con la edad avanzada, el uso de medicamentos que interactúan como los fibratos y el hipotiroidismo. Los niveles de coenzima Q10 (ubiquinona) disminuyen con el uso de estatinas; Los suplementos de CoQ10 a veces se usan para tratar la miopatía asociada a las estatinas, aunque falta evidencia de su eficacia a partir de 2017. El gen SLCO1B1 (Solute carrier organic anion transporter family member 1B1) codifica un anión orgánico transportador polipéptido que interviene en la regulación de la absorción de las estatinas. En 2008 se descubrió que una variación común en este gen aumenta significativamente el riesgo de miopatía.
Existen registros de más de 250 000 personas tratadas entre 1998 y 2001 con las estatinas atorvastatina, cerivastatina, fluvastatina, lovastatina, pravastatina y simvastatina. La incidencia de rabdomiólisis fue de 0,44 por 10.000 pacientes tratados con estatinas distintas de cerivastatina. Sin embargo, el riesgo era más de 10 veces mayor si se usaba cerivastatina o si las estatinas estándar (atorvastatina, fluvastatina, lovastatina, pravastatina o simvastatina) se combinaban con un tratamiento con fibratos (fenofibrato o gemfibrozilo). Cerivastatina fue retirada por su fabricante en 2001.
Algunos investigadores han sugerido que las estatinas hidrofílicas, como la fluvastatina, la rosuvastatina y la pravastatina, son menos tóxicas que las estatinas lipofílicas, como la atorvastatina, la lovastatina y la simvastatina, pero otros estudios no han encontrado una conexión. La lovastatina induce la expresión del gen atrogin-1, que se cree que es responsable de promover el daño de las fibras musculares. La ruptura del tendón no parece ocurrir.
Diabetes
La relación entre el uso de estatinas y el riesgo de desarrollar diabetes sigue sin estar clara y los resultados de las revisiones son contradictorios. Las dosis más altas tienen un mayor efecto, pero la disminución de la enfermedad cardiovascular supera el riesgo de desarrollar diabetes. El uso en mujeres posmenopáusicas se asocia con un mayor riesgo de diabetes. El mecanismo exacto responsable del posible aumento del riesgo de diabetes mellitus asociado con el uso de estatinas no está claro. Sin embargo, hallazgos recientes han indicado que la inhibición de HMGCoAR es un mecanismo clave. Se cree que las estatinas disminuyen las células ' captación de glucosa del torrente sanguíneo en respuesta a la hormona insulina. Se cree que una forma en que esto ocurre es al interferir con la síntesis de colesterol, que es necesaria para la producción de ciertas proteínas responsables de la absorción de glucosa en células como GLUT1.
Cáncer
Varios metaanálisis no han encontrado un mayor riesgo de cáncer y algunos metaanálisis han encontrado un riesgo reducido. Específicamente, las estatinas pueden reducir el riesgo de cáncer de esófago, cáncer colorrectal, cáncer gástrico, carcinoma hepatocelular y posiblemente cáncer de próstata. Parece que no tienen ningún efecto sobre el riesgo de cáncer de pulmón, cáncer de riñón, cáncer de mama, cáncer de páncreas o cáncer de vejiga.
Interacciones medicamentosas
La combinación de cualquier estatina con un fibrato o niacina (otras categorías de fármacos hipolipemiantes) aumenta los riesgos de rabdomiolisis a casi 6,0 por cada 10 000 años-persona. El control de las enzimas hepáticas y la creatina cinasa es especialmente prudente en los que toman estatinas en dosis altas o en los que toman combinaciones de estatinas/fibratos, y es obligatorio en el caso de calambres musculares o deterioro de la función renal.
El consumo de toronja o jugo de toronja inhibe el metabolismo de ciertas estatinas y las naranjas amargas pueden tener un efecto similar. Las furanocumarinas en el jugo de toronja (es decir, bergamotina y dihidroxibergamotina) inhiben la enzima CYP3A4 del citocromo P450, que está involucrada en el metabolismo de la mayoría de las estatinas (sin embargo, es un inhibidor importante solo de lovastatina, simvastatina y, en menor grado, atorvastatina) y algunas otros medicamentos (se pensaba que los flavonoides (es decir, naringina) eran los responsables). Esto aumenta los niveles de la estatina, aumentando el riesgo de efectos adversos relacionados con la dosis (incluyendo miopatía/rabdomiolisis). La prohibición absoluta del consumo de jugo de toronja para los usuarios de algunas estatinas es controvertida.
La Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) de EE. UU. notificó a los profesionales de la salud las actualizaciones de la información de prescripción sobre las interacciones entre los inhibidores de la proteasa y ciertas estatinas. Los inhibidores de la proteasa y las estatinas tomados juntos pueden aumentar los niveles de estatinas en la sangre y aumentar el riesgo de lesión muscular (miopatía). La forma más grave de miopatía, la rabdomiolisis, puede dañar los riñones y provocar insuficiencia renal, que puede ser fatal.
Osteoporosis y fracturas
Los estudios han encontrado que el uso de estatinas puede proteger contra la osteoporosis y las fracturas o puede inducir osteoporosis y fracturas. Un análisis retrospectivo transversal de toda la población austriaca encontró que el riesgo de contraer osteoporosis depende de la dosis utilizada.
Neuropatía
El consumo de estatinas se ha relacionado con una mayor prevalencia de neuropatía.
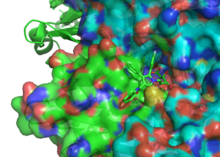
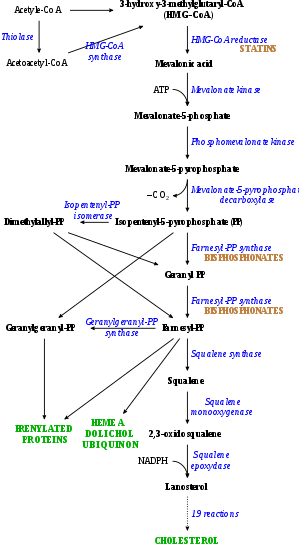
Mecanismo de acción
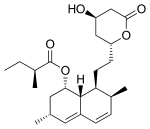
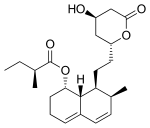
Las estatinas actúan inhibiendo competitivamente la HMG-CoA reductasa, la enzima limitante de la velocidad de la vía del mevalonato. Debido a que las estatinas tienen una estructura similar a la HMG-CoA a nivel molecular, encajarán en el sitio activo de la enzima y competirán con el sustrato nativo (HMG-CoA). Esta competencia reduce la velocidad a la que la HMG-CoA reductasa puede producir mevalonato, la siguiente molécula en la cascada que eventualmente produce colesterol. Los hongos Penicillium y Aspergillus producen una variedad de estatinas naturales como metabolitos secundarios. Estas estatinas naturales probablemente funcionen para inhibir las enzimas HMG-CoA reductasa en bacterias y hongos que compiten con el productor.
Inhibición de la síntesis de colesterol
Al inhibir la HMG-CoA reductasa, las estatinas bloquean la vía de síntesis del colesterol en el hígado. Esto es significativo porque la mayor parte del colesterol circulante proviene de la fabricación interna y no de la dieta. Cuando el hígado ya no puede producir colesterol, los niveles de colesterol en la sangre bajarán. La síntesis de colesterol parece ocurrir principalmente por la noche, por lo que las estatinas con vidas medias cortas generalmente se toman por la noche para maximizar su efecto. Los estudios han demostrado mayores reducciones de LDL y colesterol total en la simvastatina de acción corta tomada por la noche en lugar de por la mañana, pero no han mostrado diferencias en la atorvastatina de acción prolongada.
Aumento de la captación de LDL
En los conejos, las células hepáticas detectan los niveles reducidos de colesterol hepático y buscan compensar sintetizando receptores LDL para sacar el colesterol de la circulación. Esto se logra a través de proteasas que escinden las proteínas de unión de elementos reguladores de esteroles unidas a la membrana, que luego migran al núcleo y se unen a los elementos de respuesta de esteroles. Los elementos de respuesta a esteroles luego facilitan el aumento de la transcripción de varias otras proteínas, más notablemente, el receptor de LDL. El receptor de LDL se transporta a la membrana de la célula hepática y se une a las partículas de LDL y VLDL que pasan, mediando su absorción en el hígado, donde el colesterol se reprocesa en sales biliares y otros subproductos. Esto da como resultado un efecto neto de menos LDL circulando en la sangre.
Disminución de la prenilación de proteínas específicas
Las estatinas, al inhibir la vía de la HMG CoA reductasa, inhiben la síntesis posterior de isoprenoides, como farnesil pirofosfato y geranilgeranil pirofosfato. La inhibición de la prenilación de proteínas para proteínas como RhoA (y la posterior inhibición de la proteína quinasa asociada a Rho) puede estar involucrada, al menos parcialmente, en la mejora de la función endotelial, la modulación de la función inmune y otros beneficios cardiovasculares pleiotrópicos de las estatinas, así como como en el hecho de que varios otros medicamentos que reducen el LDL no han mostrado los mismos beneficios de riesgo cardiovascular en estudios que las estatinas, y también pueden explicar algunos de los beneficios observados en la reducción del cáncer con estatinas. Además, el efecto inhibitorio sobre la prenilación de proteínas también puede estar involucrado en una serie de efectos secundarios no deseados asociados con las estatinas, que incluyen dolor muscular (miopatía) y niveles elevados de azúcar en la sangre (diabetes).
Otros efectos
Como se señaló anteriormente, las estatinas exhiben una acción más allá de la actividad hipolipemiante en la prevención de la aterosclerosis a través de los llamados "efectos pleiotrópicos de las estatinas". Los efectos pleiotrópicos de las estatinas siguen siendo controvertidos. El ensayo ASTEROID mostró evidencia ecográfica directa de la regresión del ateroma durante el tratamiento con estatinas. Los investigadores plantean la hipótesis de que las estatinas previenen las enfermedades cardiovasculares a través de cuatro mecanismos propuestos (todos sujetos de una gran cantidad de investigación biomédica):
- Mejorar la función endotelial
- Modular las respuestas inflamatorias
- Mantener la estabilidad de la placa
- Prevenir la formación de coágulos sanguíneos
En 2008, el ensayo JUPITER demostró que las estatinas brindaban beneficios en personas que no tenían antecedentes de colesterol alto o enfermedad cardíaca, pero solo en aquellas con niveles elevados de proteína C reactiva de alta sensibilidad (hsCRP), un indicador de inflamación. El estudio ha sido criticado debido a fallas percibidas en el diseño del estudio, aunque Paul M. Ridker, investigador principal del ensayo JUPITER, ha respondido extensamente a estas críticas.
Haga clic en genes, proteínas y metabolitos a continuación para vincular a los artículos respectivos.
- ^ El mapa interactivo se puede editar en WikiPathways: "Statin_Pathway_WP430".
Como el objetivo de las estatinas, la HMG-CoA reductasa, es muy similar entre eucariotas y arqueas, las estatinas también actúan como antibióticos contra las arqueas al inhibir la biosíntesis de mevalonato de arqueas. Esto se ha demostrado in vivo e in vitro. Dado que los pacientes con un fenotipo de estreñimiento presentan una mayor abundancia de arqueas metanogénicas en el intestino, se ha propuesto el uso de estatinas para el tratamiento del síndrome del intestino irritable y, de hecho, puede ser uno de los beneficios ocultos del uso de estatinas.
Formularios disponibles
Las estatinas se dividen en dos grupos: derivadas de la fermentación y sintéticas. Algunos tipos específicos se enumeran en la siguiente tabla. Tenga en cuenta que las marcas asociadas pueden variar entre países.
| Statin | Imagen | Nombre de la marca | Derivación | Metabolismo | Media vida |
|---|---|---|---|---|---|
| Atorvastatin | Arkas, Ator, Atoris, Lipitor, Torvast, Totalip | Sintético | CYP3A4 | 14-19 horas. | |
| Cerivastatin | Baycol, Lipobay (retirada del mercado en agosto de 2001 debido al riesgo de rabdomiolisis grave) | Sintético | varios isoformas CYP3A | ||
| Fluvastatin | Lescol, Lescol XL, Lipaxan, Primesin | Sintético | CYP2C9 | 1-3 horas. | |
| Lovastatin | Altocor, Altoprev, Mevacor | Compuesto naturalmente producido, fermentado. Se encuentra en hongos de ostra y arroz de levadura roja | CYP3A4 | 1-3 horas. | |
| Mevastatin | Compacto | Compuesto natural encontrado en arroz de levadura roja | CYP3A4 | ||
| Pitavastatin | Alipza, Livalo, Livazo, Pitava, Zypitamag | Sintético | CYP2C9 y CYP2C8 (mínimo) | ||
| Pravastatin | Aplactina, Lipostat, Prasterol, Pravachol, Pravaselect, Sanaprav, Selectin, Selektine, Vasticor | Fermentation-derived (producto de fermentación de bacterias Nocardia autotrofica) | Non-CYP | 1-3 horas. | |
| Rosuvastatin | Colcardiol, Colfri, Crativ, Crestor, Dilivas, Exorta, Koleros, Lipidover, Miastina, Provisacor, Rosastin, Simestat, Staros | Sintético | CYP2C9 y CYP2C19 | 14-19 horas. | |
| Simvastatin | Alpheus, Krustat, Lipenil, Lipex, Liponorm, Medipo, Omistat, Rosim, Setorilin, Simbatrix, Sincol, Sinvalip, Sivastin, Sinvat, Vastgen, Vastin, Xipocol, Zocor | Fermentation-derived (simvastatina es un derivado sintético de un producto de fermentación de Aspergillus terreus) | CYP3A4 | 1-3 horas. | |
| Atorvastatina + amlodipina | Caduet, Envacar | Terapia de combinación: estatina + antagonista de calcio | |||
| Atorvastatina + perindopril + amlodipina | Lipertance, Triveram | Terapia de combinación: estatina + inhibidor de ACE + antagonista de calcio | |||
| Lovastatina + niacina extendida liberación | Advicor, Mevacor | Terapia combinada | |||
| Rosuvastatina + ezetimibe | Cholecomb, Delipid Plus, Росули плюс, Rosulip, Rosumibe, Viazet | Terapia de combinación: estatina + inhibidor de absorción de colesterol | |||
| Simvastatin + ezetimibe | Goltor, Inegy, Staticol, Vytorin, Zestan, Zevistat | Terapia de combinación: estatina + inhibidor de absorción de colesterol | |||
| Simvastatin + niacina extendida liberación | Simcor, Simcora | Terapia combinada |
La potencia reductora de LDL varía entre los agentes. La cerivastatina es la más potente (retirada del mercado en agosto de 2001 debido al riesgo de rabdomiolisis grave) seguida de (en orden decreciente de potencia) rosuvastatina, atorvastatina, simvastatina, lovastatina, pravastatina y fluvastatina. La potencia relativa de la pitavastatina aún no se ha establecido por completo, pero los estudios preliminares indican una potencia similar a la de la rosuvastatina.
Algunos tipos de estatinas se producen de forma natural y se pueden encontrar en alimentos como los hongos ostra y el arroz de levadura roja. Los ensayos controlados aleatorios han encontrado que estos alimentos reducen el colesterol circulante, pero se ha juzgado que la calidad de los ensayos es baja. Debido al vencimiento de la patente, la mayoría de las estatinas de marca de gran éxito han sido genéricas desde 2012, incluida la atorvastatina, el medicamento de marca más vendido.
| Dosis equivalentes de estatina | ||||||
|---|---|---|---|---|---|---|
| % Reducción de LDL (aprox.) | Atorvastatin | Fluvastatin | Lovastatin | Pravastatin | Rosuvastatin | Simvastatin |
| 10-20% | – | 20 mg | 10 mg | 10 mg | – | 5 mg |
| 20-30% | – | 40 mg | 20 mg | 20 mg | – | 10 mg |
| 30-40% | 10 mg | 80 mg | 40 mg | 40 mg | 5 mg | 20 mg |
| 40-45% | 20 mg | – | 80 mg | 80 mg | 5 a 10 mg | 40 mg |
| 46–50% | 40 mg | – | – | – | 10 a 20 mg | 80 mg* |
| 50-55% | 80 mg | – | – | – | 20 mg | – |
| 56–60% | – | – | – | – | 40 mg | – |
| * La dosis de 80 mg ya no se recomienda debido al mayor riesgo de rabdomiosis | ||||||
| Dosis inicial | ||||||
| Dosis inicial | 10 a 20 mg | 20 mg | 10 a 20 mg | 40 mg | 10 mg; 5 mg si hipotiroidea, √65 yo, asiática | 20 mg |
| Si el objetivo de reducción de LDL más alto | 40 mg si | 40 mg si | 20 mg si | – | 20 mg si LDL √190 mg/dL (4.87 mmol/L) | 40 mg si |
| Tiempo óptimo | Siempre | Buenas noches | Con comidas nocturnas | Siempre | Siempre | Buenas noches |
Historia
El papel del colesterol en el desarrollo de la enfermedad cardiovascular se aclaró en la segunda mitad del siglo XX. Esta hipótesis de los lípidos impulsó los intentos de reducir la carga de enfermedades cardiovasculares mediante la reducción del colesterol. El tratamiento consistió principalmente en medidas dietéticas, como una dieta baja en grasas y medicamentos mal tolerados, como clofibrato, colestiramina y ácido nicotínico. El investigador del colesterol, Daniel Steinberg, escribe que, si bien el Ensayo de prevención primaria coronaria de 1984 demostró que la reducción del colesterol podría reducir significativamente el riesgo de ataques cardíacos y angina, los médicos, incluidos los cardiólogos, no estaban convencidos en gran medida. Los científicos en entornos académicos y la industria farmacéutica comenzaron a intentar desarrollar un medicamento para reducir el colesterol de manera más efectiva. Había varios objetivos potenciales, con 30 pasos en la síntesis de colesterol a partir de acetil-coenzima A.
En 1971, Akira Endo, un bioquímico japonés que trabajaba para la compañía farmacéutica Sankyo, comenzó a investigar este problema. Las investigaciones ya habían demostrado que el cuerpo produce principalmente colesterol en el hígado con la enzima HMG-CoA reductasa. Endo y su equipo razonaron que ciertos microorganismos pueden producir inhibidores de la enzima para defenderse de otros organismos, ya que el mevalonato es un precursor de muchas sustancias requeridas por los organismos para el mantenimiento de sus paredes celulares o citoesqueleto (isoprenoides). El primer agente que identificaron fue la mevastatina (ML-236B), una molécula producida por el hongo Penicillium citrinum.
Un grupo británico aisló el mismo compuesto de Penicillium brevicompactum, lo llamó compactina y publicó su informe en 1976. El grupo británico menciona propiedades antifúngicas, sin mencionar la inhibición de la HMG-CoA reductasa. La mevastatina nunca se comercializó debido a sus efectos adversos de tumores, deterioro muscular y, a veces, la muerte en perros de laboratorio. P. Roy Vagelos, científico jefe y luego director ejecutivo de Merck & Co, se interesó y realizó varios viajes a Japón a partir de 1975. Para 1978, Merck había aislado lovastatina (mevinolina, MK803) del hongo Aspergillus terreus, comercializado por primera vez en 1987 como Mevacor.
En la década de 1990, como resultado de campañas públicas, las personas en los Estados Unidos se familiarizaron con sus niveles de colesterol y la diferencia entre el colesterol HDL y LDL, y varias compañías farmacéuticas comenzaron a producir sus propias estatinas, como pravastatina (Pravachol), fabricado por Sankyo y Bristol-Myers Squibb. En abril de 1994, se anunciaron los resultados de un estudio patrocinado por Merck, el Estudio escandinavo de supervivencia de la simvastatina. Los investigadores probaron la simvastatina, más tarde vendida por Merck como Zocor, en 4444 pacientes con colesterol alto y enfermedades del corazón. Después de cinco años, el estudio concluyó que los pacientes vieron una reducción del 35 % en su colesterol y sus posibilidades de morir de un ataque al corazón se redujeron en un 42 %. En 1995, Zocor y Mevacor crearon Merck por mil millones de dólares.
Aunque no se benefició de su descubrimiento original, Endo recibió el Premio de Japón 2006 y el Premio de Investigación Médica Clínica Lasker-DeBakey en 2008, por su investigación pionera. Endo también fue incluido en el Salón de la Fama de los Inventores Nacionales en Alexandria, Virginia en 2012. Michael S. Brown y Joseph Goldstein, quienes ganaron el Premio Nobel por trabajos relacionados con el colesterol, dijeron sobre Endo: "Los millones de personas cuyos vidas se extenderán a través de la terapia con estatinas se lo debemos todo a Akira Endo."
A partir de 2016, las afirmaciones engañosas que exageran los efectos adversos de las estatinas han recibido una amplia cobertura mediática, con el consiguiente impacto negativo en la salud pública. La controversia sobre la eficacia de las estatinas en la literatura médica se amplificó en los medios de comunicación populares a principios de la década de 2010, lo que llevó a unas 200 000 personas en el Reino Unido a dejar de usar estatinas durante un período de seis meses hasta mediados de 2016, según los autores de un estudio financiado por la Fundación Británica del Corazón. Estimaron que podría haber hasta 2,000 ataques cardíacos o accidentes cerebrovasculares adicionales en los próximos 10 años como consecuencia. Un efecto no deseado de la controversia académica sobre las estatinas ha sido la difusión de terapias alternativas científicamente cuestionables. El cardiólogo Steven Nissen de la Clínica Cleveland comentó "Estamos perdiendo la batalla por los corazones y las mentes de nuestros pacientes contra los sitios web..." promover terapias médicas no probadas. Harriet Hall ve un espectro de "negación de las estatinas" que van desde afirmaciones pseudocientíficas hasta la subestimación de los beneficios y la exageración de los efectos secundarios, todo lo cual es contrario a la evidencia científica.
Se han aprobado varias estatinas como medicamentos genéricos en los Estados Unidos:
- Lovastatina (Mevacor) en diciembre de 2001
- Pravastatina (Pravachol) en abril de 2006
- Simvastatin (Zocor) en junio de 2006
- Atorvastatina (Lipitor) en noviembre 2011
- Fluvastatina (Lescol) en abril de 2012
- Pitavastatina (Livalo) y rosuvastatina (Crestor) en 2016
- Ezetimibe/simvastatina (Vytorin) y ezetimibe/atorvastatina (Liptruzet) en 2017
Investigación
Se han realizado estudios clínicos sobre el uso de estatinas en la demencia, el cáncer de pulmón, las cataratas nucleares, la hipertensión y el cáncer de próstata y de mama. No hay evidencia de alta calidad de que las estatinas sean útiles para la neumonía. El pequeño número de ensayos disponibles no respalda el uso de estatinas como terapia adyuvante o como monoterapia en la esclerosis múltiple.
Contenido relacionado
Trombopoyetina
Prueba de gases en sangre arterial
William Burnet (médico)