Espectroscopia ultravioleta-visible
Espectroscopía UV o espectrofotometría UV-visible (UV-Vis o UV/Vis) se refiere a la absorción espectroscopia o espectroscopia de reflectancia en parte del ultravioleta y las regiones visibles adyacentes completas del espectro electromagnético. Siendo relativamente económica y fácil de implementar, esta metodología es ampliamente utilizada en diversas aplicaciones aplicadas y fundamentales. El único requisito es que la muestra absorba en la región UV-Vis, es decir, que sea un cromóforo. La espectroscopia de absorción es complementaria a la espectroscopia de fluorescencia. Los parámetros de interés, además de la longitud de onda de medición, son la absorbancia (A), la transmitancia (%T) o la reflectancia (%R), y su cambio con el tiempo.
Transiciones ópticas
La mayoría de las moléculas e iones absorben energía en el rango ultravioleta o visible, es decir, son cromóforos. El fotón absorbido excita un electrón en el cromóforo a orbitales moleculares de mayor energía, dando lugar a un estado excitado. Para los cromóforos orgánicos, se suponen cuatro posibles tipos de transiciones: π–π*, n–π*, σ–σ* y n–σ*. Los complejos de metales de transición a menudo están coloreados (es decir, absorben la luz visible) debido a la presencia de múltiples estados electrónicos asociados con orbitales d incompletos.
Aplicaciones
La espectroscopia UV/Vis se utiliza habitualmente en química analítica para la determinación cuantitativa de diversos analitos o muestras, como iones de metales de transición, compuestos orgánicos altamente conjugados y macromoléculas biológicas. El análisis espectroscópico se lleva a cabo comúnmente en soluciones, pero también se pueden estudiar sólidos y gases.
- Los compuestos orgánicos, especialmente aquellos con un alto grado de conjugación, también absorben la luz en las regiones UV o visibles del espectro electromagnético. Los solventes para estas determinaciones son a menudo agua para compuestos hidrosolubles, o etanol para compuestos orgánico-solubles. (Los solventes orgánicos pueden tener una absorción UV significativa; no todos los solventes son adecuados para su uso en la espectroscopia UV. El etanol absorbe muy débilmente a la mayoría de longitudes de onda.) La polaridad y el pH pueden afectar el espectro de absorción de un compuesto orgánico. La tirosina, por ejemplo, aumenta el coeficiente de absorción máxima y extinción molar cuando el pH aumenta de 6 a 13 o cuando disminuye la polaridad solvente.
- Mientras que los complejos de transferencia de carga también dan lugar a colores, los colores son a menudo demasiado intensos para ser utilizados para la medición cuantitativa.
La ley de Beer-Lambert establece que la absorbancia de una solución es directamente proporcional a la concentración de las especies absorbentes en la solución y la longitud del camino. Por lo tanto, para una longitud de trayectoria fija, la espectroscopia UV/Vis se puede utilizar para determinar la concentración del absorbente en una solución. Es necesario saber qué tan rápido cambia la absorbancia con la concentración. Esto puede tomarse de las referencias (tablas de coeficientes de extinción molar) o, más exactamente, determinarse a partir de una curva de calibración.
Se puede utilizar un espectrofotómetro UV/Vis como detector para HPLC. La presencia de un analito da una respuesta que se supone proporcional a la concentración. Para obtener resultados precisos, la respuesta del instrumento al analito en el desconocido debe compararse con la respuesta a un estándar; esto es muy similar al uso de curvas de calibración. La respuesta (por ejemplo, la altura del pico) para una concentración particular se conoce como factor de respuesta.
Las longitudes de onda de los picos de absorción se pueden correlacionar con los tipos de enlaces en una molécula dada y son valiosos para determinar los grupos funcionales dentro de una molécula. Las reglas de Woodward-Fieser, por ejemplo, son un conjunto de observaciones empíricas utilizadas para predecir λmax, la longitud de onda de la absorción UV/Vis más intensa, para compuestos orgánicos conjugados como dienos y cetonas. Sin embargo, el espectro por sí solo no es una prueba específica para una muestra determinada. La naturaleza del solvente, el pH de la solución, la temperatura, las altas concentraciones de electrolitos y la presencia de sustancias que interfieren pueden influir en el espectro de absorción. Las variaciones experimentales como el ancho de la rendija (ancho de banda efectivo) del espectrofotómetro también alterarán el espectro. Para aplicar la espectroscopia UV/Vis al análisis, estas variables deben controlarse o contabilizarse para identificar las sustancias presentes.
El método se usa con mayor frecuencia de forma cuantitativa para determinar las concentraciones de una especie absorbente en solución, utilizando la ley de Beer-Lambert:
- ,
Donde A es la absorción medida (formalmente dimensional pero generalmente reportada en Unidades de Absorbancia (AU)), es la intensidad de la luz del incidente en una longitud de onda dada, es la intensidad transmitida, L la longitud del camino a través de la muestra, y c la concentración de la especie absorbente. Para cada especie y longitud de onda, ε es una constante conocida como el coeficiente de absorción molar o extinción. Esta constante es una propiedad molecular fundamental en un solvente dado, a una temperatura y presión particular, y tiene unidades de .
La absorbancia y la extinción ε a veces se definen en términos del logaritmo natural en lugar del logaritmo en base 10.
La Ley de Beer-Lambert es útil para caracterizar muchos compuestos, pero no es una relación universal para la concentración y absorción de todas las sustancias. A veces se encuentra una relación polinómica de segundo orden entre la absorción y la concentración para moléculas muy grandes y complejas, como los colorantes orgánicos (Xylenol Orange o Neutral Red, por ejemplo).
La espectroscopia UV-Vis también se utiliza en la industria semiconductora para medir el grosor y las propiedades ópticas de las películas delgadas en un wafer. Los espectrómetros UV-Vis se utilizan para medir la reflectancia de la luz, y se pueden analizar a través de las ecuaciones de dispersión Forouhi-Bloomer para determinar el índice de refracción () y el coeficiente de extinción () de una película dada a través de la gama espectral medida.
Consideraciones prácticas
La ley de Beer-Lambert tiene supuestos implícitos que deben cumplirse experimentalmente para que se aplique; de lo contrario, existe la posibilidad de desviaciones de la ley. Por ejemplo, la composición química y el entorno físico de la muestra pueden alterar su coeficiente de extinción. Por lo tanto, las condiciones químicas y físicas de una muestra de prueba deben coincidir con las mediciones de referencia para que las conclusiones sean válidas. En todo el mundo, las farmacopeas como la estadounidense (USP) y la europea (Ph. Eur.) exigen que los espectrofotómetros funcionen de acuerdo con estrictos requisitos reglamentarios que abarcan factores como la luz parásita y la precisión de la longitud de onda.
Ancho de banda espectral
Es importante tener una fuente monocromática de radiación para la luz que incide sobre la celda de muestra. La monocromaticidad se mide como el ancho del "triángulo" formado por el pico de intensidad, a la mitad de la intensidad pico. Un espectrómetro dado tiene un ancho de banda espectral que caracteriza cuán monocromática es la luz incidente. Si este ancho de banda es comparable (o superior) al ancho de la línea de absorción, el coeficiente de extinción medido será erróneo. En las medidas de referencia, el ancho de banda del instrumento (ancho de banda de la luz incidente) se mantiene por debajo del ancho de las líneas espectrales. Cuando se mide un material de prueba, el ancho de banda de la luz incidente también debe ser lo suficientemente estrecho. La reducción del ancho de banda espectral reduce la energía que pasa al detector y, por lo tanto, requerirá un tiempo de medición más prolongado para lograr la misma relación señal/ruido.
Error de longitud de onda
En los líquidos, el coeficiente de extinción suele cambiar lentamente con la longitud de onda. Un pico de la curva de absorbancia (una longitud de onda donde la absorbancia alcanza un máximo) es donde la tasa de cambio en la absorbancia con la longitud de onda es menor. Las mediciones generalmente se realizan en un pico para minimizar los errores producidos por errores en la longitud de onda en el instrumento, es decir, errores debido a que tiene un coeficiente de extinción diferente al asumido.
Luz parásita
Otro factor importante importante es la pureza de la luz utilizada. El factor más importante que afecta esto es el nivel de luz parásita del monocromador.
El detector utilizado es de banda ancha; responde a toda la luz que le llega. Si una cantidad significativa de la luz que pasa a través de la muestra contiene longitudes de onda que tienen coeficientes de extinción mucho más bajos que el nominal, el instrumento informará una absorbancia incorrectamente baja. Cualquier instrumento llegará a un punto en el que un aumento en la concentración de la muestra no dará como resultado un aumento en la absorbancia informada, porque el detector simplemente está respondiendo a la luz parásita. En la práctica, la concentración de la muestra o la longitud del camino óptico deben ajustarse para colocar la absorbancia desconocida dentro de un rango que sea válido para el instrumento. A veces se desarrolla una función de calibración empírica, usando concentraciones conocidas de la muestra, para permitir mediciones en la región donde el instrumento se está volviendo no lineal.
Como guía general, un instrumento con un solo monocromador normalmente tendría un nivel de luz parásita correspondiente a unas 3 unidades de absorbancia (AU), lo que haría que las mediciones por encima de unas 2 AU fueran problemáticas. Un instrumento más complejo con doble monocromador tendría un nivel de luz parásita correspondiente a unas 6 AU, lo que permitiría medir un rango de absorbancia mucho más amplio.
Desviaciones de la ley de Beer-Lambert
A concentraciones suficientemente altas, las bandas de absorción se saturarán y mostrarán un aplanamiento de la absorción. El pico de absorción parece aplanarse porque ya se está absorbiendo cerca del 100% de la luz. La concentración a la que esto ocurre depende del compuesto particular que se esté midiendo. Una prueba que se puede usar para probar este efecto es variar la longitud de la trayectoria de la medición. En la ley de Beer-Lambert, variar la concentración y la longitud del camino tiene un efecto equivalente: diluir una solución por un factor de 10 tiene el mismo efecto que acortar la longitud del camino por un factor de 10. Si se dispone de celdas de diferentes longitudes de camino, probar si esta relación es cierta, es una forma de juzgar si se está produciendo un aplanamiento por absorción.
Las soluciones que no son homogéneas pueden mostrar desviaciones de la ley de Beer-Lambert debido al fenómeno de aplanamiento por absorción. Esto puede suceder, por ejemplo, cuando la sustancia absorbente se encuentra dentro de partículas suspendidas. Las desviaciones serán más notorias en condiciones de baja concentración y alta absorbancia. La última referencia describe una forma de corregir esta desviación.
Algunas soluciones, como el cloruro de cobre (II) en el agua, cambian visualmente a una cierta concentración debido a las condiciones cambiantes alrededor del ion coloreado (el ion de cobre divalente). Para el cloruro de cobre (II), significa un cambio de azul a verde, lo que significaría que las mediciones monocromáticas se desviarían de la ley de Beer-Lambert.
Fuentes de incertidumbre de medición
Los factores anteriores contribuyen a la incertidumbre de medición de los resultados obtenidos con la espectrofotometría UV/Vis. Si se utiliza la espectrofotometría UV/Vis en el análisis químico cuantitativo, los resultados se ven afectados adicionalmente por las fuentes de incertidumbre que surgen de la naturaleza de los compuestos y/o soluciones que se miden. Estos incluyen interferencias espectrales causadas por la superposición de bandas de absorción, desvanecimiento del color de las especies absorbentes (causado por descomposición o reacción) y posible desajuste de composición entre la muestra y la solución de calibración.
Espectrofotómetro ultravioleta-visible
El instrumento utilizado en la espectroscopia ultravioleta-visible se llama UV/Vis espectrofotómetro. Mide la intensidad de la luz después de pasar por una muestra (), y lo compara con la intensidad de la luz antes de pasar a través de la muestra (). La relación se llama transmitancia, y se expresa generalmente como un porcentaje (%T). La absorción, , se basa en la transmisión:
El espectrofotómetro UV-visible también se puede configurar para medir la reflectancia. En este caso, el espectrofotómetro mide la intensidad de la luz reflejada en una muestra (), y lo compara con la intensidad de la luz reflejada de un material de referencia () (como una baldosa blanca). La relación se llama reflectancia, y se expresa generalmente como porcentaje (%R).
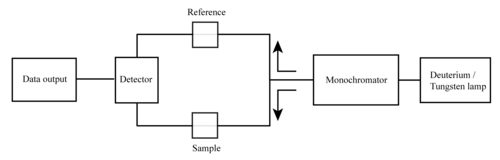
Las partes básicas de un espectrofotómetro son una fuente de luz, un soporte para la muestra, una rejilla de difracción en un monocromador o un prisma para separar las diferentes longitudes de onda de la luz y un detector. La fuente de radiación suele ser un filamento de tungsteno (300–2500 nm), una lámpara de arco de deuterio, que es continua en la región ultravioleta (190–400 nm), una lámpara de arco de xenón, que es continua desde 160 a 2000 nm; o más recientemente, diodos emisores de luz (LED) para las longitudes de onda visibles. El detector suele ser un tubo fotomultiplicador, un fotodiodo, una matriz de fotodiodos o un dispositivo de carga acoplada (CCD). Los detectores de fotodiodo único y los tubos fotomultiplicadores se utilizan con monocromadores de barrido, que filtran la luz para que solo la luz de una sola longitud de onda llegue al detector a la vez. El monocromador de barrido mueve la rejilla de difracción a "paso a paso" cada longitud de onda para que su intensidad pueda medirse en función de la longitud de onda. Los monocromadores fijos se utilizan con CCD y conjuntos de fotodiodos. Como ambos dispositivos consisten en muchos detectores agrupados en conjuntos de una o dos dimensiones, pueden recolectar luz de diferentes longitudes de onda en diferentes píxeles o grupos de píxeles simultáneamente.
Un espectrofotómetro puede ser solo haz o doble viga. En un solo instrumento de haz (como el Spectronic 20), toda la luz pasa a través de la célula de muestra. debe medirse eliminando la muestra. Este fue el diseño más antiguo y sigue en uso común tanto en laboratorios de enseñanza como industriales.
En un instrumento de doble haz, la luz se divide en dos haces antes de llegar a la muestra. Se utiliza un haz como referencia; el otro haz pasa a través de la muestra. La intensidad del haz de referencia se toma como 100 % de transmisión (o 0 de absorbancia), y la medida que se muestra es la relación de las dos intensidades del haz. Algunos instrumentos de doble haz tienen dos detectores (fotodiodos), y la muestra y el haz de referencia se miden al mismo tiempo. En otros instrumentos, los dos rayos pasan a través de un interruptor de rayos, que bloquea un rayo a la vez. El detector alterna entre medir el haz de muestra y el haz de referencia en sincronismo con el cortador. También puede haber uno o más intervalos oscuros en el ciclo del helicóptero. En este caso, las intensidades de haz medidas pueden corregirse restando la intensidad medida en el intervalo oscuro antes de tomar la relación.
En un instrumento de un solo haz, la cubeta que contiene solo un solvente debe medirse primero. Mettler Toledo desarrolló un espectrofotómetro de haz único que permite mediciones rápidas y precisas en el rango UV/VIS. La fuente de luz consiste en una lámpara de flash de xenón para las regiones de longitud de onda ultravioleta (UV), visible (VIS) e infrarrojo cercano que cubren un rango espectral de 190 a 1100 nm. Los destellos de la lámpara se enfocan en una fibra de vidrio que dirige el haz de luz hacia una cubeta que contiene la solución de muestra. El haz pasa a través de la muestra y los componentes de la muestra absorben longitudes de onda específicas. La luz restante se recoge después de la cubeta mediante una fibra de vidrio y se conduce a un espectrógrafo. El espectrógrafo consta de una rejilla de difracción que separa la luz en diferentes longitudes de onda y un sensor CCD para registrar los datos, respectivamente. De este modo, todo el espectro se mide simultáneamente, lo que permite un registro rápido.
Las muestras para la espectrofotometría UV/Vis son muy a menudo líquidos, aunque también se puede medir la absorción de gases e incluso de sólidos. Las muestras se colocan típicamente en una celda transparente, conocida como cuvette. Las cuvettes son típicamente rectangulares en forma, comúnmente con un ancho interno de 1 cm. (Este ancho se convierte en la longitud del camino, , en la ley Beer-Lambert.) Los tubos de prueba también se pueden utilizar como cuvettes en algunos instrumentos. El tipo de contenedor de muestra utilizado debe permitir que la radiación pase sobre la región espectral de interés. Las cuvettes más ampliamente aplicables están hechas de silica fundida de alta calidad o cristal de cuarzo porque son transparentes en todas las regiones UV, visibles y cercanas a infrarrojos. Las cubetas de vidrio y plástico también son comunes, aunque el vidrio y la mayoría de los plásticos absorben en la UV, lo que limita su utilidad a longitudes de onda visibles.
También se han fabricado instrumentos especializados. Estos incluyen adjuntar espectrofotómetros a los telescopios para medir los espectros de las características astronómicas. Los microespectrofotómetros UV-visible consisten en un microscopio UV-visible integrado con un espectrofotómetro UV-visible.
A menudo, un espectrofotómetro más sofisticado puede producir directamente un espectro completo de la absorción en todas las longitudes de onda de interés. En instrumentos más simples, la absorción se determina una longitud de onda a la vez y luego el operador la compila en un espectro. Eliminando la dependencia de la concentración, el coeficiente de extinción (ε) se puede determinar en función de la longitud de onda.
Microespectrofotometría
La espectroscopia UV-visible de muestras microscópicas se realiza integrando un microscopio óptico con óptica UV-visible, fuentes de luz blanca, un monocromador y un detector sensible, como un dispositivo de carga acoplada (CCD) o un tubo fotomultiplicador (PMT).. Como solo se dispone de un único camino óptico, estos son instrumentos de un solo haz. Los instrumentos modernos son capaces de medir espectros UV-visibles tanto en reflectancia como en transmisión de áreas de muestreo a escala micrométrica. Las ventajas de usar tales instrumentos es que pueden medir muestras microscópicas pero también pueden medir los espectros de muestras más grandes con alta resolución espacial. Como tal, se utilizan en el laboratorio forense para analizar los tintes y pigmentos en fibras textiles individuales, partículas de pintura microscópicas y el color de fragmentos de vidrio. También se utilizan en la ciencia de los materiales y la investigación biológica y para determinar el contenido de energía de las rocas generadoras de carbón y petróleo midiendo la reflectancia de la vitrinita. Los microespectrofotómetros se utilizan en las industrias de semiconductores y microóptica para monitorear el espesor de películas delgadas después de que han sido depositadas. En la industria de los semiconductores, se utilizan porque las dimensiones críticas de los circuitos son microscópicas. Una prueba típica de una oblea de semiconductor implicaría la adquisición de espectros de muchos puntos en una oblea con o sin patrón. El espesor de las películas depositadas se puede calcular a partir del patrón de interferencia de los espectros. Además, la espectrofotometría ultravioleta-visible se puede utilizar para determinar el espesor, junto con el índice de refracción y el coeficiente de extinción de películas delgadas. A continuación, se puede generar un mapa del espesor de la película en toda la oblea y utilizarlo con fines de control de calidad.
Aplicaciones adicionales
UV/Vis se puede aplicar para caracterizar la velocidad de una reacción química. Es ilustrativa la conversión de los isómeros amarillo-naranja y azul del ditizonato de mercurio. Este método de análisis se basa en el hecho de que la concentración es linealmente proporcional a la concentración. En el mismo enfoque permite la determinación de equilibrios entre cromóforos.
A partir del espectro de gases quemados, es posible determinar la composición química de un combustible, la temperatura de los gases y la relación aire-combustible.
Contenido relacionado
Disipación
Holografía
James dewar