Escudo Dalkon
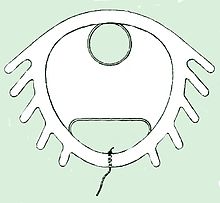
El Dalkon Shield era un dispositivo intrauterino (DIU) anticonceptivo desarrollado por Dalkon Corporation y comercializado por A.H. Robins Company. Se descubrió que el Escudo Dalkon causaba lesiones graves a un porcentaje desproporcionadamente grande de mujeres, lo que eventualmente dio lugar a numerosas demandas, en las que los jurados otorgaron millones de dólares en daños compensatorios y punitivos.
Historia

Hugh J. Davis, M.D., médico, e Irwin Lerner, ingeniero eléctrico, inventaron y solicitaron una patente para el Dalkon Shield en 1968. Dalkon Corporation tenía sólo cuatro accionistas: los inventores Davis y Lerner, su abogado. Robert Cohn y Thad J. Earl, M.D., médico de Defiance, Ohio. En 1970, A.H. Robins Company adquirió Dalkon Shield de Dalkon Corporation. En enero de 1971, Dalkon Shield salió al mercado, comenzando en Estados Unidos y Puerto Rico, encabezado por una gran campaña de marketing. En su apogeo, alrededor de 2,8 millones de mujeres utilizaron el Escudo Dalkon en los EE. UU.
En el momento de su introducción, Dalkon Shield se promocionó como una alternativa más segura en comparación con las píldoras anticonceptivas, que en ese momento eran objeto de muchas preocupaciones de seguridad. El propio Dr. Davis participó en las audiencias de Nelson de 1970, que fueron audiencias en el Congreso dirigidas por el senador Gaylord Nelson sobre la seguridad de los anticonceptivos orales. Afirmó que los anticonceptivos orales con altas dosis de hormonas eran peligrosos y que la eficacia de la píldora estaba "muy sobrevalorada".
Defecto de diseño
Mientras buscaban un material para la cuerda de cola, Davis y Learner descubrieron Supramid. Supramid era un material de sutura similar a un cable hecho de cientos de finas fibras internas de nailon revestidas por una funda exterior de nailon suave que se usaba comúnmente para reparar desgarros en los tendones de los caballos. En 1971, un supervisor de control de calidad descubrió que las cuerdas eran capaces de absorber el agua y sugirió sellar con calor los extremos de la cuerda para formar una barrera contra la mecha, pero la gerencia rechazó la idea por considerarla prohibitiva. Además de la capacidad del hilo para absorber las bacterias, el hilo también tenía propensión a deteriorarse dentro del cuerpo, lo que agrega riesgos adicionales y brinda a las bacterias otra vía para ingresar al hilo. Estas propiedades permitieron que las bacterias pasaran a través del cuello uterino hasta el útero, sin pasar por el moco cervical, que normalmente actúa como una barrera contra las infecciones.
Los informes iniciales en la literatura médica plantearon dudas sobre si su eficacia para prevenir el embarazo y la tasa de expulsión eran tan buenas como las afirmadas por el fabricante, pero no detectaron la tendencia del dispositivo a causar aborto séptico y otras infecciones graves.
Infecciones
En junio de 1973, los Centros para el Control y la Prevención de Enfermedades (CDC) llevaron a cabo una encuesta de 34,544 médicos con prácticas en ginecología u obstetricia sobre mujeres que habían sido hospitalizadas o habían muerto por complicaciones relacionadas con el uso de un DIU en el año anterior. 6 meses. Respondieron un total de 16.994 médicos, lo que produjo 3.502 informes de casos únicos de mujeres hospitalizadas en los primeros 6 meses de 1973. Con base en la tasa de respuesta de la encuesta, los CDC estimaron que durante este período de 6 meses se produjeron un total de 7.900 hospitalizaciones relacionadas con el DIU. Con base en una estimación de 3,2 millones de usuarias de DIU, los CDC estimaron una tasa anual de hospitalización relacionada con el dispositivo de 5 por 1000 usuarias de DIU. La encuesta también proporcionó cinco informes de muertes relacionadas con dispositivos, cuatro de ellos relacionados con infecciones graves. Uno de los cinco estaba asociado con el Escudo Dalkon. Con base en estos datos, los CDC estimaron una tasa de mortalidad relacionada con el DIU de 3 por millón de usuarias por año de uso, que comparó favorablemente con los riesgos de mortalidad asociados con el embarazo y otras formas de anticoncepción. Es importante destacar que la encuesta mostró que el Escudo Dalkon se asoció con una mayor tasa de complicaciones asociadas al embarazo que condujeron a la hospitalización.
En 1974, aproximadamente 2,5 millones de mujeres habían recibido el dispositivo intrauterino Dalkon. En junio de ese año, el director médico de A.H. Robins publicó una carta al editor del British Medical Journal afirmando que la empresa estaba al tanto de un "aparente aumento en el número de casos de abortos sépticos" incluidas 4 muertes, pero afirmando que "no hay evidencia de una relación directa de causa y efecto entre el uso del Escudo Dalkon y la aparición de septicemia". La carta recomendaba precauciones que incluían pruebas de embarazo para las mujeres que no tenían su período y la retirada inmediata del dispositivo en las mujeres que estaban embarazadas. Ese mismo mes, A.H. Robins suspendió las ventas del dispositivo en los Estados Unidos a instancias de la Administración de Alimentos y Medicamentos. En octubre de 1974, se publicó una serie de cuatro informes de casos de embarazos sépticos en la revista Obstretics and Gynecology. En 1975, el CDC publicó un estudio que asociaba el Escudo Dalkon con un mayor riesgo de aborto espontáneo relacionado con muerte en comparación con otros DIU.
Unas 200.000 mujeres presentaron reclamaciones contra la empresa A.H. Robins, en su mayoría relacionadas con reclamaciones asociadas con la enfermedad inflamatoria pélvica y la pérdida de fertilidad. La empresa finalmente se declaró en quiebra. Los representantes de la empresa argumentaron que las infecciones pélvicas tienen una amplia variedad de causas y que el Escudo Dalkon no era más peligroso que otras formas de control de la natalidad. Los abogados de los demandantes argumentaron que las mujeres que representaban hoy estarían sanas y fértiles si no fuera por el dispositivo. Los científicos de los CDC afirmaron que ambos argumentos tienen fundamento.
Consecuencias
Se presentaron más de 327.000 demandas y reclamaciones contra A.H. Robins Company, el mayor caso de responsabilidad extracontractual desde el amianto. El juez federal, Miles W. Lord, atrajo comentarios públicos por sus sentencias, imposiciones de responsabilidad personal y reprimendas públicas a los directores de las empresas. El costo de los litigios y los acuerdos (estimados en miles de millones de dólares) llevó a la empresa a acogerse al Capítulo 11 de protección por quiebra en agosto de 1985. Como resultado, A.H. Robins fue comprada por American Home Products (ahora Wyeth) en 1989. En ese momento, Más de 7.000 australianos estaban demandando a la empresa en relación con embarazos, enfermedades inflamatorias pélvicas, embarazos ectópicos, abortos sépticos espontáneos y perforación de útero.
En 1976, las Enmiendas de Dispositivos Médicos a la Ley de Alimentos, Medicamentos y Cosméticos obligaron a la Administración de Alimentos y Medicamentos de EE. UU., por primera vez, a exigir pruebas y aprobación de "dispositivos médicos", incluidos los DIU.
El Dalkon Shield se hizo famoso por su grave defecto de diseño: una cuerda multifilamento porosa sobre la cual las bacterias podían viajar hasta el útero de los usuarios, provocando sepsis, lesiones, abortos espontáneos y la muerte. Los dispositivos intrauterinos (DIU) modernos utilizan hilos de monofilamento, que no plantean este grave riesgo para los usuarios.
Contenido relacionado
Paroxetina
Plexo
Osteoporosis