Entonces hombre
Somán (o GD, EA 1210, Zomán, PFMP, A-255, nombre sistemático: O-metilfosfonofluoridato de pinacolilo) es una sustancia química extremadamente tóxica. Es un agente nervioso que interfiere con el funcionamiento normal del sistema nervioso de los mamíferos al inhibir la enzima colinesterasa. Es un inhibidor tanto de la acetilcolinesterasa como de la butirilcolinesterasa. Como arma química, está clasificada como arma de destrucción masiva por las Naciones Unidas de acuerdo con la Resolución 687 de la ONU. Su producción está estrictamente controlada y el almacenamiento está prohibido por la Convención de Armas Químicas de 1993, donde está clasificada como una sustancia de la Lista 1.. Soman fue el tercero de los llamados agentes nerviosos de la serie G que se descubrió junto con GA (tabún), GB (sarín) y GF (ciclosarín).
Cuando es puro, el somán es un líquido volátil, corrosivo e incoloro con un ligero olor a naftalina o fruta podrida. Más comúnmente, es de color amarillo a marrón y tiene un olor fuerte descrito como similar al alcanfor. La LCt50 para el somán es de 70 mg·min/m3 en humanos.
GD se puede espesar para usar como aerosol químico usando un copolímero acriloide. También se puede implementar como un arma química binaria; sus precursores químicos son el difluoruro de metilfosfonilo y una mezcla de alcohol pinacolílico y una amina.
Historia
Después de la Primera Guerra Mundial, durante la cual se usaron gas mostaza y fosgeno como agentes de guerra química, se firmó el Protocolo de Ginebra de 1925 en un intento de prohibir la guerra química. Sin embargo, continuaron las investigaciones sobre agentes de guerra química y su uso. En 1936, se descubrió un nuevo agente químico más peligroso cuando Gerhard Schrader de IG Farben en Alemania aisló tabun (llamado GA por el Agente A alemán en los Estados Unidos), el primer agente nervioso, mientras desarrollaba nuevos insecticidas. Este descubrimiento fue seguido por el aislamiento de sarín (designado GB por los Estados Unidos) en 1938, también descubierto por Schrader.
Durante la Segunda Guerra Mundial, la investigación sobre agentes nerviosos continuó en los Estados Unidos y Alemania. En el verano de 1944, los alemanes desarrollaron el somán, un líquido incoloro con olor a alcanfor (designado GD por los Estados Unidos). Soman demostró ser incluso más tóxico que el tabún y el sarín. El premio Nobel Richard Kuhn junto con Konrad Henkel descubrieron el somán durante la investigación sobre la farmacología del tabún y el sarín en el Instituto Kaiser Wilhelm de Investigación Médica en Heidelberg. Esta investigación fue encargada por el ejército alemán. Soman se produjo en pequeñas cantidades en una planta piloto en la fábrica de IG Farben en Ludwigshafen. Nunca se usó en la Segunda Guerra Mundial.
La Convención sobre Armas Químicas de 1993 prohibió la producción o el almacenamiento de somán. Cuando la convención entró en vigor, las partes declararon reservas mundiales de 9.057 toneladas de somán. A diciembre de 2015 se había destruido el 84% de los acopios.
La estructura cristalina del somán complejado con acetilcolinesterasa fue determinada por Millard et al. en 1999 por cristalografía de rayos X: 1som. Otras estructuras de acetilcolinesterasa resueltas con soman unido a ellas incluyen 2wfz, 2wg0 y 2wg1.
Estructura y reactividad
Soman (C(±)P(±)-soman) tiene cuatro estereoisómeros, cada uno con una toxicidad diferente, aunque muy similar. Los estereoisómeros son C(+)P(+)-soman, C(+)P(-)-soman C(-)P(-)-soman y C(-)P(+)-soman.
Soman tiene un grupo fosfonilo con un fluoruro y un hidrocarburo (grande) unido covalentemente. Por lo tanto, la estructura es similar a la del sarín, que tiene solo un grupo hidrocarburo más pequeño adjunto (isopropilo). Debido a la similitud entre las estructuras químicas, la reactividad de los dos compuestos es casi la misma. Tanto el soman como el sarín reaccionarán utilizando el grupo fosfooxígeno, que puede unirse a aminoácidos como la serina.
Síntesis
La fabricación de somán es muy similar a la fabricación de sarín. La diferencia es que el isopropanol de los procesos de sarín se reemplaza con alcohol pinacolílico:
El somán se sintetiza haciendo reaccionar alcohol pinacolílico con difluoruro de metilfosfonilo. El resultado de esta reacción es la formación de soman, que se describe como “líquido incoloro con un olor algo afrutado”. La baja presión de vapor del somán también producirá la forma gaseosa volátil del somán. Además, el fluoruro de hidrógeno ácido se formará debido a la eliminación de fluoruro y un protón. Este ácido es indirectamente peligroso para los humanos. El contacto de la piel con fluoruro de hidrógeno provocará una reacción inmediata con el agua que produce ácido fluorhídrico.
Mecanismos de acción
Soman es un agente nervioso organofosforado con un mecanismo de acción similar al Tabun. Los agentes nerviosos inhiben la acetilcolina esterasa (AChE) al formar un aducto con la enzima a través de un residuo de serina en esa enzima. Estos aductos pueden descomponerse hidrolíticamente o, por ejemplo, por la acción de algunas oximas y así regenerar la enzima. Un segundo tipo de reacción, en el que el complejo enzima-organofosfato (OP) sufre una reacción posterior, suele describirse como "envejecimiento". Una vez que el complejo enzima-OP ha envejecido, ya no es regenerado por los reactivadores de oxima comunes. La velocidad de este proceso depende del OP. Soman es un OP que estimula la tasa de envejecimiento más rápidamente disminuyendo la vida media a solo unos minutos.
AChE es una enzima involucrada en la neurotransmisión. Debido a la severa disminución de la vida media de esta enzima, la neurotransmisión se suprime en cuestión de minutos.
Metabolismo
Una vez absorbido en el cuerpo humano, el somán no solo inhibe la AChE, sino que también es un sustrato para otras esterasas. La reacción de soman con estas esterasas permite la desintoxicación del compuesto. No se conocen reacciones de intoxicación metabólica para el somán.
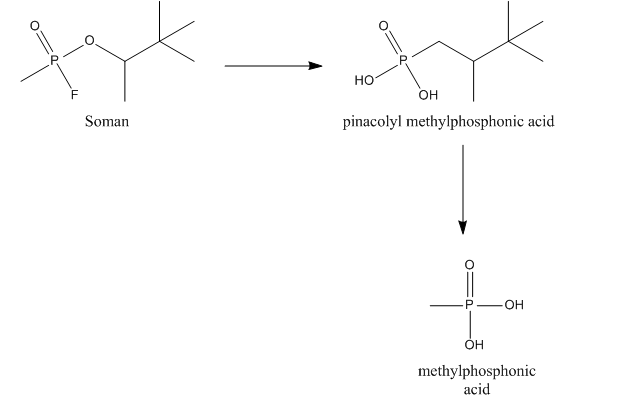
Soman puede ser hidrolizado por una denominada A-esterasa, más específicamente una diisopropilfluorofosfatasa. Esta esterasa, también llamada somanasa, reacciona con el enlace anhídrido entre el fósforo y el flúor y es responsable de la hidrólisis del fluoruro. La somanasa también hidroliza el grupo metilo del somán, lo que da como resultado la formación de ácido pinacolil metilfosfónico (PMPA), que es un inhibidor de la AChE menos potente.
Soman también puede unirse a otras esterasas, por ejemplo, AChE, colinesterasa (ChE) y carboxilesterasas (CarbE). En esta unión, el somán pierde su fluoruro. Después de unirse a AChE o ChE, el somán también pierde su grupo fosforilo, lo que lleva a la formación de ácido metilfosfónico (MPA). La unión a CarbE reduce la concentración total de somán en la sangre, lo que da como resultado una menor toxicidad. Además, CarbE participa en la desintoxicación al hidrolizar el somán a PMPA. Entonces, CarbE explica la desintoxicación de soman de dos maneras.
La importancia de la desintoxicación del somán después de la exposición se ilustró en los experimentos de Fonnum y Sterri (1981). Informaron que solo el 5 % de la DL50 inhibía la AChE en ratas, lo que provocaba efectos tóxicos agudos. Esto muestra que las reacciones metabólicas explicaron la desintoxicación del 95% restante de la dosis.
Signos y síntomas
Como el somán está estrechamente relacionado con compuestos como el sarín, las indicaciones para una intoxicación por somán son relativamente similares. Uno de los primeros signos observables de una intoxicación por soman es la miosis. Algunas, pero no todas, las indicaciones posteriores son vómitos, dolor muscular extremo y problemas del sistema nervioso periférico. Esos síntomas aparecen tan pronto como 10 minutos después de la exposición y pueden durar muchos días.
Además de los efectos tóxicos directos sobre el sistema nervioso, las personas expuestas al somán pueden experimentar efectos a largo plazo, la mayoría de los cuales son psicológicos. Los sujetos que estuvieron expuestos a una pequeña dosis de somán sufrieron graves efectos tóxicos; una vez tratados, los sujetos a menudo desarrollaron depresión, tenían pensamientos antisociales, estaban retraídos y apagados, dormían inquietos y tenían pesadillas. Estos síntomas duraron seis meses después de la exposición pero desaparecieron sin daño duradero.
Toxicidad y eficacia
Se estima que la CL50 de soman en el aire es de 70 mg min por m3. En comparación con el valor de LC50 de una rata, la concentración letal humana es mucho más baja (954,3 mg min/m3 frente a 70 mg min/m3). Para compuestos como el somán, que también puede usarse como arma, a menudo una fracción de la dosis LC50 es donde aparecen los primeros efectos. La miosis es uno de los primeros síntomas de intoxicación por soman y se puede observar en dosis inferiores al 1 % de la LC50.
Efectos en animales
Se han realizado experimentos en los que se expuso a ratas a soman para comprobar si se podían observar efectos conductuales en dosis bajas sin generar síntomas manifiestos. La exposición de las ratas a soman en una dosis de menos del 3 por ciento de la LD50 provocó alteraciones del comportamiento. La evitación activa de las ratas expuestas fue menor que la evitación de las ratas no expuestas (experimento de caja de lanzadera bidireccional). También se vieron afectados la coordinación motora (tarea de paso de obstáculos), el comportamiento de campo abierto y el comportamiento de evitación activa y pasiva. Se puede concluir que las ratas que están expuestas a soman se desempeñaron con menos éxito en tareas que requieren actividad motora y la función de estructuras superiores del sistema nervioso central (SNC) al mismo tiempo. En esto, soman tiene un efecto predominantemente central.
El conocimiento de los efectos de dosis bajas de soman y otros inhibidores de la esterasa de colina en ratas podría posiblemente usarse para explicar la incidencia relativamente alta de accidentes de avión debido a errores de los pilotos agrícolas. Si este conocimiento pudiera aplicarse a los seres humanos, se podría explicar esta alta incidencia con la disminución de la actividad de la colina esterasa debido a la exposición a pesticidas. No se sabe si se puede hacer la extrapolación de ratas a humanos.
Contenido relacionado
Β-nitruro de carbono
Evolución química
Alfonso María Jakob