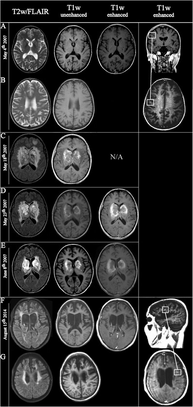
Encefalomielitis diseminada aguda
La encefalomielitis diseminada aguda (ADEM), o encefalomielitis desmielinizante aguda, es una enfermedad autoinmune rara caracterizada por un ataque súbito y generalizado de inflamación en el cerebro y la médula espinal. Además de causar que el cerebro y la médula espinal se inflamen, ADEM también ataca los nervios del sistema nervioso central y daña su aislamiento de mielina, lo que, como resultado, destruye la materia blanca. A menudo se desencadena por una infección viral o vacunas.
Los síntomas de ADEM se asemejan a los síntomas de la esclerosis múltiple (EM), por lo que la enfermedad en sí se clasifica en la clasificación de las enfermedades limítrofes de la esclerosis múltiple. Sin embargo, ADEM tiene varias características que lo distinguen de MS. A diferencia de la EM, ADEM ocurre generalmente en niños y se caracteriza por fiebre rápida, aunque los adolescentes y adultos también pueden contraer la enfermedad. ADEM consiste en un solo brote, mientras que la EM se caracteriza por varios brotes (o recaídas), durante un largo período de tiempo. Se notifican recaídas después de ADEM en hasta una cuarta parte de los pacientes, pero la mayoría de estas enfermedades 'multifásicas' las presentaciones posteriores a ADEM probablemente representen a la EM. ADEM también se distingue por una pérdida de conciencia, coma y muerte, lo cual es muy raro en la EM, excepto en casos severos.
Afecta a aproximadamente 8 de cada 1.000.000 de personas al año. Aunque se presenta en todas las edades, la mayoría de los casos reportados son en niños y adolescentes, con una edad promedio de 5 a 8 años. La enfermedad afecta a hombres y mujeres casi por igual. ADEM muestra una variación estacional con mayor incidencia en los meses de invierno y primavera, lo que puede coincidir con mayores infecciones virales durante estos meses. La tasa de mortalidad puede llegar al 5%; sin embargo, la recuperación completa se observa en el 50 al 75 % de los casos con un aumento en las tasas de supervivencia de hasta el 70 al 90 % con cifras que incluyen también una discapacidad residual menor. El tiempo promedio para recuperarse de los brotes de ADEM es de uno a seis meses.
ADEM produce múltiples lesiones inflamatorias en el cerebro y la médula espinal, particularmente en la sustancia blanca. Por lo general, se encuentran en la sustancia blanca subcortical y central y en la unión gris-blanca cortical de ambos hemisferios cerebrales, el cerebelo, el tronco del encéfalo y la médula espinal, pero también pueden estar involucradas la sustancia blanca periventricular y la sustancia gris de la corteza, los tálamos y los ganglios basales.
Cuando una persona tiene más de un episodio desmielinizante de ADEM, la enfermedad se denomina encefalomielitis diseminada recurrente o encefalomielitis diseminada multifásica (MDEM). También se ha descrito un curso fulminante en adultos.
Signos y síntomas
ADEM tiene un inicio abrupto y un curso monofásico. Los síntomas generalmente comienzan de 1 a 3 semanas después de la infección. Los principales síntomas incluyen fiebre, dolor de cabeza, náuseas y vómitos, confusión, deterioro de la visión, somnolencia, convulsiones y coma. Aunque inicialmente los síntomas suelen ser leves, empeoran rápidamente en el transcurso de horas o días, con un tiempo promedio de máxima gravedad de aproximadamente cuatro días y medio. Los síntomas adicionales incluyen hemiparesia, paraparesia y parálisis de los nervios craneales.
ADEM en COVID-19
Los síntomas neurológicos fueron la principal presentación de la COVID-19, que no se correlacionó con la gravedad de los síntomas respiratorios. Llama la atención la alta incidencia de ADEM con hemorragia. Es probable que la inflamación cerebral sea causada por una respuesta inmunitaria a la enfermedad y no por un neurotropismo. El análisis del LCR no fue indicativo de un proceso infeccioso, el deterioro neurológico no estuvo presente en la fase aguda de la infección y los hallazgos de neuroimagen no fueron típicos de los trastornos tóxicos y metabólicos clásicos. El hallazgo de lesiones periventriculares bilaterales relativamente asimétricas aliadas con afectación profunda de la sustancia blanca, que también pueden estar presentes en la unión de la sustancia blanca grisácea cortical, tálamos, ganglios basales, cerebelo y tronco encefálico, sugiere un proceso agudo de desmielinización. Además, también se encontraron lesiones hemorrágicas de sustancia blanca, grupos de macrófagos relacionados con lesión axonal y apariencia similar a ADEM en la sustancia blanca subcortical.
Causas
Desde el descubrimiento de la especificidad anti-MOG frente al diagnóstico de esclerosis múltiple se considera que la ADEM es una de las posibles causas clínicas de encefalomielitis asociada a anti-MOG.
Sobre cómo aparecen los anticuerpos anti-MOG en el suero de los pacientes existen varias teorías:
- Un desafío antígeno anterior se puede identificar en aproximadamente dos tercios de las personas. Algunas infecciones virales pensaban inducir ADEM incluyen virus de influenza, dengue, enterovirus, sarampión, paperas, rubéola, varicella zoster, virus Epstein-Barr, citomegalovirus, virus herpes simplex, hepatitis A, coxsackievirus y COVID-19. Las infecciones bacterianas incluyen Mycoplasma pneumoniae, Borrelia burgdorferi, Leptospira y Streptococci beta-hemolítica.
- Exposición a vacunas: La única vacuna probada relacionada con ADEM es la forma Semple de la vacuna contra la rabia, pero la hepatitis B, la pertussis, la difteria, el sarampión, las paperas, la rubéola, el neumoco, la varicela, la gripe, la encefalitis japonesa y las vacunas contra la poliomielitis han sido implicadas. La mayoría de los estudios que correlacionan la vacuna con el inicio del ADEM utilizan pequeñas muestras o estudios de casos. Los estudios epidemiológicos a gran escala (por ejemplo, de la vacuna MMR o la vacuna contra la viruela) no muestran un mayor riesgo de ADEM después de la vacunación. Un límite superior para el riesgo de ADEM de vacunación contra el sarampión, si existe, se puede estimar que es 10 por millón, que es mucho menor que el riesgo de desarrollar ADEM de una infección de sarampión real, que es aproximadamente 1 por 1.000 casos. Para una infección de rubéola, el riesgo es 1 por 5.000 casos. Algunas vacunas tempranas, más tarde se mostraron contaminadas con tejido anfitriona de naftalenos clorados, tenían tasas de incidencia de ADEM tan altas como 1 en 600.
- En casos raros, el ADEM parece seguir de trasplante de órganos.
Diagnóstico
El término ADEM se ha utilizado de manera inconsistente en diferentes momentos. Actualmente, el estándar internacional comúnmente aceptado para la definición de caso clínico es el publicado por el International Pediatric MS Study Group, revisión 2007.
Dado que la definición es clínica, actualmente se desconoce si todos los casos con ADEM son positivos para autoanticuerpos anti-MOG, pero en cualquier caso, parece estar fuertemente relacionado con el diagnóstico de ADEM.
Diagnóstico diferencial
Esclerosis múltiple
Si bien la ADEM y la EM involucran desmielinización autoinmune, difieren en muchos aspectos clínicos, genéticos, de imágenes e histopatológicos. Algunos autores consideran que la EM y sus formas límite constituyen un espectro, difiriendo únicamente en la cronicidad, la gravedad y el curso clínico, mientras que otros las consideran enfermedades discretamente diferentes.
Por lo general, ADEM aparece en niños después de un desafío antigénico y permanece monofásico. Sin embargo, ADEM ocurre en adultos y también puede ser clínicamente multifásico.
Los problemas para el diagnóstico diferencial aumentan debido a la falta de acuerdo para una definición de esclerosis múltiple. Si la EM se definiera únicamente por la separación en el tiempo y el espacio de las lesiones desmielinizantes como hizo McDonald, no sería suficiente para marcar la diferencia, ya que algunos casos de ADEM cumplen estas condiciones. Por ello, algunos autores proponen establecer la línea de separación en la forma de las lesiones alrededor de las venas, siendo por tanto "desmielinización perivenosa vs. confluente".
La patología de ADEM es muy similar a la de la EM con algunas diferencias. El sello patológico de ADEM es la inflamación perivenular con "mangas de desmielinización" limitadas. Sin embargo, pueden aparecer placas tipo EM (desmielinización confluente)
Las placas en la materia blanca en la EM están claramente delineadas, mientras que la cicatriz glial en la ADEM es suave. Los axones están mejor conservados en las lesiones ADEM. La inflamación en la ADEM es muy diseminada y mal delimitada y, por último, las lesiones son estrictamente perivenosas, mientras que en la EM se disponen alrededor de las venas, pero no de forma tan marcada.
Sin embargo, la coexistencia de desmielinización perivenosa y confluente en algunos individuos sugiere una superposición patogénica entre la encefalomielitis aguda diseminada y la esclerosis múltiple, y la clasificación errónea incluso con biopsia o incluso ADEM post mortem en adultos puede progresar a EM
Encefalomielitis diseminada multifásica
Cuando la persona tiene más de un episodio desmielinizante de ADEM, la enfermedad se denomina encefalomielitis diseminada recurrente o encefalomielitis diseminada multifásica (MDEM).
Se ha encontrado que los autoanticuerpos anti-MOG están relacionados con este tipo de ADEM
Se ha descrito otra variante de ADEM en adultos, también relacionada con autoanticuerpos anti-MOG, que se ha denominado encefalomielitis diseminada fulminante y se ha informado que clínicamente es ADEM, pero que muestra lesiones similares a las de la EM en la autopsia. Se ha clasificado dentro de las enfermedades inflamatorias desmielinizantes asociadas a anti-MOG.
Leucoencefalitis hemorrágica aguda
La leucoencefalitis hemorrágica aguda (AHL o AHLE), la encefalomielitis hemorrágica aguda (AHEM), la leucoencefalitis hemorrágica necrotizante aguda (ANHLE), el síndrome de Weston-Hurst o la enfermedad de Hurst, es una forma hiperaguda y con frecuencia fatal de ADEM. La AHL es relativamente rara (se han informado menos de 100 casos en la literatura médica a partir de 2006), se observa en aproximadamente el 2% de los casos de ADEM y se caracteriza por vasculitis necrosante de las vénulas y hemorragia y edema. La muerte es común en la primera semana y la mortalidad general es de alrededor del 70%, pero la creciente evidencia apunta a resultados favorables después del tratamiento intensivo con corticosteroides, inmunoglobulinas, ciclofosfamida y plasmaféresis. Alrededor del 70% de los sobrevivientes muestran déficits neurológicos residuales, pero algunos sobrevivientes han mostrado un déficit sorprendentemente pequeño considerando la magnitud de la sustancia blanca afectada.
Esta enfermedad se ha asociado ocasionalmente con colitis ulcerosa y enfermedad de Crohn, paludismo, sepsis asociada con el depósito de inmunocomplejos, intoxicación por metanol y otras afecciones subyacentes. También se ha informado una asociación anecdótica con la EM.
Los estudios de laboratorio que respaldan el diagnóstico de AHL son: leucocitosis periférica, pleocitosis del líquido cefalorraquídeo (LCR) asociada con glucosa normal y aumento de proteínas. En las imágenes por resonancia magnética (MRI), las lesiones de AHL generalmente muestran hiperintensidades extensas de la sustancia blanca ponderadas en T2 y con recuperación de la inversión atenuada por líquido (FLAIR) con áreas de hemorragias, edema significativo y efecto de masa.
Tratamiento
No se han realizado ensayos clínicos controlados sobre el tratamiento con ADEM, pero el estándar es un tratamiento agresivo destinado a reducir rápidamente la inflamación del SNC. El tratamiento de primera línea ampliamente aceptado son las dosis altas de corticosteroides intravenosos, como la metilprednisolona o la dexametasona, seguidas de 3 a 6 semanas de dosis orales gradualmente más bajas de prednisolona. Los pacientes tratados con metilprednisolona han mostrado mejores resultados que los tratados con dexametasona. Las disminuciones orales de menos de tres semanas de duración muestran una mayor probabilidad de recaída y tienden a mostrar peores resultados. Se ha informado que otras terapias antiinflamatorias e inmunosupresoras muestran un efecto beneficioso, como la plasmaféresis, altas dosis de inmunoglobulina intravenosa (IgIV), mitoxantrona y ciclofosfamida. Estas se consideran terapias alternativas, utilizadas cuando los corticosteroides no se pueden usar o no muestran un efecto.
Existe cierta evidencia que sugiere que los pacientes pueden responder a una combinación de metilprednisolona e inmunoglobulinas si no responden a ninguno de los dos por separado. En un estudio de 16 niños con ADEM, 10 se recuperaron por completo después de una dosis alta de metilprednisolona, un caso grave que no respondió a los esteroides se recuperó por completo después de IV Ig; los cinco casos más graves, con ADAM y neuropatía periférica grave, fueron tratados con dosis altas combinadas de metilprednisolona e inmunoglobulina, dos quedaron parapléjicos, uno tenía discapacidades motoras y cognitivas y dos se recuperaron. Una revisión reciente del tratamiento de ADEM con IgIV (de la cual el estudio anterior constituyó la mayor parte de los casos) encontró que el 70 % de los niños mostró una recuperación completa después del tratamiento con IgIV o IgIV más corticosteroides. Un estudio del tratamiento con IgIV en adultos con ADEM mostró que la IgIV parece más eficaz en el tratamiento de trastornos sensoriales y motores, mientras que los esteroides parecen más eficaces en el tratamiento de deficiencias cognitivas, de conciencia y de rigor. Este mismo estudio encontró un sujeto, un hombre de 71 años que no había respondido a los esteroides, que respondió a un tratamiento con IgIV 58 días después del inicio de la enfermedad.
Pronóstico
La recuperación completa se observa en el 50 al 70 % de los casos, con un rango de recuperación del 70 al 90 % con alguna discapacidad residual menor (generalmente evaluada mediante medidas como mRS o EDSS), el tiempo promedio de recuperación es de uno a seis meses. La tasa de mortalidad puede ser tan alta como 5 a 10%. Los peores resultados se asocian con la falta de respuesta a la terapia con esteroides, síntomas neurológicos inusualmente graves o un inicio repentino. Los niños tienden a tener resultados más favorables que los adultos, y los casos que se presentan sin fiebre tienden a tener peores resultados. Este último efecto puede deberse a los efectos protectores de la fiebre oa que el diagnóstico y el tratamiento se buscan más rápidamente cuando hay fiebre.
ADEM puede progresar a EM. Se considerará EM si algunas lesiones aparecen en diferentes momentos y áreas cerebrales.
Déficits motores
Se estima que los déficits motores residuales permanecen en alrededor del 8 al 30 % de los casos, con un rango de gravedad que va desde torpeza leve hasta ataxia y hemiparesia.
Neurocognitivo
Los pacientes con enfermedades desmielinizantes, como la EM, han mostrado déficits cognitivos incluso cuando existe una discapacidad física mínima. La investigación sugiere que se observan efectos similares después de ADEM, pero que los déficits son menos graves que los observados en la EM. En un estudio de seis niños con ADEM (edad media de presentación 7,7 años) se evaluaron una serie de pruebas neurocognitivas después de un promedio de 3,5 años de recuperación. Los seis niños se desempeñaron en el rango normal en la mayoría de las pruebas, incluido el CI verbal y el CI de rendimiento, pero se desempeñaron al menos una desviación estándar por debajo de las normas para su edad en al menos un dominio cognitivo, como atención compleja (un niño), memoria a corto plazo (un hijo) y la conducta/afecto internalizante (dos hijos). Las medias grupales para cada dominio cognitivo estaban todas dentro de una desviación estándar de las normas de edad, lo que demuestra que, como grupo, eran normales. Estos déficits fueron menos graves que los observados en niños de edad similar con diagnóstico de EM.
Otro estudio comparó diecinueve niños con antecedentes de ADEM, de los cuales 10 tenían cinco años de edad o menos en ese momento (edad promedio de 3,8 años, evaluados un promedio de 3,9 años después) y nueve eran mayores (edad promedio de 7,7 años). y en el momento de ADEM, probado un promedio de 2,2 años más tarde) a diecinueve controles emparejados. Las puntuaciones en las pruebas de coeficiente intelectual y el rendimiento educativo fueron más bajas para el grupo ADEM de inicio joven (coeficiente intelectual promedio de 90) en comparación con los grupos de inicio tardío (coeficiente intelectual promedio de 100) y los grupos de control (coeficiente intelectual promedio de 106), mientras que los niños con inicio tardío de ADEM obtuvieron puntajes más bajos en el procesamiento verbal velocidad. Una vez más, las medias de todos los grupos estuvieron dentro de una desviación estándar de los controles, lo que significa que, si bien los efectos fueron estadísticamente confiables, los niños, en su conjunto, aún se encontraban dentro del rango normal. También hubo más problemas de comportamiento en el grupo de inicio temprano, aunque se sugiere que esto puede deberse, al menos en parte, al estrés de la hospitalización a una edad temprana.
Investigación
Actualmente se está investigando la relación entre ADEM y la encefalomielitis asociada a anti-MOG. Se ha propuesto una nueva entidad denominada MOGDEM.
Sobre los modelos animales, el modelo animal principal para la EM, la encefalomielitis autoinmune experimental (EAE), también es un modelo animal para la ADEM. Al ser una enfermedad monofásica aguda, la EAE se parece mucho más a la ADEM que a la EM.
Contenido relacionado
Clozapina
Prueba de Mantoux
Fenilcetonuria